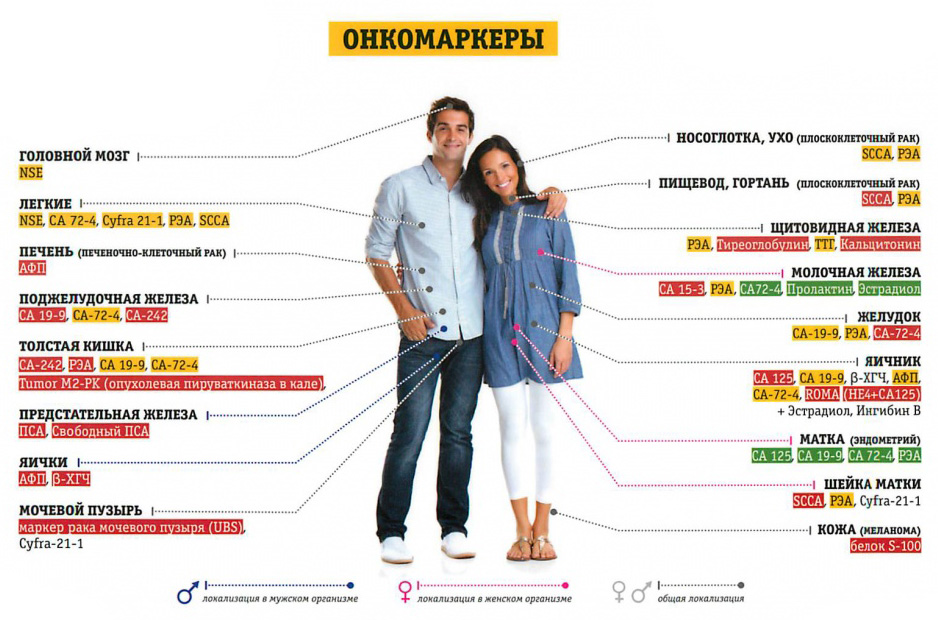
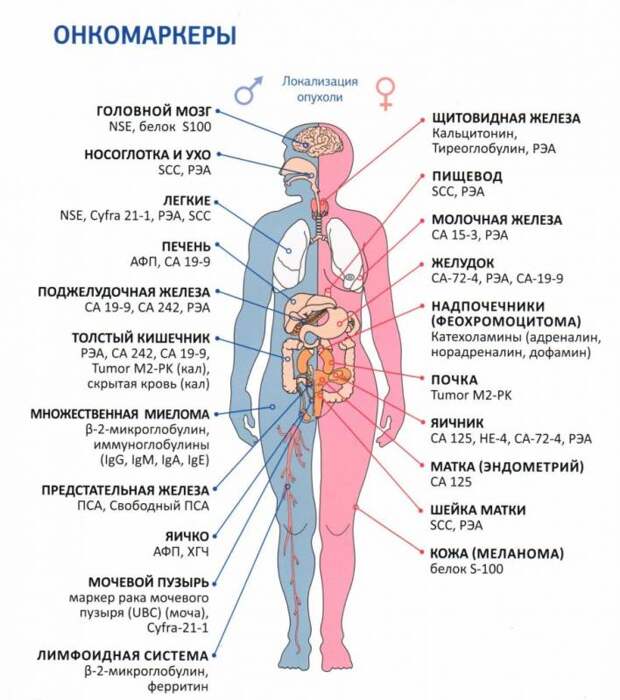
Что такое онкомаркеры и о чем свидетельствуют их показатели
Онкомаркеры — это особенные специфические белки/антигены, образующиеся в крови. В норме они выделяются клетками в незначительном количестве и выполняют в организме разнообразные функции. Однако при наличии злокачественного процесса концентрация этих веществ резко возрастает – онкомаркер может выделяться как самими опухолевыми клетками, так и здоровыми тканями, окружающими новообразование.
Ценностью исследования уровня онкомаркеров является возможность обнаружить патологический процесс задолго до появления первых проявлений заболевания. Кроме того, подобный анализ нередко ставит окончательную точку в сложных диагностических ситуациях.
Анализы крови на онкомаркеры обладают высокой информативностью при соблюдении рекомендаций перед сдачей:
- употребление алкоголя и курения до проведения анализа не рекомендуются;
- анализ проводят с утра натощак, приём пищи следует осуществлять за 8-12 часов до проведения забора крови;
- пить жидкость можно в неограниченных количествах;
- от приёма медикаментозных препаратов и различных медицинских манипуляция следует отказаться, а также уведомить о них своего врача;
- повышенная физическая активность также не рекомендуется;
- при проведении анализа у женщин также учитывают менструальный цикл женщины: анализ проводят в определённые дни.

Различные маркеры характеризуют различные опухоли. В некоторых случаях несколько маркеров характеризуют одну и ту же форму рака, тогда для повышения достоверности результатов одновременно проводят анализ нескольких опухолевых маркеров. Также один и тот же онкомаркер может свидетельствовать о нескольких формах рака.
- ПСА или простато-специфический антиген.
Значительное повышение уровня ПСА в сыворотке иногда обнаруживается при гипертрофии предстательной железы, а также при воспалительных её заболеваниях. Также, следует учитывать, что пальцевое ректальное исследование, цистоскопия, колоноскопия, трансуретральная биопсия, лазерная терапия, задержка мочи могут вызвать более или менее выраженный и длительный подъём уровня ПСА.
 Влияние этих процедур на уровень ПСА максимально выражено на следующий день после их проведения, причём наиболее значительно — у больных с гипертрофией простаты. Исследование ПСА в таких случаях рекомендуется проводить не ранее чем через 7 дней после проведения перечисленных процедур. Уровень ПСА повышается при доброкачественных и злокачественных заболеваниях предстательной железы. При этом при карциноме простаты больше увеличивается доля связанной фракции, поэтому соотношение между свободным и общим ПСА уменьшается.
Влияние этих процедур на уровень ПСА максимально выражено на следующий день после их проведения, причём наиболее значительно — у больных с гипертрофией простаты. Исследование ПСА в таких случаях рекомендуется проводить не ранее чем через 7 дней после проведения перечисленных процедур. Уровень ПСА повышается при доброкачественных и злокачественных заболеваниях предстательной железы. При этом при карциноме простаты больше увеличивается доля связанной фракции, поэтому соотношение между свободным и общим ПСА уменьшается. - РЭА или раково-эмбриональный антиген. Норма онкомаркера — до 5 нг/мл, 5-8 мг на мл рассматривается как пограничное состояние, а патологией является содержание этого онкомаркера в количестве выше 8 нг/мл. В данном случае возможно развитие рака легких, рака прямой или толстой кишки, желудка, яичников, рак груди, щитовидной или поджелудочной железы.

- Онкомаркер СА-125 вырабатывается раковой опухолью яичника. Норма — до 30 МЕ/мл. Уровень 30-40 МЕ/мл означает высокий риск развития рака, при содержании этого онкомаркера в количестве больше 40 МЕ/мл врач уже предполагает наличие раковой опухоли яичника.
- СА-19-9 — вырабатывается при развитии рака поджелудочной железы.
 Норма — до 30 МЕ/мл, опасные значения — 30-40 МЕ/мл, выше 40 МЕ/мл — развивается раковое новообразование.
Норма — до 30 МЕ/мл, опасные значения — 30-40 МЕ/мл, выше 40 МЕ/мл — развивается раковое новообразование.Уровень CА 19-9 повышается при злокачественных новообразованиях: рак поджелудочной железы; рак желчного пузыря и желчных путей; рак мочевого пузыря; первичный рак печени; рак желудка; рак прямой кишки; рак сигмовидной кишки; рак молочной железы; рак яичников; рак матки. Неонкологическая патология, которая сопровождается повышением уровня CА 19-9: цирроз печени; холецистит; муковисцидоз; гепатиты; желчекаменная болезнь.
- СА-15-3 — онкомаркер рака груди. Норма — не более 38 МЕ/мл.
Повышение уровня CA 15-3 наблюдается при злокачественных новообразованиях: рак молочной железы; бронхогенный рак; рак желудка; рак печени; рак поджелудочной железы; рак яичников; рак шейки матки; рак матки; рак эндометрия. Неонкологическая патология: доброкачественные заболевания молочных желез; цирроз печени; беременность в III триместре; аутоиммунные заболевания.
Важно помнить! Отклонение результатов от нормы не всегда является показателем онкологии.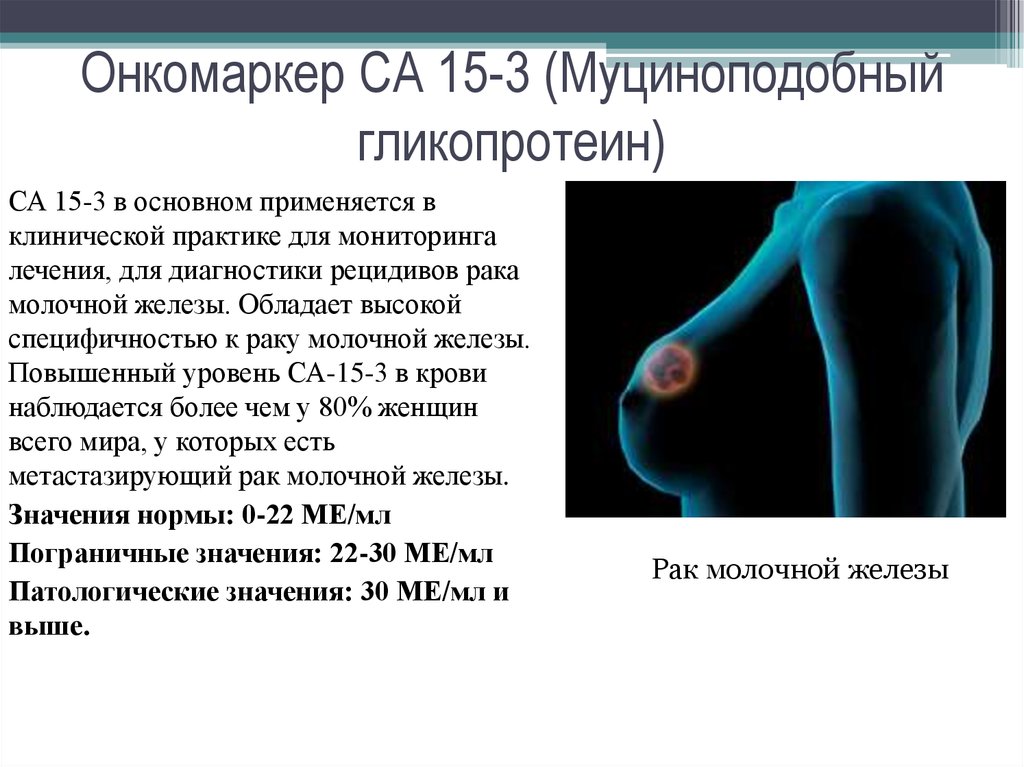
что это за анализ, когда назначают, расшифровка
Содержание:
- Что такое АФП онкомаркер, причины изменения его нормы.
- Показания к проведению анализа.
- Как подготовиться к анализу?
- Техника проведения анализа и расшифровка.
В медицине известно более 200 различных онкомаркеров, среди которых эффективными считаются лишь двадцать. В их число входят АФП и ХГЧ онкомаркеры. Их особенностью является то, что они специфичны и не специфичны одновременно по отношению к патологическим уплотнениям в организме.
Что собой представляет АФП и по каким причинам меняется его норма
Известно, что АФП онкомаркер – это белковое вещество, которое вырабатывается эмбриональными клетками в организме развивающегося плода, клетками печени у взрослых и опухолевыми, если опухоль образуется.
Проконсультироваться с израильским специалистомВ отличие от других, данное вещество всегда присутствует в организме в определенных количествах. Его снижение или увеличение в организме взрослого человека по отношению к норме является сигналом о возможном новообразовании в организме, которое может быть как доброкачественное, так и злокачественное. Если АФП-белок снижается у беременной женщины, скорее всего, имеют место патологии плода.
Увеличение или снижение нормы данного вещества не являются однозначным диагнозом, но являются вектором для дальнейших действий.
Учитывая особенности, онкомаркер делится на два вида – специфичный и не специфичный. В первом случае рост его количества говорит о развитии патологии, то есть продуцируется опухолью.
Таким образом, следует заключить, что AF-protein имеет антираковое действие.
Показания к прохождению обследования
Зная, что АФП онкомаркер – это белковое образование, которое помогает выявить опасную патологию задолго до ее клинического обнаружения и проявления каких-либо симптомов, в ряде случаев следует пройти обследование.Основными показаниями к сдаче анализа на онкомаркры служат:
- Генетическая предрасположенность к онкозаболеваниям.
- Хронические болезни печени, гепатиты всех видов, симптомы цирроза.
- Подозрения на присутствие в организме уплотнений.
- Предраковые состояния.
- Обнаруженные доброкачественные опухоли с высоким риском перерождения в злокачественные.
- Контроль хода лечения и после его завершения с целью прогнозирования рецидива.

- После удаления патологического новообразования.
- Для прогноза риска метастизирования зловредных патологий.
Также узнать, что показывает онкомаркер АФП, необходимо беременным женщинам. В данном случае типичным считается положение, когда его уровень высок. Это связано с тем, что эмбрион воспринимается организмом как чужеродное тело, и он пытается защищаться. А вот если Альфа-белок снижен, следует подозревать патологии у плода, например, Даун синдром, трисомия и многие другие. В то же время, превышение и без того высокого уровня белка также говорит о проблемах с развитием плода вплоть до риска его внутриутробной смерти.
Требования к подготовке пациента перед сдачей анализа
Проверка на АФП онкомаркер – это, что называется, предупреждение рака за счет его раннего выявления и начала лечения, будет эффективной, если правильно подготовиться.
Каких-то особых требований к пациенту нет, но необходимо обязательно соблюсти эти рекомендации:
Отказаться от пищи не менее чем за 8-10 часов до начала анализа. Допускается только негазированная вода, в том числе и утром перед процедурой. Допускается только негазированная вода, в том числе и утром перед процедурой. |
| Предупредить стрессы и физические нагрузки за сутки до начала обследования. Лучше всего провести вечер в спокойной обстановке. |
| Не посещать массаж и любые виды диагностики за сутки до анализа. |
| Прекратить прием лекарственных средств за 8 часов до тестирования (по согласованию с доктором). |
| Отказаться от приема алкоголя, крепкого чая, соков и кофе, не курить за 12 часов до сдачи крови. |
Считается, что лучшим временем для процедуры является утренний промежуток с 8 до 12 часов.
Женщинам следует проконсультироваться с доктором на предмет выбора лучшего дня для тестирования с точки зрения менструального цикла.
Когда проверять норму АФП онкомаркера у женщин в положении и в период лактации, определяет доктор, выбрав оптимальный период и дав индивидуальные рекомендации по подготовке.
Как проводится анализ на онкомаркер
Чтобы проверить, что АФП онкомаркер повышен, понижен или в норме, необходимо сдать венозную кровь в специализированной лаборатории. Материалом для исследования служит выделенная аппаратным способом сыворотка, в которую вводят антитела. Результат их взаимодействия и есть реакция, которая ставится доктором и выносится вердикт: есть патология либо имеется только риск.Расшифровку онкомаркера АФП выполняет та же лаборатория, в которой проводится анализ. Единицей измерения показателей является международная единица на миллилитр крови (МЕ/мл).
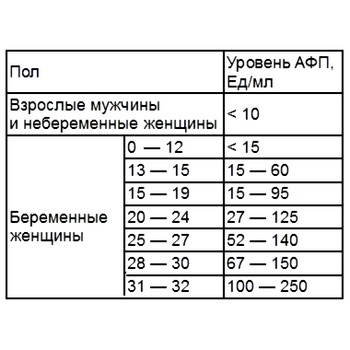
Для здоровых мужчин и не рожавших, не беременных женщин является нормой показатель в 0,5 – 5,5 МЕ/мл. Повышение этой нормы до 10 МЕ/мл говорит о развитии новообразования, и в 95% случаев речь идет о злокачественном уплотнении.
Увеличение количества Альфа-белка более 10 МЕ/мл определяется за 3-4 месяца до появления первых симптомов.
Если результат показывает увеличение нормы онкомаркера АФП в пределах от 5,5 до 10 МЕ/мл, это указывает на наличие заболеваний печени воспалительного характера.
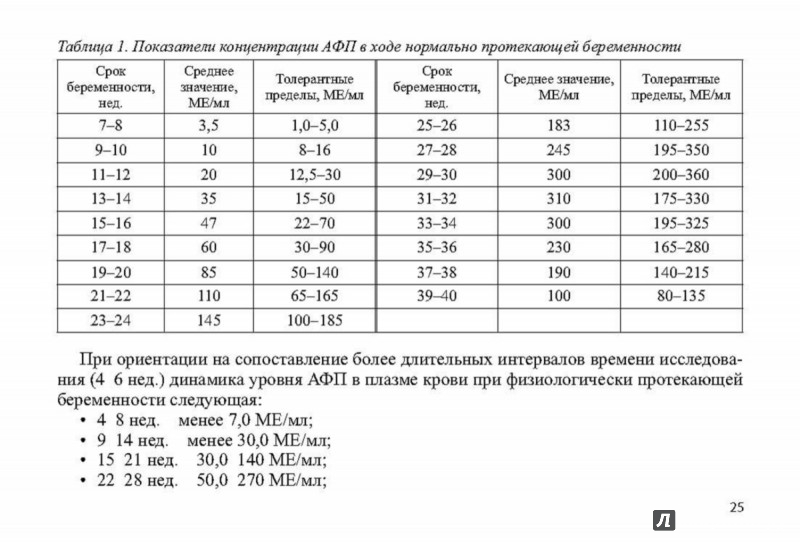
Что касается женщин в положении, то для них определены такие нормы в зависимости от периода беременности:
| 15 недель | от 15,6 до 62,4 МЕ/мл |
| 16 недель | от 16,8 до 66,4 МЕ/мл |
| 18 недель | от 22,4 до 88,8 МЕ/мл |
| 20 недель | от 29,6 до 119,2 МЕ/мл |
Увеличение или снижение этих норм говорит о проблемах с плодом, при этом женщина может чувствовать себя хорошо.
Так, если онкомаркеры АФП при расшифровке нормы дают слишком высокие показатели, это может быть признаком наличия таких болезней у будущего ребенка:
- Печеночный некроз.
- Пупковая грыжа.
- Отклонения в развитии путей мочеиспускания и многие другие.
Обратите внимание, что для достоверности результатов, необходимо дополнительно сделать анализ на гормон ХГЧ и пройти инструментальную диагностику. Только всестороннее обследование в специализированном центре и грамотная расшифровка результатов может служить основанием для постановки диагноза и назначения лечения.
Юлия Гринберг
врач-онколог
Доктор Юлия Гринберг занимает должность старшего врача крупнейшей частной медицинской клиники «Ассута» и является ведущим экспертом по радиотерапии и онкологии в МЦ «Ассута».
Онкомаркеры гепатоцеллюлярной карциномы
1. El-Serag HB, Marrero JA, Rudolph L, Reddy KR. Диагностика и лечение гепатоцеллюлярной карциномы. Гастроэнтерология. 2008; 134:1752–1763. [PubMed] [Google Scholar]
2. Trinchet JC, Alperovitch A, Bedossa P, Degos F, Hainaut P, Beers BV. Эпидемиология, профилактика, скрининг и диагностика гепатоцеллюлярной карциномы. Бык Рак. 2009;96:35–43. (На французском языке) [PubMed] [Google Scholar]
3. Debruyne EN, Delanghe JR. Диагностика и мониторинг гепатоцеллюлярной карциномы с помощью альфа-фетопротеина: новые аспекты и приложения. Клин Чим Акта. 2008;395:19–26. [PubMed] [Google Scholar]
4. Сингхал А., Джаяраман М., Дханасекаран Д.Н., Кохли В. Молекулярные и сывороточные маркеры гепатоцеллюлярной карциномы: прогностические инструменты для прогноза и рецидива. Crit Rev Oncol Hematol. 2012;82:116–140. [PubMed] [Google Scholar]
Молекулярные и сывороточные маркеры гепатоцеллюлярной карциномы: прогностические инструменты для прогноза и рецидива. Crit Rev Oncol Hematol. 2012;82:116–140. [PubMed] [Google Scholar]
5. Leerapun A, Suravarapu SV, Bida JP, et al. Полезность агглютинин-реактивного альфа-фетопротеина Lens culinaris в диагностике гепатоцеллюлярной карциномы: оценка в популяции, направленной в США. Клин Гастроэнтерол Гепатол. 2007;5:394–402. [Бесплатная статья PMC] [PubMed] [Google Scholar]
6. Kobayashi M, Hosaka T, Ikeda K, et al. Высокочувствительный анализ AFP-L3% полезен для прогнозирования рецидива гепатоцеллюлярной карциномы после радикального лечения до и после операции. Гепатология Res. 2011;41:1036–1045. [PubMed] [Google Scholar]
7. Джу М., Чи Дж. Г., Ли Х. Экспрессия HSP70 и HSP27 при гепатоцеллюлярной карциноме. J Korean Med Sci. 2005; 20:829–834. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Luk JM, Lam CT, Siu AF, et al. Протеомное профилирование гепатоцеллюлярной карциномы в китайской когорте выявило активацию белков теплового шока (Hsp27, Hsp70, GRP78) и связанные с ними прогностические значения. Протеомика. 2006;6:1049–1057. [PubMed] [Google Scholar]
Протеомика. 2006;6:1049–1057. [PubMed] [Google Scholar]
9. Shin E, Ryu HS, Kim SH, Jung H, Jang JJ, Lee K. Клинико-патологическое значение белка теплового шока 70 и экспрессии глутаминсинтетазы при гепатоцеллюлярной карциноме. J Hepatobiliary Pancreat Sci. 2011; 18: 544–550. [PubMed] [Google Scholar]
10. Tremosini S, Forner A, Boix L, et al. Проспективная валидация иммуногистохимической панели (глипикан 3, белок теплового шока 70 и глутаминсинтетаза) в биоптатах печени для диагностики очень ранней гепатоцеллюлярной карциномы. Кишка. 2012;61:1481–1487. [PubMed] [Академия Google]
11. Diehl JA, Yang W, Rimerman RA, Xiao H, Emili A. Hsc70 регулирует накопление циклина D1 и циклин D1-зависимой протеинкиназы. Мол Селл Биол. 2003; 23:1764–1774. [Бесплатная статья PMC] [PubMed] [Google Scholar]
12. Calderwood SK, Khaleque MA, Sawyer DB, Ciocca DR. Белки теплового шока при раке: шапероны туморогенеза. Тенденции биохимических наук. 2006; 31: 164–172. [PubMed] [Google Scholar]
13. Filmus J, Capurro M, Rast J. Glypicans. Геном биол. 2008; 9:224. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Filmus J, Capurro M, Rast J. Glypicans. Геном биол. 2008; 9:224. [Бесплатная статья PMC] [PubMed] [Google Scholar]
14. Zittermann SI, Capurro MI, Shi W, Filmus J. Растворимый глипикан 3 ингибирует рост гепатоцеллюлярной карциномы in vitro и in vivo. Инт Джей Рак. 2010; 126:1291–1301. [PubMed] [Google Scholar]
15. Zittermann SI, Capurro MI, Shi W, Filmus J. Glypican-3 способствует росту гепатоцеллюлярной карциномы, стимулируя каноническую передачу сигналов Wnt. Рак Рез. 2005; 65: 6245–6254. [PubMed] [Google Scholar]
16. Shirakawa H, Kumnuma T, Nishimura Y, et al. Глипикан-3 является полезным диагностическим маркером компонента гепатоцеллюлярной карциномы при раке печени человека. Int J Oncol. 2009 г.;34:649–656. [PubMed] [Google Scholar]
17. Guido M, Roskams T, Pontisso P, et al. Антиген плоскоклеточного рака в канцерогенезе печени человека. Джей Клин Патол. 2008; 61: 445–447. [PubMed] [Google Scholar]
18. Trerotoli P, Fransvea E, Angelotti U, et al. Тканевая экспрессия антигена плоскоклеточного рака (SCCA) обратно пропорциональна размеру опухоли при ГЦР. Мол Рак. 2009; 8:29. [Статья бесплатно PMC] [PubMed] [Google Scholar]
Тканевая экспрессия антигена плоскоклеточного рака (SCCA) обратно пропорциональна размеру опухоли при ГЦР. Мол Рак. 2009; 8:29. [Статья бесплатно PMC] [PubMed] [Google Scholar]
19. Giannelli G, Marinosci F, Sgarra C, Lupo L, Dentico P, Antonaci S. Клиническая роль тканевых и сывороточных уровней антигена SCCA при гепатоцеллюлярной карциноме. Инт Джей Рак. 2005;116:579–583. [PubMed] [Google Scholar]
20. Beneduce L, Castaldi F, Marino M, et al. Комплексы антиген-иммуноглобулин М плоскоклеточной карциномы как новые биомаркеры гепатоцеллюлярной карциномы. Рак. 2005; 103: 2558–2565. [PubMed] [Google Scholar]
21. Pontisso P, Quarta S, Caberlotto C, et al. Прогрессирующее увеличение иммунных комплексов SCCA-IgM у больных циррозом связано с развитием гепатоцеллюлярной карциномы. Инт Джей Рак. 2006; 119: 735–740. [PubMed] [Академия Google]
22. Kladney RD, Bulla GA, Guo L, et al. GP73, новый белок, локализованный в комплексе Гольджи, активируется вирусной инфекцией. Ген. 2000; 249:53–65. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Ген. 2000; 249:53–65. [Бесплатная статья PMC] [PubMed] [Google Scholar]
23. Zhang F, Gu Y, Li X, Wang W, He J, Peng T. Повышенная экспрессия фосфопротеина 2 Гольджи (GOLPh3) в ткани аденокарциномы легкого. Клин Биохим. 2010;43:983–991. [PubMed] [Google Scholar]
24. Fritzsche FR, Kristiansen G, Riener MO, Dietel M, Oelrich B. Экспрессия GOLPh3 может служить диагностическим маркером при семиномах. БМЦ Урол. 2010;10:4. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Fritzsche FR, Riener MO, Dietel M, Moch H, Jung K, Kristiansen G. Экспрессия GOLPh3 при почечно-клеточном раке. БМЦ Урол. 2008; 8:15. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Kristiansen G, Fritzsche FR, Wassermann K, et al. Экспрессия белка GOLPh3 как нового тканевого биомаркера рака предстательной железы: значение для тканевой диагностики. Бр Дж Рак. 2008; 99: 939–948. [Бесплатная статья PMC] [PubMed] [Google Scholar]
27. Shi Y, Chen J, Li L, et al. Изучение диагностической ценности белка Гольджи GP73 и его генетического анализа при первичной карциноме печени. Лечение рака Technol Res. 2011; 10: 287–294. [PubMed] [Google Scholar]
Лечение рака Technol Res. 2011; 10: 287–294. [PubMed] [Google Scholar]
28. Tian L, Wang Y, Xu D, et al. Серологический белок АФП/Гольджи 73 может быть новым диагностическим параметром заболеваний печени. Инт Джей Рак. 2011; 129:1923–1931. [PubMed] [Google Scholar]
29. Riener MO, Stenner F, Liewen H, et al. Экспрессия фосфопротеина Гольджи 2 (GOLph3) в опухолях печени и его значение в качестве сывороточного маркера при гепатоцеллюлярных карциномах. Гепатология. 2009; 49: 1602–1609. [PubMed] [Google Scholar]
30. Zhou Y, Yin X, Ying J, Zhang B. Белок Гольджи 73 в сравнении с альфа-фетопротеином как биомаркер гепатоцеллюлярной карциномы: диагностический метаанализ. БМК Рак. 2012;12:17. [Бесплатная статья PMC] [PubMed] [Google Scholar]
31. Mao YL, Yang HY, Xu HF, et al. Значение гликопротеина Гольджи 73, нового онкомаркера в диагностике гепатоцеллюлярной карциномы: первичное исследование. Чжунхуа И Сюэ За Чжи. 2008; 88: 948–951. (На китайском языке) [PubMed] [Google Scholar]
32. Дрейк Р.Р., Швеглер Э.Е., Малик Г., Диас Дж., Блок Т., Мехта А., Семмес О.Дж. Стратегии захвата лектина в сочетании с масс-спектрометрией для обнаружения биомаркеров гликопротеинов сыворотки. Мол клеточная протеомика. 2006; 5: 1957–1967. [PubMed] [Академия Google]
Дрейк Р.Р., Швеглер Э.Е., Малик Г., Диас Дж., Блок Т., Мехта А., Семмес О.Дж. Стратегии захвата лектина в сочетании с масс-спектрометрией для обнаружения биомаркеров гликопротеинов сыворотки. Мол клеточная протеомика. 2006; 5: 1957–1967. [PubMed] [Академия Google]
33. Чжан И, Дэн ЗС, Ляо ММ, Ван Н, Чжан XQ, Ю ХИ, Чжан ЮД. Связанный с опухолью гликопротеин-72 является новым маркером плохой выживаемости при гепатоцеллюлярной карциноме. Патол Онкол Рез. 2012;18:911–916. [PubMed] [Google Scholar]
34. Миленик Д.Э., Брэди Э.Д., Гарместани К., Альберт П.С., Абдулла А., Брехбил М.В. Улучшенная эффективность лучевой терапии, нацеленной на альфа-частицы: двойное нацеливание на рецептор-2 эпидермального фактора роста человека и ассоциированный с опухолью гликопротет в 72. Рак. 2010;116:1059–1066. [Бесплатная статья PMC] [PubMed] [Google Scholar]
35. Mracek T, Stephens NA, Gao D, et al. Повышенная продукция ZAG подкожной жировой тканью связана с потерей веса у пациентов с раком желудочно-кишечного тракта. Бр Дж Рак. 2011; 104:441–447. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Бр Дж Рак. 2011; 104:441–447. [Бесплатная статья PMC] [PubMed] [Google Scholar]
36. Wang F, Geng Y, Zhang WM, Geng X. Идентификация белка ZAG в качестве нового кандидата серологического биомаркера рака печени. Adv Mater Res. 2012; 340:383–389. [Google Scholar]
37. Naraki T, Kohno N, Saito H, Fujimoto Y, Ohhira M, Morita T, Kohgo Y. Содержание гамма-карбоксиглутаминовой кислоты в дез-гамма-карбоксипротромбине, связанном с гепатоцеллюлярной карциномой. Биохим Биофиз Акта. 2002; 1586: 287–29.8. [PubMed] [Google Scholar]
38. Nakamura S, Nouso K, Sakaguchi K, et al. Чувствительность и специфичность дез-гамма-карбоксипротромбина для диагностики пациентов с гепатоцеллюлярной карциномой зависит от размера опухоли. Am J Гастроэнтерол. 2006;101:2038–2043. [PubMed] [Google Scholar]
39. Baek YH, Lee JH, Jang JS, et al. Диагностическая роль и корреляция с системами стадирования PIVKA-II по сравнению с ОВП. Гепатогастроэнтерология. 2009; 56: 763–767. [PubMed] [Академия Google]
40. Ямамото К., Имамура Х., Мацуяма Ю. и др. Значение альфа-фетоптеина и дез-гамма-карбоксипротромбина у пациентов с гепатоцеллюлярной карциномой, перенесших гепатэктомию. Энн Сург Онкол. 2009;16:2795–2804. [PubMed] [Google Scholar]
Ямамото К., Имамура Х., Мацуяма Ю. и др. Значение альфа-фетоптеина и дез-гамма-карбоксипротромбина у пациентов с гепатоцеллюлярной карциномой, перенесших гепатэктомию. Энн Сург Онкол. 2009;16:2795–2804. [PubMed] [Google Scholar]
41. Yamamoto K, Imamura H, Matsuyama Y, et al. AFP, AFP-L3, DCP и GP73 в качестве маркеров для мониторинга ответа на лечение и рецидивов, а также в качестве суррогатных маркеров клинико-патологических переменных ГЦК. J Гастроэнтерол. 2010;45:1272–1282. [PubMed] [Академия Google]
42. Yao DF, Dong ZZ, Yao M. Специфические молекулярные маркеры при гепатоцеллюлярной карциноме. Гепатобилиарная система поджелудочной железы Dis Int. 2007; 6: 241–247. [PubMed] [Google Scholar]
43. Cui R, He J, Zhang F, et al. Диагностическое значение белка, индуцированного отсутствием витамина К (PIVKAII), и специфической для гепатомы полосы сывороточной гамма-глутамилтрансферазы (GGTII) в качестве маркеров гепатоцеллюлярной карциномы, комплементарных альфа-фетопротеину. Бр Дж Рак. 2003; 88: 1878–1882. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Бр Дж Рак. 2003; 88: 1878–1882. [Бесплатная статья PMC] [PubMed] [Google Scholar]
44. Wang CS, Lin CL, Lee HC, et al. Полезность дез-гамма-карбоксипротромбина сыворотки в обнаружении гепатоцеллюлярной карциномы. Мир J Гастроэнтерол. 2005; 11:6115–6119. [Бесплатная статья PMC] [PubMed] [Google Scholar]
45. Tangkijvanich P, Tosukhowong P, Bunyongyod P, et al. Альфа-L-фукозидаза как сывороточный маркер гепатоцеллюлярной карциномы в Таиланде. Общественное здравоохранение J Trop Med из Юго-Восточной Азии. 1999; 30:110–114. [PubMed] [Google Scholar]
46. Фаузи Монтасер М., Амин Сакр М., Омар Халифа М. Альфа-L-фукозидаза как онкомаркер гепатоцеллюлярной карциномы. Араб Дж. Гастроэнтерол. 2012;13:9–13. [PubMed] [Google Scholar]
47. Pillai AA, Fimmel CJ. Новые сывороточные биомаркеры ГЦК. Клин Гастроэнтерол. 2012; 27: 247–262. [Google Scholar]
48. Zhou L, Liu J, Luo F. Сывороточные онкомаркеры для выявления гепатоцеллюлярной карциномы. Мир J Гастроэнтерол. 2006; 12:1175–1181. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2006; 12:1175–1181. [Бесплатная статья PMC] [PubMed] [Google Scholar]
49. Balzarini P, Benetti A, Invernici G, et al. Трансформирующий фактор роста-бета1 индуцирует микрососудистые аномалии за счет понижающей модуляции молекулы адгезии нервных клеток при гепатоцеллюлярной карциноме человека. Лаборатория Инвест. 2012;92: 1297–1309. [PubMed] [Google Scholar]
50. Dong ZZ, Yao DF, Yao M, et al. Клиническое влияние TGF-beta1 плазмы и циркулирующей мРНК TGF-beta1 в диагностике гепатоцеллюлярной карциномы. Гепатобилиарная система поджелудочной железы Dis Int. 2008; 7: 288–295. [PubMed] [Google Scholar]
51. Xiang ZL, Zeng ZC, Fan J, et al. Профилирование экспрессии генов в фиксированных тканях выявило индуцируемый гипоксией фактор-1α, VEGF и матриксную металлопротеиназу-2 в качестве биомаркеров метастазирования в лимфатические узлы при гепатоцеллюлярной карциноме. Клин Рак Рез. 2011;17:5463–5472. [PubMed] [Академия Google]
52. Zhang L, Wang JN, Tang JM, et al.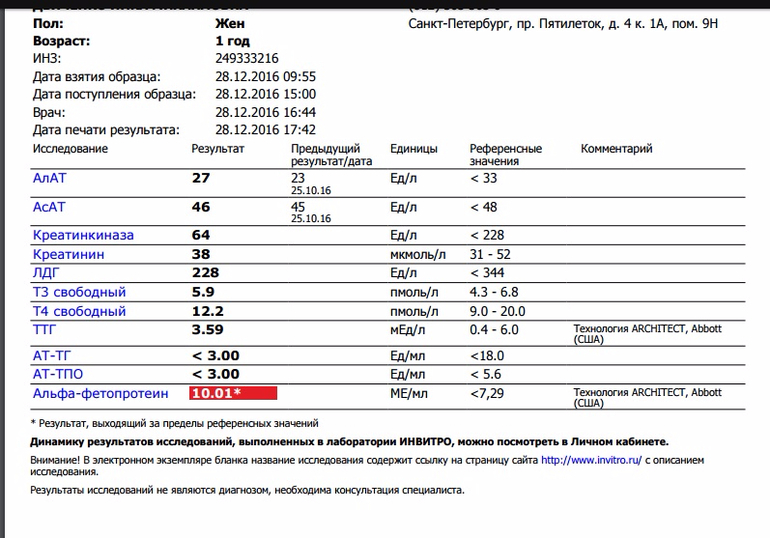 VEGF необходим для роста и миграции клеток гепатоцеллюлярной карциномы человека. Mol Biol Rep. 2012; 39: 5085–5093. [Бесплатная статья PMC] [PubMed] [Google Scholar]
VEGF необходим для роста и миграции клеток гепатоцеллюлярной карциномы человека. Mol Biol Rep. 2012; 39: 5085–5093. [Бесплатная статья PMC] [PubMed] [Google Scholar]
53. Zhi H, Zhan J, Deng QL, et al. Послеоперационное обнаружение мРНК АФП в периферической крови больных печеночно-клеточным раком и его корреляция с рецидивом. Чжунхуа Чжун Лю За Чжи. 2007; 29: 112–115. (На китайском языке) [PubMed] [Google Scholar]
54. Yamamoto Y, Kosaka N, Tanaka M, et al. МикроРНК-500 как потенциальный диагностический маркер гепатоцеллюлярной карциномы. Биомаркеры. 2009 г.;14:529–538. [PubMed] [Google Scholar]
55. Xiong Y, Fang JH, Yun JP, et al. Влияние микроРНК-29 на апоптоз, онкогенность и прогноз гепатоцеллюлярной карциномы. Гепатология. 2010;51:836–845. [PubMed] [Google Scholar]
56. Hou J, Lin L, Zhou W, et al. Идентификация микрономов в печени человека и гепатоцеллюлярной карциноме показывает, что миР-199a/b-3p является терапевтической мишенью для гепатоцеллюлярной карциномы. Раковая клетка. 2011;19:232–243. [PubMed] [Google Scholar]
Раковая клетка. 2011;19:232–243. [PubMed] [Google Scholar]
57. Xu Y, Xia F, Ma L, Shan J, et al. МикроРНК-122 повышает чувствительность раковых клеток ГЦК к адриамицину и винкристину посредством модулирования экспрессии МЛУ и индукции остановки клеточного цикла. Рак Летт. 2011; 310:160–169. [PubMed] [Google Scholar]
58. Volinia S, Calin GA, Liu CG, et al. Сигнатура экспрессии микроРНК солидных опухолей человека определяет мишени раковых генов. Proc Natl Acad Sci USA. 2006; 103: 2257–2261. [Бесплатная статья PMC] [PubMed] [Google Scholar]
59. Medina PP, Nolde M, Slack FJ. Зависимость от OncomiR в модели пре-В-клеточной лимфомы, индуцированной микроРНК-21, in vivo. Природа. 2010; 467:86–90. [PubMed] [Google Scholar]
60. Meng F, Henson R, Wehbe-Janek H, Ghoshal K, Jacob ST, Patel T. МикроРНК-21 регулирует экспрессию гена-супрессора опухоли PTEN при гепатоцеллюлярном раке человека. Гастроэнтерология. 2007; 133: 647–58. [Бесплатная статья PMC] [PubMed] [Google Scholar]
61.


 Влияние этих процедур на уровень ПСА максимально выражено на следующий день после их проведения, причём наиболее значительно — у больных с гипертрофией простаты. Исследование ПСА в таких случаях рекомендуется проводить не ранее чем через 7 дней после проведения перечисленных процедур. Уровень ПСА повышается при доброкачественных и злокачественных заболеваниях предстательной железы. При этом при карциноме простаты больше увеличивается доля связанной фракции, поэтому соотношение между свободным и общим ПСА уменьшается.
Влияние этих процедур на уровень ПСА максимально выражено на следующий день после их проведения, причём наиболее значительно — у больных с гипертрофией простаты. Исследование ПСА в таких случаях рекомендуется проводить не ранее чем через 7 дней после проведения перечисленных процедур. Уровень ПСА повышается при доброкачественных и злокачественных заболеваниях предстательной железы. При этом при карциноме простаты больше увеличивается доля связанной фракции, поэтому соотношение между свободным и общим ПСА уменьшается.
 Норма — до 30 МЕ/мл, опасные значения — 30-40 МЕ/мл, выше 40 МЕ/мл — развивается раковое новообразование.
Норма — до 30 МЕ/мл, опасные значения — 30-40 МЕ/мл, выше 40 МЕ/мл — развивается раковое новообразование.