Антигистаминные препараты: первое и второе поколения
Аллергия готовься!
Для начала выясним, что способствует развитию аллергической реакции. От чего у нас могут появится внезапный кожный зуд, отек слизистой дыхательных путей, боли в животе и прочие проявления острой аллергии? Виной тому — выброс гистамина, медиатора, который выделяется в ответ на попадание аллергена.
Поэтому в борьбе с проявлениями аллергии важное место занимает прием препаратов, блокирующих рецепторы гистамина, снижающих его влияние на организм. Они называются антигистаминными. Существует два поколения антигистаминных лекарственных препаратов.1, 2 Рассмотрим их подробнее.
Антигистаминные препараты 1 поколения
Каждое их поколение – это своеобразный эволюционный виток в развитии лекарственных средств. Чем они новее, тем благоприятнее их профиль безопасности, риск формирования лекарственной устойчивости ниже, а продолжительность действия выше.2
Первое поколение появилось в начале 20 века, и их эффекты связаны с блокирующим действием на гистаминовые рецепторы.
К сожалению, у антигистаминных препаратов 1 поколения есть ряд серьезных побочных эффектов, значительно ограничивающих их применение. Дело в том, что действующие вещества проникают через гематоэнцефалический барьер (своего рода физиологический фильтр между кровеносной системой и центральной нервной системой, через который в мозг поступают питательные, биоактивные вещества и часть лекарственных средств), где происходит их связывание с рецепторами головного мозга, развивается блокада центральных серотониновых и м-холинорецепторов. Это может стать причиной развития седативного эффекта разной степени выраженности, от незначительного до сильного.
Есть и другие побочные эффекты — сухость во рту, усиление обструкции (непроходимости) дыхательных путей, повышение вязкости мокроты, тахикардия, нечеткость зрения. Из негативных свойств стоит отметить развитие тахифилаксии, то есть снижения эффекта через определенный промежуток приема, обычно через 15-20 дней.
Наиболее известные антигистаминные препараты 1 поколения:
-
Димедрол.
-
Мебгидролин.
Может вызывать чувство головокружения, торможение психической активности. Из-за раздражающего влияния на слизистую желудка рекомендуется принимать после еды. -
Хлоропирамин.
Может использоваться при конъюнктивите и аллергии на коже. Для быстрого эффекта назначается в инъекциях.1, 2
Антигистаминные препараты 2 поколения
Препараты 2 поколения отличаются минимальным влиянием на серотониновые и, так называемые, м-холинорецепторы, а также тем, что к ним очень чувствительны гистаминовые рецепторы.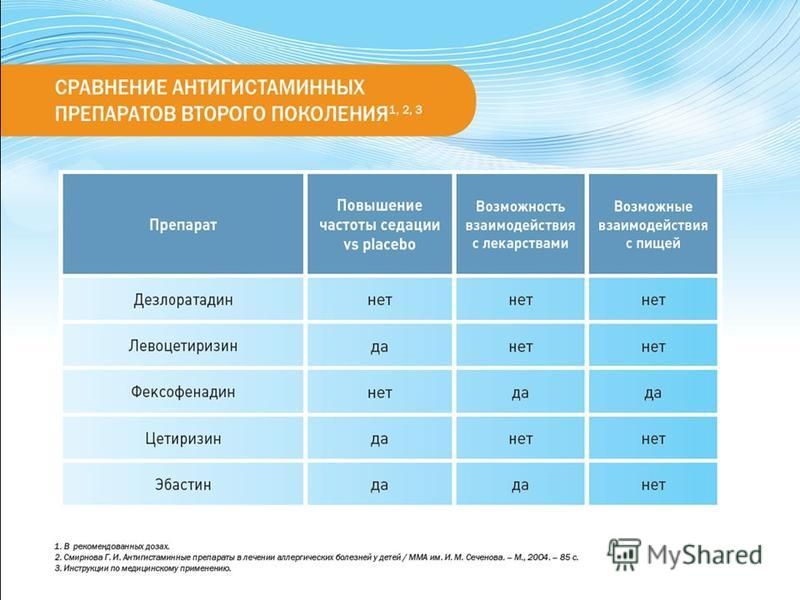
Они практически не вызывают седативного действия, нет у них и эффекта тахифилаксии, поэтому они могут назначаться длительно (по рекомендации врача). Однако стоит помнить, что препараты 2 поколения могут оказывать нежелательное воздействие на сердце, поэтому при их длительном приеме необходимо контролировать работу сердечной мышцы.1
Антигистаминные препараты второго поколения:
-
Лоратадин
Действует длительно, до 24 часов. Снимает зуд, отеки, нормализует проницаемость капилляров. -
Цетиризин
Применяется для предотвращения и снижения симптомов аллергии. Действует быстро, эффект отмечается примерно через 20 минут и сохраняется больше суток.3 -
Эбастин.
Назначается при проявления аллергии на коже и слизистой глаз. Не проникает в головной мозг, поэтому на нервную систему и психические реакции влияние Эбастина минимально.
Не проникает в головной мозг, поэтому на нервную систему и психические реакции влияние Эбастина минимально.
Активные метаболиты препаратов 2 поколения
Существуют абсолютно современные разработки, которые практически лишены недостатков лекарств от аллергии предыдущих поколений. Они не влияют на сердце и центральную нервную систему, не подавляют психические реакции, не приводят к привыканию.
К этим препаратам можно отнести фексофенадин и дезлоратадин. Первый показан при сезонном аллергическом рините и при хронической крапивнице, препятствует выбросу гистамина и развитию реакций на аллерген. При этом действие начинается примерно через 1 час после приема дозы, и длится до суток. Второй препарат назначается при аллергическом насморке, крапивнице. Он блокирует выброс биологически-активных факторов аллергии и предупреждает симптомы заболевания. Снимает спазм, уменьшает отеки и зуд, нормализует проницаемость капилляров. Эффект появляется относительно быстро, примерно в течение 30 минут после приема дозы и продолжается до 24 часов.
Антигистаминные препараты в лечении аллергического ринита | Гусева
1. Астафьева Н.Г., Баранов А.А., Вишнева Е.А., Дайхес Н.А., Жестков А.В., Ильина Н.И. и др. Аллергический ринит. Клинические рекомендации Российской ассоциации аллергологов и клинических иммунологов, Национальной медицинской ассоциации оториноларингологов, Союза педиатров России, 2019. Режим доступа: http://raaci.ru/dat/pdf/allergic_rhinitis-project.pdf.
2. Okubo K., Kurono Y., Ichimura K., Enomoto T., Okamoto Y., Kawauchi H. et al.; Japanese Society of Allergology. Japanese guidelines for allergic rhinitis 2017. Allergol Int. 2017;66(2):205–219. doi: 10.1016/j.alit.2016.11.001.
3. Wang D., Clement P., Smitz J., De Waele M., Derde M.P. Correlations between complaints, inflammatory cells and mediator concentrations in nasal secretions after nasal allergen challenge and during natural allergen exposure.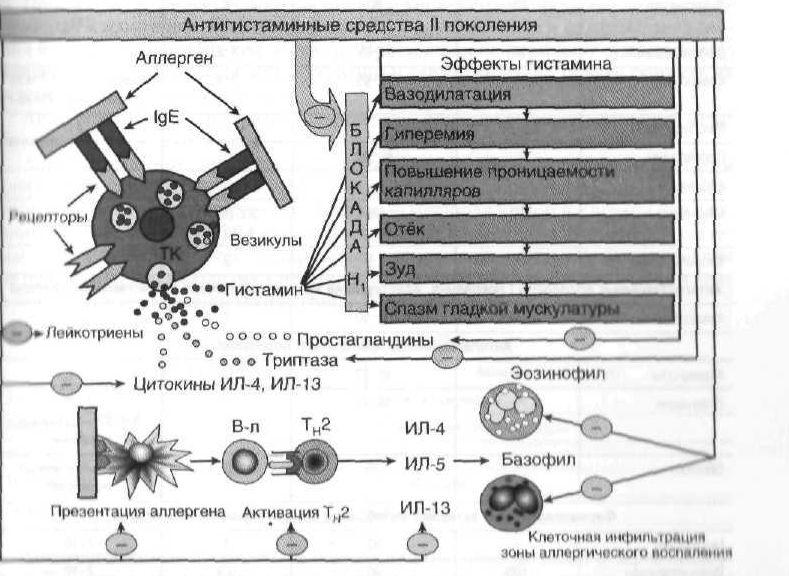
4. Хаитов Р.М., Ильина Н.И. (ред.). Аллергология и иммунология: национальное руководство. М.: ГЭОТАР-Медиа; 2009. 656 с. Режим доступа: https://www.rosmedlib.ru/book/ISBN9785970409039.html.
5. Pawankar R., Bunnag C., Khaltaev N., Bousquet J. Allergic Rhinitis and Its Impact on Asthma in Asia Pacific and the ARIA Update 2008. World Allergy Organ J. 2012;5(3):212–217. doi: 10.1097/WOX.0b013e318201d831.
 10.4.370.
10.4.370.7. Zhang L., Han D., Huang D., Wu Y., Dong Z., Xu G. et al. Prevalence of selfreported allergic rhinitis in eleven major cities in Сhina. Int Arch Allergy Immunol. 2009;149(1):47–57. doi: 10.1159/000176306.
8. Angier E., Willington J., Scadding G., Holmes S., Walker S. Management of allergic and non-allergic rhinitis: a primary care summary of the BSACI guideline. Prim Care Respir J. 2010;19(3):217–222. doi: 10.4104/pcrj.2010.00044.
9. Colás C., Galera H., Añibarro B., Soler R., Navarro A., Jáuregui I., Peláez A. Disease severity impairs sleep quality in allergic rhinitis (The SOMNIAAR study). Clin Exp Allergy. 2012;42(7):1080–1087. doi: 10.1111/j.1365-2222.2011.03935.x.
10.
11. Mandhane S.N., Shah J.H., Thennati R. Allergic rhinitis: an update on disease, present treatments and future prospects. Int Immunopharmacol. 2011;11(11):1646–1662. doi: 10.1016/j.intimp.2011.07.005.
12. Wang Y., Ghoshal A.G., Bin Abdul Muttalif A.R., Lin H.-C., Thanaviratananich S., Bagga S. et al. Quality of Life and Economic Burden of Respiratory Disease in Asia-Pacific – Asia-Pacific Burden of Respiratory Diseases Study. Value Health Reg Issues. 2016;9:72–77. doi: 10.1016/j.vhri.2015.11.004.
13. Соболенко Т.М. Применение Н1-антигистаминных средств в клинической практике: проблемы и решения. Медицинские новости. 2016;(3):4–9. Режим доступа: https://cyberleninka.ru/article/n/primenenie-n1-antigistaminnyh-sredstv-v-klinicheskoy-praktike-problemy-i-resheniya.
Медицинские новости. 2016;(3):4–9. Режим доступа: https://cyberleninka.ru/article/n/primenenie-n1-antigistaminnyh-sredstv-v-klinicheskoy-praktike-problemy-i-resheniya.
14. Kawauchi H., Yanai K., Wang D.Y., Itahashi K., Okubo K. Antihistamines for Allergic Rhinitis Treatment from the Viewpoint of Nonsedative Properties. Int J Mol Sci. 2019;20(1):213. doi: 10.3390/ijms20010213.
15. Church M.K., Church D.S. Pharmacology of antihistamines. Indian J Dermatol. 2013;58(3):219–224. doi: 10.4103/0019-5154.110832.
16. Wallace D.V., Dykewicz M.S., Bernstein D.I., Blessing-Moore J., Cox L., Khan D.A. et al. The diagnosis and management of rhinitis: an updated practice parameter. J Allergy Clin Immunol. 2008;122(2):1–84. doi: 10.1016/j.jaci.2008.06.003.
17. Карева Е.Н. Выбор антигистаминного препарата: взгляд фармаколога. РМЖ. 2016;(12):811–816. Режим доступа: https://www.rmj.ru/articles/allergologiya/vybor-antigistaminnogo-preparata-vzglyad-farmakologa5803/
Карева Е.Н. Выбор антигистаминного препарата: взгляд фармаколога. РМЖ. 2016;(12):811–816. Режим доступа: https://www.rmj.ru/articles/allergologiya/vybor-antigistaminnogo-preparata-vzglyad-farmakologa5803/
18. Picado C. Rupatadine: pharmacological profile and its use in the treatment of allergic disorders. Expert Opin Pharmacother. 2006;7(14):1989– 2001. doi: 10.1517/14656566.7.14.1989.
19. Kowal K., DuBuske L. Bilastine as a potential treatment in allergic rhinitis. Am J Rhinol Allergy. 2014;28(4):312–316. doi: 10.2500/ajra.2014.28.4049.
20. Wolthers O.D. Bilastine: a new nonsedating oral h2 antihistamine for treatment of allergic rhinoconjunctivitis and urticaria. Biomed Res Int. 2013;2013:626837. doi: 10.1155/2013/626837.
21. Bosma R., van den Bor J., Vischer H.F., Labeaga L., Leurs R. The long duration of action of the second generation antihistamine bilastine coincides with its long residence time at the histamine h2 receptor. Eur J Pharmacol. 2018;838:107–111. doi: 10.1016/j.ejphar.2018.09.011.
Bosma R., van den Bor J., Vischer H.F., Labeaga L., Leurs R. The long duration of action of the second generation antihistamine bilastine coincides with its long residence time at the histamine h2 receptor. Eur J Pharmacol. 2018;838:107–111. doi: 10.1016/j.ejphar.2018.09.011.
22. Brożek J.L., Bousquet J., Agache I., Agarwal A., Bachert C., Bosnic-Anticevich S. et al. Allergic Rhinitis and its Impact on Asthma (ARIA) guidelines – 2016 revision. J Allergy Clin Immunol. 2017;140(4):950–958. doi: 10.1016/j.jaci.2017.03.050.
23. Recto M.T., Gabriel M.T., Kulthanan K., Tantilipikorn P., Aw D.C., Lee T.H. et al. Selecting optimal second-generation antihistamines for allergic rhinitis and urticaria in Asia. Clin Mol Allergy. 2017;15:19. doi: 10.1186/s12948-017-0074-3.
24. Jauregizar N., de la Fuente L., Lucero M.L., Sologuren A., Leal N., Rodríguez M. Pharmacokinetic-pharmacodynamic modelling of the antihistaminic (h2) effect of bilastine. Clin Pharmacokinet. 2009;48(8):543–554. doi: 10.2165/11317180-000000000-00000.
Jauregizar N., de la Fuente L., Lucero M.L., Sologuren A., Leal N., Rodríguez M. Pharmacokinetic-pharmacodynamic modelling of the antihistaminic (h2) effect of bilastine. Clin Pharmacokinet. 2009;48(8):543–554. doi: 10.2165/11317180-000000000-00000.
25. Sádaba B., Gómez-Guiu A., Azanza J.R., Ortega I., Valiente R. Oral availability of bilastine. Clin Drug Investig. 2013;33(5):375–381. doi: 10.1007/s40261-013-0076-y.
26. Kuna P., Bachert C., Nowacki Z., van Cauwenberge P., Agache I., Fouquert L. et al.; Bilastine International Working Group. Efficacy and safety of bilastine 20 mg compared with cetirizine 10 mg and placebo for the symptomatic treatment of seasonal allergic rhinitis: a randomized, doubleblind, parallel-group study. Clin Exp Allergy. 2009;39(9):1338–1347. doi: 10.1111/j.1365-2222.2009.03257.x.
27. Bachert C., Kuna P., Sanquer F., Ivan P., Dimitrov V., Gorina M.M. et al; Bilastine International Working Group. Comparison of the efficacy and safety of bilastine 20 mg vs desloratadine 5 mg in seasonal allergic rhinitis patients. Allergy. 2009;64(1):158–165. doi: 10.1111/j.1398-9995.2008.01813.x.
Bachert C., Kuna P., Sanquer F., Ivan P., Dimitrov V., Gorina M.M. et al; Bilastine International Working Group. Comparison of the efficacy and safety of bilastine 20 mg vs desloratadine 5 mg in seasonal allergic rhinitis patients. Allergy. 2009;64(1):158–165. doi: 10.1111/j.1398-9995.2008.01813.x.
28. Annesi-Maesano I., Beyer A., Marmouz F., Mathelier-Fusade P., Vervloet D., Bauchau V. Concurrent allergic diseases: a cross-sectional study in a French population. Allergy. 2006;61(3):390–391. doi: 10.1111/j.1398-9995.2006.01019.x.
29. Conen S., Theunissen E.L., Van Oers A.C., Valiente R., Ramaekers J.G. Acute and subchronic effects of bilastine (20 and 40 mg) and hydroxyzine (50 mg) on actual driving performance in healthy volunteers. J Psychopharmacol. 2011;25(11):1517–1523. doi: 10.1177/0269881110382467.
30. Demonte A., Guanti M.B., Liberati S., Biffi A., Fernando F., Fainello M., Pepe P. Bilastine safety in drivers who need antihistamines: new evidence from high-speed simulator driving test on allergic patients. Eur Rev Med Pharmacol Sci. 2018;22(3):820–828. doi: 10.26355/eurrev_201802_14318.
Demonte A., Guanti M.B., Liberati S., Biffi A., Fernando F., Fainello M., Pepe P. Bilastine safety in drivers who need antihistamines: new evidence from high-speed simulator driving test on allergic patients. Eur Rev Med Pharmacol Sci. 2018;22(3):820–828. doi: 10.26355/eurrev_201802_14318.
31. Graff C., Struijk J.J., Kanters J.K., Andersen M.P., Toft E., Tyl B. Effects of bilastine on T-wave morphology and the QTc interval: a randomized, doubleblind, placebo-controlled, thorough QTc study. Clin Drug Investig. 2012;32(5):339–351. doi: 10.2165/11599270-000000000-00000.
32. Horak F., Zieglmayer P., Zieglmayer R., Lemell P. The effects of bilastine compared with cetirizine, fexofenadine, and placebo on allergen-induced nasal and ocular symptoms in patients exposed to aeroallergen in the Vienna Challenge Chamber. Inflamm Res. 2010;59(5):391–398. doi: 10.1007/s00011-009-0117-4.
doi: 10.1007/s00011-009-0117-4.
33. Antonijoan R., Coimbra J., García-Gea C., Puntes M., Gich I., Campo C. et al. Comparative efficacy of bilastine, desloratadine and rupatadine in the suppression of wheal and flare response induced by intradermal histamine in healthy volunteers. Curr Med Res Opin. 2017;33(1):129–136. doi: 10.1080/03007995.2016.1240665.
34. Church M.K., Tiongco-Recto M., Ridolo E., Novák Z. Bilastine: a lifetime companion for the treatment of allergies. Curr Med Res Opin. 2020;36(3):445–454. doi: 10.1080/03007995.2019.1681134.
Антигистаминные препараты нового поколения: перечень и обзор
Распространённые пищевые аллергены.Как хорошо подать читателю статью об антигистаминных препаратах? Первым делом нужно заявить, что аллергия — страшная болезнь, которая косит людей миллионами, а лет через тридцать поразит всё население. Потом — сообщить, что у нас и только у нас можно прочесть про эффективные лекарства последнего поколения. Но признаемся сразу: на самом деле всё гораздо сложнее, а последнее поколение не такое уж и последнее. Ниже мы постараемся рассказать об антигистаминных препаратах всё, что только можно впихнуть в небольшую журнальную статью.
Напугать аллергической эпидемией можно, но сложно. Аллергических заболеваний много, их непросто собрать в кучку и подсчитать. Возьмём, к примеру, пыльцу — один из самых распространённых аллергенов. Международное исследование астмы и аллергии у детей, в котором принимали участие почти два миллиона человек из 105 стран, показало, что аллергии на пыльцу подвержены 22% подростков по всему миру. Этот показатель отличается в зависимости от региона: в Африке он составляет 29,5%, в Океании — 39,8%, в Северной Европе — 12,3%. Но эти данные учёные получили не в ходе тестов, а с помощью анкет. Их достоверность зависит от того, ошибались участники исследования или нет. А такое случается — к примеру, исследование, посвящённое аллергии на пенициллин показало, что болезнь обнаруживается только у 22% пациентов, которые на неё жалуются.
С пищевой аллергией тоже не всё так просто. Результаты исследований отличаются, в зависимости от того, какими методами пользовались учёные. Золотым стандартом в диагностике пищевой аллергии считается двойная слепая плацебо-контролируемая пищевая провокационная проба — во время этой процедуры пациент съедает предполагаемый аллерген под присмотром врача. На английском название метода часто сокращают до забавного «ди-би-пи-си-эф-си» — DBPCFC. В 2013 году Европейская академия аллергологии и клинической иммунологии выпустила метаобзор исследований пищевой аллергии. Он показал, что учёные редко проводили DBPCFC, и полагались, в основном, на кожные пробы и анализы IgE, хотя эти методы существенно преувеличивают частоту заболевания. Если верить тому, что говорили сами участники исследований, распространённость пищевой аллергии в Европе составляет 5,9%. Но пищевые пробы показали 0,9% — это примерно в шесть с половиной раз меньше.
Как бы то ни было, тех, кто уже столкнулся с аллергией, статистика не особенно заботит — нужно чем-то лечиться. Желательно, так, чтобы не ощущать сонливости и других «побочек». Все знают, что от аллергии нужно пить антигистаминные препараты, но не всем известно, что ими к тому же лечат язвы, нарколепсию, а в будущем собираются воевать с болезнями Альцгеймера, Паркинсона, шизофренией и эпилепсией. Чтобы понять, как это лекарства одного класса лечат всё подряд и куда бежать аллергику, начнём с самого начала — с гистамина. Вещество, с которым нам предстоит бороться, — что оно делает?
Проще сказать, чего гистамин не делает. Он расширяет кровеносные сосуды («сужает любые») и увеличивает их проницаемость, способствует выделению желудочного сока, вызывает сокращение гладких мышц (в том числе, бронхов) и чесотку. А ещё работает как медиатор в головном мозге: регулирует сон и пробуждение, снижает судорожную активность, влияет на потребление пищи и воды, участвует в регуляции температуры тела и в процессе обучения. И, конечно, контролирует иммунный ответ: аллергический насморк, чихание и непереносимость котиков — это всё он, гистамин.
Как одному веществу удаётся выполнять столько разных функций? Дело в том, что в организме есть четыре типа рецепторов к гистамину, они расположены в разных органах и тканях. В мозге, гладкой мускулатуре, кровеносных сосудах и некоторых других тканях — рецепторы первого типа, h2. В слизистой желудка, гладкой мускулатуре, тканях сердца, хрящевой ткани и т. д. — рецепторы второго типа, h3. h4 «живут», в основном, в центральной нервной системе, например, в базальных ганглиях и гиппокампе, а в небольших количествах их можно найти в сердечно-сосудистой и пищеварительной системе. h5 локализованы в тканях кишечника, костном мозге, лейкоцитах, тимусе, селезёнке и др.
Воздействие гистамина на организм зависит от того, с каким рецептором он свяжется, поэтому для разных задач нужны разные лекарства. Антигистаминные препараты делят на h2-, h3-, h4-, h5-блокаторы. Если вы слышите фразу «антигистаминные препараты последнего (или нового) поколения», речь идёт о h2-блокаторах, которые используются для лечения аллергии. h3-блокаторы на поколения не делят, h4-блокаторы только начинают выходить на рынок, а до появления первых h5-антигистаминов на прилавках ещё далеко. Именно h2-блокаторы (их ещё называют «антагонистами» или «обратными агонистами» — в зависимости от типа) лечат аллергию.
Русская Википедия говорит о четырёх поколениях h2-блокаторов, но это неверно: на самом деле их всего два. Существование «новейших препаратов третьего поколения» — миф, но фармацевтические компании иногда используют этот термин в рекламных целях, а сайты об аллергии с удовольствием пишут на эту тему и вводят читателей в заблуждение. Давайте разберёмся, по какому принципу h2-блокаторы делятся на поколения.
Первые лекарства от аллергии легко преодолевали преграду между кровью и головным мозгом — так называемый гематоэнцефалический барьер (ГЭБ) — и вызывали сонливость. Помните, мы говорили о том, что гистамин регулирует сон и пробуждение? Он стимулирует активность мозга и отвечает за бодрствование — неудивительно, что подавление работы рецепторов в ЦНС производит седативный эффект. Кроме того, антигистамины первого поколения (например, хлоропирамин, известный нам как «Супрастин», и клемастин, который мы знаем под именем «Тавегил») приводят к нарушению памяти и концентрации, снижают способность к обучению и продуктивность. Вдобавок их приходится пить несколько раз в день, а приём на ночь не помогает избежать «побочек» — в общем, первое поколение лекарств было скорее «необходимым злом», чем «счастливым избавлением». Европейский консорциум по изучению аллергических заболеваний и бронхиальной астмы (Global Allergy and Asthma European Network) даже рекомендовал запретить безрецептурную продажу этих препаратов после того, как в 2010 году закончил исследование рисков.
Со временем учёные разработали вещества, которые «перебирались» из крови в мозг в меньших количествах или вовсе не могли этого сделать — их назвали «препаратами второго поколения». Вот они:
- акривастин
- цетиризин
- азеластин
- олопатадин
- лоратадин
- кетотифен
- рупатадин
- мизоластин
- эбастин
- биластин
- бепотастин
- терфенадин
- хифенадин
- левокабастин
- астемизол
Препараты второго поколения не вызывали сонливости в стандартной дозе (а некоторые — даже при значительном её повышении), при этом таблетки хватало на целый день. Но некоторые из них плохо действовали на сердце. У астемизола и терфенадина этот эффект был настолько выражен, что во многих странах их сняли с продажи.
Ещё через несколько лет учёные получили производные (метаболиты и стереоизомеры) препаратов второго поколения, которые, по словам производителей, были более эффективными, не вызывали сонливости и не вредили сердцу. Вот эти лекарства:
- левоцетиризин (торговые наименования «Ксизал», «Гленцет», «Супрастинекс», «Цезера», «Эльцет», «Зодак Экспресс»)
- дезлоратадин («Дезал», «Лоратек», «Лордестин», «Эриус», «Неокларитин»)
- фексофенадин («Аллегра», «Телфаст», «Фексофаст», «Фексадин», «Фексофен»)
Некоторые называли эти вещества «препаратами третьего поколения». Исследователи начали горячо спорить о том, к какому поколению они относятся и на каком, собственно, основании. Чтобы положить конец дискуссиям, в начале 2000-х Британское общество аллергологов и врачей-иммунологов инициировало создание Консенсуса по антигистаминным препаратам нового поколения (Consensus Group on New Generation Antihistamines). 17 экспертов из Соединённого королевства, Италии, Канады, США и Японии определили критерии, которым должны соответствовать препараты третьего поколения:
- отсутствие кардиотоксичности;
- отсутствие взаимодействия с другими препаратами;
- отсутствие влияния на ЦНС.
Специалисты проанализировали данные опубликованных клинических исследований и пришли к выводу, что «препаратом третьего поколения» не может называться ни одно из существующих лекарств. Тем не менее, в некоторых научных работах левоцетиризин, дезлоратадин, фексофенадин и норастемизол до сих пор неофициально так величают. Давайте разберёмся, что это за препараты, какие у них побочные действия, кому можно их принимать, а кому не рекомендуется. Всё познаётся в сравнении, поэтому мы оформили данные в виде таблицы — так проще понять, чем лекарства схожи, а чем отличаются:
| Дози | Начинает действо | Макси | Длите | Распро | Кому нельзя | Кому можно, но осторожно | |
|---|---|---|---|---|---|---|---|
| левоцетиризин — изомер цетиризина | 5 мг | 1 час | 0,9 часов | минимум 24 часа | Сонливость, головная боль, головокружение, сухость во рту, утомляемость, слабость, назофарингит, фарингит, боли в животе, тошнота, повышение температуры | Беременным, кормящим матерям, детям до 6 месяцев (и капли, и таблетки), детям до 6 лет (таблетки, капли уже можно), людям с гиперчувствительностью к левоцетиризину, цетиризину, гидроксизину или другим компонентам препарата, терминальной стадией почечной недостаточности и тем, кто проходит гемодиализ | Пожилым пациентам, больным эпилепсией, людям с заболеваниями почек или склонным к возникновению судорог, а также пациентам с повреждением спинного мозга или предстательной железы, необходимо проконсультироваться с врачом; не рекомендуется совмещать лекарство с алкоголем и другими депрессантами |
| дезлоратадин — метаболит лоратадина | 5 мг | 2 часа | 1—3 часа | минимум 24 часа | Головная боль, сухость во рту, утомляемость, расстройство желудка, сонливость, головокружение, боль в мышцах, дисменорея | Беременным, кормящим матерям, детям до 6 месяцев (и сироп, и таблетки), детям до 12 лет (таблетки, сироп уже можно), людям с гиперчувствительностью к дезлоратадину, лоратадину или другим компонентам препарата | Людям с заболеваниями почек необходимо проконсультироваться с врачом |
| фексофенадин — метаболит терфенадина | 120/180 мг | 2 часа | 2,6 часа | 24 часа | Головная боль, головокружение, сонливость, диарея, тошнота, боль в мышцах, кашель | Беременным, кормящим матерям, детям до 12 лет, людям с гиперчувствительностью к одному из компонентов препарата | Пожилым людям, людям с сердечно-сосудистыми заболеваниями (в том числе, в прошлом), а также тем, у кого нарушена работа печени или почек, необходимо проконсультироваться с врачом |
Если кратко суммировать эти данные: идеального чудо-средства не существует, у каждого есть свои достоинства, недостатки и особенности. Самый быстродействующий препарат — левоцетиризин, но он же производит самый сильный седативный эффект. MedlinePlus, сервис национальной медицинской библиотеки США, на который ссылается FDA, предупреждает потребителей: не спешите садиться за руль, приняв левоцетиризин, сначала выясните, как он на вас действует. Самым «бодрым» считается фексофенадин: это лекарство практически не вызывает сонливости, поэтому его рекомендуют пилотам и тем, кому нужна бдительность и быстрота реакции. Зато фексофенадин может похвастаться самой большой дозировкой — 120 или 180 мг, в то время как другим препаратам хватает 5 мг. А кроме того, его нельзя давать детям младше 12 лет: эффективность и безопасность для них в рамках клинических исследований не проверяли. Самым маленьким аллергикам может подойти левоцетиризин или дезлоратадин (принимают в форме сиропа или капель уже через полгода после рождения), но ни одно из лекарств не рекомендуют беременным и кормящим матерям.
Насколько новые метаболиты и изомеры препаратов второго поколения лучше своих «родителей»? Сложно сказать. Сравнительных клинических испытаний на людях немного, а те, что есть, основаны на маленьких выборках и подчас противоречат друг другу. Терфенадин перестали продавать из-за того, что очень плохо влиял на сердце. Его производное — фексофенадин — практически лишено этого недостатка. А вот дальше начинаются разночтения. Одно исследование утверждает, что новое лекарство подавляет аллергические реакции лучше, чем предшественник — это клиническое испытание спонсировал разработчик фексофенадина, компания Hoechst Marion Roussel. В другой работе сравнивали эффективность нескольких лекарств второго поколения: цетиризина, эбастина, эпинастина, фексофенадина, терфенадина и лоратадина. Выяснилось, что фексофенадин слабее своего предшественника, а лучше всего с аллергией борется цетиризин. Исследование финансировал разработчик цетиризина UCB Pharma.
Работы, в которых сопоставляли эффективность левоцетиризина и цетиризина, показывают, что препараты одинаково действенны или указывают на незначительное преимущество «родительского» вещества. Но нужно учитывать, что левоцетиризин достигает тех же результатов при вдвое меньшей дозе. А вот в том, что касается влияния на центральную нервную систему, новое лекарство, похоже, так и не смогло обогнать предшественника. Учёные проанализировали седативный эффект двух веществ и пришли к выводу, что пациенты, у которых цетиризин вызывает сонливость, вряд ли будут иначе реагировать на его изомер (в этом исследовании выборка тоже была небольшой).
Дезлоратадин, фексофенадин и левоцетиризин нельзя назвать «Антигистаминными препаратами 3.0» — им больше подходит «2+». И всё-таки они вредят сердцу меньше, чем более ранние лекарства второго поколения и не так угнетают ЦНС, как средства из первого. Даже когда участникам клинических испытаний дезлоратадин и левоцетиризин давали в дозах в четыре раза выше нормы, ни у одного из них не появилось настолько серьёзных побочных эффектов, чтобы прекратить лечение. Повторять этот эксперимент на себе не стоит: если вы решили связать свою жизнь с антигистаминными препаратами последнего — второго — поколения, лучше посоветоваться с врачом. Самую достоверную информацию о лекарствах можно найти в официальных инструкциях и Государственном реестре лекарственных средств.
*Внимание! В таблице перечислены не все побочные эффекты! Перед применением любого из препаратов прочтите инструкцию или проконсультируйтесь с врачом (а лучше — и то, и другое).
ФАРМАТЕКА » h2-антигистаминные препараты в педиатрической практике
Гистамин является одним из важнейших биогенных аминов, принимает участие во многих физиологических и патологических процессах в организме человека. В настоящее время известно 4 типа гистаминовых рецепторов. Наибольшаю роль в развитии аллергических реакций принадлежит h2-рецепторам. История антигистаминных препаратов насчитывает около 70 лет. Эти лекарственные средства оказывают противоаллергический и противовоспалительный эффекты. В настоящее время на фармацевтическом рынке представлено достаточно большое количество антигистаминных препаратов, однако не все они могут быть применены в отношении детей до 6-тимесячного возраста. В статье освещены данные о гистаминовых рецепторах и агонистах h2-рецепторов, использующихся в педиатрической практике: типах препаратов, формах выпуска, эффективности, безопасности и применении.
Гистамин – один из важнейших медиаторов, относящийся к биогенным аминам и синтезирующийся из аминокислоты гистидина путем декарбоксилирования в тучных клетках и базофилах. Гистамин принимает участие во многих физиологических и патологических процессах в организме человека.
Действие гистамина осуществляется посредством взаимодействия со специфическими гистаминовыми рецепторами, расположенными на клетках различных тканей. Они относятся к обширному семейству рецепторов, ассоциированных с G-белками (GPCRs – G protein-coupled receptors). Группа GPCRs принимает активное участие в трансмиссии внеклеточных сигналов через клеточную мембрану путем специфического распознавания и связывания разнообразных лигандов, таких как белки, ионы, нейропередатчики и даже световые стимулы (фотоны). GPCRs широко представлены в организме и принимают участие во многих процессах – как физиологических, так и патологических, таких как обоняние, вкус, зрение, когнитивные функции, эмоции, иммунный ответ, в т.ч. аллергия, а также в регуляции деятельности сердечно-сосудистой, нервной, пищеварительной, дыхательной и других систем организма [1].
К настоящему времени описано четыре типа гистаминовых рецепторов (табл. 1), среди которых наиболее изучены h2- и h3-рецепторы.
В развитии аллергии принимают участие в основном h2-гистаминовые рецепторы, однако к настоящему времени накоплены данные о роли h5-гистаминовых рецепторов при иммунопатологических состояниях, в частности при аллергических болезнях [7–9]. Обсуждается возможность применения препаратов, воздействующих на h5-гистаминовые рецепторы при различных заболеваниях, в т.ч. при аллергии [10]. h3-гистаминовые рецепторы также могут участвовать в развитии аллергических проявлений [11, 12].
Интересно, что все GPCRs обладают конститутивной (спонтанной) рецепторной активностью, т.е. их активность проявляется даже в отсутствие агониста и его связи с рецептором [13]. Это наглядно объясняется моделью равновесного состояния рецептора: одновременного существования его спонтанно активных и неактивных форм. Под воздействием различных агентов может происходить нарушение равновесия и смещение в сторону активации (в случае гистаминовых рецепторов – под воздействием гистамина) или, напротив, в сторону неактивного состояния рецептора (при воздействии блокаторов h2-гистаминовых рецепторов). Кроме того, существуют нейтральные агонисты, которые связываются и с активной, и с неактивной формами рецепторов, сохраняя их равновесное состояние. Исходя из вышесказанного, h2-антигистаминные средства, по сути, являются не блокаторами, а обратными агонистами рецепторов, хотя до настоящего времени традиционно сохраняется привычная терминология [1].
Действие гистамина на h2-рецепторы представлено широким разнообразием клинических проявлений:
- со стороны кожи – отек, гиперемия, ощущение зуда, высыпания;
- верхние дыхательные пути – зуд, чихание, отек слизистой оболочки носа и придаточных пазух, увеличение секреции слизи;
- нижние дыхательные пути – отек стенки бронхов, гиперсекреция и бронхоспазм;
- слизистая оболочка глаз – зуд, гиперемия, отек и слезотечение;
- желудочно-кишечный тракт – боли в животе, рвота, диарея, усиление выработки слизи, пепсина и соляной кислоты;
- сердечно-сосудистая система – системная артериальная гипотензия и нарушение сердечного ритма.
Гистамину принадлежит одна из ключевых ролей в развитии таких аллергических заболеваний, как атопический дерматит, аллергический ринит, бронхиальная астма, аллергический конъюнктивит, крапивница, а также системных анафилактических реакций [14].
Активация h2-гистаминовых рецепторов сопровождается активацией фосфолипазы C, D и A2 что в итоге приводит к высвобождению ионов кальция Ca2+ и, соответственно, к активации функции клетки. Кроме того, повышается активность ядерного фактора kB (NF-kB), что сопряжено с продукцией провоспалительных цитокинов и молекул межклеточной адгезии, таких как P-селектин, ICAM-1 (Inter-Cellular Adhesion Molecule 1), VCAM-1 (Vascular cell adhesion molecule 1), iNOS, фактора некроза опухоли α (ФНО-α), гранулоцитарно-макрофагального колониестимулирующего фактора (ГМ-КСФ), интерлейкина-1β (ИЛ-1β), ИЛ-6. Установлено, что NF-kB играет немаловажную роль в активации лимфоцитов; в частности, способствует дифференцировке Т-хелперных клеток 2-го типа, что особенно актуально при аллергических заболеваниях. Повышенный уровень NF-kB обнаруживается у больных различными типами аллергии, в т.ч. бронхиальной астмой [15]. Таким образом, h2-гистаминовые рецепторы не только участвуют в ранней фазе аллергической реакции, но и обладают более широкими иммунологическими свойствами, в т.ч. играют немаловажную роль в развитии поздней фазы аллергического воспаления. Следовательно, противоаллергическое действие антигистаминных препаратов многопланово и включает в т.ч. противовоспалительный эффект [11].
История создания этих лекарственных средств берет начало с 1937 г., когда был синтезирован первый h2-антигистаминный препарат, который не использовался как лекарственное средство ввиду своей токсичности [16]. Клиническое применение антигистаминных средств началось в 1942 г. с препарата антерган, за которым последовали дифенгидрамин (1945), хлорфенирамин, бромфенирамин и прометазин [17]. Восьмидесятые годы двадцатого столетия ознаменовались активным развитием группы антигистаминных средств, включая появление препаратов второй генерации [18].
h2-антигистаминные средства являются препаратами выбора при аллергическом рините, аллергическом конъюнктивите, крапивнице, используются в терапии атопического дерматита, системных аллергических реакций [14, 19, 20].
В настоящее время на фармацевтическом рынке представлено достаточно большое количество h2-антигистаминных средств. Традиционная классификация этих препаратов делит их на две группы: I и II поколений (табл. 2).
Препараты I поколения являются неселективными агонистами h2-гистаминовых рецепторов, нередко проявляя активность в отношении рецепторов других биоактивных аминов, и, соответственно, могут оказывать антихолинергический, анти-α-адренергический и антисеротониновый эффекты. Кроме того, обладая высокой липофильностью, эти препараты хорошо проникают через гематоэнцефалический барьер и взаимодействуют с центральными h2-гистаминовыми рецепторами. Эти свойства обусловливают следующее: h2-антигистаминные средства I поколения часто оказывают седативный эффект (а у ряда больных, напротив, парадоксальное возбуждение), могут вызывать сухость слизистых оболочек, сгущение бронхиального секрета, запор или диарею, тошноту и тахикардию. Хотя надо отметить, что частота подобных эффектов может существенно различаться у разных препаратов и отдельных больных.
Побочные эффекты h2-антиги-стаминных препаратов I поколения могут как носить нежелательный характер, так и быть полезными в ряде клинических ситуаций; например, седация может быть необходимой ряду больных при выраженном кожном зуде. Взаимодействие препаратов с холинергическими рецепторами дополнительно способствует уменьшению зуда и чихания, нередко существенно нарушающих самочувствие больных аллергическим ринитом.
В целях безопасного применения h2-антигистаминных препаратов I поколения врачу следует помнить, что их не следует применять одновременно с антихолинергическими средствами (ингибиторами моноаминооксидазы, синтетическими противосудорожными препаратами, М-холиноблокаторами, нейролептиками, трициклическими антидепрессантами, средствами для лечения паркинсонизма). Соблюдать осторожность больным язвенной болезнью, сердечно-сосудистыми заболеваниями, диабетом, глаукомой [11].
Кроме того, препараты I поколения (клемастин, хлоропирамин) имеют инъекционные лекарственные формы, что делает их незаменимыми при купировании острых аллергических реакций (крапивницы, ангионевротического отека) или для премедикации перед диагностическими и хирургическими вмешательствами [14, 21, 22].
Существенным преимуществом препаратов I поколения остается наличие топических лекарственных форм для интраназального, внутриконъюнктивального и накожного применения (табл. 3).
В настоящее время не рекомендовано широкое использование h2-антигистаминных препаратов I поколения для системного применения, однако их топические формы включены в большинство современных руководств по аллергическому риниту и конъюнктивиту [19, 23]. При применении этих препаратов достигается быстрый (через 15 минут), значимый противоаллергический эффект и практически отсутствуют системные побочные эффекты [21]. Есть исследования, позволяющие предполагать потенциальную противовоспалительную активность топических антигистаминных средств [24].
Единственным h2-антигистамин-ным препаратом накожного применения является диметинден, выпускается он в форме геля и эмульсии, разрешен детям с 1-го месяца. При топическом использовании диметинден проявляет противогистаминное и антикининовое действия, вследствие чего развиваются противозудный и местноанестезирующий эффекты [25]. Таким образом, диметинден можно применять при различных зудящих дерматозах. Вышеперечисленные свойства позволяют использовать накожные формы препарата в лечении солнечных ожогов [26] и при зуде, сопровождающем высыпания при ветряной оспе [27].
Антигистаминные препараты II поколения отличаются селективным воздействием на h2-гистаминовые рецепторы, практически не проникают через гематоэнцефалический барьер, что уменьшает вероятность развития седативного эффекта при их применении. Согласно данным исследований, среди препаратов этой группы при однократном приеме среднетерапевтической дозы связь с центральными h2-гистаминовыми рецепторами менее 0,1 % обнаружена у фексофенадина, при этом в психомоторном тесте эффект этого препарата на ЦНС не отличался от плацебо [28], в то время как цетиризин продемонстрировал связь с h2-гистаминовыми рецепторами в 12,5–25,2 % [29]. Имеются данные, позволяющие предполагать меньшую вероятность развития седативного эффекта у левоцетиризина по сравнению с цетиризином [30] и незначительную – у дезлоратадина [31, 32].
Для антигистаминных препаратов II поколения характерны более высокая аффинность к h2-гистаминовым рецепторам и, соответственно, более длительный эффект по сравнению со средствами I поколения, что позволяет применять большинство из них не чаще одного раза в сутки.
h2-антигистаминные препараты II поколения в настоящее время считаются препаратами выбора при аллергическом рините, крапивнице, других зудящих дерматозах [14, 19, 20, 33–36].
Ряд антигистаминных препаратов проявляет кардиотоксичность: аритмогенную активность вплоть до жизнеугрожающих форм аритмии. В связи с этим во многих странах, в т.ч. и в России, запрещены к применению астемизол и тербинафин. При приеме доз, превышающих среднетерапевтические, удлинение интервала QT на ЭКГ и развитие аритмий возможны у прометазина [37] и дифенгидрамина [38].
Многие антигистаминные средства метаболизируются в печени с участием цитохрома P450, в связи с чем не рекомендован их одновременный прием с ингибиторами этого фермента: ряд противогрибковых препаратов (итраконазол, кетоконазол), многие макролиды, некоторые антидепрессанты, циметидин и др. [11] Печеночному метаболизму не подвергаются цетиризин и левоцетиризин [39]¸ минимально – фексофенадин [40].
Немаловажное значение в педиатрической практике имеет наличие специальных детских лекарственных форм и возраст-разрешенный диапазон применения препаратов.
В настоящее время в России ни один h2-антигистаминный препарат II поколения не разрешен к применению детьми до 6 месяцев. В этой возрастной категории врач может назначать лишь диметинден и хлоропирамин (с 1 месяца), при этом детская лекарственная форма для перорального применения (капли) есть только у диметиндена. Другие препараты, использующиеся в более старшем возрасте и имеющие детские лекарственные формы, включают цетиризин (капли, сироп), ципрогептадин (сироп), левоцетиризин (капли), лоратадин (сироп, суспензия) и дезлоратадин (сироп).
Таким образом, h2-антигистаминные средства в настоящее время представлены широкой линейкой препаратов, которые могут быть использованы в педиатрической практике с учетом возраста ребенка, типа заболевания, особенностей преморбидного фона и сопутствующей патологии.
Л.Р. Селимзянова – к.м.н., с.н.с. отдела стандартизации и клинической фармакологии ФГБУ НЦЗД РАМН, ассистент кафедры педиатрии и детской ревматологии ГБОУ ВПО Первый МГМУ им. И.М. Сеченова Минздрава России
Е.А. Вишнева – к.м.н., ведущий научный сотрудник отдела стандартизации и клинической фармакологии ФГБУ НЦЗД РАМН
Е.А. Промыслова – научный сотрудник отдела стандартизации и клинической фармакологии ФГБУ НЦЗД РАМН
АСТЕМИЗОЛ-ЛХФЗ.Эффективный отечественный антигистаминный препарат второго поколения
В отечественной медицинской практике уже на протяжении многих лет для лечения аллергических заболеваний используют антигистаминные препараты І поколения — клемастин, мебгидролин, хлоропирамин, дифенгидрамин и др. Однако практически все блокаторы Н1-гистаминовых рецепторов I поколения наряду с воздействием на гистаминовые рецепторы оказывают влияние на холинергические рецепторы, а также проникают через гематоэнцефалический барьер. В связи с этим в ряде случаев они снижают способность к концентрации внимания, вызывают сонливость, сухость слизистой оболочки полости рта, носа и горла, нарушение мочеиспускания и ухудшение зрения. Антигистаминные препараты І поколения не рекомендуется амбулаторно назначать лицам, работа которых требует повышенного внимания (водители, операторы сложных механизмов и т.д.).
Антигистаминные препараты ІІ поколения практически лишены этих недостатков благодаря их высокой избирательной активности в отношении Н1-рецепторов. Одним из представителей антигистаминных препаратов ІІ поколения является АСТЕМИЗОЛ–ЛХФЗ (астемизол) производства ОАО «Луганский ХФЗ».
АСТЕМИЗОЛ-ЛХФЗ — сильнодействующий селективный блокатор Н1-гистаминовых рецепторов ІІ поколения. Препарат действует длительно, не оказывает влияния на ЦНС и холинергические рецепторы. Однократный прием данного лекарственного средства полностью обеспечивает противоаллергический эффект в течение 24 ч. АСТЕМИЗОЛ-ЛХФЗ быстро и хорошо всасывается в пищеварительном тракте. Максимальная концентрация в плазме крови достигается через 1–2 ч после приема внутрь. В печени препарат превращается в десметиластемизол. Период полувыведения астемизола составляет 1–2 дня, а его основного метаболита — 9–13 дней. Астемизол не проникает через гематоэнцефалический барьер, выводится в основном в виде метаболитов с желчью. Не связывается с мускариновыми и дофаминовыми рецепторами, обладает слабой антисеротониновой активностью, не оказывает седативного действия, не потенцирует действия снотворных и седативных средств, анальгетиков. Отличается высокой активностью и длительностью действия.
АСТЕМИЗОЛ-ЛХФЗ показан для лечения аллергических ринитов (сезонного и хронического), конъюнктивита, крапивницы и других аллергических заболеваний. Препарат рекомендуется принимать внутрь по 1 таблетке (0,01 г) в сутки. Курс лечения в среднем составляет 3–4 нед. При необходимости его можно продлить.
Противопоказанием к применению АСТЕМИЗОЛА-ЛХФЗ является период беременности и кормления грудью, повышенная чувствительность к препарату. Следует избегать применения препарата у пациентов с тяжелыми заболеваниями печени. У лиц с предрасположенностью к удлинению интервала Q–T после применения АСТЕМИЗОЛА-ЛХФЗ на ЭКГ может отмечаться его удлинение, а также нарушения ритма сердца. Поэтому АСТЕМИЗОЛ-ЛХФЗ не следует назначать пациентам с удлиненным интервалом Q–T, а также с признаками гипокалиемии.
При строгом соблюдении рекомендуемых доз АСТЕМИЗОЛ-ЛХФЗ хорошо переносится. Препарат не потенцирует действие алкоголя. Не рекомендуется одновременно принимать астемизол и кетоконазол.
В 1998 г. в Украинской фармацевтической академии (сейчас — Национальная фармацевтическая академия Украины) подrel=»nofollow»> руководством доктора медицинских наук, профессора С.Б. Попова было проведено сравнительное исследование клинической эффективности препаратов АСТЕМИЗОЛ-ЛХФЗ и Астемизол (астемизол) компании «ICN Polfa Rzeszow» (препарат сравнения). В исследовании принимали участие 45 больных с аллергическими дерматозами и отеком Квинке, 30 из которых получали АСТЕМИЗОЛ–ЛХФЗ, 15 — препарат сравнения (оба — в дозе 10 мг 1 раз в сутки) на протяжении 5–7 дней. Степень клинических проявлений заболевания оценивали на основании выраженности объективных и субъективных симптомов (заложенность носа, ринорея, чиханье, слезотечение и т.д.) по 4-балльной шкале (0 баллов — симптомы отсутствуют, 1 балл — симптомы незначительно выражены, 2 балла — симптомы средней степени выраженности, 3 балла — тяжелой степени выраженности).
Под влиянием указанных препаратов уменьшалась выраженность клинических проявлений аллергии — кожного зуда, гиперемии, крапивницы и т.д. Терапевтический эффект был отмечен уже к концу 1-х суток. Исчезновение симптомов аллергии происходило в такой последовательности: к концу 1-х суток существенно уменьшалась выраженность кожного зуда, на 2-е сутки зуд исчезал практически у всех больных, гиперемия исчезала на 3-и сутки, элементы кожной сыпи — на 3–5-е сутки. Полный клинический эффект отмечался к концу 6-х суток лечения. В табл. 1 представлены данные о динамике клинических проявлений аллергии под влиянием лечения АСТЕМИЗОЛОМ-ЛХФЗ и препаратом сравнения. Оба лекарственных средства одинаково эффективно устраняют такие симптомы, как заложенность носа, ринорея, чиханье, зуд в носу и т.д.
Таблица 1 Динамика клинических проявлений аллергии под влиянием лечения АСТЕМИЗОЛОМ-ЛХФЗ и препаратом сравнения (в баллах) |
Симптом | До лечения | После лечения | |
АСТЕМИЗОЛОМ-ЛХФЗ | препаратом сравнения | ||
| Заложен-ность носа | 2,66±0,06 | 1,13±0,08* | 1,23±0,07* |
| Ринорея | 2,64±0,04 | 0,78±0,05* | 0,76±0,05* |
| Чиханье | 2,52±0,03 | 1,45±0,06* | 1,58±0,04* |
| Зуд в носу | 2,33±0,03 | 0,34±0,04* | 0,44±0,05* |
| * Достоверные изменения по отношению к группе контроля до лечения. |
АСТЕМИЗОЛ-ЛХФЗ и препарат сравнения в целом не вызывали существенных изменений показателей общего клинического анализа крови, за исключением достоверного уменьшения СОЭ и количества эозинофилов, которые играют важную роль в патогенезе аллергии (табл. 2).
Таблица 2 Влияние лечения с использованием АСТЕМИЗОЛА-ЛХФЗ и препарата сравнения на показатели общего клинического анализа крови |
Показатель | До лечения | После лечения | |
АСТЕМИЗОЛОМ-ЛХФЗ | препаратом сравнения | ||
| Эритроциты, • 1012/л | 4,52±0,16 | 4,43±0,30 | 4,44±0,12 |
| Гемоглобин, г/л | 124,9±2,1 | 126,1±3,2 | 124,3±3,4 |
| Цветовой показатель | 0,92±0,02 | 0,93±0,01 | 0,92±0,04 |
| Лейкоциты, • 109/л | 7,58±0,17 | 6,49±1,12 | 6,41±1,26 |
| Палочкоядерные, % | 2,49±0,02 | 2,46±0,04 | 2,71±0,02 |
| Сегментоядерные, % | 62,3±0,88 | 64,7±0,59 | 65,3±0,46 |
| Моноциты, % | 5,1±0,03 | 5,2±0,04 | 5,5±0,09 |
| Лимфоциты, % | 18,4±1,09 | 18,7±1,12 | 18,1±1,22 |
| Эозинофилы, % | 7,89±0,04 | 3,34±0,06* | 3,45±0,04* |
| Тромбоциты, • 109/л | 209,4±4,5 | 205,2±2,4 | 208,2±2,0 |
| СОЭ, мм/ч | 15,9±0,13 | 8,90±0,33* | 9,20±0,28* |
| * Достоверные изменения по отношению к группе контроля до лечения. |
Существенного влияния АСТЕМИЗОЛА-ЛХФЗ на некоторые печеночные пробы — активность аланинаминотрансферазы и аспартатаминотрансферазы, уровень общего белка, а также на концентрацию общего холестерина в крови не зафиксировано.
При применении астемизола возможно возникновение побочных реакций, проявляющихся парестезиями, миалгиями, артралгиями и расстройством сна. В процессе проведения клинических исследований на 4–5-е сутки отмечено по одному случаю возникновения бессонницы в группах пациентов, которые принимали АСТЕМИЗОЛ-ЛХФЗ и препарат сравнения. При этом пациенты предъявляли жалобы на бессонницу до лечения астемизолом, в связи с чем ее не расценивали как побочный эффект. Случаев выраженного побочного действия и непереносимости астемизола не выявлено.
На основании результатов клинического исследования проведена суммарная оценка эффективности сравниваемых препаратов, которая показала, что клиническая эффективность АСТЕМИЗОЛА–ЛХФЗ составляет почти 90% и практически не отличается от таковой препарата сравнения.
Таким образом, АСТЕМИЗОЛ-ЛХФЗ — современное антигистаминное средство ІІ поколения, эффективно устраняющее симптомы аллергии.
Публикация подготовлена по материалам,
предоставленным ОАО «Луганский ХФЗ»
ТЕЛФАСТ: с антигистаминным препаратом третьего поколения — в третье тысячелетие
Антигистаминные препараты нашли широкое применение в клинической практике. Однако использование лекарственных средств этой группы ограничивается определенными неблагоприятными воздействиями — седативным эффектом (препараты первого поколения в терапевтических дозах, второго поколения в высоких дозах) и кардиотоксическим влиянием (препараты второго поколения). В 1996 г. на рынке США появился первый представитель антигистаминных препаратов третьего поколения — АЛЛЕГРА / ТЕЛФАСТ (фексофенадин), который является оригинальным препаратом компании «Авентис Фарма». В 2000 г. объем продаж препарата АЛЛЕГРА / ТЕЛФАСТ в мире составил 1,166 млрд евро. Эксперты прогнозируют дальнейшее увеличение объема продаж этого препарата, который сегодня представлен на основных фармацевтических рынках мира. Недавно фексофенадин производства компании «Авентис Фарма» появился и в Украине под торговым названием ТЕЛФАСТ.
Спектр практического применения антигистаминных препаратов, которые уменьшают выраженность неблагоприятных реакций, вызванных гиперпродукцией гистамина, довольно широк. Клиницистами накоплен значительный опыт применения данных препаратов, поскольку первые из них появились на мировом фармацевтическом рынке еще в 40-е годы ХХ в. Установлено, что наряду с выраженным терапевтическим эффектом антигистаминные препараты первого поколения (фенирамин, клемастин, хлорфенирамин, ципрогептадин, прометазин, гидроксизин) имеют ряд существенных недостатков, обусловленных их проникновением через гематоэнцефалический барьер с последующим воздействием на Н3-рецепторы, что клинически проявляется седативным эффектом, сонливостью, ухудшением психомоторной функции, повышением аппетита, увеличением массы тела, дисфункцией пищеварительного тракта, нарушением зрения и др. В связи с этим прием данных препаратов противопоказан лицам, работа которых требует повышенного внимания: водителям, пилотам и др. Седативный эффект усиливается под действием алкоголя и других веществ, угнетающих ЦНС (например, транквилизаторов). Кроме того, многие антигистаминные препараты первого поколения обладают антихолинергической активностью, что может привести к возникновению таких побочных эффектов, как ощущение сухости во рту, нарушение мочеиспускания, импотенция и др.
В начале 80-х годов появились первые антигистаминные препараты второго поколения (терфенадин, астемизол, лоратадин, цетиризин), которые по антиаллергической активности были сопоставимы с препаратами первого поколения, но не оказывали седативного эффекта в стандартных дозах. В научной литературе имеются сообщения о том, что при определенных условиях антигистаминные препараты второго поколения (астемизол, терфенадин) способны вызывать нарушения ритма сердца, в частности желудочковые аритмии, причем в некоторых случаях — фатальные вследствие блокирования ионных каналов, которые контролируют реполяризацию миокарда. В 1990 г. Управление по контролю за пищевыми продуктами и лекарственными препаратами США (FDA) организовало специальное заседание Комитета экспертов по легочным и антиаллергическим препаратам с целью проанализировать более 20 случаев серьезных нарушений ритма, связанных с применением антигистаминных препаратов. В результате на упаковке одного из представителей антигистаминных препаратов второго поколения — терфенадина — появилось предостережение об указанном побочном эффекте, а возможность безрецептурного применения этого лекарственного средства была подвергнута сомнению. После того как на рынке США появился антигистаминный препарат третьего поколения АЛЛЕГРА / ТЕЛФАСТ, FDA в 1997 г. потребовало запрещения применения терфенадина.
Необходимо отметить, что терапевтический эффект терфенадина практически полностью обусловлен его активным метаболитом — фексофенадином. При нарушении функции печени метаболизм терфенадина замедляется, вследствие чего концентрация неизмененного препарата в крови повышается. Накапливаясь, терфенадин отрицательно воздействует на проводимость миокарда.
В связи с этим ученые пошли по пути создания нового лекарственного препарата третьего поколения на основе активного метаболита терфенадина — фексофенадина, который избирательно связывается с периферическими Н1-рецепторами, не проникает через гематоэнцефалический барьер и не оказывает кардиотоксического действия даже при назначении в высоких дозах.
ТЕЛФАСТ (фексофенадин) — препарат на основе активного карбоксилированного метаболита терфенадина был зарегистрирован в США в июле 1996 г. после клинических исследований, продолжавшихся всего около 2 лет (от начала клинических исследований до подачи заявки на регистрацию). Когда стало ясно, что фексофенадин практически не влияет на электрофизиологию сердца, то по предложению FDA данный препарат был зарегистрирован как более безопасная альтернатива терфенадину. С появлением ТЕЛФАСТА повысились требования FDA к безопасности антигистаминных средств. С этого времени прилагаются усилия к созданию лекарственных препаратов на основе активных метаболитов антигистаминных препаратов второго поколения, что позволяет полностью избежать нежелательных побочных эффектов.
ТЕЛФАСТ быстро всасывается после приема внутрь. Максимальная его концентрация в крови достигается через 1–3 ч, эффект длится около 24 ч. При этом 60–70% препарата связывается с белками плазмы крови, не подвергается биотрансформации в печени и выводится в практически неизмененном виде. Это позволяет достигать предсказуемых уровней фексофенадина в плазме крови и ограничивать пределы индивидуальных колебаний его концентрации даже при сниженной функции печени. ТЕЛФАСТ не оказывает существенного влияния на калиевые каналы кардиомиоцитов и не вызывает удлинения интервала Q—T при применении в дозах, которые в 10 раз превышают стандартную терапевтическую дозу — 120 мг/сут. Прочное связывание с Н1-рецепторами, а также белками плазмы крови обеспечивает пролонгированное действие препарата, поэтому ТЕЛФАСТ целесообразно принимать в дозе 120 или 180 мг 1 раз в сутки.
Как уже было отмечено ранее, ТЕЛФАСТ не проникает через гематоэнцефалический барьер и поэтому не оказывает седативного эффекта. В отличие от препаратов первого и второго поколения ТЕЛФАСТ можно назначать лицам, работа которых требует повышенного внимания (водителям, операторам сложных механизмов и др.). Более того, в США, Великобритании, Австралии и Бразилии ТЕЛФАСТ официально разрешено принимать даже летчикам.
Поскольку фексофенадин не подвергается биотрансформации в печени, он не взаимодействует с другими лекарственными средствами, которые метаболизируются в этом органе (например, эритромицином и кетоконазолом).
При проведении клинических испытаний частота побочных эффектов (головная боль, сонливость, тошнота, головокружение и усталость) при приеме ТЕЛФАСТА была аналогична таковой при приеме плацебо. Недавно в Оклахомском университете (США) завершилось клиническое испытание, результаты которого свидетельствуют о полной безопасности применения фексофенадина у детей.
ТЕЛФАСТ выпускается в форме таблеток, покрытых оболочкой, содержащих 120 и 180 мг фексофенадина. Единственным противопоказанием к его назначению является гиперчувствительность к компонентам, входящим в состав препарата.
Таким образом, на смену антигистаминным препаратам первого и второго поколения, при применении которых только в организме пациента образуются селективные антагонисты Н1-рецепторов и ряд других побочных продуктов, пришел представитель третьего поколения —ТЕЛФАСТ компании «Авентис Фарма» на основе активного компонента терфенадина — фексофенадина. Благодаря этому ТЕЛФАСТ является эффективным противоаллергическим препаратом, не оказывающим седативного, кардиотоксического, а также других побочных действий даже при применении в высоких дозах. Поскольку фексофенадин поступает в организм в «готовой» для связывания с Н1-рецепторами форме, его действие при пероральном применении проявляется сразу же после всасывания в кровь принятого внутрь препарата. ТЕЛФАСТ прост и безопасен в применении, обладает пролонгированным действием, в связи с чем его можно назначать в дозе 120 или 180 мг один раз в сутки.
|
Клиническая больница №122 имени Л.Г.Соколова Федерального Медико-Биологического Агентства
18.06.2021 График работы call-центра
Call-центр ФГБУ СЗОНКЦ им. Л.Г. Соколова ФМБА России продолжает работать по сокращенному графику
16.06.2021 Работаем в обычном режиме
Уважаемые
пациенты! Сообщаем вам, что стационар, Центральная поликлиника, а также филиал
№ 2 на ул.Красина, д.4 продолжают работать в обычном режиме!
11.06.2021 Расписание работы call-центра на ближайшие дни
Уважаемые пациенты, просим ознакомиться с расписанием работы call-центра на ближайшие дни!
09.06.2021 Благодарность за вклад в охрану здоровья
Сегодня генеральный директор ФГБУ СЗОНКЦ им.Л.Г.Соколова ФМБА России В.М.Колабутин и заместитель генерального директора — медицинский директор В.А.Ратников получили благодарность Законодательного собрания Санкт-Петербурга
07.06.2021 Инфекционное поражение скелета
Организм человека устроен таким образом, что при определенных обстоятельствах натурально сам себя убивает. Как это происходит и можно ли предупредить трагедию — в эксклюзивном интервью 5-tv.ru рассказал кандидат медицинских наук, врач травматолог-ортопед высшей категории Александр Кравцов
25.05.2021 Конгресс Радиология-2021
Сотрудники ФГБУ СЗОНКЦ им. Л.Г. Соколова ФМБА России приняли участие в юбилейном конгрессе Радиология-2021
21.05.2021 Второе мнение врача-проктолога
В настоящее время имеется большое разнообразие способов и методов
лечения заболеваний прямой кишки и перианальной области. Не всегда возможно
получить полную информацию о способе лечения того или иного заболевания и альтернативных
методах, которые зачастую могут быть не менее эффективными и стоить намного
меньше. Предлагаем вам получить второе мнение врача-проктолога
21.05.2021 Реабилитация после COVID-19
Специалистами ФГБУ «СЗОНКЦ им.Л.Г.Соколова ФМБА России» разработан ряд лечебных программ, направленных на эффективное восстановление здоровья пациентов, перенесших новую коронавирусную инфекцию. Читайте в этой новости подробности о восстановительном лечении
20.05.2021 Клещевой энцефалит. Общая информация и профилактика
Весна вступает в свои права, не за горами лето, а значит, наступает сезон выездов горожан на дачные участки и в лесные зоны отдыха.
Эпидемиологи ФГБУ СЗОНКЦ им. Л.Г. Соколова ФМБА России просят внимательно ознакомиться с информацией о том, как постараться избежать укусов клещей, как профилактировать заболевания, которые переносят клещи и что делать, если клещ вас все-таки укусил.
20.05.2021 ВМП по профилю «Сердечно-сосудистая хирургия»
ФГБУ СЗОНКЦ им. Л.Г. Соколова ФМБА России в 2021 году
оказывает высокотехнологичную медицинскую помощь по профилю «сердечно-сосудистая хирургия»
17.05.2021 Пластическая хирургия амбулаторно. Новые услуги
В Хирургическом отделении Центральной
поликлиники ФГБУ СЗОНКЦ им. Л.Г. Соколова ФМБА
России квалифицированными и опытными хирургами проводится
консультативный прием и выполнение хирургических вмешательств по профилю пластическая хирургия
04.05.2021 Сосудистые хирурги работают по профилю!
Центр сосудистой хирургии ФГБУ СЗОНКЦ им. Л.Г. Соколова ФМБА России вновь оказывает плановую и экстренную оперативную и консервативную помощь пациентам с различными заболеваниями артерий и вен
03.05.2021 Перфузионная сцинтиграфия легких
Отделение радиоизотопной диагностики возобновляет выполнение перфузионной сцинтиграфии легких
29.04.2021 Брахитерапия
ФГБУ «СЗОНКЦ им. Л.Г. Соколова ФМБА России» в 2021 году оказывает высокотехнологичную медицинскую помощь по профилю: брахитерапия при локализованном раке
предстательной железы.
28.04.2021 Оздоровительная озонокислородная терапия
В Дневном стационаре Центральной поликлиники проводятся оздоровительные сеансы общей озонокислородной терапии после перенесенной Ковид-инфекции и при общих заболеваниях.
26.04.2021 Хирургическое лечение ожирения
На фоне соблюдения диеты, физической нагрузки, фармакотерапии только около 10% больных ожирением могут достичь желаемого результата лечения, но и в этом случае результат может быть не стойким. Через некоторое время вес возвращается.
26.04.2021 Доступна оплата услуг в режиме онлайн
Напоминаем, что для удобства наших пациентов создана система, позволяющая оплатить услуги, оказываемые в ФГБУ СЗОНКЦ им. Л.Г. Соколова ФМБА России в онлайн-режиме, теперь для оплаты услуг не требуется стоять в очереди!
20.04.2021 Лечение грыж живота без госпитализации и общего наркоза
Современные
миниинвазивные хирургические технологии позволяют устранить без госпитализации большинство неосложненных
пупочных, паховых или бедренных грыж . С использованием современных сетчатых имплантов
возможности стационарозамещающих технологий в этом направлении хирургии
значительно расширились
14.04.2021 Анкета для оценки качества условий оказания услуг медицинскими организациями
Уважаемые пациенты! Просим вас уделить немного времени на заполнение анкеты, это поможет нам повысить качество оказания медицинских услуг в нашем учреждении
13.04.2021 Кабинет экстракорпоральной гемокоррекции
ФГБУ СЗОНКЦ им. Л.Г. Соколова ФМБА России информирует о том, что в составе отделения трансфузиологии клиники работает Кабинет экстракорпоральной гемокоррекции (КЭГ), где проводится комплексное лечение методами эфферентной терапии (экстракорпоральной гемокоррекции) в амбулаторном и стационарном режимах.
Новости 1 — 20 из 1059
Начало | Пред. | 1 2 3 4 5 | След. | Конец | Все
антигистаминных препаратов 2-го поколения | Лекарства, безрецептурные препараты и травы
О медицинских препаратах и болезнях
Клинический справочникMedscape — это самый авторитетный и доступный медицинский справочник для врачей и медицинских работников, доступный в Интернете и на всех основных мобильных устройствах. Все материалы бесплатны.
Клиническая информация отражает опыт и практические знания ведущих врачей и фармацевтов из ведущих академических медицинских центров США и всего мира.
Темы являются всеобъемлющими и охватывают более 30 медицинских специальностей, включая:
Заболевания и состоянияБолее 6000 научно обоснованных и проверенных врачами статей о болезнях и состояниях организованы для быстрого и исчерпывающего ответа на клинические вопросы и предоставления подробной информации в поддержку постановки диагноза, лечения и принятия других клинических решений. Темы богато иллюстрированы более чем 40 000 клинических фотографий, видео, диаграмм и рентгенографических изображений.
ПроцедурыБолее 1000 статей о клинических процедурах содержат четкие пошаговые инструкции и включают обучающие видеоролики и изображения, позволяющие клиницистам освоить новейшие методы или улучшить свои навыки в процедурах, которые они выполняли ранее.
АнатомияБолее 100 статей по анатомии содержат клинические изображения и схемы основных систем и органов человеческого тела. Статьи помогают понять анатомию, связанную с лечением определенных состояний и выполнением процедур.Они также могут облегчить беседы между врачом и пациентом.
Монографии по лекарствамПредоставлено более 7100 монографий по рецептурным и безрецептурным лекарствам, а также по соответствующим фирменным лекарствам, травам и добавкам. Также включены изображения наркотиков.
Средство проверки взаимодействия с наркотикамиНаша программа проверки взаимодействия с лекарственными препаратами обеспечивает быстрый доступ к десяткам тысяч взаимодействий между фирменными и непатентованными лекарствами, лекарствами, отпускаемыми без рецепта, и добавками.Относитесь к умеренным взаимодействиям с серьезными противопоказаниями для одновременного приема до 30 лекарств, трав и добавок.
Формулярная информацияПолучите доступ к справочной информации по лекарственным препаратам в рамках плана медицинского страхования при поиске конкретного лекарства и сэкономьте время и силы для вас и вашего пациента. Выберите из нашего полного списка из более чем 1800 планов страхования во всех 50 штатах США. Настройте свою учетную запись Medscape с учетом планов медицинского страхования, которые вы принимаете, чтобы необходимая вам информация сохранялась и была готова каждый раз, когда вы ищите лекарство на нашем сайте или в приложении Medscape.Легко сравнивайте статус уровней препаратов одного класса при выборе альтернативного препарата для вашего пациента.
Медицинские калькуляторыMedscape Reference содержит 129 медицинских калькуляторов, охватывающих формулы, весы и классификации. Кроме того, в нашем справочнике по лекарствам есть более 600 монографий по лекарственным препаратам, в которых есть встроенные калькуляторы дозирования.
Коллекции изображенийСотни слайд-шоу с богатыми изображениями визуально привлекают и бросают вызов читателям, расширяя их знания как об общих, так и о необычных заболеваниях, презентациях клинических случаев и текущих противоречиях в медицине.
MEDLINEЩелкните ссылки по темам о лекарствах и заболеваниях в нашем клиническом справочнике, чтобы просмотреть клинические данные в MEDLINE. Кроме того, поищите в базе данных MEDLINE журнальные статьи.
Medscape — ведущее онлайн-направление для медицинских работников, ищущих клиническую информацию. В дополнение к клиническим справочным инструментам Medscape предлагает:
Новости медицины Узнать большеДополнительное медицинское образование Узнать больше
Антигистаминные препараты — AMBOSS
Последнее обновление: 9 марта 2021 г.
Резюме
Гистамин — это биологически активное вещество, которое усиливает воспалительные и иммунные реакции организма, регулирует физиологические функции кишечника и действует как нейротрансмиттер.Антигистаминные препараты — это препараты, которые противодействуют этим эффектам, блокируя или ингибируя гистаминовые рецепторы (H-рецепторы). Они классифицируются как h2 или h3 в зависимости от типа нацеленного на H-рецептор. h2-антигистаминные препараты в основном используются для лечения аллергических реакций и заболеваний, опосредованных тучными клетками. Этот подтип делится на два поколения. В то время как антигистаминные препараты первого поколения имеют центральное действие и, таким образом, также используются в качестве седативных средств, антигистаминные препараты второго поколения имеют меньшее центральное действие и используются в основном как противоаллергические препараты.Антигистаминные препараты h3 показаны в первую очередь при желудочном рефлюксе, поскольку они снижают выработку желудочной кислоты за счет обратимого блокирования гистаминовых рецепторов h3 в париетальных клетках слизистой оболочки желудка. Большинство антигистаминных препаратов h2 и h3 противопоказаны во время беременности и детства. Н2-антигистаминные препараты первого поколения особенно противопоказаны при закрытоугольной глаукоме и стенозе привратника.
Обзор
Антигистаминные препараты
Действие антигистаминных средств
[1]Ссылки: [2]
H2-антигистаминные препараты
Примеры
- Антигистаминные препараты первого поколения
- Антигистаминные препараты второго поколения
- Лоратадин
- Дезлоратадин
- Цетиризин
- Левоцетиризин
- Азеластин
- Фексофенадин
Общая физиология
Эффекты
Побочные эффекты
- Седативный эффект (значительно менее выраженный у антигистаминных препаратов второго поколения из-за их ограниченной активности ЦНС)
- Антихолинергические эффекты, например.g., сухость во рту и глазах, мидриаз, задержка мочи, тахикардия, головокружение, шум в ушах (в основном с антигистаминными препаратами первого поколения)
- Анти-α-адренергические эффекты, например, постуральная гипотензия (может привести к падению), увеличение веса
- Головные боли
Показания
Антигистаминные препараты неэффективны при острых наследственных приступах ангионевротического отека. [3]
Противопоказания
Ссылки: [2]
Антигистаминные препараты h3
Примеры
- Ранитидин [4]
- Фамотидин
- Низатидин
Общая физиология
Эффекты
Конкурентный, обратимый антагонизм гистаминовых рецепторов h3 (G s рецептор, связанный с белком) на париетальные клетки → ↓ активность аденилилциклазы → уровни ↓ ↓ ↓ ЦАМФиназы → ↓ Активность → ↓ фосфорилирование и активация H + / K + АТФаза → ↓ секреция желудочной кислоты (H + )
Побочные эффекты
Показания
Относительные противопоказания
Выпить стакан H 2 O перед ужином: блокаторы h3 нужно принимать перед ужином.
Каталожные номера: [2]
Ссылки
- Nzeako UC. Наследственный ангионевротический отек. Arch Intern Med . 2001; 161 (20): с.2417. DOI: 10.1001 / archinte.161.20.2417. | Открыть в режиме чтения QxMD
- Кацунг Б., Тревор А. Фундаментальная и клиническая фармакология . McGraw-Hill Education ; 2014 г.
- FDA требует удаления с рынка всех продуктов с ранитидином (Zantac). https://www.fda.gov/news-events/press-announcements/fda-requests-removal-all-ranitidine-products-zantac-market . Обновлено: 1 апреля 2020 г. Дата обращения: 15 декабря 2020 г.
- Оздемир П.Г. и соавт. Оценка влияния антигистаминных препаратов на настроение, качество сна, сонливость и беспокойство во сне. Международный журнал психиатрии в клинической практике . 2014; 18 (3): с.161-168. DOI: 10.3109 / 13651501.2014.9. | Открыть в режиме чтения QxMD
Вариантное влияние антигистаминных препаратов первого и второго поколения как ключ к разгадке механизма их действия на рефлекс чихания при простуде | Клинические инфекционные болезни
Абстракция
Лечение антигистаминными препаратами первого поколения уменьшает чихание, ринорею, массу носовой слизи и, в некоторых случаях, кашель у субъектов с экспериментальной или естественной простудой; однако лечение антигистаминными препаратами второго поколения не было эффективным при этих жалобах в испытаниях с участием субъектов с естественной простудой.В этой статье сообщается об отрицательных результатах клинического исследования лоратадина, антигистаминного препарата второго поколения, у взрослых на модели заражения риновирусом. Это открытие в строго контролируемых условиях модели заражения подтверждает более ранние отрицательные исследования антигистаминных препаратов второго поколения при естественных простудных заболеваниях. Антигистаминные препараты первого поколения блокируют как гистаминовые, так и мускариновые рецепторы, а также преодолевают гематоэнцефалический барьер. Антигистаминные препараты второго поколения в основном блокируют гистаминовые рецепторы и не проникают через гематоэнцефалический барьер.Эффективность антигистаминных препаратов первого поколения в блокировании чихания при простуде может быть связана в первую очередь с нейрофармакологическими манипуляциями с гистаминовыми и мускариновыми рецепторами в продолговатом мозге.
Индивидуальные симптомы простуды обусловлены множественными и в некоторой степени специфическими путями воспаления [1]. Считается, что чихание является результатом высвобождения гистамина из тучных клеток носа и базофилов, которые активируются вирусной инфекцией простуды. Это мнение подтверждается данными о том, что интраназальное введение гистамина у нормальных добровольцев вызывало чихание, тогда как интраназальное воздействие других медиаторов — нет [2].Кроме того, лечение антигистаминными препаратами первого поколения очень эффективно для уменьшения чихания у пациентов с экспериментальной и естественной простудой [3–5]. Поэтому удивительно, что, в отличие от аллергического ринита, у пациентов с простудой не повышается уровень гистамина в носовых секретах [6–9], хотя сообщается о повышении чувствительности слизистой оболочки носа к гистамину [10–13].
Антигистаминные препараты первого и второго поколения являются конкурентными антагонистами гистамина на участке h2-рецептора [14].Дополнительной фармакологической активностью антигистаминных препаратов первого, но не второго поколения, является конкурентный антагонизм ацетилхолина в отношении нейрональных и нервно-мышечных мускариновых рецепторов. Антигистаминные препараты первого поколения также проникают через гематоэнцефалический барьер и, таким образом, обладают потенциалом активности в головном мозге; антигистаминные препараты второго поколения — нет. При ограниченном тестировании и несмотря на их активность по блокированию H2, антигистаминные препараты второго поколения оказались неэффективными в подавлении чихания у пациентов с естественной простудой [15–18].
Эти данные поднимают интересный вопрос о механизме действия антигистаминных препаратов первого поколения на уменьшение чихания у пациентов с простудой и о неэффективности антигистаминных препаратов второго поколения в этой ситуации. Кроме того, исследования естественного холода связаны с определенными техническими проблемами, такими как трудности с включением пациентов на ранних стадиях простуды, когда эффективность лечения измеряется наиболее точно [19]. Поэтому было бы желательно подтвердить результаты исследований естественного холода путем тестирования антигистаминного препарата второго поколения на модели заражения риновирусом, что обеспечивает более высокую точность измерения чихания.В этой статье сообщается о клиническом испытании антигистаминного препарата второго поколения, лоратадина, у взрослых с экспериментальной риновирусной простудой, а также рассматриваются возможные участки действия антигистаминных препаратов первого и второго поколения. Хотя исследование изначально было разработано для определения того, снижает ли лоратадин путем подавления экспрессии молекулы межклеточной адгезии-1 (ICAM-1) на эпителиальных клетках носа уровень риновирусной инфекции, оно предоставляет ранее отсутствующую информацию о результатах тестирования второго поколения антигистаминный препарат в режиме вирусного заражения.
Материалы и методы
Субъекты . В исследовании приняли участие 66 взрослых добровольцев из Шарлоттсвилля, штат Вирджиния, с титрами нейтрализующих антител ≤2 к риновирусу типа 16. Субъекты должны были не иметь симптомов простуды и лихорадки (> 37,8 ° C) в течение 1 недели до включения в испытание и не иметь в анамнезе гиперчувствительности к антигистаминным препаратам. Кроме того, исключались пациенты, если у них был (или имелся в анамнезе) аллергический ринит, бронхиальная астма или другие заболевания нижних дыхательных путей, такие как хроническая обструктивная болезнь легких или эмфизема легких.Исключались субъекты с историей злоупотребления алкоголем и наркотиками, а также добровольцы, которые принимали исследуемые препараты в течение 30 дней, антигистаминные препараты и / или препараты от простуды в течение 14 дней, ингибиторы моноаминоксидазы в течение 7 дней, астемизол в течение 90 дней или любые другие лекарства. думал, что мешает изучению препарата. Другие критерии исключения включали беременность или период лактации, глаукому, а также почечные, печеночные, эндокринные, пищеварительные, мочеполовые, неврологические или психологические заболевания. Протокол был рассмотрен Комитетом по исследованиям человека Университета Вирджинии.
Исследуемый препарат . Лоратадин применялся в таблетках по 10 мг. Таблетки плацебо были идентичны таблеткам лоратадина, но содержали фармакологически инертные ингредиенты.
Вирусный вызов . Интраназальное заражение риновирусом типа 16 выполняли крупными каплями с использованием 0,5 мл (0,25 мл на ноздрю) пула инокулята, содержащего 100 инфекционных доз 50 / мл (TCID 50 / мл) вируса для культуры ткани. Пробу выполняли дважды с 20-минутным интервалом между испытаниями.Пул посевного материала был протестирован на безопасность от посторонних агентов [20].
Меры по заражению . Смывы из носа собирали за 8 дней до и непосредственно перед инокуляцией контрольного вируса, чтобы определить, были ли субъекты инфицированы вирусом дикого типа. После заражения вирусом каждое утро перед введением лекарства собирали смывы из носа. Смывки культивировали на риновирус в течение 5 дней после заражения эмбриональными клетками легких человека (WI-38).Изоляты были идентифицированы как риновирус типа 16 путем нейтрализации типоспецифическим антителом. Венозную кровь брали за 7 дней до лечения и через 14–21 день после интраназальной инокуляции для измерения гомотипических нейтрализующих антител [21].
Меры по оценке болезни . Наличие и тяжесть симптомов определяли ежедневно, начиная с первого дня лечения, за 7 дней до заражения вирусом, в общей сложности в течение 13 дней. Данные о симптомах собирались непосредственно перед введением лоратадина или плацебо медсестрой, которая записывала оценку субъектом тяжести симптомов за предшествующие 24 часа по 5-балльной шкале (0 — «нет»; 1 — «легкая»; 2 , «Умеренная»; 3 — «тяжелая»; 4 — «очень тяжелая») [22].Оцениваемые симптомы включали чихание, насморк, заложенность носа, боль в горле, кашель, головную боль, недомогание и озноб. Общий балл симптомов определяли путем сложения баллов тяжести симптомов в течение 5-дневного периода после вирусного заражения. Оценка для каждого симптома, присутствующего непосредственно перед заражением, вычиталась из каждой из ежедневных оценок для этого симптома.
Оценка тяжести заболевания также включала ежедневные измерения массы носового секрета [23]. Каждый испытуемый ежедневно записывал количество кашля и чихания.Измерения назальной секреции и подсчет кашля и чихания начинали после того, как субъекты были помещены в отель после заражения. Перед тем, как покинуть отель в последний день, испытуемых спрашивали, не простужались ли они, по их мнению,. Информация о возникновении и серьезности любых побочных эффектов собиралась ежедневно и оценивалась как «нет», «легкая», «умеренная» или «тяжелая».
Опытный образец . Испытание представляло собой 13-дневное одноцентровое рандомизированное двойное слепое плацебо-контролируемое исследование в параллельных группах с участием здоровых добровольцев в возрасте 18–40 лет любого пола.Лоратадин или плацебо вводили каждое утро между 6 часами утра. и 8 часов утра, в дни 1–13 исследования, с вирусным заражением на 8 день. Субъекты были случайным образом распределены для получения лечения или плацебо, и их статус лечения не учитывался, как и наблюдатели, записывающие клиническую информацию.
Анализ данных . Для сравнения пропорций использовался точный критерий Фишера. Тест t использовался для сравнения порядковых и интервальных данных.Результаты вероятностного тестирования были двусторонними.
Результаты
Субъекты . Из 66 включенных в исследование субъектов 34 получали лоратадин, а 32 — плацебо. Четыре субъекта в группе лоратадина и один в группе плацебо были инфицированы диким штаммом риновируса на момент включения в исследование. Они были исключены из оценки, как и 1 субъект плацебо, который прекратил прием лекарств после развития мигренозной головной боли на 10 день, оставив 60 оцениваемых субъектов для анализа.
Уровень заражения . Двадцать восемь (93%) из 30 субъектов, получавших лоратадин, и 24 (80%) из 30 субъектов, получавших плацебо, выделяли контрольный вирус в носовую жидкость в течение ≥1 дня ( P = 0,25; таблица 1). Среднее количество дней, в течение которых выделялся вирус, было одинаковым для всех зараженных добровольцев и для всех инфицированных добровольцев в 2 группах. Гомотипические ответы антител наблюдались у 12 (40%) из 30 субъектов, получавших лоратадин, и у 11 (37%) из 30 субъектов, получавших плацебо.Частота инфицирования (выделение вируса и / или повышение уровня антител) составляла 29 (97%) из 30 в группе лоратадина и 24 (80%) из 30 в группе плацебо ( P = 0,1).
Таблица 1
Показатели инфицирования и заболеваемости взрослых экспериментальными риновирусными простудными заболеваниями, получавших лоратадин или плацебо.
Таблица 1
Показатели инфицирования и заболеваемости среди взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Титры вирусов .Как и ожидалось, средние геометрические титры вируса достигли пика на второй день после заражения вирусом (фигура 2А). Титры вирусов были одинаковыми в 2 группах, хотя наблюдалась тенденция к снижению титров в группе плацебо на 2-й день.
Рисунок 2
Геометрические средние (± SE) вирусные титры, средние (± SE) массы носовой слизи и средние (± SE) баллы симптомов у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Рис. 2
Геометрические средние (± SE) титры вирусов, средние (± SE) массы носовой слизи и средние (± SE) баллы симптомов у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Возникновение болезни . Двадцать три (79%) из 29 инфицированных субъектов, получавших лоратадин, и 14 (58%) из 24 инфицированных субъектов, получавших плацебо, соответствовали модифицированным критериям Джексона для болезни ( P = 0,2).
Оценка симптомов 9000 4. Средние (± SE) баллы тяжести чихания были аналогичными в течение первых 3 дней и имели тенденцию к снижению в группе плацебо на четвертый день (рисунок 1). Средние (± стандартная ошибка) общие баллы симптомов были одинаковыми в 2 группах (рис. 2В).Показатели ринореи, как правило, были ниже в группе плацебо на 2 и 3 дни, но обратная картина наблюдалась на 4 и 5 дни (рисунок 2D). Средние (± SE) показатели обструкции носа, боли в горле и кашля были одинаковыми в двух группах (рисунок 2C, рисунок 2F, рисунок 2G). Средние (± SE) баллы по шкале головной боли и недомогания в последние дни болезни были ниже в группе лоратадина (рисунок 2H, рисунок 2I).
Рисунок 1
Средние (± SE) баллы тяжести чихания у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Рисунок 1
Средние (± SE) баллы тяжести чихания у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Масса слизи из носа . Наблюдалась устойчивая тенденция к снижению веса назального секрета в группе плацебо (рисунок 2C). Общее среднее значение ± стандартная ошибка (стандартная ошибка) массы носовой слизи за 5 дней составило 27,1 ± 4,0 г для группы лоратадина и 19,7 ± 5,2 г для группы плацебо ( P = 0,3).
Уровни ICAM-1 .Средние (± SE) уровни ICAM-1 в носовой жидкости выросли по сравнению с исходным уровнем на 2-й день и достигли пика на 3-й день. Уровни были одинаковыми в обеих группах (рис. 3).
Рисунок 3
Средние (± SE) уровни ICAM-1 в носовой жидкости у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Рисунок 3
Средние (± SE) уровни ICAM-1 в носовой жидкости у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Неблагоприятные события .У одного субъекта в группе плацебо была мигрень и рвота, а у другого — рвота. В остальном о нежелательных явлениях не сообщалось.
Обсуждение
Что касается первоначальной цели исследования, не наблюдалось различий между группами, получавшими лоратадин, и группами, получавшими плацебо, по скорости выделения вируса, титрам вирусов, общей частоте инфицирования, частоте заболеваний или количеству симптомов. Уровни ICAM-1 в назальном секрете в 2 группах также были сходными.
Результаты также показали отсутствие терапевтического эффекта лоратадина при чихании. Это подтверждает более раннюю работу с пациентами с естественной простудой, у которых антигистаминные препараты второго поколения были неэффективны в снижении чихания [15–18]. Почему антигистаминные препараты первого поколения эффективны для уменьшения чихания при простуде [3, 5], а антигистаминные препараты второго поколения не представляют интереса. Антигистаминные препараты первого поколения, помимо их способности блокировать h2-рецепторы, также блокируют мускариновые рецепторы и преодолевают гематоэнцефалический барьер [14].Антигистаминные препараты второго поколения представляют собой специфические блокаторы H2-рецепторов без других признанных фармакологических свойств и не проникают через гематоэнцефалический барьер.
Информация о неврологических путях рефлекса чихания поступает в основном из работы на животных [24, 25]. Рефлекс чихания проходит по периферическим нервам и через продолговатый мозг. Нейрофармакология чихания включает H2, мускариновые и никотиновые рецепторы. При простуде рефлекс чихания начинается в носу с инфицирования носовых клеток вирусом простуды (рис. 4).Нет никаких доказательств того, что активация базофилов и тучных клеток с высвобождением гистамина происходит при простудных заболеваниях; однако предполагается, что свободные нервные окончания решетчатой ветви тройничного нерва стимулируются медиаторами воспаления, такими как брадикинин [1]. Затем нервный импульс проходит по афферентным нервным волокнам к сенсорному ядру тройничного нерва в продолговатом мозге и достигает соседнего центра чихания [26–28]. Затем через другой синапс импульс поступает в верхнее парасимпатическое слюнное ядро лицевого нерва.Здесь он пересекает синапс и перемещается по преганглионарным волокнам большого каменистого нерва к клиновидно-небному ганглию. Этот путь передачи при чихании подтверждается тем фактом, что инъекция алкоголя в клиновидно-небный ганглий блокирует рефлекс чихания [29]. Затем импульс проходит через другой синапс (в основном никотиновый, отчасти мускариновый) и через постганглионарные волокна к синапсам (мускариновым) слизистых желез и кровеносных сосудов, которые затем стимулируются. Возникающая в результате секреция желез и транссудация сосудов рестимулируют свободные нервные окончания тройничного нерва, по которому импульс перенаправляется к ядру тройничного нерва, а затем к центру чихания в продолговатом мозге.Когда рестимуляции центра чихания достаточно, импульс затем направляется интрамедуллярными волокнами в синапсы нескольких дыхательных центров в ретикулярной формации, а оттуда — в синапсы дыхательных нейронов блуждающего, диафрагмального и межреберных нервов. Затем через никотиновые синапсы нервный импульс стимулирует мышечные сокращения, ответственные за чихание.
Рисунок 4
Путь рефлекса чихания
Рисунок 4
Путь рефлекса чихания
Нос — это первое место, где гистамин может участвовать в патогенезе чихания и где антигистаминные препараты могут подавлять рефлекс чихания.H2-рецепторы присутствуют на свободных нервных окончаниях тройничного нерва [30]. Против возможности того, что слизистая оболочка носа является основным местом действия антигистаминных препаратов первого поколения, является открытие, что не было обнаружено повышения уровня гистамина в носовых секретах во время простуды [6–9]. Кроме того, в более ранних исследованиях естественного холода и в текущем исследовании антигистаминные препараты второго поколения, несмотря на то, что они достигают слизистой оболочки носа и обладают активностью блокирования h2, оказались неэффективными для уменьшения чихания [15–18]; однако, поскольку слизистая оболочка носа, по-видимому, имеет повышенную чувствительность к гистамину во время простуды [10,1–13], нельзя полностью исключить роль носовых участков.
Следующее возможное место для антигистаминного препарата первого поколения, блокирующего чихание, находится в продолговатом мозге, где синаптические соединения присутствуют в нескольких местах. И h2, и мускариновые рецепторы были идентифицированы в определенных областях мозга [14, 31]. Такие рецепторы могут быть потенциальными мишенями для действия антигистаминных препаратов первого, но не второго поколения; однако синаптические медиаторы, которые участвуют в рефлексе чихания в продолговатом мозге, не охарактеризованы.Наблюдаемая неспособность антигистаминных препаратов второго поколения уменьшить чихание при простуде подтверждает возможность важности этих участков.
Мускариновая активность отвечает исключительно за парасимпатическую стимуляцию секреции желез и расширение сосудов с последующей транссудацией. Ожидается, что антихолинергическая активность антигистаминных препаратов первого поколения будет действовать на этих участках. Это подтверждается документально подтвержденным эффектом антигистаминных препаратов первого поколения по уменьшению объема выделения жидкости из носа во время простуды [3, 4].Второй афферентный импульс к мозговому веществу снова инициируется раздражением свободных нервных окончаний тройничного нерва. Транссудация сосудов приводит к высвобождению кининогена с образованием кинина [14]. Это событие предоставляет средства для прямой стимуляции свободных нервных окончаний кининами, а также гистамином, высвобождаемым из тучных клеток при стимуляции кининами. Это обеспечивает еще одну возможную мишень для действия антигистаминного препарата. Кроме того, когда нервный импульс перенаправляется к мозговому веществу, h2 и мускариновые синаптические участки могут блокироваться антигистаминными препаратами первого поколения, как описано выше.С этого момента, когда в процесс вовлекаются мотонейроны, передача по нервам зависит от никотинергических рецепторов и, следовательно, не будет восприимчива к действию антигистаминных препаратов.
Этот анализ предполагает, что важное место терапевтического действия антигистаминных препаратов первого поколения на чихание находится в продолговатом мозге, где могут быть задействованы как h2, так и мускариновые рецепторы. Известно, что рецепторы h2 присутствуют в высоких концентрациях в гипоталамусе, где гистамин действует как нейромедиатор, помогая регулировать уровень бодрствования [14].Этим объясняется сонливость, связанная с использованием антигистаминных препаратов первого поколения. Из-за высокой концентрации рецепторов h2 в гипоталамусе и из-за того, что парасимпатические нервные волокна возникают из гипоталамуса и активируются им, вероятно, что гистамин играет роль в передаче сигнала в этой области.
Известно также, что антигистаминные препараты первого поколения помогают уменьшить тошноту, связанную с укачиванием [31]. Скополамин, антихолинергический препарат, который проникает через гематоэнцефалический барьер, является эффективным средством лечения укачивания, тогда как атропин, который не так легко проникает через гематоэнцефалический барьер, не эффективен.Противошумный эффект скополамина частично зависит от блокирования мускариновых рецепторов вестибулярных ядер и постремной зоны головного мозга. Другие ядра ствола мозга также могут использовать систему мускариновых рецепторов, что подтверждает идею о том, что мускариновые рецепторы в ЦНС являются частью рефлекса чихания. В настоящее время не имеется полной информации о мозговых синапсах и нейротрансмиттерах, участвующих в рефлексе чихания, и в этой области необходимы дальнейшие исследования; однако имеющаяся информация свидетельствует о том, что для эффективного лечения чихания при простуде необходимы соединения, которые преодолевают гематоэнцефалический барьер и обладают активностью блокирования как h2, так и мускаринов.
Список литературы
1,. ,,.Риновирус
,Клиническая вирусология
,1997
Нью-Йорк
Черчилль Ливингстон
(стр.1025
—47
) 2,,.Физиологические реакции на интраназальное дозозависимое введение гистамина, метахолина, брадикинина и простагландина у взрослых добровольцев с назальной аллергией и без нее
,J Allergy Clin Immunol
,1990
, vol.86
(стр.924
—35
) 3,.Эффективность лечения риновирусной простуды бромфенирамина малеатом
,Clin Infect Dis
,1997
, vol.25
(стр.1188
—94
) 4,,,,,.Рандомизированное контролируемое исследование клемастина фумарата для лечения экспериментальных риновирусных простуд
,Clin Infect Dis
,1996
, vol.22
(стр.656
—62
) 5« и др.Эффективность клемастина фумарата для лечения ринореи и чихания, связанных с простудой
,Clin Infect Dis
,1997
, vol.25
(стр.824
—30
) 6,,,,.Гистамин в назальном секрете
,Int Arch Allergy Appl Immunol
,1978
, vol.57
(стр.193
—200
) 7,,,,,.Ответственен ли гистамин за симптомы риновирусной простуды: посмотрите на медиаторы воспаления после инфекции
,Pediatr Infect Dis J
,1988
, vol.7
(стр.218
—22
) 8,,,,,.Анализ назального секрета при экспериментальных риновирусных инфекциях верхних дыхательных путей
,J Allergy Clin Immunol
,1993
, vol.92
(стр.722
—31
) 9,.Уровень гистамина в назальном секрете и сыворотке может быть повышен при вирусной инфекции дыхательных путей
,Int Arch Allergy Appl Immunol
,1982
, vol.67
(стр.380
—3
) 10,,, et al.Экспериментальная инфекция риновирусом 16 усиливает высвобождение гистамина после бронхопровокации антигена у субъектов с аллергией
,Am Rev Respir Dis
,1991
, vol.144
(стр.1267
—73
) 11,,, et al.Зеркало-сосудистая экссудативная гиперреактивность при простуде, вызванной коронавирусом человека
,Thorax
,1994
, vol.49
(стр.121
—7
) 12,,,,.Влияние экспериментальной инфекции риновирусом 39 на назальную реакцию на гистамин и воздействие холодного воздуха у субъектов с аллергией и неаллергией
,J Allergy Clin Immunol
,1994
, vol.93
(стр.534
—42
) 13.Вирусные инфекции и аллергические заболевания
,Clin Exper Allergy
,1991
, vol.1
(S21)
(стр.68
—71
) 14,. ,,,,.Гистамин, брадикинин и их антагонисты
,Goodman & Gilman’s фармакологическая основа терапии
,1996
9-е издНью-Йорк
McGraw-Hill
(стр.581
—600
) 15,,.Неэффективность перорального терфенадина при естественной простуде: доказательства против гистамина как посредника симптомов простуды
,Pediatr Infect Dis J
,1988
, vol.7
(стр.215
—42
) 16,.Оценка перорального применения терфенадина для лечения простуды
,Ann Allergy
,1991
, vol.67
(стр.593
—7
) 17,.Эффективность терфенадина при лечении простуды: двойное слепое сравнение с плацебо
,Eur J Pharmacol
,1988
, vol.34
(стр.35
—40
) 18,.Антигистаминные препараты девяностых
,Clin Rev Allergy
,1993
, vol.11
(стр.111
—53
) 19,,.Влияние вариации сигнала, смещения, шума и величины эффекта на статистическую значимость в исследованиях лечения простуды
,Antiviral Res
,1996
, vol.29
(стр.287
—95
) 20« и др..Обновленные рекомендации по тестированию на безопасность вирусных инокулятов, используемых в добровольных экспериментах на риновирусных простудных заболеваниях.
,Прогресс в медицинской вирусологии. Vol 39
,1992
Basel
Karger
(стр.256
—63
) 21,,,. ,.Риновирус
,Диагностические процедуры для вирусных, риккетсиозных и хламидийных инфекций
,1989
, т.142
6-е издВашингтон, округ Колумбия
Американская ассоциация общественного здравоохранения
(стр.811
—5
) 22,,,.Передача простуды добровольцам в контролируемых условиях. I. Простуда как клиническое проявление
,Arch Intern Med
,1958
, vol.101
(стр.267
—78
) 23,,,,,.Двойное слепое плацебо-контролируемое клиническое испытание влияния хлорфенирамина на реакцию носовых дыхательных путей, среднего уха и евстахиевой трубы на провокационную риновирусную инфекцию
,Pediatr Infect Dis J
,1988
, vol.7
(стр.229
—38
) 24,.Нейронные механизмы чихания
,Am J Physiol
,1975
, vol.229
(стр.770
—6
) 25,,,.Область ствола мозга, вызывающая чихание
,Brain Research
,1990
, vol.511
(стр.265
—70
) 26,,.Неспособность чихать как проявление новообразования костного мозга
,Неврология
,1991
, т.41
(стр.1675
—6
) 27,.Кашель и другие респираторные рефлексы
,Прогресс в респираторных исследованиях. Vol. 23
,1979
Базель, Швейцария
Karger
(стр.218
—23
) 28,.Световой рефлекс чихания: обзор и обсуждение литературы
,Неврология
,1993
, vol.43
(стр.868
—71
) 29.Чихание: его физиология и лечение
,Глаз Ухо Нос Горло Пн
,1975
, vol.54
(стр.449
—53
) 30,. ,.Нос и инфекция
,Нос: физиология верхних дыхательных путей и атмосферная среда
,1982
Амстердам
Elsevier Biomedical
(стр.399
—422
) 31,. ,,,,.Агонисты и антагонисты мускариновых рецепторов
,Goodman & Gilman’s фармакологические основы терапии
,1996
9th edNew York
McGraw-Hill
(стр.141
—60
)© 2001 Американское общество инфекционных болезней
Вариантный эффект антигистаминных препаратов первого и второго поколения как ключ к разгадке механизма их действия на рефлекс чихания при простуде | Клинические инфекционные болезни
Абстракция
Лечение антигистаминными препаратами первого поколения уменьшает чихание, ринорею, массу носовой слизи и, в некоторых случаях, кашель у субъектов с экспериментальной или естественной простудой; однако лечение антигистаминными препаратами второго поколения не было эффективным при этих жалобах в испытаниях с участием субъектов с естественной простудой.В этой статье сообщается об отрицательных результатах клинического исследования лоратадина, антигистаминного препарата второго поколения, у взрослых на модели заражения риновирусом. Это открытие в строго контролируемых условиях модели заражения подтверждает более ранние отрицательные исследования антигистаминных препаратов второго поколения при естественных простудных заболеваниях. Антигистаминные препараты первого поколения блокируют как гистаминовые, так и мускариновые рецепторы, а также преодолевают гематоэнцефалический барьер. Антигистаминные препараты второго поколения в основном блокируют гистаминовые рецепторы и не проникают через гематоэнцефалический барьер.Эффективность антигистаминных препаратов первого поколения в блокировании чихания при простуде может быть связана в первую очередь с нейрофармакологическими манипуляциями с гистаминовыми и мускариновыми рецепторами в продолговатом мозге.
Индивидуальные симптомы простуды обусловлены множественными и в некоторой степени специфическими путями воспаления [1]. Считается, что чихание является результатом высвобождения гистамина из тучных клеток носа и базофилов, которые активируются вирусной инфекцией простуды. Это мнение подтверждается данными о том, что интраназальное введение гистамина у нормальных добровольцев вызывало чихание, тогда как интраназальное воздействие других медиаторов — нет [2].Кроме того, лечение антигистаминными препаратами первого поколения очень эффективно для уменьшения чихания у пациентов с экспериментальной и естественной простудой [3–5]. Поэтому удивительно, что, в отличие от аллергического ринита, у пациентов с простудой не повышается уровень гистамина в носовых секретах [6–9], хотя сообщается о повышении чувствительности слизистой оболочки носа к гистамину [10–13].
Антигистаминные препараты первого и второго поколения являются конкурентными антагонистами гистамина на участке h2-рецептора [14].Дополнительной фармакологической активностью антигистаминных препаратов первого, но не второго поколения, является конкурентный антагонизм ацетилхолина в отношении нейрональных и нервно-мышечных мускариновых рецепторов. Антигистаминные препараты первого поколения также проникают через гематоэнцефалический барьер и, таким образом, обладают потенциалом активности в головном мозге; антигистаминные препараты второго поколения — нет. При ограниченном тестировании и несмотря на их активность по блокированию H2, антигистаминные препараты второго поколения оказались неэффективными в подавлении чихания у пациентов с естественной простудой [15–18].
Эти данные поднимают интересный вопрос о механизме действия антигистаминных препаратов первого поколения на уменьшение чихания у пациентов с простудой и о неэффективности антигистаминных препаратов второго поколения в этой ситуации. Кроме того, исследования естественного холода связаны с определенными техническими проблемами, такими как трудности с включением пациентов на ранних стадиях простуды, когда эффективность лечения измеряется наиболее точно [19]. Поэтому было бы желательно подтвердить результаты исследований естественного холода путем тестирования антигистаминного препарата второго поколения на модели заражения риновирусом, что обеспечивает более высокую точность измерения чихания.В этой статье сообщается о клиническом испытании антигистаминного препарата второго поколения, лоратадина, у взрослых с экспериментальной риновирусной простудой, а также рассматриваются возможные участки действия антигистаминных препаратов первого и второго поколения. Хотя исследование изначально было разработано для определения того, снижает ли лоратадин путем подавления экспрессии молекулы межклеточной адгезии-1 (ICAM-1) на эпителиальных клетках носа уровень риновирусной инфекции, оно предоставляет ранее отсутствующую информацию о результатах тестирования второго поколения антигистаминный препарат в режиме вирусного заражения.
Материалы и методы
Субъекты . В исследовании приняли участие 66 взрослых добровольцев из Шарлоттсвилля, штат Вирджиния, с титрами нейтрализующих антител ≤2 к риновирусу типа 16. Субъекты должны были не иметь симптомов простуды и лихорадки (> 37,8 ° C) в течение 1 недели до включения в испытание и не иметь в анамнезе гиперчувствительности к антигистаминным препаратам. Кроме того, исключались пациенты, если у них был (или имелся в анамнезе) аллергический ринит, бронхиальная астма или другие заболевания нижних дыхательных путей, такие как хроническая обструктивная болезнь легких или эмфизема легких.Исключались субъекты с историей злоупотребления алкоголем и наркотиками, а также добровольцы, которые принимали исследуемые препараты в течение 30 дней, антигистаминные препараты и / или препараты от простуды в течение 14 дней, ингибиторы моноаминоксидазы в течение 7 дней, астемизол в течение 90 дней или любые другие лекарства. думал, что мешает изучению препарата. Другие критерии исключения включали беременность или период лактации, глаукому, а также почечные, печеночные, эндокринные, пищеварительные, мочеполовые, неврологические или психологические заболевания. Протокол был рассмотрен Комитетом по исследованиям человека Университета Вирджинии.
Исследуемый препарат . Лоратадин применялся в таблетках по 10 мг. Таблетки плацебо были идентичны таблеткам лоратадина, но содержали фармакологически инертные ингредиенты.
Вирусный вызов . Интраназальное заражение риновирусом типа 16 выполняли крупными каплями с использованием 0,5 мл (0,25 мл на ноздрю) пула инокулята, содержащего 100 инфекционных доз 50 / мл (TCID 50 / мл) вируса для культуры ткани. Пробу выполняли дважды с 20-минутным интервалом между испытаниями.Пул посевного материала был протестирован на безопасность от посторонних агентов [20].
Меры по заражению . Смывы из носа собирали за 8 дней до и непосредственно перед инокуляцией контрольного вируса, чтобы определить, были ли субъекты инфицированы вирусом дикого типа. После заражения вирусом каждое утро перед введением лекарства собирали смывы из носа. Смывки культивировали на риновирус в течение 5 дней после заражения эмбриональными клетками легких человека (WI-38).Изоляты были идентифицированы как риновирус типа 16 путем нейтрализации типоспецифическим антителом. Венозную кровь брали за 7 дней до лечения и через 14–21 день после интраназальной инокуляции для измерения гомотипических нейтрализующих антител [21].
Меры по оценке болезни . Наличие и тяжесть симптомов определяли ежедневно, начиная с первого дня лечения, за 7 дней до заражения вирусом, в общей сложности в течение 13 дней. Данные о симптомах собирались непосредственно перед введением лоратадина или плацебо медсестрой, которая записывала оценку субъектом тяжести симптомов за предшествующие 24 часа по 5-балльной шкале (0 — «нет»; 1 — «легкая»; 2 , «Умеренная»; 3 — «тяжелая»; 4 — «очень тяжелая») [22].Оцениваемые симптомы включали чихание, насморк, заложенность носа, боль в горле, кашель, головную боль, недомогание и озноб. Общий балл симптомов определяли путем сложения баллов тяжести симптомов в течение 5-дневного периода после вирусного заражения. Оценка для каждого симптома, присутствующего непосредственно перед заражением, вычиталась из каждой из ежедневных оценок для этого симптома.
Оценка тяжести заболевания также включала ежедневные измерения массы носового секрета [23]. Каждый испытуемый ежедневно записывал количество кашля и чихания.Измерения назальной секреции и подсчет кашля и чихания начинали после того, как субъекты были помещены в отель после заражения. Перед тем, как покинуть отель в последний день, испытуемых спрашивали, не простужались ли они, по их мнению,. Информация о возникновении и серьезности любых побочных эффектов собиралась ежедневно и оценивалась как «нет», «легкая», «умеренная» или «тяжелая».
Опытный образец . Испытание представляло собой 13-дневное одноцентровое рандомизированное двойное слепое плацебо-контролируемое исследование в параллельных группах с участием здоровых добровольцев в возрасте 18–40 лет любого пола.Лоратадин или плацебо вводили каждое утро между 6 часами утра. и 8 часов утра, в дни 1–13 исследования, с вирусным заражением на 8 день. Субъекты были случайным образом распределены для получения лечения или плацебо, и их статус лечения не учитывался, как и наблюдатели, записывающие клиническую информацию.
Анализ данных . Для сравнения пропорций использовался точный критерий Фишера. Тест t использовался для сравнения порядковых и интервальных данных.Результаты вероятностного тестирования были двусторонними.
Результаты
Субъекты . Из 66 включенных в исследование субъектов 34 получали лоратадин, а 32 — плацебо. Четыре субъекта в группе лоратадина и один в группе плацебо были инфицированы диким штаммом риновируса на момент включения в исследование. Они были исключены из оценки, как и 1 субъект плацебо, который прекратил прием лекарств после развития мигренозной головной боли на 10 день, оставив 60 оцениваемых субъектов для анализа.
Уровень заражения . Двадцать восемь (93%) из 30 субъектов, получавших лоратадин, и 24 (80%) из 30 субъектов, получавших плацебо, выделяли контрольный вирус в носовую жидкость в течение ≥1 дня ( P = 0,25; таблица 1). Среднее количество дней, в течение которых выделялся вирус, было одинаковым для всех зараженных добровольцев и для всех инфицированных добровольцев в 2 группах. Гомотипические ответы антител наблюдались у 12 (40%) из 30 субъектов, получавших лоратадин, и у 11 (37%) из 30 субъектов, получавших плацебо.Частота инфицирования (выделение вируса и / или повышение уровня антител) составляла 29 (97%) из 30 в группе лоратадина и 24 (80%) из 30 в группе плацебо ( P = 0,1).
Таблица 1
Показатели инфицирования и заболеваемости взрослых экспериментальными риновирусными простудными заболеваниями, получавших лоратадин или плацебо.
Таблица 1
Показатели инфицирования и заболеваемости среди взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Титры вирусов .Как и ожидалось, средние геометрические титры вируса достигли пика на второй день после заражения вирусом (фигура 2А). Титры вирусов были одинаковыми в 2 группах, хотя наблюдалась тенденция к снижению титров в группе плацебо на 2-й день.
Рисунок 2
Геометрические средние (± SE) вирусные титры, средние (± SE) массы носовой слизи и средние (± SE) баллы симптомов у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Рис. 2
Геометрические средние (± SE) титры вирусов, средние (± SE) массы носовой слизи и средние (± SE) баллы симптомов у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Возникновение болезни . Двадцать три (79%) из 29 инфицированных субъектов, получавших лоратадин, и 14 (58%) из 24 инфицированных субъектов, получавших плацебо, соответствовали модифицированным критериям Джексона для болезни ( P = 0,2).
Оценка симптомов 9000 4. Средние (± SE) баллы тяжести чихания были аналогичными в течение первых 3 дней и имели тенденцию к снижению в группе плацебо на четвертый день (рисунок 1). Средние (± стандартная ошибка) общие баллы симптомов были одинаковыми в 2 группах (рис. 2В).Показатели ринореи, как правило, были ниже в группе плацебо на 2 и 3 дни, но обратная картина наблюдалась на 4 и 5 дни (рисунок 2D). Средние (± SE) показатели обструкции носа, боли в горле и кашля были одинаковыми в двух группах (рисунок 2C, рисунок 2F, рисунок 2G). Средние (± SE) баллы по шкале головной боли и недомогания в последние дни болезни были ниже в группе лоратадина (рисунок 2H, рисунок 2I).
Рисунок 1
Средние (± SE) баллы тяжести чихания у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Рисунок 1
Средние (± SE) баллы тяжести чихания у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Масса слизи из носа . Наблюдалась устойчивая тенденция к снижению веса назального секрета в группе плацебо (рисунок 2C). Общее среднее значение ± стандартная ошибка (стандартная ошибка) массы носовой слизи за 5 дней составило 27,1 ± 4,0 г для группы лоратадина и 19,7 ± 5,2 г для группы плацебо ( P = 0,3).
Уровни ICAM-1 .Средние (± SE) уровни ICAM-1 в носовой жидкости выросли по сравнению с исходным уровнем на 2-й день и достигли пика на 3-й день. Уровни были одинаковыми в обеих группах (рис. 3).
Рисунок 3
Средние (± SE) уровни ICAM-1 в носовой жидкости у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Рисунок 3
Средние (± SE) уровни ICAM-1 в носовой жидкости у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Неблагоприятные события .У одного субъекта в группе плацебо была мигрень и рвота, а у другого — рвота. В остальном о нежелательных явлениях не сообщалось.
Обсуждение
Что касается первоначальной цели исследования, не наблюдалось различий между группами, получавшими лоратадин, и группами, получавшими плацебо, по скорости выделения вируса, титрам вирусов, общей частоте инфицирования, частоте заболеваний или количеству симптомов. Уровни ICAM-1 в назальном секрете в 2 группах также были сходными.
Результаты также показали отсутствие терапевтического эффекта лоратадина при чихании. Это подтверждает более раннюю работу с пациентами с естественной простудой, у которых антигистаминные препараты второго поколения были неэффективны в снижении чихания [15–18]. Почему антигистаминные препараты первого поколения эффективны для уменьшения чихания при простуде [3, 5], а антигистаминные препараты второго поколения не представляют интереса. Антигистаминные препараты первого поколения, помимо их способности блокировать h2-рецепторы, также блокируют мускариновые рецепторы и преодолевают гематоэнцефалический барьер [14].Антигистаминные препараты второго поколения представляют собой специфические блокаторы H2-рецепторов без других признанных фармакологических свойств и не проникают через гематоэнцефалический барьер.
Информация о неврологических путях рефлекса чихания поступает в основном из работы на животных [24, 25]. Рефлекс чихания проходит по периферическим нервам и через продолговатый мозг. Нейрофармакология чихания включает H2, мускариновые и никотиновые рецепторы. При простуде рефлекс чихания начинается в носу с инфицирования носовых клеток вирусом простуды (рис. 4).Нет никаких доказательств того, что активация базофилов и тучных клеток с высвобождением гистамина происходит при простудных заболеваниях; однако предполагается, что свободные нервные окончания решетчатой ветви тройничного нерва стимулируются медиаторами воспаления, такими как брадикинин [1]. Затем нервный импульс проходит по афферентным нервным волокнам к сенсорному ядру тройничного нерва в продолговатом мозге и достигает соседнего центра чихания [26–28]. Затем через другой синапс импульс поступает в верхнее парасимпатическое слюнное ядро лицевого нерва.Здесь он пересекает синапс и перемещается по преганглионарным волокнам большого каменистого нерва к клиновидно-небному ганглию. Этот путь передачи при чихании подтверждается тем фактом, что инъекция алкоголя в клиновидно-небный ганглий блокирует рефлекс чихания [29]. Затем импульс проходит через другой синапс (в основном никотиновый, отчасти мускариновый) и через постганглионарные волокна к синапсам (мускариновым) слизистых желез и кровеносных сосудов, которые затем стимулируются. Возникающая в результате секреция желез и транссудация сосудов рестимулируют свободные нервные окончания тройничного нерва, по которому импульс перенаправляется к ядру тройничного нерва, а затем к центру чихания в продолговатом мозге.Когда рестимуляции центра чихания достаточно, импульс затем направляется интрамедуллярными волокнами в синапсы нескольких дыхательных центров в ретикулярной формации, а оттуда — в синапсы дыхательных нейронов блуждающего, диафрагмального и межреберных нервов. Затем через никотиновые синапсы нервный импульс стимулирует мышечные сокращения, ответственные за чихание.
Рисунок 4
Путь рефлекса чихания
Рисунок 4
Путь рефлекса чихания
Нос — это первое место, где гистамин может участвовать в патогенезе чихания и где антигистаминные препараты могут подавлять рефлекс чихания.H2-рецепторы присутствуют на свободных нервных окончаниях тройничного нерва [30]. Против возможности того, что слизистая оболочка носа является основным местом действия антигистаминных препаратов первого поколения, является открытие, что не было обнаружено повышения уровня гистамина в носовых секретах во время простуды [6–9]. Кроме того, в более ранних исследованиях естественного холода и в текущем исследовании антигистаминные препараты второго поколения, несмотря на то, что они достигают слизистой оболочки носа и обладают активностью блокирования h2, оказались неэффективными для уменьшения чихания [15–18]; однако, поскольку слизистая оболочка носа, по-видимому, имеет повышенную чувствительность к гистамину во время простуды [10,1–13], нельзя полностью исключить роль носовых участков.
Следующее возможное место для антигистаминного препарата первого поколения, блокирующего чихание, находится в продолговатом мозге, где синаптические соединения присутствуют в нескольких местах. И h2, и мускариновые рецепторы были идентифицированы в определенных областях мозга [14, 31]. Такие рецепторы могут быть потенциальными мишенями для действия антигистаминных препаратов первого, но не второго поколения; однако синаптические медиаторы, которые участвуют в рефлексе чихания в продолговатом мозге, не охарактеризованы.Наблюдаемая неспособность антигистаминных препаратов второго поколения уменьшить чихание при простуде подтверждает возможность важности этих участков.
Мускариновая активность отвечает исключительно за парасимпатическую стимуляцию секреции желез и расширение сосудов с последующей транссудацией. Ожидается, что антихолинергическая активность антигистаминных препаратов первого поколения будет действовать на этих участках. Это подтверждается документально подтвержденным эффектом антигистаминных препаратов первого поколения по уменьшению объема выделения жидкости из носа во время простуды [3, 4].Второй афферентный импульс к мозговому веществу снова инициируется раздражением свободных нервных окончаний тройничного нерва. Транссудация сосудов приводит к высвобождению кининогена с образованием кинина [14]. Это событие предоставляет средства для прямой стимуляции свободных нервных окончаний кининами, а также гистамином, высвобождаемым из тучных клеток при стимуляции кининами. Это обеспечивает еще одну возможную мишень для действия антигистаминного препарата. Кроме того, когда нервный импульс перенаправляется к мозговому веществу, h2 и мускариновые синаптические участки могут блокироваться антигистаминными препаратами первого поколения, как описано выше.С этого момента, когда в процесс вовлекаются мотонейроны, передача по нервам зависит от никотинергических рецепторов и, следовательно, не будет восприимчива к действию антигистаминных препаратов.
Этот анализ предполагает, что важное место терапевтического действия антигистаминных препаратов первого поколения на чихание находится в продолговатом мозге, где могут быть задействованы как h2, так и мускариновые рецепторы. Известно, что рецепторы h2 присутствуют в высоких концентрациях в гипоталамусе, где гистамин действует как нейромедиатор, помогая регулировать уровень бодрствования [14].Этим объясняется сонливость, связанная с использованием антигистаминных препаратов первого поколения. Из-за высокой концентрации рецепторов h2 в гипоталамусе и из-за того, что парасимпатические нервные волокна возникают из гипоталамуса и активируются им, вероятно, что гистамин играет роль в передаче сигнала в этой области.
Известно также, что антигистаминные препараты первого поколения помогают уменьшить тошноту, связанную с укачиванием [31]. Скополамин, антихолинергический препарат, который проникает через гематоэнцефалический барьер, является эффективным средством лечения укачивания, тогда как атропин, который не так легко проникает через гематоэнцефалический барьер, не эффективен.Противошумный эффект скополамина частично зависит от блокирования мускариновых рецепторов вестибулярных ядер и постремной зоны головного мозга. Другие ядра ствола мозга также могут использовать систему мускариновых рецепторов, что подтверждает идею о том, что мускариновые рецепторы в ЦНС являются частью рефлекса чихания. В настоящее время не имеется полной информации о мозговых синапсах и нейротрансмиттерах, участвующих в рефлексе чихания, и в этой области необходимы дальнейшие исследования; однако имеющаяся информация свидетельствует о том, что для эффективного лечения чихания при простуде необходимы соединения, которые преодолевают гематоэнцефалический барьер и обладают активностью блокирования как h2, так и мускаринов.
Список литературы
1,. ,,.Риновирус
,Клиническая вирусология
,1997
Нью-Йорк
Черчилль Ливингстон
(стр.1025
—47
) 2,,.Физиологические реакции на интраназальное дозозависимое введение гистамина, метахолина, брадикинина и простагландина у взрослых добровольцев с назальной аллергией и без нее
,J Allergy Clin Immunol
,1990
, vol.86
(стр.924
—35
) 3,.Эффективность лечения риновирусной простуды бромфенирамина малеатом
,Clin Infect Dis
,1997
, vol.25
(стр.1188
—94
) 4,,,,,.Рандомизированное контролируемое исследование клемастина фумарата для лечения экспериментальных риновирусных простуд
,Clin Infect Dis
,1996
, vol.22
(стр.656
—62
) 5« и др.Эффективность клемастина фумарата для лечения ринореи и чихания, связанных с простудой
,Clin Infect Dis
,1997
, vol.25
(стр.824
—30
) 6,,,,.Гистамин в назальном секрете
,Int Arch Allergy Appl Immunol
,1978
, vol.57
(стр.193
—200
) 7,,,,,.Ответственен ли гистамин за симптомы риновирусной простуды: посмотрите на медиаторы воспаления после инфекции
,Pediatr Infect Dis J
,1988
, vol.7
(стр.218
—22
) 8,,,,,.Анализ назального секрета при экспериментальных риновирусных инфекциях верхних дыхательных путей
,J Allergy Clin Immunol
,1993
, vol.92
(стр.722
—31
) 9,.Уровень гистамина в назальном секрете и сыворотке может быть повышен при вирусной инфекции дыхательных путей
,Int Arch Allergy Appl Immunol
,1982
, vol.67
(стр.380
—3
) 10,,, et al.Экспериментальная инфекция риновирусом 16 усиливает высвобождение гистамина после бронхопровокации антигена у субъектов с аллергией
,Am Rev Respir Dis
,1991
, vol.144
(стр.1267
—73
) 11,,, et al.Зеркало-сосудистая экссудативная гиперреактивность при простуде, вызванной коронавирусом человека
,Thorax
,1994
, vol.49
(стр.121
—7
) 12,,,,.Влияние экспериментальной инфекции риновирусом 39 на назальную реакцию на гистамин и воздействие холодного воздуха у субъектов с аллергией и неаллергией
,J Allergy Clin Immunol
,1994
, vol.93
(стр.534
—42
) 13.Вирусные инфекции и аллергические заболевания
,Clin Exper Allergy
,1991
, vol.1
(S21)
(стр.68
—71
) 14,. ,,,,.Гистамин, брадикинин и их антагонисты
,Goodman & Gilman’s фармакологическая основа терапии
,1996
9-е издНью-Йорк
McGraw-Hill
(стр.581
—600
) 15,,.Неэффективность перорального терфенадина при естественной простуде: доказательства против гистамина как посредника симптомов простуды
,Pediatr Infect Dis J
,1988
, vol.7
(стр.215
—42
) 16,.Оценка перорального применения терфенадина для лечения простуды
,Ann Allergy
,1991
, vol.67
(стр.593
—7
) 17,.Эффективность терфенадина при лечении простуды: двойное слепое сравнение с плацебо
,Eur J Pharmacol
,1988
, vol.34
(стр.35
—40
) 18,.Антигистаминные препараты девяностых
,Clin Rev Allergy
,1993
, vol.11
(стр.111
—53
) 19,,.Влияние вариации сигнала, смещения, шума и величины эффекта на статистическую значимость в исследованиях лечения простуды
,Antiviral Res
,1996
, vol.29
(стр.287
—95
) 20« и др..Обновленные рекомендации по тестированию на безопасность вирусных инокулятов, используемых в добровольных экспериментах на риновирусных простудных заболеваниях.
,Прогресс в медицинской вирусологии. Vol 39
,1992
Basel
Karger
(стр.256
—63
) 21,,,. ,.Риновирус
,Диагностические процедуры для вирусных, риккетсиозных и хламидийных инфекций
,1989
, т.142
6-е издВашингтон, округ Колумбия
Американская ассоциация общественного здравоохранения
(стр.811
—5
) 22,,,.Передача простуды добровольцам в контролируемых условиях. I. Простуда как клиническое проявление
,Arch Intern Med
,1958
, vol.101
(стр.267
—78
) 23,,,,,.Двойное слепое плацебо-контролируемое клиническое испытание влияния хлорфенирамина на реакцию носовых дыхательных путей, среднего уха и евстахиевой трубы на провокационную риновирусную инфекцию
,Pediatr Infect Dis J
,1988
, vol.7
(стр.229
—38
) 24,.Нейронные механизмы чихания
,Am J Physiol
,1975
, vol.229
(стр.770
—6
) 25,,,.Область ствола мозга, вызывающая чихание
,Brain Research
,1990
, vol.511
(стр.265
—70
) 26,,.Неспособность чихать как проявление новообразования костного мозга
,Неврология
,1991
, т.41
(стр.1675
—6
) 27,.Кашель и другие респираторные рефлексы
,Прогресс в респираторных исследованиях. Vol. 23
,1979
Базель, Швейцария
Karger
(стр.218
—23
) 28,.Световой рефлекс чихания: обзор и обсуждение литературы
,Неврология
,1993
, vol.43
(стр.868
—71
) 29.Чихание: его физиология и лечение
,Глаз Ухо Нос Горло Пн
,1975
, vol.54
(стр.449
—53
) 30,. ,.Нос и инфекция
,Нос: физиология верхних дыхательных путей и атмосферная среда
,1982
Амстердам
Elsevier Biomedical
(стр.399
—422
) 31,. ,,,,.Агонисты и антагонисты мускариновых рецепторов
,Goodman & Gilman’s фармакологические основы терапии
,1996
9th edNew York
McGraw-Hill
(стр.141
—60
)© 2001 Американское общество инфекционных болезней
Вариантный эффект антигистаминных препаратов первого и второго поколения как ключ к разгадке механизма их действия на рефлекс чихания при простуде | Клинические инфекционные болезни
Абстракция
Лечение антигистаминными препаратами первого поколения уменьшает чихание, ринорею, массу носовой слизи и, в некоторых случаях, кашель у субъектов с экспериментальной или естественной простудой; однако лечение антигистаминными препаратами второго поколения не было эффективным при этих жалобах в испытаниях с участием субъектов с естественной простудой.В этой статье сообщается об отрицательных результатах клинического исследования лоратадина, антигистаминного препарата второго поколения, у взрослых на модели заражения риновирусом. Это открытие в строго контролируемых условиях модели заражения подтверждает более ранние отрицательные исследования антигистаминных препаратов второго поколения при естественных простудных заболеваниях. Антигистаминные препараты первого поколения блокируют как гистаминовые, так и мускариновые рецепторы, а также преодолевают гематоэнцефалический барьер. Антигистаминные препараты второго поколения в основном блокируют гистаминовые рецепторы и не проникают через гематоэнцефалический барьер.Эффективность антигистаминных препаратов первого поколения в блокировании чихания при простуде может быть связана в первую очередь с нейрофармакологическими манипуляциями с гистаминовыми и мускариновыми рецепторами в продолговатом мозге.
Индивидуальные симптомы простуды обусловлены множественными и в некоторой степени специфическими путями воспаления [1]. Считается, что чихание является результатом высвобождения гистамина из тучных клеток носа и базофилов, которые активируются вирусной инфекцией простуды. Это мнение подтверждается данными о том, что интраназальное введение гистамина у нормальных добровольцев вызывало чихание, тогда как интраназальное воздействие других медиаторов — нет [2].Кроме того, лечение антигистаминными препаратами первого поколения очень эффективно для уменьшения чихания у пациентов с экспериментальной и естественной простудой [3–5]. Поэтому удивительно, что, в отличие от аллергического ринита, у пациентов с простудой не повышается уровень гистамина в носовых секретах [6–9], хотя сообщается о повышении чувствительности слизистой оболочки носа к гистамину [10–13].
Антигистаминные препараты первого и второго поколения являются конкурентными антагонистами гистамина на участке h2-рецептора [14].Дополнительной фармакологической активностью антигистаминных препаратов первого, но не второго поколения, является конкурентный антагонизм ацетилхолина в отношении нейрональных и нервно-мышечных мускариновых рецепторов. Антигистаминные препараты первого поколения также проникают через гематоэнцефалический барьер и, таким образом, обладают потенциалом активности в головном мозге; антигистаминные препараты второго поколения — нет. При ограниченном тестировании и несмотря на их активность по блокированию H2, антигистаминные препараты второго поколения оказались неэффективными в подавлении чихания у пациентов с естественной простудой [15–18].
Эти данные поднимают интересный вопрос о механизме действия антигистаминных препаратов первого поколения на уменьшение чихания у пациентов с простудой и о неэффективности антигистаминных препаратов второго поколения в этой ситуации. Кроме того, исследования естественного холода связаны с определенными техническими проблемами, такими как трудности с включением пациентов на ранних стадиях простуды, когда эффективность лечения измеряется наиболее точно [19]. Поэтому было бы желательно подтвердить результаты исследований естественного холода путем тестирования антигистаминного препарата второго поколения на модели заражения риновирусом, что обеспечивает более высокую точность измерения чихания.В этой статье сообщается о клиническом испытании антигистаминного препарата второго поколения, лоратадина, у взрослых с экспериментальной риновирусной простудой, а также рассматриваются возможные участки действия антигистаминных препаратов первого и второго поколения. Хотя исследование изначально было разработано для определения того, снижает ли лоратадин путем подавления экспрессии молекулы межклеточной адгезии-1 (ICAM-1) на эпителиальных клетках носа уровень риновирусной инфекции, оно предоставляет ранее отсутствующую информацию о результатах тестирования второго поколения антигистаминный препарат в режиме вирусного заражения.
Материалы и методы
Субъекты . В исследовании приняли участие 66 взрослых добровольцев из Шарлоттсвилля, штат Вирджиния, с титрами нейтрализующих антител ≤2 к риновирусу типа 16. Субъекты должны были не иметь симптомов простуды и лихорадки (> 37,8 ° C) в течение 1 недели до включения в испытание и не иметь в анамнезе гиперчувствительности к антигистаминным препаратам. Кроме того, исключались пациенты, если у них был (или имелся в анамнезе) аллергический ринит, бронхиальная астма или другие заболевания нижних дыхательных путей, такие как хроническая обструктивная болезнь легких или эмфизема легких.Исключались субъекты с историей злоупотребления алкоголем и наркотиками, а также добровольцы, которые принимали исследуемые препараты в течение 30 дней, антигистаминные препараты и / или препараты от простуды в течение 14 дней, ингибиторы моноаминоксидазы в течение 7 дней, астемизол в течение 90 дней или любые другие лекарства. думал, что мешает изучению препарата. Другие критерии исключения включали беременность или период лактации, глаукому, а также почечные, печеночные, эндокринные, пищеварительные, мочеполовые, неврологические или психологические заболевания. Протокол был рассмотрен Комитетом по исследованиям человека Университета Вирджинии.
Исследуемый препарат . Лоратадин применялся в таблетках по 10 мг. Таблетки плацебо были идентичны таблеткам лоратадина, но содержали фармакологически инертные ингредиенты.
Вирусный вызов . Интраназальное заражение риновирусом типа 16 выполняли крупными каплями с использованием 0,5 мл (0,25 мл на ноздрю) пула инокулята, содержащего 100 инфекционных доз 50 / мл (TCID 50 / мл) вируса для культуры ткани. Пробу выполняли дважды с 20-минутным интервалом между испытаниями.Пул посевного материала был протестирован на безопасность от посторонних агентов [20].
Меры по заражению . Смывы из носа собирали за 8 дней до и непосредственно перед инокуляцией контрольного вируса, чтобы определить, были ли субъекты инфицированы вирусом дикого типа. После заражения вирусом каждое утро перед введением лекарства собирали смывы из носа. Смывки культивировали на риновирус в течение 5 дней после заражения эмбриональными клетками легких человека (WI-38).Изоляты были идентифицированы как риновирус типа 16 путем нейтрализации типоспецифическим антителом. Венозную кровь брали за 7 дней до лечения и через 14–21 день после интраназальной инокуляции для измерения гомотипических нейтрализующих антител [21].
Меры по оценке болезни . Наличие и тяжесть симптомов определяли ежедневно, начиная с первого дня лечения, за 7 дней до заражения вирусом, в общей сложности в течение 13 дней. Данные о симптомах собирались непосредственно перед введением лоратадина или плацебо медсестрой, которая записывала оценку субъектом тяжести симптомов за предшествующие 24 часа по 5-балльной шкале (0 — «нет»; 1 — «легкая»; 2 , «Умеренная»; 3 — «тяжелая»; 4 — «очень тяжелая») [22].Оцениваемые симптомы включали чихание, насморк, заложенность носа, боль в горле, кашель, головную боль, недомогание и озноб. Общий балл симптомов определяли путем сложения баллов тяжести симптомов в течение 5-дневного периода после вирусного заражения. Оценка для каждого симптома, присутствующего непосредственно перед заражением, вычиталась из каждой из ежедневных оценок для этого симптома.
Оценка тяжести заболевания также включала ежедневные измерения массы носового секрета [23]. Каждый испытуемый ежедневно записывал количество кашля и чихания.Измерения назальной секреции и подсчет кашля и чихания начинали после того, как субъекты были помещены в отель после заражения. Перед тем, как покинуть отель в последний день, испытуемых спрашивали, не простужались ли они, по их мнению,. Информация о возникновении и серьезности любых побочных эффектов собиралась ежедневно и оценивалась как «нет», «легкая», «умеренная» или «тяжелая».
Опытный образец . Испытание представляло собой 13-дневное одноцентровое рандомизированное двойное слепое плацебо-контролируемое исследование в параллельных группах с участием здоровых добровольцев в возрасте 18–40 лет любого пола.Лоратадин или плацебо вводили каждое утро между 6 часами утра. и 8 часов утра, в дни 1–13 исследования, с вирусным заражением на 8 день. Субъекты были случайным образом распределены для получения лечения или плацебо, и их статус лечения не учитывался, как и наблюдатели, записывающие клиническую информацию.
Анализ данных . Для сравнения пропорций использовался точный критерий Фишера. Тест t использовался для сравнения порядковых и интервальных данных.Результаты вероятностного тестирования были двусторонними.
Результаты
Субъекты . Из 66 включенных в исследование субъектов 34 получали лоратадин, а 32 — плацебо. Четыре субъекта в группе лоратадина и один в группе плацебо были инфицированы диким штаммом риновируса на момент включения в исследование. Они были исключены из оценки, как и 1 субъект плацебо, который прекратил прием лекарств после развития мигренозной головной боли на 10 день, оставив 60 оцениваемых субъектов для анализа.
Уровень заражения . Двадцать восемь (93%) из 30 субъектов, получавших лоратадин, и 24 (80%) из 30 субъектов, получавших плацебо, выделяли контрольный вирус в носовую жидкость в течение ≥1 дня ( P = 0,25; таблица 1). Среднее количество дней, в течение которых выделялся вирус, было одинаковым для всех зараженных добровольцев и для всех инфицированных добровольцев в 2 группах. Гомотипические ответы антител наблюдались у 12 (40%) из 30 субъектов, получавших лоратадин, и у 11 (37%) из 30 субъектов, получавших плацебо.Частота инфицирования (выделение вируса и / или повышение уровня антител) составляла 29 (97%) из 30 в группе лоратадина и 24 (80%) из 30 в группе плацебо ( P = 0,1).
Таблица 1
Показатели инфицирования и заболеваемости взрослых экспериментальными риновирусными простудными заболеваниями, получавших лоратадин или плацебо.
Таблица 1
Показатели инфицирования и заболеваемости среди взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Титры вирусов .Как и ожидалось, средние геометрические титры вируса достигли пика на второй день после заражения вирусом (фигура 2А). Титры вирусов были одинаковыми в 2 группах, хотя наблюдалась тенденция к снижению титров в группе плацебо на 2-й день.
Рисунок 2
Геометрические средние (± SE) вирусные титры, средние (± SE) массы носовой слизи и средние (± SE) баллы симптомов у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Рис. 2
Геометрические средние (± SE) титры вирусов, средние (± SE) массы носовой слизи и средние (± SE) баллы симптомов у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Возникновение болезни . Двадцать три (79%) из 29 инфицированных субъектов, получавших лоратадин, и 14 (58%) из 24 инфицированных субъектов, получавших плацебо, соответствовали модифицированным критериям Джексона для болезни ( P = 0,2).
Оценка симптомов 9000 4. Средние (± SE) баллы тяжести чихания были аналогичными в течение первых 3 дней и имели тенденцию к снижению в группе плацебо на четвертый день (рисунок 1). Средние (± стандартная ошибка) общие баллы симптомов были одинаковыми в 2 группах (рис. 2В).Показатели ринореи, как правило, были ниже в группе плацебо на 2 и 3 дни, но обратная картина наблюдалась на 4 и 5 дни (рисунок 2D). Средние (± SE) показатели обструкции носа, боли в горле и кашля были одинаковыми в двух группах (рисунок 2C, рисунок 2F, рисунок 2G). Средние (± SE) баллы по шкале головной боли и недомогания в последние дни болезни были ниже в группе лоратадина (рисунок 2H, рисунок 2I).
Рисунок 1
Средние (± SE) баллы тяжести чихания у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Рисунок 1
Средние (± SE) баллы тяжести чихания у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Масса слизи из носа . Наблюдалась устойчивая тенденция к снижению веса назального секрета в группе плацебо (рисунок 2C). Общее среднее значение ± стандартная ошибка (стандартная ошибка) массы носовой слизи за 5 дней составило 27,1 ± 4,0 г для группы лоратадина и 19,7 ± 5,2 г для группы плацебо ( P = 0,3).
Уровни ICAM-1 .Средние (± SE) уровни ICAM-1 в носовой жидкости выросли по сравнению с исходным уровнем на 2-й день и достигли пика на 3-й день. Уровни были одинаковыми в обеих группах (рис. 3).
Рисунок 3
Средние (± SE) уровни ICAM-1 в носовой жидкости у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Рисунок 3
Средние (± SE) уровни ICAM-1 в носовой жидкости у взрослых с экспериментальной риновирусной простудой, получавших лоратадин или плацебо.
Неблагоприятные события .У одного субъекта в группе плацебо была мигрень и рвота, а у другого — рвота. В остальном о нежелательных явлениях не сообщалось.
Обсуждение
Что касается первоначальной цели исследования, не наблюдалось различий между группами, получавшими лоратадин, и группами, получавшими плацебо, по скорости выделения вируса, титрам вирусов, общей частоте инфицирования, частоте заболеваний или количеству симптомов. Уровни ICAM-1 в назальном секрете в 2 группах также были сходными.
Результаты также показали отсутствие терапевтического эффекта лоратадина при чихании. Это подтверждает более раннюю работу с пациентами с естественной простудой, у которых антигистаминные препараты второго поколения были неэффективны в снижении чихания [15–18]. Почему антигистаминные препараты первого поколения эффективны для уменьшения чихания при простуде [3, 5], а антигистаминные препараты второго поколения не представляют интереса. Антигистаминные препараты первого поколения, помимо их способности блокировать h2-рецепторы, также блокируют мускариновые рецепторы и преодолевают гематоэнцефалический барьер [14].Антигистаминные препараты второго поколения представляют собой специфические блокаторы H2-рецепторов без других признанных фармакологических свойств и не проникают через гематоэнцефалический барьер.
Информация о неврологических путях рефлекса чихания поступает в основном из работы на животных [24, 25]. Рефлекс чихания проходит по периферическим нервам и через продолговатый мозг. Нейрофармакология чихания включает H2, мускариновые и никотиновые рецепторы. При простуде рефлекс чихания начинается в носу с инфицирования носовых клеток вирусом простуды (рис. 4).Нет никаких доказательств того, что активация базофилов и тучных клеток с высвобождением гистамина происходит при простудных заболеваниях; однако предполагается, что свободные нервные окончания решетчатой ветви тройничного нерва стимулируются медиаторами воспаления, такими как брадикинин [1]. Затем нервный импульс проходит по афферентным нервным волокнам к сенсорному ядру тройничного нерва в продолговатом мозге и достигает соседнего центра чихания [26–28]. Затем через другой синапс импульс поступает в верхнее парасимпатическое слюнное ядро лицевого нерва.Здесь он пересекает синапс и перемещается по преганглионарным волокнам большого каменистого нерва к клиновидно-небному ганглию. Этот путь передачи при чихании подтверждается тем фактом, что инъекция алкоголя в клиновидно-небный ганглий блокирует рефлекс чихания [29]. Затем импульс проходит через другой синапс (в основном никотиновый, отчасти мускариновый) и через постганглионарные волокна к синапсам (мускариновым) слизистых желез и кровеносных сосудов, которые затем стимулируются. Возникающая в результате секреция желез и транссудация сосудов рестимулируют свободные нервные окончания тройничного нерва, по которому импульс перенаправляется к ядру тройничного нерва, а затем к центру чихания в продолговатом мозге.Когда рестимуляции центра чихания достаточно, импульс затем направляется интрамедуллярными волокнами в синапсы нескольких дыхательных центров в ретикулярной формации, а оттуда — в синапсы дыхательных нейронов блуждающего, диафрагмального и межреберных нервов. Затем через никотиновые синапсы нервный импульс стимулирует мышечные сокращения, ответственные за чихание.
Рисунок 4
Путь рефлекса чихания
Рисунок 4
Путь рефлекса чихания
Нос — это первое место, где гистамин может участвовать в патогенезе чихания и где антигистаминные препараты могут подавлять рефлекс чихания.H2-рецепторы присутствуют на свободных нервных окончаниях тройничного нерва [30]. Против возможности того, что слизистая оболочка носа является основным местом действия антигистаминных препаратов первого поколения, является открытие, что не было обнаружено повышения уровня гистамина в носовых секретах во время простуды [6–9]. Кроме того, в более ранних исследованиях естественного холода и в текущем исследовании антигистаминные препараты второго поколения, несмотря на то, что они достигают слизистой оболочки носа и обладают активностью блокирования h2, оказались неэффективными для уменьшения чихания [15–18]; однако, поскольку слизистая оболочка носа, по-видимому, имеет повышенную чувствительность к гистамину во время простуды [10,1–13], нельзя полностью исключить роль носовых участков.
Следующее возможное место для антигистаминного препарата первого поколения, блокирующего чихание, находится в продолговатом мозге, где синаптические соединения присутствуют в нескольких местах. И h2, и мускариновые рецепторы были идентифицированы в определенных областях мозга [14, 31]. Такие рецепторы могут быть потенциальными мишенями для действия антигистаминных препаратов первого, но не второго поколения; однако синаптические медиаторы, которые участвуют в рефлексе чихания в продолговатом мозге, не охарактеризованы.Наблюдаемая неспособность антигистаминных препаратов второго поколения уменьшить чихание при простуде подтверждает возможность важности этих участков.
Мускариновая активность отвечает исключительно за парасимпатическую стимуляцию секреции желез и расширение сосудов с последующей транссудацией. Ожидается, что антихолинергическая активность антигистаминных препаратов первого поколения будет действовать на этих участках. Это подтверждается документально подтвержденным эффектом антигистаминных препаратов первого поколения по уменьшению объема выделения жидкости из носа во время простуды [3, 4].Второй афферентный импульс к мозговому веществу снова инициируется раздражением свободных нервных окончаний тройничного нерва. Транссудация сосудов приводит к высвобождению кининогена с образованием кинина [14]. Это событие предоставляет средства для прямой стимуляции свободных нервных окончаний кининами, а также гистамином, высвобождаемым из тучных клеток при стимуляции кининами. Это обеспечивает еще одну возможную мишень для действия антигистаминного препарата. Кроме того, когда нервный импульс перенаправляется к мозговому веществу, h2 и мускариновые синаптические участки могут блокироваться антигистаминными препаратами первого поколения, как описано выше.С этого момента, когда в процесс вовлекаются мотонейроны, передача по нервам зависит от никотинергических рецепторов и, следовательно, не будет восприимчива к действию антигистаминных препаратов.
Этот анализ предполагает, что важное место терапевтического действия антигистаминных препаратов первого поколения на чихание находится в продолговатом мозге, где могут быть задействованы как h2, так и мускариновые рецепторы. Известно, что рецепторы h2 присутствуют в высоких концентрациях в гипоталамусе, где гистамин действует как нейромедиатор, помогая регулировать уровень бодрствования [14].Этим объясняется сонливость, связанная с использованием антигистаминных препаратов первого поколения. Из-за высокой концентрации рецепторов h2 в гипоталамусе и из-за того, что парасимпатические нервные волокна возникают из гипоталамуса и активируются им, вероятно, что гистамин играет роль в передаче сигнала в этой области.
Известно также, что антигистаминные препараты первого поколения помогают уменьшить тошноту, связанную с укачиванием [31]. Скополамин, антихолинергический препарат, который проникает через гематоэнцефалический барьер, является эффективным средством лечения укачивания, тогда как атропин, который не так легко проникает через гематоэнцефалический барьер, не эффективен.Противошумный эффект скополамина частично зависит от блокирования мускариновых рецепторов вестибулярных ядер и постремной зоны головного мозга. Другие ядра ствола мозга также могут использовать систему мускариновых рецепторов, что подтверждает идею о том, что мускариновые рецепторы в ЦНС являются частью рефлекса чихания. В настоящее время не имеется полной информации о мозговых синапсах и нейротрансмиттерах, участвующих в рефлексе чихания, и в этой области необходимы дальнейшие исследования; однако имеющаяся информация свидетельствует о том, что для эффективного лечения чихания при простуде необходимы соединения, которые преодолевают гематоэнцефалический барьер и обладают активностью блокирования как h2, так и мускаринов.
Список литературы
1,. ,,.Риновирус
,Клиническая вирусология
,1997
Нью-Йорк
Черчилль Ливингстон
(стр.1025
—47
) 2,,.Физиологические реакции на интраназальное дозозависимое введение гистамина, метахолина, брадикинина и простагландина у взрослых добровольцев с назальной аллергией и без нее
,J Allergy Clin Immunol
,1990
, vol.86
(стр.924
—35
) 3,.Эффективность лечения риновирусной простуды бромфенирамина малеатом
,Clin Infect Dis
,1997
, vol.25
(стр.1188
—94
) 4,,,,,.Рандомизированное контролируемое исследование клемастина фумарата для лечения экспериментальных риновирусных простуд
,Clin Infect Dis
,1996
, vol.22
(стр.656
—62
) 5« и др.Эффективность клемастина фумарата для лечения ринореи и чихания, связанных с простудой
,Clin Infect Dis
,1997
, vol.25
(стр.824
—30
) 6,,,,.Гистамин в назальном секрете
,Int Arch Allergy Appl Immunol
,1978
, vol.57
(стр.193
—200
) 7,,,,,.Ответственен ли гистамин за симптомы риновирусной простуды: посмотрите на медиаторы воспаления после инфекции
,Pediatr Infect Dis J
,1988
, vol.7
(стр.218
—22
) 8,,,,,.Анализ назального секрета при экспериментальных риновирусных инфекциях верхних дыхательных путей
,J Allergy Clin Immunol
,1993
, vol.92
(стр.722
—31
) 9,.Уровень гистамина в назальном секрете и сыворотке может быть повышен при вирусной инфекции дыхательных путей
,Int Arch Allergy Appl Immunol
,1982
, vol.67
(стр.380
—3
) 10,,, et al.Экспериментальная инфекция риновирусом 16 усиливает высвобождение гистамина после бронхопровокации антигена у субъектов с аллергией
,Am Rev Respir Dis
,1991
, vol.144
(стр.1267
—73
) 11,,, et al.Зеркало-сосудистая экссудативная гиперреактивность при простуде, вызванной коронавирусом человека
,Thorax
,1994
, vol.49
(стр.121
—7
) 12,,,,.Влияние экспериментальной инфекции риновирусом 39 на назальную реакцию на гистамин и воздействие холодного воздуха у субъектов с аллергией и неаллергией
,J Allergy Clin Immunol
,1994
, vol.93
(стр.534
—42
) 13.Вирусные инфекции и аллергические заболевания
,Clin Exper Allergy
,1991
, vol.1
(S21)
(стр.68
—71
) 14,. ,,,,.Гистамин, брадикинин и их антагонисты
,Goodman & Gilman’s фармакологическая основа терапии
,1996
9-е издНью-Йорк
McGraw-Hill
(стр.581
—600
) 15,,.Неэффективность перорального терфенадина при естественной простуде: доказательства против гистамина как посредника симптомов простуды
,Pediatr Infect Dis J
,1988
, vol.7
(стр.215
—42
) 16,.Оценка перорального применения терфенадина для лечения простуды
,Ann Allergy
,1991
, vol.67
(стр.593
—7
) 17,.Эффективность терфенадина при лечении простуды: двойное слепое сравнение с плацебо
,Eur J Pharmacol
,1988
, vol.34
(стр.35
—40
) 18,.Антигистаминные препараты девяностых
,Clin Rev Allergy
,1993
, vol.11
(стр.111
—53
) 19,,.Влияние вариации сигнала, смещения, шума и величины эффекта на статистическую значимость в исследованиях лечения простуды
,Antiviral Res
,1996
, vol.29
(стр.287
—95
) 20« и др..Обновленные рекомендации по тестированию на безопасность вирусных инокулятов, используемых в добровольных экспериментах на риновирусных простудных заболеваниях.
,Прогресс в медицинской вирусологии. Vol 39
,1992
Basel
Karger
(стр.256
—63
) 21,,,. ,.Риновирус
,Диагностические процедуры для вирусных, риккетсиозных и хламидийных инфекций
,1989
, т.142
6-е издВашингтон, округ Колумбия
Американская ассоциация общественного здравоохранения
(стр.811
—5
) 22,,,.Передача простуды добровольцам в контролируемых условиях. I. Простуда как клиническое проявление
,Arch Intern Med
,1958
, vol.101
(стр.267
—78
) 23,,,,,.Двойное слепое плацебо-контролируемое клиническое испытание влияния хлорфенирамина на реакцию носовых дыхательных путей, среднего уха и евстахиевой трубы на провокационную риновирусную инфекцию
,Pediatr Infect Dis J
,1988
, vol.7
(стр.229
—38
) 24,.Нейронные механизмы чихания
,Am J Physiol
,1975
, vol.229
(стр.770
—6
) 25,,,.Область ствола мозга, вызывающая чихание
,Brain Research
,1990
, vol.511
(стр.265
—70
) 26,,.Неспособность чихать как проявление новообразования костного мозга
,Неврология
,1991
, т.41
(стр.1675
—6
) 27,.Кашель и другие респираторные рефлексы
,Прогресс в респираторных исследованиях. Vol. 23
,1979
Базель, Швейцария
Karger
(стр.218
—23
) 28,.Световой рефлекс чихания: обзор и обсуждение литературы
,Неврология
,1993
, vol.43
(стр.868
—71
) 29.Чихание: его физиология и лечение
,Глаз Ухо Нос Горло Пн
,1975
, vol.54
(стр.449
—53
) 30,. ,.Нос и инфекция
,Нос: физиология верхних дыхательных путей и атмосферная среда
,1982
Амстердам
Elsevier Biomedical
(стр.399
—422
) 31,. ,,,,.Агонисты и антагонисты мускариновых рецепторов
,Goodman & Gilman’s фармакологические основы терапии
,1996
9th edNew York
McGraw-Hill
(стр.141
—60
)© 2001 Американское общество инфекционных болезней
Определение, типы и побочные эффекты
Антигистаминные препараты — это класс лекарств, обычно используемых для лечения симптомов аллергии. Эти препараты помогают лечить состояния, вызванные слишком большим количеством гистамина — химического вещества, вырабатываемого иммунной системой вашего организма. Антигистаминные препараты чаще всего используют люди, у которых есть аллергические реакции на пыльцу и другие аллергены.Они также используются для лечения множества других состояний, таких как проблемы с желудком, простуды, беспокойство и многое другое.
Что такое аллергия?
Ваше тело защищает вас от многих угроз. Ребра защищают сердце и легкие от травм. Ваша кожа защищает ваше тело от внешних факторов, таких как солнце, ветер и бактерии, которые могут вызывать болезни и инфекции. Ресницы защищают глаза от мусора. А внутренняя система защиты вашего тела — ваша иммунная система — борется с веществами, которые попадают в ваш организм и считаются «чужеродными».”
Аллергия возникает, когда ваша иммунная система чрезмерно реагирует на «чужеродное» вещество. В случае аллергии вас беспокоят вещества, которые обычно безвредны и не беспокоят некоторых людей, такие как пыль или шерсть животных! Ваше тело рассматривает эти вещества как «чужеродные», что затем вызывает чрезмерную реакцию защитной системы вашего тела, которая включает выброс гистамина. Вещества, вызывающие чрезмерную реакцию, называются аллергенами. Возникающие при этом симптомы называются аллергической реакцией.
Аллергия — одно из самых распространенных хронических заболеваний в мире. Они есть у 40-50 миллионов человек в Соединенных Штатах.
Что такое гистамин?
Гистамин — это важное химическое вещество, которое участвует во многих различных процессах в организме. Он стимулирует секрецию желудочного сока, участвует в воспалении, расширяет кровеносные сосуды, влияет на сокращение мышц в кишечнике и легких и влияет на частоту сердечных сокращений. Он также помогает передавать сообщения между нервными клетками и помогает жидкости перемещаться через стенки кровеносных сосудов.Гистамин также выделяется, если ваше тело сталкивается с угрозой со стороны аллергена. Гистамин вызывает набухание и расширение сосудов, что приводит к симптомам аллергии.
Какие вещества или аллергены вызывают аллергию?
Восемь самых распространенных вещей, которые могут вызвать аллергическую реакцию у некоторых людей, включают:
- Еда.
- Пыль.
- Пыльца.
- Перхоть домашних животных, слюна или моча.
- Mold.
- Укусы и укусы насекомых.
- Латекс.
- Некоторые лекарства / лекарства.
Какие аллергические симптомы вызывают гистамины?
Слишком много гистамина, вызванное чрезмерной чувствительностью вашего организма и чрезмерной реакцией на аллерген, вызывает множество симптомов. Симптомы включают:
- Застой, кашель.
- Хрипы, одышка.
- Усталость (утомляемость).
- Кожный зуд, крапивница и другие кожные высыпания.
- Зудящие, красные, слезящиеся глаза.
- Насморк, заложенность носа или чихание.
- Бессонница.
- Тошнота и рвота.
Что такое антигистаминные препараты?
Антигистаминный препарат — это лекарство, отпускаемое по рецепту или без рецепта, которое блокирует некоторые функции гистамина. «Анти» означает «против», поэтому антигистаминные препараты — это лекарства, которые действуют против или блокируют гистамин.
Как классифицируются антигистаминные препараты?
Антигистаминные препараты делятся на два основных подтипа. Первый подтип называется антагонистами рецептора H-1 или блокаторами H-1.Этот подтип антигистаминных препаратов используется для лечения симптомов аллергии. Второй подтип называется антагонистами рецептора H-2 или блокаторами H-2. Они используются для лечения желудочно-кишечных заболеваний, включая гастроэзофагеальную рефлюксную болезнь [ГЭРБ] (также называемую кислотным рефлюксом), пептические язвы, гастрит, укачивание, тошноту и рвоту. Структура наименования (H-1 и H-2) сообщает врачам и ученым о типе клеток и местонахождении рецептора гистамина, который блокирует антигистаминный препарат.
Подтип блокаторов H-1 подразделяется на две группы — антигистаминные препараты первого поколения и антигистаминные препараты второго поколения.
В чем разница между антигистаминными препаратами первого и второго поколения?
Как следует из названия, антигистаминные препараты первого поколения были одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA). Они начали утверждаться в Соединенных Штатах в 1930-х годах и применяются до сих пор.
Они воздействуют на рецепторы гистамина в головном и спинном мозге вместе с другими типами рецепторов. Наиболее примечательным в этом поколении антигистаминных препаратов является то, что они проникают через гематоэнцефалический барьер, что приводит к сонливости.
Антигистаминные препараты второго поколения были одобрены FDA и впервые появились на рынке в 1980-х годах. Антигистаминные препараты второго поколения не проникают через гематоэнцефалический барьер в такой степени, как антигистаминные препараты первого поколения, и поэтому не вызывают сонливость при стандартных дозировках. Антигистаминные препараты второго поколения считаются более безопасными, чем антигистаминные препараты первого поколения, поскольку они не вызывают сонливость и взаимодействуют с меньшим количеством лекарств.
Каковы некоторые примеры антигистаминных препаратов H-1 первого и второго поколения и блокаторов H-2?
Существует множество рецептурных и безрецептурных антигистаминных препаратов H-1.Если у вас аллергия, вы, вероятно, принимаете антигистаминный препарат H-1. Вот несколько примеров безрецептурных и рецептурных блокаторов H-1 первого поколения:
Вот несколько примеров безрецептурных и рецептурных блокаторов H-1 второго поколения:
Если вы принимаете антигистаминные препараты для лечения проблем с желудком, вы, скорее всего, принимаете антигистаминный препарат H-2. Вот несколько примеров антигистаминных препаратов H-2:
Какие еще заболевания лечат антигистаминные препараты, помимо аллергии?
Лечение антигистаминными препаратами H-1:
- Аллергический ринит / сенная лихорадка.
- Аллергический конъюнктивит.
- Крапивница и другие кожные высыпания.
- Простуда.
- Пищевая аллергия.
- Повышенная чувствительность к некоторым лекарствам.
- Укусы и укусы насекомых.
Антигистаминные препараты H-1 первого поколения также лечат:
- Бессонница.
- Морская болезнь.
- Беспокойство.
Лечение антигистаминными препаратами H-2:
- Изжога.
- Гастроэофагеальная рефлюксная болезнь (ГЭРБ).
- Язвы двенадцатиперстной кишки и желудка.
- Синдром Золлингера-Эллисона.
Другие состояния, которые лечат антигистаминные препараты, включают:
- Анорексия.
- Головные боли.
- Анафилаксия.
- Головокружение.
- Болезнь Паркинсона (для уменьшения жесткости и тремора).
- Некоторые виды боли в костях.
Ваш лечащий врач может назначить антигистаминные препараты даже при других заболеваниях.
Каковы побочные эффекты антигистаминных препаратов?
Вы и ваш лечащий врач должны обсудить конкретные антигистаминные препараты и вместе решить, перевешивают ли потенциальные преимущества антигистаминных препаратов его потенциальные побочные эффекты.
Некоторые из распространенных побочных эффектов антигистаминных препаратов первого поколения включают:
- Сонливость.
- Сухость во рту, сухость в глазах.
- Затуманенное или двоение в глазах.
- Головокружение и головная боль.
- Низкое артериальное давление.
- Утолщение слизистой в дыхательных путях.
- Учащенное сердцебиение.
- Затрудненное мочеиспускание и запор.
Некоторые из распространенных побочных эффектов антигистаминных препаратов второго поколения включают:
- Головная боль.
- Кашель.
- Усталость.
- Боль в горле.
- Боль или дискомфорт в животе
- Тошнота или рвота.
Общие побочные эффекты антигистаминных препаратов H-2 включают:
- Сонливость.
- Боль в суставах или мышцах.
- Головная боль.
- Путаница у пожилых людей.
- Головокружение.
- Набухание и болезненность груди.
В каких лекарственных формах доступны антигистаминные препараты?
Антигистаминные препараты бывают нескольких форм, в том числе:
- Жидкости.
- Лосьоны.
- Сиропы.
- гелей.
- Глазные капли.
- Таблетки.
- Спреи назальные.
- Кремы.
- Капсул.
- Суппозитории.
Как узнать, какой антигистаминный препарат принимать?
Поскольку существует так много антигистаминных препаратов, как безрецептурных, так и по рецепту, и поскольку они используются для лечения множества различных состояний, вам может потребоваться помощь в выяснении, какое лекарство принимать.При незначительных недомоганиях, вероятно, можно принимать безрецептурные препараты. Вы можете прочитать этикетку на упаковке и сопоставить свои симптомы с обозначенными симптомами. Кроме того, не стесняйтесь спрашивать фармацевта. Они хорошо осведомлены о действиях, эффектах и побочных эффектах лекарств. Возможно, вам придется попробовать разные антигистаминные препараты (но не более одного за раз, если только ваш врач не назначит вам лечение), чтобы найти лучшее лекарство для лечения ваших симптомов.
Если вам нужен рецептурный антигистаминный препарат, вы и ваш лечащий врач будете работать вместе, чтобы выяснить, какое лекарство подойдет вам лучше всего.Многие лекарства взаимодействуют с антигистаминными препаратами, поэтому ваш лечащий врач захочет знать, какие у вас заболевания и какие лекарства вы принимаете в настоящее время. Они также захотят узнать, беременны ли вы, планируете ли вы забеременеть или кормите грудью. Некоторые антигистаминные препараты не рекомендуются во время беременности, поскольку в очень высоких дозах они могут вызвать врожденные дефекты. Антигистаминные препараты могут проникать в грудное молоко, поэтому вам следует проконсультироваться со своим врачом перед применением антигистаминных препаратов, если вы кормите грудью.
Дети и пожилые люди более чувствительны к действию антигистаминных препаратов, поэтому использование этих продуктов у таких пациентов будет уделено особому вниманию. Никогда не давайте детям младше четырех лет безрецептурные антигистаминные препараты от кашля и простуды. Эти лекарства могут вызывать опасные для жизни побочные эффекты.
Могут ли антигистаминные препараты вызывать лихорадку?
Лихорадка не является одним из побочных эффектов антигистаминных препаратов.
Могут ли антигистаминные препараты вызывать запор?
Да, некоторые антигистаминные препараты, такие как дифенгидрамин, действительно вызывают запор как побочный эффект.
Могут ли антигистаминные препараты вызывать головокружение?
Да. Головокружение — частый побочный эффект некоторых антигистаминных препаратов.
Могут ли антигистаминные препараты вызывать депрессию?
Одно исследование с участием 92 человек с хроническим зудом показало, что пациенты, принимавшие антигистаминные препараты цетиризин и гидроксизин, сообщали об усилении депрессии и тревоги. Влияние всех антигистаминных препаратов на расстройства настроения еще предстоит изучить.
Могут ли антигистаминные препараты вызывать высокое кровяное давление?
Если вы уже принимаете лекарства от высокого кровяного давления, их сочетание с антигистаминными препаратами может увеличить частоту сердечных сокращений и повысить кровяное давление.Поговорите со своим врачом о возможных вариантах.
Могут ли антигистаминные препараты вызывать увеличение веса?
Антигистаминные препараты могут привести к увеличению веса, да. По этой причине используется один антигистаминный препарат ципрогептадин. Известно, что гистамин снижает аппетит, поэтому антигистаминные препараты нейтрализуют его.
Какие антигистаминные препараты можно принимать вместе?
Антигистаминные препараты нельзя комбинировать, если это не рекомендовано вашим лечащим врачом под их руководством и контролем.Антигистаминные препараты следует использовать только по назначению, иначе у вас могут возникнуть серьезные побочные эффекты. Внимательно читайте этикетки.
Что делать, если антигистаминные препараты не действуют?
Поговорите со своим лечащим врачом, фармацевтом или аллергологом, чтобы помочь вам найти способы лечения аллергии. Некоторые аллергии можно лечить с помощью противоотечных средств или иммунотерапии.
Могу ли я принимать антигистаминные препараты, если я беременна или кормлюсь грудью?
Безопаснее всего поговорить со своим врачом, если вы беременны, планируете забеременеть или кормите грудью.Исследования на животных показали, что некоторые антигистаминные препараты могут вызывать врожденные дефекты. Небольшое количество антигистаминных препаратов передается вашему ребенку, если вы кормите его грудью. По этим причинам ваш лечащий врач захочет поговорить с вами и сделать осторожный выбор (или другой выбор), если есть какие-либо опасения за вашу безопасность или безопасность вашего ребенка.
Безопасны ли антигистаминные препараты для собак?
Дифенгидрамин — распространенное лекарство, используемое для лечения аллергии, крапивницы, пищевой аллергии, беспокойства и других состояний у собак.Тем не менее, вам следует проконсультироваться с ветеринаром по поводу использования дифенгидрамина у вашего питомца. Дозировка для собак зависит от их веса, плюс ваш ветеринар захочет осмотреть вашу собаку, чтобы убедиться, что антигистаминный препарат является правильным препаратом для постановки правильного диагноза. Если требуется антигистаминный препарат, ваш ветеринар может прописать препарат, специфичный для животных, и в дозировке, подходящей для вашего питомца.
Вызывают ли антигистаминные препараты деменцию?
Длительный прием некоторых антигистаминных препаратов может повысить риск развития деменции.Дифенгидрамин (Бенадрил®) блокирует действие нейромедиатора ацетилхолина. Этот нейромедиатор жизненно важен для памяти и обучения. Дифенгидрамин увеличивал риск деменции на 54% в одном исследовании на 3000 пациентов, которое длилось семь лет.
Какие вопросы я должен задать своему врачу?
- Какой антигистаминный препарат мне подойдет больше всего?
- Как правильно принимать прописанные антигистаминные препараты?
- Какие побочные эффекты могут возникнуть при приеме рекомендованных лекарств?
- Какой антигистаминный препарат не помешает принимать лекарства, которые я сейчас принимаю?
- Когда и при каких условиях имеет смысл принимать антигистаминные препараты, которые вызывают у меня сонливость?
- Могу ли я нормально жить, принимая это лекарство? Могу я водить машину? Могу ли я работать с тяжелой техникой?
- Могу ли я принимать антигистаминные препараты, если я беременна, планирую забеременеть или кормлю грудью?
- Можно ли безопасно давать моему ребенку антигистаминные препараты?
- Каковы будут последствия, если я не приму антигистаминные препараты для лечения аллергии?
Записка из клиники Кливленда
Гистамин на вашей стороне.Химическое вещество делает все возможное, чтобы регулировать, помогать вашему сердцу и легким и защищать ваше тело от чужеродных аллергенов, среди прочего. Но он может быть сверхчувствительным или чрезмерно острым, и в этом могут помочь антигистаминные препараты. Если у вас аллергия, желудочные симптомы или какие-либо другие состояния и симптомы, упомянутые в этой статье, поговорите со своим врачом о возможных вариантах. Ваши симптомы можно вылечить.
Всегда уточняйте у своего лечащего врача и фармацевта, есть ли у вас опасения по поводу антигистаминных препаратов, и всегда следуйте указаниям на этикетках!
H 1 Антигистаминные препараты: текущее состояние и направления на будущее | Журнал Всемирной организации по аллергии
H
1 антигистаминные препаратыH 1 антигистаминные препараты первого поколения потенциально вызывают широкий спектр побочных эффектов во многих системах организма (таблица 5) [2–4, 20, 40].Однако основная проблема заключается в том, что все антигистаминные препараты первого поколения H 1 , даже при введении в дозах, рекомендованных производителем, имеют склонность влиять на нейротрансмиссию гистамина на рецепторах H 1 в ЦНС. Это потенциально приводит к неблагоприятным симптомам со стороны ЦНС, таким как сонливость, седативный эффект, сонливость, утомляемость и головная боль. Что еще более важно, это потенциально ухудшает когнитивные функции, память и психомоторные функции. Позитронно-эмиссионная томография с [11] C-доксепином в качестве лиганда, излучающего позитроны, показала, что эти препараты занимают более 70% рецепторов H 1 в ЦНС [41].Проникновение через гематоэнцефалический барьер связано с их липофильностью, относительно низкой молекулярной массой и отсутствием распознавания субстрата оттоком P-гликопротеинового насоса, экспрессируемого на просветных поверхностях нефенестрированных эндотелиальных клеток в сосудистой сети ЦНС. Проникновение в центральную нервную систему также задокументировано в рандомизированных контролируемых исследованиях, включающих электроэнцефалографический мониторинг, измерение латентности сна и стандартизованные тесты производительности, начиная от простых тестов на время реакции до сложных сенсомоторных задач, например, вождения под компьютерным контролем [2–4, 10, 42, 43].
Таблица 5 Неблагоприятные эффекты H первого поколения 1 Антигистаминные препараты по сравнению с H второго поколения 1 Антигистаминные препаратыНарушение функции ЦНС от H первого поколения 1 антигистаминных препаратов в обычных дозах было зарегистрировано в отсутствие ЦНС симптомы. Толерантность к неблагоприятным воздействиям на ЦНС не обязательно. После приема одного из этих старых лекарств перед сном у некоторых людей на следующее утро наблюдаются остаточные побочные эффекты со стороны ЦНС, так называемое антигистаминное похмелье.Эффекты ЦНС антигистамина первого поколения H 1 аналогичны эффектам, вызываемым этанолом или другими химическими веществами, действующими на ЦНС, и усугубляются ими [2, 3]. Перспективные долгосрочные рандомизированные контролируемые исследования безопасности этих старых антигистаминных препаратов H 1 никогда не публиковались.
Второе поколение антигистаминных препаратов H
1Напротив, новые антигистаминные препараты H 1 плохо проникают в ЦНС и занимают от 0% (фексофенадин в дозах до 360 мг) до 30% (цетиризин, см. Выше). -помеченные дозы 20 мг) рецепторов H 1 в ЦНС, как подтверждено исследованиями позитронно-эмиссионной томографии.Результаты этих исследований хорошо коррелируют с электроэнцефалографическим мониторингом, включая тесты на задержку сна, и со стандартизованными тестами производительности. Следовательно, антигистаминные препараты второго поколения H 1 имеют низкую вероятность воздействия на ЦНС, хотя некоторые из них, такие как цетиризин и лоратадин, потенциально могут вызывать седативный эффект при превышении рекомендованных производителем доз. Фексофенадин в дозах до 360 мг в день включительно является наименее седативным из этих препаратов и поэтому считается антигистаминным препаратом H 1 , который выбирают пилоты авиакомпаний и люди, нуждающиеся в других критических с точки зрения безопасности условиях [2–4 , 10, 42, 43]
Антигистаминные препараты второго поколения H 1 не усугубляют действие на ЦНС одновременного приема алкоголя или других веществ, действующих на ЦНС.В реальных исследованиях по мониторингу рецептурных событий, проведенных у тысяч людей с аллергическим ринитом в течение первых 30 дней после введения нового антигистаминного препарата H 1 в Соединенном Королевстве, низкий риск седативного действия был зарегистрирован для цетиризина, дезлоратадина, фексофенадина , левоцетиризин и лоратадин [44, 45].
Потенциальная сердечная токсичность антигистаминных препаратов H 1 , возникающая из-за блокады сердечных ионных токов, чаще всего тока I Kr , не является эффектом антигистаминного класса H 1 .После отзыва регулирующих органов для астемизола и терфенадина почти два десятилетия назад используемые антигистаминные препараты второго поколения H 1 не имеют потенциальных побочных эффектов со стороны сердца (таблица 5) [2–4].
Опубликованы рандомизированные контролируемые испытания, подтверждающие долгосрочную безопасность этих препаратов. К ним относятся рандомизированные контролируемые замаскированные исследования продолжительностью от 6 до 12 месяцев с дезлоратадином, фексофенадином и левоцетиризином у взрослых и продолжительностью от 12 до 18 месяцев с цетиризином, левоцетиризином и лоратадином у очень маленьких детей [20, 21, 46 –48].
H
1 -антигистаминные передозировкиПосле передозировки антигистаминными препаратами первого поколения H 1 преобладают симптомы со стороны ЦНС (таблица 5). У взрослых эти симптомы обычно приводят к сильной сонливости, спутанности сознания и коме. У младенцев и детей может возникнуть парадоксальное возбуждение ЦНС с симптомами раздражительности, гиперактивности, бессонницы, галлюцинаций и судорог. Некоторые антигистаминные препараты первого поколения H 1 также потенциально могут вызывать дозозависимые побочные эффекты со стороны сердца, включая синусовую тахикардию, рефлекторную тахикардию, наджелудочковые аритмии и после преднамеренной большой передозировки, например дифенгидрамин 0.От 5 до 1 г зарегистрировано удлинение интервала QT при желудочковых аритмиях и пуантах с торсами [2–5].
Смертельные случаи, приписываемые антигистаминным препаратам первого поколения H 1 , вызванные случайной передозировкой, самоубийством или убийством (младенцев), описаны в литературе уже более шести десятилетий [40]. В токсикологические центры США так часто поступают сообщения о передозировках дифенгидрамина, что для облегчения их лечения были опубликованы научно обоснованные руководства [49].
Массивные (например, до 20-30-кратные) передозировки антигистаминных препаратов второго поколения H 1 , таких как цетиризин, фексофенадин и лоратадин, не были причинно связаны с серьезными нежелательными явлениями со стороны ЦНС или сердечно-сосудистыми заболеваниями или летальными исходами (Таблица 5 ) [2, 3, 34].
Использование антигистаминных препаратов H
1 у пожилых людейПожилые люди имеют повышенную уязвимость к побочным эффектам любых химических веществ, действующих на ЦНС. Широкое использование антигистаминных препаратов первого поколения H 1 не только для лечения аллергического риноконъюнктивита и крапивницы, но также для лечения бессонницы и других клинических проблем вызывает особую озабоченность из-за их способности преодолевать гематоэнцефалический барьер и нарушать нейротрансмиссию в ЦНС. 1 рецепторов и вызывают неблагоприятные эффекты ЦНС, такие как сонливость, спутанность сознания и возбуждение.
Полимедикация распространена среди пожилых людей, поэтому потенциал взаимодействия антигистаминных препаратов первого поколения H 1 с другими лекарственными средствами или растительными продуктами в этой возрастной группе повышен. Потенциальные антимускариновые эффекты, такие как мидриаз, сухость глаз и сухость во рту, задержка мочи, колебание мочеиспускания и запор, а также потенциальные анти- α -адренергические эффекты, такие как головокружение и гипотензия, от антигистаминных препаратов первого поколения H 1 также вызывают беспокойство. (Таблица 5) [2–4, 20].
Использование антигистаминных препаратов H
1 при беременности и кормлении грудьюРегулирующие органы, такие как FDA США и Европейское агентство по лекарственным средствам, тщательно исследуют все лекарства на предмет потенциальной тератогенности. № H 1 Антигистаминные препараты были отнесены к категории A FDA, что означает отрицательные исследования на животных и отрицательные данные на людях. Некоторые антигистаминные препараты H 1 , включая хлорфенирамин, дифенгидрамин, цетиризин, левоцетиризин, лоратадин и офтальмологический состав эмедастина, были определены FDA категории B.Это означает, что либо исследования на животных не показали никаких побочных эффектов, а данные на людях отсутствуют, либо исследования на животных показали побочные эффекты, но исследования на людях не показали этих эффектов. Поэтому эти лекарства считаются относительно безопасными для использования при беременности. Другие антигистаминные препараты H 1 обозначены как Категория C. Это означает, что либо исследования на животных положительны, и данные на людях отсутствуют, либо данные на животных или людях отсутствуют.H 1 антигистаминные препараты, не одобренные для использования в США, например эбастин, мизоластин и рупатадин, не классифицируются FDA (таблица 5) [2, 3].
H 1 антигистаминные препараты выделяются в грудное молоко. Младенцы грудного возраста получают примерно 0,1% от пероральной дозы для матери. Сообщалось, что антигистаминные препараты первого поколения H 1 вызывают седативный эффект и другие побочные эффекты у этих младенцев (таблица 5) [2, 3].
Применение антигистаминных препаратов H
1 у младенцев и детей раннего возрастаАнтигистаминные препараты первого поколения H 1 широко используются у младенцев и маленьких детей не только при аллергическом риноконъюнктивите и крапивнице, но также при простуде, кашле и других недугах , и для облегчения бессонницы.Из-за отсутствия данных об эффективности и опасений по поводу безопасности производителям в США и некоторых других странах настоятельно рекомендуется отозвать отпускаемые без рецепта препараты от простуды и кашля для детей младше 2 лет и добавить предупреждение: «Не применение для успокоения детей », на этикетке препаратов антигистаминного препарата Н 1 первого поколения [5, 50].

 Не проникает в головной мозг, поэтому на нервную систему и психические реакции влияние Эбастина минимально.
Не проникает в головной мозг, поэтому на нервную систему и психические реакции влияние Эбастина минимально.