Множественная миелома | Симптомы и лечение множественной миеломы
Лечение множественнной миеломы
Больные нуждаются в серьезном поддерживающем лечении. Амбулаторная поддерживающая терапия помогает сохранить плотность костной ткани. Анальгетики и паллиативные дозы лучевой терапии (18-24 Гр) могут облегчить боль в костях. Однако лучевая терапия может препятствовать проведению курсовой химиотерапии. Все больные должны также получать бифосфонаты, которые уменьшают риск развития осложнений со стороны скелета, облегчают боль в костях и обладают антиопухолевой активностью.
Адекватная гидратация является профилактикой повреждения почек. Даже больные с длительной, массивной протеинурией Бенс-Джонса (10-30 г/сутки) могут сохранить функцию почек, если они поддерживают диурез более 2000 мл/ сутки. У больных с протеинурией Бенс-Джонса дегидратация, сопровождающая введение высокоосмолярного внутривенного контраста, может вызвать острую почечную недостаточность.
Для лечения гиперкальциемии используются обильная гидратация и бифосфонаты, иногда совместно с преднизолоном 60-80 мг внутрь в сутки. Хотя большинство больных не нуждаются в приеме аллопуринола, прием 300 мг в сутки показан при наличии почечной недостаточности или симптомов гиперурикемии.
Показано проведение профилактической вакцинации против пневмококковой инфекции и гриппа. Назначение антибиотиков производится при документированной бактериальной инфекции и не рекомендуется рутинное профилактическое назначение антибиотиков. Профилактическое введение внутривенного иммуноглобулина может снизить риск инфекционных осложнений, обычно назначается больным с частыми рецидивирующими инфекциями.
Рекомбинантный эритропоэтин (40 000 ЕД подкожно 3 раза в неделю) применяют у больных с анемией, не корригируемой химиотерапией. Если анемия приводит к нарушениям со стороны сердечно-сосудистой системы, используют трансфузии эритроцитной массы. При развитии синдрома гипервязкости проводится плазмаферез. Проведение химиотерапии показано для уменьшения сывороточного или мочевого М-протеина. Постцитостатическая нейтропения может способствовать развитию инфекционных осложнений.
Стандартная химиотерапия обычно состоит из курсов перорального мелфалана [0,15мг/(кг х сут) внутрь] и преднизолона (20 мг 3 раза в день) каждые 6 недель с оценкой ответа через 3-6 месяцев. Полихимиотерапия может проводиться с применением различных режимов с внутривенным введением препаратов. Эти режимы не улучшают долговременную выживаемость по сравнению с комбинацией мелфалана и преднизолона, но могут обеспечивать более быстрый ответ у больных с дисфункцией почек. Проведение аутологичной трансплантации гемопоэтических стволовых клеток показано больным моложе 70 лет с адекватной функцией сердца, печени, легких и почек со стабильным течением болезни или хорошим ответом после нескольких курсов стандартной химиотерапии. Этим больным проводится начальная химиотерапия винкристином, доксорубицином и дексаметазоном или дексаметазоном с талидомидом. При необходимости назначения миелоидного ростового фактора препараты, угнетающие функцию костного мозга, алкилирующие агенты и препараты нитрозомочевины не назначаются. Проведение аллогенной трансплантации с немиелоаблативными режимами кондиционирования (например, низкие дозы циклофосфомида и флударабина или лучевой терапии) у некоторых больных может улучшать выживаемость без признаков заболевания до 5-10 лет вследствие снижения токсичности и наличия иммунного аллогенного антимиеломного эффекта. Этот метод показан больным моложе 55 лет с хорошим физиологическим резервом. При рецидиве или рефрактерной миеломе применяются новые препараты (талидомид, иммуномодуляторные препараты, ингибиторы протеасом), эффективность этих препаратов в качестве терапии 1-й линии изучается.
Поддерживающая терапия проводится нехимиотерапевтическими препаратами, включая интерферон, которые обеспечивают продолжительный эффект, но имеют некоторые побочные действия. Применение глюкокортикоидов в качестве поддерживающей терапии изучается.
Множественная миелома > Клинические протоколы МЗ РК
Дифференциальный диагноз[11-13]
Дифференциальный диагноз ММ основывается на результатах лабораторных тестов и клинических данных. Следует иметь ввиду, что плазмоцитоз в сочетании с умеренно выраженной парапротеинемией может наблюдаться прицелом ряде других заболеваний и реактивных состояний. Клинические проявления ММ чрезвычайно разнообразны, но в значительной мере они определяются нарушением продукции кроветворных клеток, склонностью к инфекционным осложнениям, наличием и выраженностью литических изменений костей скелета (главным образом, плоских костей) и нарушением функции почек. Однако, в первую очередь следует обратить внимание на наличие трех основных критериев, которые являются ведущими при диагностике ММ:
· Моноклональный иммуноглобулин при иммуноэлектрофорезе, (главные диагностические критерии – пик моноклонального IgG составляет более 3.5/100 мл, IgA – более 2.0/100 мл или секреция легких цепей с мочой- более 1.0 за 24 часа)
Диагноз множественной миеломы не вызывает сомнений при наличии двух первых признаков, третий – является дополнительным, так как отсутствие остеодеструкций не исключает ММ, а выявление совершенно недостаточно для постановки диагноза.
Доброкачественные моноклональные гаммапатии (MGUS). Главный диагностический критерий доброкачественной парапротеинемии – не прогрессирование, сохранение устойчивого уровня моноколонального парапротеина в течение длительного времени без развитая дополнительных симптомов. При электрофоретическом исследовании белков сывороток крови: содержание не вовлеченных в моноклональный пик иммуноглобулинов при МГ нормальное, тогда как при ММ – сниженное.Важное значение имеет стабильность уровня парапротеина, поэтому обязательно повторное его исследование с интервалом в 4-6 месяцев. В отличие от ММ, при которой наблюдается снижение содержания нормальных иммуглобулинов, у больных с МГ их содержание обычно остается в пределах нормы. Гиперкальциемия не типична для МГ. Выявление в костном мозге моноклональных плазматических клеток свидетельствует в пользу ММ. При фенотипировании при ММ выявляются резидуальные поликлональные плазматические клетки (CD38, CD138, CD19, CD56, CD28, CD117 и sIG) при МГ частота их выявления существенно ниже[12].
· уровень парапротеина: IgG в крови ≤30 г/л, IgА в крови ≤20 г/л, BJ-протеин в моче ≤1 г/24 ч;
· <10 % плазматических клеток в костном мозге;
· отсутствие костных поражений и других симптомов, связанных с болезнью, прежде всего анемии, гиперкальциемии, почечной недостаточности;
· отсутствие клинических и лабораторных признаков амилоидоза или болезни отложения легких/тяжелых цепей иммуноглобулинов.
Первичный амилоидоз. При амилоидозе в крови и моче часто находят моноклональный белок, в том числе и Бенс-Джонса, в костном мозге – плазмоцитоз. Но при содержании в костном мозге более 10% плазматических клеток с тенденцией к нарастанию и выявлении остедеструктивного синдрома диагноз ММ становится более вероятным. Основной и наиболее объективный метод диагностики амилоидоза – биопсия органов или ткани (почек, селезенки, печени, слизистой оболочки кишечника, десны, костного мозга, лимфатических узлов, кожи и подкожной клетчатки). Окончательно диагноз верифицируется на основании результатов гистологического исследования биоптатов ткани после окраски Конго красным. Под электронным микроскопом определяется типичная для всех видов амилоида фибриллярная структура белковых отложений. [13]
POEMS синдром. POEMS- это аббревиатура, состоящая из первых букв английских терминов, обозначающих наиболее характерные признаки и симптомы данного синдрома (osteosclerotic myeloma: Polyneuropathy — полинейропатия, Organomegaly-органомегалия, Endocrinopathy — эндокринопатия, Monoclonalprotein – моноклональная гаммапатия, Skinchanges – поражения кожи). POEMS-синдром – это моноклональное заболевание из плазматических клеток, сопровождающееся симптомами и/или признаками периферической нейропатии, остеостклеротическими поражениями, болезнью Кастлемана (ангиофолликулярная гиперплазия лимфоузлов), органомегалии, эндокринопатии (за исключением сахарного диабета или гипотиреоза), отек, типичные изменения кожи, и/или отек диска зрительного нерва. Эти пациенты, как правило, имеют повышенные уровни сыворотки VEGF (vascular endothelial growth factor — фактор роста эндотелия сосудов). Симптомы полинейропатии при классической ММ встречаются редко, а если они присутствуют, то как правило, из-за наличия амилоидоза. Наличие анемии, гиперкальциемии, почечной недостаточности, патологические переломы, и высокий процент плазматических клеток в костном мозге – это то, что отличает классическую ММ от синдрома POEMS. [11]
Миеломная болезнь — Виды рака
Что такое миеломная болезнь?
Это опухолевое заболевание, возникающее из плазматических клеток крови (подтип лейкоцитов, т.е. белых кровяных телец). У здорового человека эти клетки участвуют в процессах иммунной защиты, вырабатывая антитела. При миеломной болезни (ее еще называют миеломой) в костном мозге и в костях накапливаются измененные плазматические клетки, что нарушает образование нормальных клеток крови и структуру костной ткани. Иногда можно услышать о миеломе костей, миеломной болезни позвоночника, почек или крови, но это не совсем верные названия. Миеломная болезнь уже подразумевает поражение кроветворной системы и костей.
Классификация миеломной болезни
Болезнь неоднородна, можно выделить следующие варианты:
моноклональная гаммапатия неясного генеза — это группа заболеваний, при которых избыточное количество В-лимфоцитов (это клетки крови, которые участвуют в иммунных реакциях) одного вида (клона) вырабатывают аномальные иммуноглобулины разных классов, которые накапливаются в разных органах и нарушают их работу (очень часто страдают почки).
лимфоплазмацитарная лимфома (или неходжкинская лимфома), при которой очень большое количество синтезирующихся иммуноглобулинов класса М повреждает печень, селезенку, лимфоузлы.
плазмацитома бывает двух видов: изолированная (поражает только костный мозг и кости) и экстрамедуллярная (накопление плазматических клеток происходит в мягких тканях, например, в миндалинах или носовых пазухах). Изолированная плазмацитома костей в некоторых случаях переходит во множественную миелому, но не всегда.
Множественная миелома составляет до 90% всех случаев заболевания и обычно затрагивает несколько органов.
Также выделяют:
асимптоматическую (тлеющую, бессимптомную миелому)
миелому с анемией, поражением почек или костей, т.е. с симптомами.
Код миеломы по МКБ-10: С90.
Стадии миеломной болезни
Стадии определяют в зависимости от количества в сыворотке крови бета-2 микроглобулина и альбумина.
1 стадия миеломы: уровень бета-2 микроглобулина менее 3,5 мг/л, а уровень альбумина равен 3,5 г/дл или более.
2 стадия миеломы: бета-2 микроглобулин колеблется между 3,5 мг/л и 5, 5 мг/л или же уровень альбумина ниже 3,5, тогда как бета-2 микроглобулин ниже 3,5.
3 стадия миеломы: уровень бета-2 микроглобулина в сыворотке составляет более 5,5 мг/л.
Причины и патогенез миеломной болезни
Причины миеломы неизвестна. Есть ряд факторов, повышающих риск заболеть:
Возраст. До 40 лет миеломной болезнью почти не болеют, после 70 лет риск развития заболевания значительно повышен
Мужчины болеют чаще женщин
У людей с черным цветом кожи риск миеломы в два раза выше, чем у европейцев или азиатов
Имеющаяся моноклональная гаммапатия. У 1 из 100 человек гаммапатия трансформируется в множественную миелому
Семейная история заболевания миеломой или гаммапатией
Патология иммунитета (ВИЧ или применение лекарств, подавляющих иммунитет)
Воздействие радиации, пестицидов, удобрений
Костный мозг в обычных условиях вырабатывает строго определенное количество В-лимфоцитов и плазматических клеток. При миеломной болезни их выработка выходит из-под контроля, костный мозг заполняется аномальными плазматическими клетками, а образование нормальных лейкоцитов и эритроцитов снижается. При этом вместо антител, полезных в борьбе с инфекциями, такие клетки производят белки, способные повреждать почки.
Симптомы и признаки миеломной болезни
Признаки, которые помогут заподозрить миелому:
Боль в костях, особенно в ребрах и позвоночнике
Патологические переломы костей
Частые, повторяющиеся случаи инфекционных заболеваний
Выраженная общая слабость, постоянная усталость
Потеря веса
Постоянная жажда
Кровотечения из десен или носовые, у женщин — обильные менструации
Головная боль, головокружение
Тошнота и рвота
Зуд кожи
Диагностика миеломной болезни
Поставить диагноз бывает сложно, так как при миеломной болезни нет какой-то явной опухоли, которую можно заметить, а иногда заболевание вообще протекает без каких-либо симптомов.
Диагностикой миеломной болезни обычно занимается врач-гематолог. Во время расспроса врач выявляет основные симптомы заболевания у данного пациента, выясняет, нет ли кровотечений, боли в костях, частых простуд. Затем проводят дополнительные исследования, необходимые для точной постановки диагноза и определения стадии болезни.
Клинический анализ крови при миеломе часто указывает на увеличение вязкости крови и повышение скорости оседания эритроцитов (СОЭ). Нередко снижено количество тромбоцитов и эритроцитов, гемоглобина.
В результатах анализа крови на электролиты часто повышен уровень кальция; по данным биохимического анализа увеличено количество общего белка, определяются маркеры нарушения функции почек — высокие цифры мочевины, креатинина.
Анализ крови на парапротеин проводят для оценки типа и количества аномальных антител (парапротеинов).
В моче часто определяют патологический белок (белок Бенс-Джонса), который представляет собой моноклональные легкие цепи иммуноглобулинов.
На рентгенограмме костей (черепа, позвоночника, бедренных и тазовых костей) видны характерные для миеломы повреждения.
Пункция костного мозга — самый точный способ диагностики. Тонкой иглой берут кусочек костного мозга, обычно прокол делают в области грудины или кости таза. Затем полученный изучают под микроскопом в лаборатории на предмет перерожденных плазматических клеток и проводят цитогенетическое исследование для выявления изменений в хромосомах.
Компьютерная томография, магнитно-резонансная томография, ПЭТ-сканирование позволяют выявить участки повреждения в них.
Способы лечения миеломной болезни
В настоящее время используют разные методы лечения, прежде всего лекарственную терапию, при которой препараты применяют в разных комбинациях.
Таргетная терапия с использованием лекарства (бортезомиб, карфилзомиб (не зарегистрирован в России), которые за счет влияния на синтез белков вызывают гибель плазматических клеток.
Терапия биологическими препаратами, такие как талидомид, леналидомид, помалидомид, стимулируют собственную иммунную систему бороться с опухолевыми клетками.
Химиотерапия циклофосфаном и мелфаланом, которые тормозят рост и приводят к гибели быстрорастущих клеток опухоли.
Кортикостероидная терапия (дополнительное лечение, которое усиливает эффект основных препаратов).
Бисфосфонаты (памидронат, золендроновая кислота) назначают для повышения плотности костной ткани.
Обезболивающие, в том числе наркотические анальгетики, применяют при сильных болях (очень частая жалоба при миеломной болезни), для облегчения состояния пациента применяют хирургические методы и лучевая терапия.
Хирургическое лечение требуется, например, для фиксации позвонков с помощью пластин или других приспособлений, так как происходит разрушение костной ткани, в том числе позвоночника.
После проведения химиотерапии часто проводят пересадку костного мозга, при этом наиболее эффективной и безопасной является аутологичная трансплантация стволовых клеток костного мозга, Для осуществления этой процедуры проводят забор стволовых клеток красного костного мозга. затем назначают химиотерапию (как правило, высокими дозами противоопухолевых препаратов), которая уничтожает раковые клетки. После окончания полного курса лечения делают операцию по пересадке забранных ранее образцов, и в результате начинают расти нормальные клетки красного костного мозга.
Некоторые формы заболевания (прежде всего “тлеющая” меланома) не требуют срочного и активного лечения. Химиотерапия вызывает тяжелые побочные эффекты и в некоторых случаях — осложнения, а эффекты на течение болезни и прогноз при бессимптомной “тлеющей” миеломной болезни сомнителен. В таких случаях проводят регулярное обследование и при первых признаках обострения процесса начинают лечение. План контрольных исследований и регулярность их проведения врач устанавливает индивидуально для каждого пациента, и очень важно соблюдать эти сроки и все рекомендации врача.
Осложнения миеломной болезни
Сильные боли в костях, требующие назначения эффективных обезболивающих средств
Почечная недостаточность с необходимостью гемодиализа
Частые инфекционные заболевания, в т.ч. воспаление легких (пневмонии)
Истончение костей с переломами (патологические переломы)
Анемия, требующая переливания крови
Прогноз при миеломной болезни
При “тлеющей” миеломе заболевание может не прогрессировать десятки лет, но необходимо регулярное наблюдение у врача, чтобы вовремя заметить признаки активизации процесса, при этом появление очагов разрушения костей или увеличение в костном мозге количества плазматических клеток выше 60% говорит об обострении заболевания (и ухудшении прогноза).
Выживаемость при миеломе зависит от возраста и общего состояния здоровья. В настоящее время в целом прогноз стал оптимистичнее, чем еще 10 лет назад: 77 из 100 больных миеломой человек будут жить как минимум год, 47 из 100 — как минимум 5 лет, 33 из 100 — как минимум 10 лет.
Причины смерти при миеломной болезни
Чаще всего к смерти приводят инфекционные осложнения (например, пневмония), а также фатальные кровотечения (связанные с низким количеством тромбоцитов в крови и нарушениями свертываемости), переломы костей, тяжелая почечная недостаточность, тромбоэмболия легочной артерии.
Питание при миеломной болезни
Рацион при миеломе должен быть разнообразным, содержать достаточное количество овощей и фруктов. Рекомендуют уменьшить потребление сладостей, консервов и готовых полуфабрикатов. Специальной диеты можно не придерживаться, но так как миеломе часто сопутствует анемия, то желательно регулярно есть продукты, богатые железом (постное красное мясо, сладкий перец, изюм, брюссельская капуста, брокколи, манго, папайя, гуава).
В одном из исследований было продемонстрировано, что употребление куркумы предупреждает резистентность к химиотерапии. Исследования на мышах показали, что куркумин может замедлять рост раковых клеток. Также добавление в пищу куркумы во время химиотерапии может несколько облегчить тошноту и рвоту.
Все изменения в диете нужно согласовывать с лечащим врачом, особенно во время химиотерапии.
Множественная миелома: прогноз
Множественная миелома: прогноз
Множественная миелома: прогноз
Врачи часто используют показатели выживаемости в качестве стандарта для обсуждения прогноза множественной миеломы. Показатели выживаемости основаны на предыдущих исходах болезни большого количества пациентов. Важно отметить, что прогноз каждого пациента сугубо индивидуален и зависит от конкретной клинической картины и истории болезни.
На прогноз могут повлиять многие факторы, среди которых возраст, общее состояние здоровья, качество лечения и реакция болезни на терапию.
Важно помнить, что прогноз – это приблизительная оценка. Варианты лечения и прогноз миеломной болезни у конкретного человека зависят от множества факторов, одним из которых является стадия рака на момент постановки диагноза. Чем раньше диагностирована множественная миелома, тем лучше прогноз. Другим фактором, влияющим на прогноз, является возраст пациента. Молодые люди, как правило, имеют более высокие шансы на стабильную ремиссию, чем пожилые.
У некоторых пациентов миелома может протекать бессимптомно и прогрессировать медленно. При своевременном применение современных методов лечения рака крови и наступлении полной ремиссии, прогноз миеломной болезни у этих пациентов, как правило, очень благоприятный. В случае плохого функционирования почек и наличия быстро растущих раковых клеток, наоборот, прогноз будет неблагоприятным.
Существует так называемая «медиана выживаемости», обозначающая время выживания большинства пациентов с диагностированной болезнью. Это время определяется от начала времени лечения.
Международная медиана выживаемости содержит следующие данные относительно продолжительности жизни пациентов на разных этапах выявления и лечения болезни:
- I стадия – выживаемость 62 месяца;
- II стадия – выживаемость около 44 месяцев;
- III стадия – выживаемость составляет 29 месяцев.
Но по определению, половина пациентов живет больше, чем указано в медиане выживаемости. Также стоит учитывать, что методы терапии постоянно совершенствуются, поэтому прогноз множественной миеломы улучшается ото дня ко дню.
В целом прогноз миеломной болезни приблизительно следующий:
- Около 77% пациентов с диагнозом миелома живут, по крайней мере, год после постановки диагноза.
- Около 47% живут минимум 5 лет.
- Около 33% пациентов живут, по крайней мере, 10 лет.
Как и при других видах онкологии, прогноз миеломной болезни зависит от стадии, на которой она была выявлена. На ранней стадии болезнь не имеет типичных симптомов рака крови или повреждений кости. Первая стадия характеризуется небольшим количеством клеток опухоли и повреждение кости является относительно небольшим. На второй стадии опухоль повреждает костную ткань. Третья стадия болезни характеризуется большим количеством патогенных клеток и несколькими областями поражения кости.
Следует помнить, что множественная миелома может развиваться и иметь разные диагнозы, например миелома Бенс-Джонса, поэтому и прогноз у разных пациентов может меняться. У некоторых людей болезнь развивается очень медленно, поэтому прогноз будет лучше, но такие вопросы следует обсуждать со своим лечащим врачом. Перед тем, как сделать обоснованное предположение относительно прогнозирования вероятности излечения врач должен проанализировать ряд факторов.
Помимо стадии рака есть дополнительные факторы, влияющие на прогноз. К таким факторам относится общее состояние здоровья пациента и нуждается ли он в постороннем уходе. Общее состояние здоровья имеет отношение к выживанию потому, что от него зависит, насколько человек сможет выдержать интенсивные методы лечения, способствующие полному излечению или контролю миеломы более длительное время.
Врачи и исследователи непрестанно ищут новые способы прогнозирования развития миеломы и влияющие на прогноз факторы.
[contact-form-7 404 «Not Found»]
что это такое, лечение, степени, стадии, прогноз, симптомы, диагностика, причины
Что такое множественная миелома
Множественная миелома является злокачественной плазмоклеточной опухолью, продуцирующей моноклональные иммуноглобулины, которые внедряются в прилежащую костную ткань и разрушают ее. Диагностика основана на выявлении М-протеина (иногда присутствует в моче, никогда — в сыворотке крови) и характерных костных поражений, протеинурии легких цепей, избыточного количества плазматических клеток в костном мозге. Специфическое лечение включает в себя традиционную химиотерапию в сочетании с бортезомибом, леналидомидом, талидомидом, кортикостероидами, мелфаланом (высокие дозы), в последующем выполняется трансплантация аутологичных стволовых клеток периферической крови.
Распространенность множественной миеломы составляет 2-4 случая/100 000 человек. Соотношение мужчин и женщин 1,6:1, медиана возраста — 65 лет. Этиология заболевания неизвестна, хотя рассматривается роль хромосомных и генетических факторов, радиации, химических веществ.
В норме плазматические клетки образуются из В-лимфоцитов и продуцируют иммуноглобулины, которые состоят из тяжёлых и лёгких цепей. Нормальные иммуноглобулины поликлональны, что означает, что они образуют множество тяжёлых цепей, и каждой может соответствовать каппа или лямбда лёгкие цепи определённых типов. Миеломные плазматические клетки вырабатывают только тяжёлые или лёгкие цепи иммуноглобулинов одного типа, моноклональный белок называют парапротеином. В некоторых случаях синтезируются только лёгкие цепи, и такой белок обнаруживается в моче, как протеинурия Бене-Джонса.
Классификация множественной миеломы
| Тип парапротеина | Относительная частота (%) |
|---|---|
| IgG | 55 |
| IgA | 21 |
| Только лёгкие цепи | 22 |
| Другие (D, Е, несекретирующие) | 2 |
Патофизиология множественной миеломы
М-протеин, продуцируемый злокачественными плазматическими клетками, относится к IgG у 55% пациентов, к IgA — у 20% пациентов; независимо от вида иммуноглобулина в 40% случаев возникает протеинурия Бенс-Джонса,при которой в моче обнаруживаются свободные моноклональные легкие цепи к или А. У 15-20% пациентов плазматические клетки секретируют только белок Бенс-Джонса. Около 1% случаев миеломы ассоциировано с IgD.
Характерно развитие диффузного остеопороза или появление отдельных остеолитических поражений, обычно в костях таза, черепа, позвонках, ребрах. Данные поражения обусловлены замещением нормальной костной ткани растущей плазмоцитарной опухолью, а также воздействием цитокинов, которые секретируются злокачественными плазматическими клетками, они вызывают активацию остеокластов и супрессию остеобластов. Остеолитические поражения обычно носят множественный характер, в редких случаях образуются солитарные интрамедуллярные массы. Значительная потеря костной ткани также может сопровождаться гиперкальциемией. Внекостные солитарные плазмоцитомы возникают редко, однако они могут встречаться во всех типах тканей, особенно в верхних отделах респираторного тракта.
Почечная недостаточность у многих пациентов может присутствовать уже на момент установления диагноза либо развиваться в ходе болезни, данное осложнение может иметь несколько причин, основную роль играет отложение депозитов легких цепей в дистальных канальцах и наличие гиперкальциемии. Часто развивается анемия, обусловленная заболеванием почек или супрессией эритропоэза опухолевыми клетками.
У некоторых пациентов наблюдается повышенная восприимчивость к бактериальным инфекциям. В результате применения новых методов лечения возрастает частота вирусных инфекций, особенно герпетических. Вторичный амилоидоз развивается у 10% пациентов с миеломой, чаще всего данное осложнение встречается у пациентов с протеинурией Бенс-Джонса А-типа.
Проявления множественной миеломы могут быть вариабельны.
Малое число злокачественных плазматических клеток циркулируют с кровью, большая их часть в костном мозге. Злокачественные клетки продуцируют цитокины, которые стимулируют остеокласты, вызывая абсорбцию костной сети. Лизис кости сопровождается болями в костях, переломами и гиперкальциемией. Поражение костного мозга приводит к анемии или панцитопении. Причина заболевания неизвестна.
Симптомы и признаки множественной миеломы
Заболеваемость множественной миеломой составляет 4/100 000 новых случаев в год с соотношением мужчин и женщин 2:1. Средний возраст выявленных больных — 60—70 лет, и заболевание чаще встречают в странах Африки и Карибского бассейна.
Наиболее распространенными проявлениями являются персистирующие боли в костях (особенно в области спины или грудной клетки). Однако в большинстве случаев диагноз устанавливается по результатам обычных лабораторных тестов, которые выявляют увеличение уровня общего белка в крови или наличие протеинурии. Характерны патологические переломы, вследствие поражения позвонков может происходить компрессия спинного мозга с развитием параплегии. Необходимо отметить, что наличие анемии может быть преимущественной или единственной причиной диагностического поиска. В небольшом количестве случаев наблюдаются проявления, характерные для синдрома гипервязкости. Типичными симптомами являются периферическая нейропатия, синдром запястного канала, патологическая кровоточивость, признаки гиперкальциемии (к примеру, полидипсия). Также может развиваться почечная недостаточность. Лимфаденопатия и гепатоспленомегалия нехарактерны.
Диагностика множественной миеломы
Множественную миелому необходимо подозревать у пациентов старше 40 лет с наличием персистирующих болей в костях неясной этиологии (особенно ночью или в покое), других типичных симптомов, необъяснимых лабораторных отклонений. Лабораторная диагностика включает в себя выполнение стандартных анализов крови, электрофореза белков, рентгенографии.
К стандартным анализам крови относятся OAK, определение уровня СОЭ, биохимический анализ. Анемия присутствует у 80% пациентов, обычно она имеет нормоцитарно-нормохромный характер и отличается формированием «монетных столбиков». Часто наблюдается повышение уровня мочевины, сывороточного креатинина, ЛДГ, мочевой кислоты. Иногда снижается анионный интервал. Гиперкальциемия на момент установления диагноза присутствует у 10% пациентов.
Сывороточный электрофорез выявляет наличие М-протеина приблизительно у 80-90% пациентов. У остальных 10-20% пациентов обычно присутствуют только свободные моноклональне легкие цепи или IgO. В таких случаях наличие М-протеина почти всегда возможно выявить при проведении электрофореза белков мочи. Проведение иммунофиксационного электрофореза позволяет идентифицировать класс иммуноглобулинов, к которому относится М-протеин. С помощью данного метода часто можно обнаружить легкие цепи белка, если иммуноэлектрофорез сыворотки крови дает ложноотрицательный результат. Таким образом, иммунофиксационный электрофорез должен выполняться при наличии значительного клинического подозрения на наличие множественной миеломы даже при отрицательном результате стандартного исследования сыворотки крови. Анализ структуры легких цепей с определением соотношения к и А-цепей позволяет верифицировать диагноз. Кроме того, анализ структуры легких цепей может проводиться с целью мониторинга эффективности лечения и получения прогностических данных. Если диагноз верифицирован либо имеет крайне высокую клиническую вероятность, измеряется сывороточный уровень β2-микроглобулина; его содержание часто повышено, уровень альбумина, наоборот, может быть снижен. Существует новая международная классификация, которая использует данные показатели (уровень сывороточного альбумина и β2-микроглобулина) для определения тяжести заболевания и прогноза.
Проводится рентгенологическое исследование костей скелета, которое в 80% случаев выявляет наличие штампованных литических поражений или диффузного остеопороза. Радионуклидное сканирование костей обычно неинформативно. МРТ позволяет получить более детальную картину, она выполняется при наличии локальных болей или неврологической симптоматики.
Также выполняется аспирационная биопсия, в биоптате выявляется наличие плазматических клеток, расположенных диффузно или в виде скоплений; диагноз миеломы устанавливается при наличии >10% клеток данного типа. Тем не менее поражение костного мозга может носить очаговый характер, поэтому в некоторых образцах, полученных от пациентов с миеломой, можно обнаружить <10% плазматических клеток. При хромосомном исследовании костного мозга можно обнаружить специфические кариотипические аномалии плазматических клеток, наличие которых ассоциировано с различиями в продолжительности жизни пациента.
При отсутствии М-протеина в сыворотке крови диагностика миеломы основана на выявлении протеинурии Бенс-Джонса >300 мг/24 часа, остеолитических поражений (при отсутствии достоверных сведений о метастазировании злокачественной опухоли или наличии гранулематозных заболеваний), наличии в костном мозге плазматических клеток, расположенных диффузно или в виде скоплений.
Дополнительные критерии, важные для диагноза
- Уровень щелочной фосфатазы в плазме и сканирование костей нормальны при отсутствии переломов или костных мозолей.
- Исследование β2-микроглобулина сыворотки — пенный показатель прогноза.
- Нормальный уровень иммуноглобулинов, т.е. отсутствие ослабления иммунитета, заставляет усомниться в диагнозе.
- Только около 5% больных при постоянном СОЭ выше 100 мм/ч имеют миелому
Прогноз множественной миеломы
Заболевание является прогрессирующим и неизлечимым, однако в последнее время медиана выживаемости увеличилась и превысила 5 лет в результате успехов в терапии. К неблагоприятным прогностическим факторам относится низкий сывороточный уровень альбумина и высокий уровень β2-микроглобулина. У пациентов с почечной недостаточностью, рефрактерной к терапии, прогноз также плохой.
Поскольку множественная миелома является потенциально смертельным заболеванием, полезно обсудить возможность паллиативного лечения, в котором должны принимать участие не только врачи, в него должны быть вовлечены члены семьи и друзья пациента. Необходимо обсуждение таких вопросов, как назначение опекуна (который в т.ч. будет принимать важные решения медицинского характера), использование зонда для искусственного кормления, обезболивание.
При стандартной терапии средняя выживаемость больных составляет примерно 40 мес. Признаки плохого прогноза — высокий β2-микроглобулин, низкий альбумин, низкий гемоглобин или высокий кальций. Аутотрансплантация улучшает выживаемость и качество жизни больных, поскольку замедляет прогрессирование костных поражений. При стандартном лечении менее 5% больных живут более 10 лет.
Лечение множественной миеломы
- При наличии симптомов заболевания назначается химиотерапия.
- Талидомид, бортезомиб, леналидомид в сочетании с кортикостероидами и/или химиотерапией.
- Возможна поддерживающая терапия.
- Возможна трансплантация стволовых клеток.
- Возможна лучевая терапия.
- Лечение осложнений (анемии, гиперкальциемии, почечной недостаточности, инфекций, поражений костей).
Если у больного отсутствует симптоматика, лечения не требуется.
В течение последнего десятилетия в лечении миеломы наблюдается значительный прогресс. Целью терапии является долгосрочная выживаемость. У пациентов с симптомным течением лечение направлено на уничтожение злокачественных клеток и коррекцию осложнений. У пациентов с бессимптомным течением, вероятно, польза от лечения отсутствует, поэтому оно, как правило, не проводится до развития клинических проявлений и осложнений. Тем не менее пациенты, имеющие достоверные признаки литических поражений или потери костной ткани (остеопения или остеопороз), должны ежемесячно получать инфузии золедроновой кислоты или памидроната с целью снижения риска осложнений со стороны костей скелета.
Лечение, направленное на уничтожение злокачественных клеток. До недавнего времени традиционная химиотерапия включала в себя только пероральный прием мелфалана и преднизона в форме 4-6-недельных курсов с ежемесячной оценкой ответа на лечение. Согласно современным исследованиям, улучшение результатов лечения наблюдается при добавлении к терапии бортезомиба или талидомида. Другие химиотерапевтические препараты, в т.ч. алкилирующие (циклофосфамид, доксорубицин, его новый аналоглипосомальный пегилированный доксорубицин), также более эффективны в комбинации с талидомидом и бортезомибом. Во многих случаях эффективен прием бортезомиба, талидомида или леналидомида в сочетании с глюкокортикоидами и/или химиотерапевтическими препаратами.
Ответ на химиотерапию оценивается по таким признакам, как снижение уровня М-протеина в сыворотке крови и моче, повышение количества эритроцитов, улучшение функции почек (у пациентов с признаками почечной недостаточности).
Аутологичная трансплантация стволовых клеток, данный метод эффективен при стабильном течении заболевания или наличии ответа на лечение после нескольких начальных циклов терапии. При выполнении аллогенной трансплантации стволовых клеток после немиелоаблативного режима (низкие дозы циклофосфамида и флударабина) или лучевой терапии в низких дозах у некоторых пациентов можно достичь безрецидивной выживаемости в течение 5-10 лет. Тем не менее аллогенная трансплантация стволовых клеток остается экспериментальным методом в связи с высоким уровнем заболеваемости и летальности, связанной с реакцией «трансплантат против хозяина».
При рецидивирующем или рефрактерном течении миеломы может применяться комбинация бортезомиба и талидомида (или его нового аналога леналидомида) в сочетании с химиотерапевтическими препаратами или кортикостероидами. Данные препараты обычно комбинируются с другими эффективными средствами, ранее не применявшимися у конкретного пациента. Однако пациенты с длительной ремиссией могут отвечать на повторный курс терапии, аналогичной той, которая привела к ремиссии.
Делаются попытки к назначению поддерживающей терапии, не содержащей химиотерапевтических препаратов, она основана на интерфероне-α, применение которого продлевает период ремиссии, однако не оказывает влияния на продолжительность жизни, кроме того, данный метод лечения ассоциирован с выраженными побочными эффектами. При наличии ответа на режимы, основанные на кортикостероидах, изолированное применение кортикостероидов эффективно в качестве поддерживающей терапии.Также в качестве поддерживающей терапии может применяться талидомид. В настоящее время проводятся исследования по применению поддерживающей терапии бортезомибом и леналидомидом у пациентов, ранее отвечавших только на указанные препараты или комбинированную терапию.
Лечение осложнений. Помимо прямого цитотоксического действия на злокачественные клетки терапия должна быть направлена на лечение осложнений, таких как анемия, гиперкальциемия, почечная недостаточность, инфекции, поражения костей.
Анемия может успешно лечиться путем применения рекомбинантного эритропоэтина (40 000 ME п/к 1 раз в неделю) у пациентов с недостаточным ответом на химиотерапию. Если анемия сопровождается кардиоваскулярными или выраженными системными симптомами, необходимо переливание эритроцитарной массы. При появлении признаков гипервязкости показано применение плазмафереза.
Гиперкальциемия успешно лечится путем применения салиуреза и в/в бисфосфонатов, в некоторых случаях может потребоваться введение преднизолона. В большинстве случаев необходимость в назначении аллопуринола отсутствует. Тем не менее его применение показано при высоком уровне мочевой кислоты в сыворотке крови, больших размерах опухоли, высоком риске синдрома лизиса опухоли.
Риск нарушения функции почек можно снизить путем потребления достаточного количества жидкости.
Инфекционные осложнения наиболее вероятны на фоне нейтропении, индуцированной химиотерапией. У пациентов, получавших новые антимиеломные препараты, чаще наблюдаются случаи инфекций, вызываемых вирусом herpes zoster. При выявлении бактериальной инфекции назначается антибиотикотерапия; тем не менее профилактическое применение антибиотиков, как правило, не рекомендуется. Профилактическое назначение противовирусной терапии может быть показано при приеме некоторых препаратов. Внутривенное введение иммуноглобулинов с профилактической целью может снижать риск инфицирования, однако данный метод применяется в основном у пациентов с рецидивирующими инфекциями. С профилактической целью показана иммунизация пневмококковой и противогриппозной вакциной.
Скелетные поражения требуют масштабной поддерживающей терапии. Для предупреждения дальнейшей потери костной ткани пациент должен сохранять подвижность, а также принимать дополнительные препараты кальция и витамина D. Для купирования болей в костях могут применяться анальгетики и лучевая терапия в паллиативных дозах (18-24 Гр). Однако лучевая терапия может снижать переносимость установленных цитотоксических доз препаратов, принимаемых в рамках системной химиотерапии. В большинстве случаев, особенно при наличии литических костных поражений, генерализованного остеопороза или остеопении, необходимо ежемесячное введение в/в бисфосфонатов (памидронат или золедроновая кислота). Бисфосфонаты эффективны при лечении скелетных осложнений, они уменьшают боли в костях, возможно, обладают противоопухолевым действием.
Первая помощь
- Повышенное потребление жидкости в целях борьбы с нарушением почечной функции и гиперкальциемией.
- Аналгезия в связи с болями в костях.
- Бисфосфонаты для уменьшения гиперкальциемии и отдаления других повреждений скелета.
- Аллопуринол для профилактики уратной нефропатии.
- Плазмаферез, при необходимости, для борьбы с повышенной вязкостью крови.
Химиотерапия
У слабых пожилых пациентов эффективен мелфалан внутрь, у лиц молодого возраста ответ на лечение может улучшить внутривенное введение лекарств. Высокие дозы внутривенного мелфалана хорошо переносятся даже людьми старше 65 лет и дают хороший клинический ответ.
Лечение продолжают, пока уровень парапротеина не перестанет падать. Эту ситуацию называют «фазой плато», и она может продолжаться недели или годы. Последующий рецидив лечению поддаётся хуже. Лучевое лечение
Оно эффективно при локализованных болях в костях, не снимаемых обычными анальгетиками, а так же, при патологических переломах. Оно полезно также как неотложное лечение компрессии спинного мозга, вызванной экстрадуральной плазмацитомой.
Трансплантация
Стандартное лечение не излечивает миелому. Аутотрансплантация стволовых клеток улучшает качество жизни и увеличивает выживаемость. Всем перспективным больным в возрасте до 65 лет следует предложить внутривенную химиотерапию до максимального эффекта и затем аутотрансплантацию стволовых клеток. Аллотрансплантацией костного мозга некоторых больных можно вылечить, поэтому этот метод лечения нужно принимать во внимание у больных в возрасте моложе 55 лет, при наличии брата или сестры, которые могут быть донором. Аутотрансплантация уменьшенной интенсивности может улучшить результаты, снижая связанную с трансплантацией смертность и расширяя верхнюю возрастную границу.
Бисфосфонаты
Долговременное лечение бисфосфонатами уменьшает боли в костях и поражения скелета. Эти препараты защищают кости и могут вызвать апоптоз злокачественных плазматических клеток.
Талидомид
Препарат оказывает антиангиогенное действие на кровеносные сосуды опухоли и обладает иммуномодулирующим свойством. Показано, что в небольших дозах он эффективен при рефрактерной миеломе, и описан положительный ответ у 50% больных комбинации талидомида с дексаметазоном. Сейчас проходят исследования использования талидомида как дополнения к другим видам лечения на ранних стадиях болезни. Препарат может вызвать сонливость, запоры и периферическую нейропатию. Препарат обладает тератогенным свойством, крайне важно, чтобы женщины детородного возраста использовали адекватную контрацепцию.
Другие новые препараты включают ингибитор протеасом бортезомиб, который активен при миеломе на поздних стадиях, и производные талидомида, которые проходят клинические испытания.
лечение, симптомы, стадии, прогноз жизни, виды и причины
Миелома – это патология крови, имеющая злокачественный характер. Развивается болезнь в костном мозге из переродившихся клеток крови. Заболевание относят к парапротеинемическим гемобластозам. Онкологический процесс сопровождается повышенным продуцированием атипичных белков иммуноглобулина. Встречается миелома достаточно редко, чаще страдают люди с тёмным оттенком кожи. Выявить болезнь на начальном этапе сложно, поэтому лечение часто начинается уже в запущенной стадии.
Характеристика заболевания
Миелома характеризуется злокачественным процессом активного разрастания в полости спинного мозга моноклональных плазмоцитов, продуцирующих патологический белок – парапротеин. Болезнь представляет собой непрекращающееся созревание и перерождение В-лимфоцитов в плазмоциты. Плазмоцит – это клетка, секретирующая иммуноглобулин. При миеломе моноклональные плазмоциты не погибают, а продолжают размножаться. Увеличение количества патогенов перемещается в костный мозг, что провоцирует снижение основных элементов крови.
Атипичные иммуноглобулины проникают в ткани других органов, накапливаясь в межклеточном пространстве. В первую очередь, патогены накапливаются в тканях почек, печени, селезенки и т.д. – органах с повышенным кровоснабжением.
Миеломная болезнь связана с замещением здоровых клеток атипичными иммуноглобулинами. Патогенез патологических плазмоцитов с выработкой биологически активных веществ вызывает развитие следующих эффектов:
- повышается уровень остеокластов, что провоцирует ломкость и хрупкость костей позвоночника, конечностей и т.д.;
- снижаются защитные функции организма;
- увеличивается уровень эластичных волокон с фиброгенами, что приводит к постоянному образованию капиллярных кровотечений и синяков;
- печёночные клетки активно разрастаются, провоцируя снижение свёртываемости крови;
- нарушенный белковый состав вызывает заболевания почек.
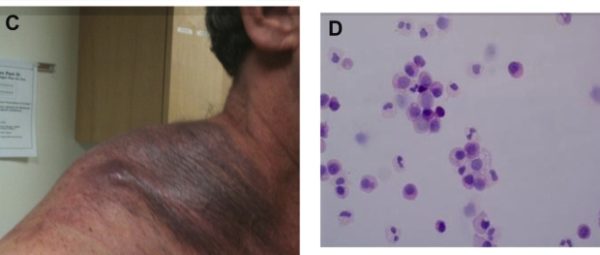

Проявления миеломы
При миеломной болезни рост моноклональных плазмоцитов не контролируется и их уровень постоянно увеличивается. Из-за этого процесса миелома относится к злокачественным патологиям крови – гемобластозам.
Возникает заболевание обычно у взрослых людей после 40 лет. У мужчин болезнь диагностируется чаще, чем у женщин. Опухоль растёт медленно – до появления первых симптомов может пройти более 20 лет. После постановки диагноза, по наличию сопутствующей симптоматики человек живет в среднем в пределах 2 лет. Поэтому миелома часто воспринимается как рак крови.
Код по МКБ-10 у патологии С90 «Множественная миелома и злокачественные плазмоклеточные новообразования». Определить болезнь можно по наличию белков класса IgE, характеризуется присутствием Е-миеломы.
Разновидности миеломы
Классификация миеломной болезни основывается на структурном составе опухоли с расположением атипичных патогенов в зоне костного мозга.
В зависимости от количества очагов поражения различают формы:
- Солитарная форма определяется единичным очагом в любом участке кости с костным мозгом или на ткани лимфатического узла, что является главным отличием от множественной миеломы.
- Множественная миелома отличается формированием нескольких очагов поражения с наличием костного мозга. Встречается чаще всего в области лопаток, ребер, костях черепа, в кистях, ногах и т.д.
Обычно диагностируется поражение организма множественной патологией. Многочисленная концентрация патогенных новообразований в организме имеет схожие признаки проявления с солитарной.
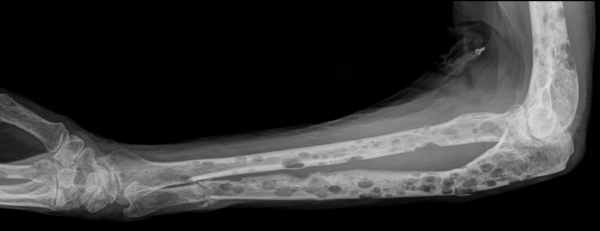

Проявления множественной миеломы в костях
В зависимости от клеточной структуры выделяют виды:
- Плазмоклеточная миелома отличается высоким уровнем зрелых плазмоцитов, вырабатывающих парапротеин. Патология развивается медленно, но постоянный процесс выработки белка затрудняет курс терапии. Плазматический миеломатоз распространяется на другие органы и системы.
- Плазмобластной тип характеризуется преобладанием плазмобластов, секретирующих белок в незначительном объёме. Дифференциальная патология отличается быстрым ростом и легко поддаётся терапии.
- Полиморфноклеточный и мелкоклеточный вид отличаются разрастанием плазмоцитов на ранних сроках формирования болезни. Считаются самыми опасными формами по степени роста и распространения в организме.
При множественной патологии различают диффузную и диффузно-очаговую форму.
Согласно иммунохимическим признакам вырабатываемых парапротеинов различают:
- заболевание лёгких цепей – миелома Бенс-Джонса;
- с высоким содержанием определенного типа белка (А, G и M-градиент) – миеломы A, G и M;
- несекретирующая форма;
- диклоновый вид;
- миелома М.
Болезнь протекает в 3 стадии:
- на 1 стадии обычно признаки отсутствуют;
- 2 стадия характеризуется появлением выраженных симптомов;
- на 3 стадии наблюдается распространение атипичных клеток в других органах.
Признаки заболевания
На начальном этапе болезнь развивается скрытно – выраженная клиника отсутствует. При раке клетки постепенно распространяются по организму, поражая внутренние полости плоских костей – зону лопаток, позвонков и черепа, а также трубчатые кости.
В медицинской практике есть примеры диагностирования миелосаркомы – онкологического процесса, формируемого тельцами белого кровотока. При дальнейшем развитии на поверхности костей появляются наросты овальной формы с мягкой эластичной консистенцией, что приводит к разрушению костной структуры.
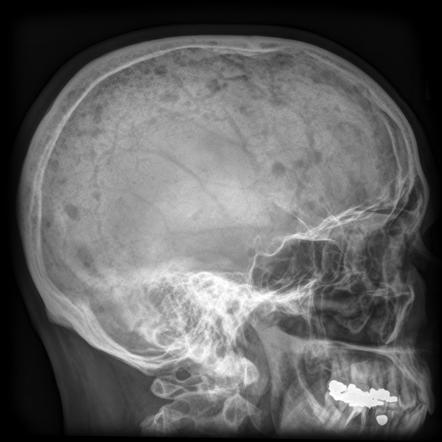

Разрушение костной структуры миеломой
В основном присутствуют следующие симптомы миеломы:
- нарушения в работе органов пищеварения;
- температура тела постоянно меняется – может подняться до термальных показаний и сразу снизиться;
- мышечная слабость на фоне быстрой утомляемости;
- показатели основных элементов крови характеризуют признаки анемии;
- наблюдаются частые болезни инфекционного характера;
- болевые синдромы в области мягких тканей с чувством дискомфорта;
- частый сердечный ритм – 100-120 ударов в минуту;
- в зоне подреберья присутствует чувство тяжести;
- сильные боли в области головы;
- гиперкальциемия позвонка приводит к внутренним изменениям структуры;
- миеломаляция развивается, когда дифференцированная опухоль сдавливает соседние ткани;
- нефропатия развивается при поражении почечных клеток.
При появлении первых симптомов болезни нужно обратиться к врачу и пройти обследование организма, чтобы определить тип патологии. Лечение на начальном этапе формирования гарантирует положительный эффект и быстрое выздоровление.
Причины появления патологии
Причины возникновения опухоли врачам точно не известны. Считается, что болезнь передается по наследству. Спровоцировать выработку атипичных патогенов могут следующие факторы:


- пожилой возраст пациента;
- наследственная предрасположенность;
- воздействие радиоактивных веществ;
- взаимодействие с химическими соединениями и канцерогенными веществами;
- болезни инфекционного характера;
- стрессовое состояние;
- генетические нарушения;
- заболевания крови – гепатит, анемия.
Вызвать структурные изменения в костном мозге может любой фактор внутренних изменений организма или влияние внешних признаков.
Диагностика заболевания
Чтобы поставить точный диагноз, пациенту рекомендуется лабораторная и инструментальная диагностика организма. Тлеющая болезнь в области спинного мозга может протекать длительное время бессимптомно. Если выявить миелому на ранних сроках, можно вылечиться быстрее и полностью.
Врач для обследования больного использует лабораторные и рентгенологические методы:
- проводится общий осмотр, собирается история болезни и полный анамнез;
- общий анализ крови при миеломе выявляет высокий уровень СОЭ с пониженным гемоглобином, тромбоцитозом, эритроцитов и альбумином;
- анализ мочи показывает повышенное содержание кальция и белка;
- рентген назначается для исследования структурных изменений костей;
- компьютерная (КТ) и магнитно-резонансная томография (МРТ) дают детальную информацию патологии;
- назначается процедура трепанобиопсии костного мозга с последующим проведением цитологического исследования.
Особое внимание уделяется количественному уровню иммуноглобулина в составе крови. На КТ можно определить степень поражения других органов. Болезнь по симптоматике часто выглядит как рак крови, поэтому врачи более тщательно исследуют организм больного с исключением возможных патологий.


Лечение болезни
Лечит болезнь гематолог в условиях стационара, и поддерживая контроль состояния пациента. Миелома и болезнь Вальденстрема считаются родственными, но с наличием серьёзных различий. Обе патологии успешно лечатся в Германии, Израиле и в России лучшими гематологическими центрами. Эффективным методом терапии патологии является пересадка костного мозга – проводится с использованием донорских стволовых клеток.
За опухолью на начальном этапе врачи предпочитают просто наблюдать, не используя терапевтические процедуры. Пациент регулярно сдает кровь и мочу на исследование состава на предмет патологических изменений.
При появлении выраженных симптомов болезни применяется химиотерапия с использованием лекарственных препаратов из группы цитостатиков. Процедура может быть стандартной или высокодозной. Часто используются следующие препараты – Мелферан, Циклофосфан, Карфилзомиб, Сарколизин, Бортезомиб и Леналидомид. Для больных в возрасте 65 лет применяется лекарство – Алкеран, Преднизолон, Циклофосфан или Винкристин. Костная миелома эффективно лечится с использованием бисфосфонатов – Аредией, Бондронатом и Бонефосом.
Облучение гамма-лучами рекомендуется при наличии болевых синдромов или диагнозе костной патологии с присутствием серьезных очагов разрушений, в курсе терапии солитарной миеломы и во время последней стадии, в качестве паллиативного метода. Дополнительно назначают Дексаметазон.
Иммунотерапия заключается в приеме альфа2-интерферона большими дозами на протяжении нескольких лет – это позволяет предотвратить нежелательные последствия и рецидив. При диагнозе почечной недостаточности применяются диуретики, специальное питание и плазмаферез (переливание крови). Процедура гемодиализа – очищенная лимфома обогащается необходимыми микроэлементами. Антибиотики требуются при наличии воспалительных процессов.
Хирургическое вмешательство используется во время поражений позвоночника, нервных окончаний и кровеносных сосудов. Также может применяться для фиксации скелетных костей при переломах.
Рекомендуется выполнять все клинические рекомендации лечащего врача – это позволит предотвратить тяжелые осложнения и остановить онкологический процесс.
Диета
Для положительного эффекта в процессе терапевтических процедур пациенту назначается специальная диета. Сбалансированный рацион питания снимает излишнюю нагрузку с органов пищеварительного тракта и восполняет витаминный дисбаланс.
Больному рекомендуется исключить из рациона:
- сладкие мучные продукты;
- выпечку из белой муки;
- жирную и жареную пищу на растительном масле;
- сладости на основе шоколада;
- супы на бульоне из жирных сортов мяса;
- маринованые и копчёные продукты;
- блюда из бобовых, перловки и пшена;
- молоко с кисломолочными продуктами;
- сладкие газированные напитки с квасом и соки из тетрапака.


Питаться рекомендуется часто и маленькими порциями. На фоне лейкоцитарной нормы можно употреблять варёные куриные яйца, рыбу, говядину и кролика с курицей в отварном виде. Печень можно тушить с небольшим количеством сметаны, каши на воде, овощи варёные или на пару и вчерашний хлеб.
Пониженный лейкоцитарный ряд разрешает употребление рисовой каши без молока, суп из риса на бульоне из нежирных сортов мяса, продукты с высоким содержанием кальция и витаминов В и С.
Во время курсов химиотерапии нужно поддерживать норму потребления жидкости на уровне 3 литров – ягодные компоты, кисели, отвар из ягод шиповника, зелёный чай.
Правильный и сбалансированный рацион питания позволяет увеличить продолжительность жизни больного.
Прогноз терапии
Сколько проживет конкретный пациент, точно сказать не сможет ни один врач. На процент выживаемости влияет ряд факторов – стадия и тип патологии, физическое состояние больного на фоне психологического настроя.
Прогноз жизни в среднем составляет от 3 до 5 лет. В каждом случае срок индивидуален. Большую роль играет самочувствие пациента и процесс терапии – правильные и своевременные процедуры увеличивают срок жизни.
Врачи советуют обращаться в поликлинику при появлении любых подозрительных симптомов – это гарантирует раннее обнаружение болезни и полное выздоровление с предотвращением негативных последствий.
Выберите город, желаемую дату, нажмите кнопку «найти» и запишитесь на приём без очереди:
Множественная миелома: прогнозы лечения, степени
Множественная миелома относится к онкологическим заболеваниям. Эта болезнь кровяных клеток, которые вырабатывает костный мозг. При хаотичном и бесконтрольном их делении заболевание ведет к тому, что начинает разрушаться костная ткань.
Симптомы множественной миеломы
К симптомам множественной миеломы относятся:
- Боли в костях. Часто болезненные ощущения локализуются в ребрах и спине.
- Жажда. Больного постоянно преследует сухость во рту и желание пить воду.
- Частые позывы к мочеиспусканию.
- Потеря веса. Человек начинает стремительно худеть.
- Постоянное чувство усталости. Слабость присутствует на протяжении всего дня.
- Тошнота и рвота могут присутствовать у некоторых больных.
- Понижение иммунитета. Отсюда частые заболевания на вирусные и простудные заболевания.

Формы и степени заболевания
Принято рассматривать несколько видов множественной миеломы:
- Миелома, которая имеет очаговые, диффузные и диффузно – очаговые поражения костного скелета человека.
- Миелома может носить разную степень активности. Встречаются вялотекущие формы заболевания, активные и агрессивные.
Причины
Причины, которые вызывают онкологическое заболевание, до сегодняшнего дня неизвестны. Предполагается, что толчком к началу бесконтрольного деления клеток бывает воздействие химических и токсических веществ, ионизирующего излучения, антигенная стимуляция, а также генетическая предрасположенность к образованию раковых клеток.
Диагностика
Диагностика множественной миеломы проходит в условиях онкологических центров. Врач может поставить такой диагноз на основании результатов:
- Осмотра врача,
- Анализов крови (общего клинического и биохимического),
- Полного рентгенологического исследования скелета больного,
- Аспирационной биопсии костного мозга,
- Трепанобиопсии костного мозга.
- Иммуноэлектрофореза белков крови и мочи,
- Магнитно – резонансной томографии (МРТ),
- Компьютерной томографии (КТ),
- Позитронной – эмиссионной томографии (ПЭТ),
- Денситометрии костей.
Врач на своё усмотрение может назначить дополнительные исследования: молекулярные, цитогенетические и другие.
Диагноз «множественная миелома» ставится при:
- Повышенном количестве плазматических клеток в костном мозге (более 10%),
- Концентрации М-протеина в крови и моче (более 30 г/дл),
- Повышенном содержании кальция в крови,
- Анемии,
- Нарушение в работе почек,
- Болях в костях.
Лечение множественной миеломы
Одно и то же заболевание лечится разными препаратами и разными химиотерапевтическими схемами. Каждый пациент имеет свои индивидуальные особенности, возраст, стадию болезни, степень агрессивности и т.д. Основываясь на все эти факторы, врач подбирает лучшую схему для лечения каждого пациента.
Есть такие пациенты, которым не требуется лечение. Показано только наблюдение за своим состоянием и контролем анализов.
Другим больным будет рекомендована только местная терапия, которая будет направлена на предотвращение инфекционных заболеваний, лечение анемии и уменьшение количества аномальных клеток.
Все методики, которыми сегодня лечат больных на множественную миелому, направлены на продление жизни пациента. Полного выздоровления от этой болезни пока не найдено.
Множественную миелому в сегодняшних онкологических больницах и центрах лечат с помощью:
- Химиотерапии. Данное заболевание лечат препаратами таргетного ряда. К нему относятся препараты Талидомид, Леналидомид и Бортезомид (Велкейд).
- Гормонотерапии.
- Трансплантации стволовых клеток.
Основной вид лечения, химиотерапия, имеет множество побочных эффектов (тошнота, рвота, падение лейкоцитов, облысение, нарушение в работе печени и почек, сердечные заболевания и др). Эти побочные эффекты частично снимаются сопроводительной терапией.
На основании специальных исследований определяется агрессивность миеломы. Соответственно, для таких форм заболевания понадобятся современные новые препараты.
Чем раньше начат процесс лечения множественной миеломы, тем больше шансов на то, что болезнь будет локализована. Однако и запущенные формы заболевания поддаются контролю роста раковых клеток и продлению жизни при соответственном лечении.
Осложнения и последствия
Осложнения как от самой болезни, так от проведения химиотерапии довольно серьезные. Довольно часто у больных множественной миеломой случаются переломы. Это происходит из-за хрупкости костей. Во время болезни кости теряют много кальция. Болезнь также вызывает анемию (низкий уровень гемоглобина). Почечная недостаточность, слабость, кровоточивость также сопровождают многих больных миеломой.
Надо опасаться больных на вирусные и инфекционные заболевания. Так, как иммунитет понижен, больные множественной миеломой, часто заболевают на сопутствующие простудные заболевания. Химиотерапия ещё больше ослабляет здоровье человека. Часто присоединяется нейропения, тромбоцитопения, гранулоцитопения и проблемы с печенью и почками.
Профилактика множественной миеломы
Невозможно назвать действия, которые могли бы стать профилактическими методами данной болезни. Так как до сегодняшнего дня неизвестны причины, которые вызывают это заболевание. Правильный образ жизни, занятия спортом, ежедневные прогулки, регулярное и правильное питание, жизнь без стрессов – все это не может сто процентов уберечь от возникновения множественной миеломы. Но увеличит шанс на то, что эта болезнь не поселится в здоровом теле.
Прогнозы, продолжительность жизни
Прогнозы дело неблагодарное, но существует определенная статистика, которую ведут крупные международные институты здравоохранения. Эта статистика говорит о том, что за последнее десятилетие общая выживаемость людей, больных множественной миеломой, увеличилась.
Успех лечения каждого пациента зависит от многих факторов:
- От возраста больного,
- От психологического состояния,
- От общего состояния организма,
- От эффективности выбранного лечения,
- От типа и стадии заболевания,
Хоть множественная миелома не поддается полному излечению, не стоит падать духом. В арсенале сегодняшней медицины имеется много способов лечения для того, чтоб остановить прогрессирование болезни. Больные люди получили шанс на продолжение жизни.
Понимание прогноза множественной миеломы
Один из самых сложных вопросов в онкологии: «Сколько мне осталось жить?»
Пациенты часто сообщают об этом своим врачам после постановки диагноза рака и периодически во время их болезни.
Конечно, на этот вопрос невозможно ответить, потому что мы, врачи, редко можем предсказать, что ждет конкретного пациента в будущем. Мы, вероятно, можем оценить средние значения, но ни один пациент не является средним; каждый уникален.Столкнувшись с этой дилеммой, каждый врач реагирует по-своему. Некоторые предоставляют средние значения, некоторые — нет.
Тем не менее, это невероятно сложно для всех. Пациенты имеют право иметь некоторое представление о прогнозе, но в то же время врачи считают, что не имеют права давать оценки, которых они сами не понимают.
Эта и без того озадачивающая проблема усугубляется при множественной миеломе, потому что общие результаты выживания значительно различаются в зависимости от множества различных переменных, называемых прогностическими факторами.Понимание этих факторов имеет решающее значение не только для врачей, желающих проконсультировать пациентов и выбрать правильную терапию, но и для пациентов, которые часто слышат об этих «факторах риска» или «маркерах высокого риска» от других пациентов, из Интернета и т. Д.
Во-первых, важно признать, что общая выживаемость отдельного пациента с миеломой определяется не только маркерами агрессивной биологии болезни (например, хромосомными аномалиями высокого риска), но также и факторами хозяина (например,g., возраст и общее состояние здоровья) и степень миеломы (стадия).
Во-вторых, каждый из этих факторов по-разному влияет на выживаемость, и с каждым из них нужно подходить по-разному.
Стратегия преодоления хромосомных аномалий высокого риска отличается от стратегий преодоления проблем, связанных с преклонным возрастом, другими проблемами со здоровьем или почечной недостаточностью. Даже в пределах общей группы хромосомных аномалий высокого риска, с некоторыми аномалиями, возможно, придется бороться несколько иначе, чем с другими.
Таким образом, не существует простого и единообразного способа преодоления «высокого риска». Это будет зависеть от того, что именно является фактором высокого риска и что можно сделать с этим конкретным фактором.
В-третьих, со временем все меняется. Например, реакция на терапию (хорошая или плохая) может сильно повлиять на результат и нарушить предыдущие расчеты выживаемости. Точно так же пациенты могут приобретать новые хромосомные аномалии, которые изменяют динамику заболевания и его лечения.
С учетом вышесказанного мы можем теперь обсудить, какие варианты доступны для борьбы с каждым фактором риска.
К факторам хозяина обычно подходят, изменяя интенсивность лечения.
Таким образом, у пациентов пожилого возраста мы избегаем трансплантации стволовых клеток и часто снижаем дозу и интенсивность химиотерапии, чтобы минимизировать токсические побочные эффекты и максимально контролировать миелому.
Для пациентов с почечной недостаточностью мы пробуем такие методы, как плазмаферез и химиотерапия с лекарствами, которые действуют быстро, чтобы попытаться быстро обратить повреждение почек.
Стадия заболевания при миеломе менее важна для выбора терапии, чем при других формах рака.Однако лечение миеломы может быть изменено в отдельных ситуациях в зависимости от стадии заболевания.
Например, у пациентов с множественной миеломой I стадии по системе стадирования Durie-Salmon, у которых есть единственное поражение кости, одного облучения может быть достаточно, в то время как системное лечение необходимо для более поздних стадий.
Биология болезни действительно является одним из наиболее важных факторов, определяющих исход. Среди пациентов с одинаковым возрастом, общим состоянием здоровья и стадией заболевания выживаемость может широко варьироваться в зависимости от маркеров агрессивной биологии болезни.
В настоящее время мы рассматриваем делецию 17p, транслокации t (14; 16), t (14; 20), профилирующую сигнатуру экспрессии генов высокого риска, высокий уровень лактатдегидрогеназы и лейкоз плазматических клеток как факторы высокого риска.
Однако не все пациенты с этими маркерами имеют миелому высокого риска.
Например, недавнее исследование, проведенное моим коллегой доктором Шаджи Кумаром, показывает, что наличие трисомии (дополнительной копии одной или нескольких хромосом) может нейтрализовать эффекты высокого риска определенных факторов высокого риска (т.е., т (14; 16), т (14; 20) и 17п).
Аналогичным образом, транслокация t (4; 14) ранее считалась фактором высокого риска, но недавние исследования показывают, что индукция на основе Velcade (бортезомиб), трансплантация стволовых клеток и консолидация / поддержание на основе Velcade могут быть эффективными против этого. фактор риска.
Какие варианты лечения миеломы высокого риска? В настоящее время ведутся интенсивные исследования по увеличению выживаемости в этой популяции пациентов.
В зависимости от возраста пациента и других проблем со здоровьем варианты лечения различаются, но их много.Большинство исследователей полагают, что лучшая стратегия в целом при миеломе высокого риска — это попытаться добиться полного ответа или как можно более близкого к нему, а затем попытаться поддерживать его.
Хотя важно предоставить пациентам с миеломой высокого риска некоторые данные, чтобы ответить на вопросы о прогнозе, также важно отметить, что ни один маркер не является идеальным. У всех нас есть пациенты с делецией 17p, которые очень хорошо себя чувствуют в течение многих, многих лет и которые бросают вызов предсказаниям учебников.
Наконец, хотя мы составляем планы лечения на основе рассмотренных выше групп факторов риска (факторы хозяина, стадия, маркеры высокого риска), они могут меняться в зависимости от ответа на такую терапию.
Прогрессирующая миелома во время терапии обычно является признаком того, что нам необходимо изменить планы и схемы лечения. Однако ответ на терапию сложен и зависит от множества факторов.
Достаточно сказать, что, хотя отличный ответ на терапию всегда желателен, мы не можем увлекаться только цифрами. Например, есть пациенты, которые очень медленно реагируют на терапию и никогда не достигают полного ответа, но при этом достигают некоторых из лучших показателей выживаемости.
Более важно осознавать, что взаимодействие между ответом и результатом является сложным, и нет нужды горевать из-за неспособности достичь полного ответа.
Я знаю, что эта колонка, вероятно, вызывает больше вопросов, чем дает ответов. Моя цель — подчеркнуть, что оценка и понимание прогнозов — непростая задача.
Я считаю, что хорошо информированные пациенты с миеломой могут работать со своими врачами, чтобы получить полное представление о своей уникальной ситуации и спланировать наиболее подходящую стратегию лечения.
Доктор С. Винсент Раджкумар — профессор медицины в клинике Майо в Рочестере, штат Миннесота. Его исследования сосредоточены на клинических, эпидемиологических и лабораторных исследованиях миеломы и связанных с ней заболеваний.
Фотография доктора С. Винсента Раджкумара, профессора клиники Майо.
.Множественная миелома: стадии | Cancer.Net
НА ЭТОЙ СТРАНИЦЕ: Вы узнаете, как врачи описывают рост или распространение миеломы. Это называется этапом. Используйте меню для просмотра других страниц.
Стадия — это способ описания того, где находится рак, распространился ли он и где он распространился, а также влияет ли он на другие части тела.
Врачи используют диагностические тесты, чтобы определить стадию рака, поэтому определение стадии может быть неполным, пока не будут завершены все тесты.Знание стадии помогает врачу решить, какой вид лечения лучше всего, и может помочь предсказать прогноз пациента, который является шансом на выздоровление. Существуют разные описания стадий для разных типов рака.
При миеломе важно начать с того, испытывает ли пациент симптомы. Обычно людей с впервые диагностированной миеломой классифицируют как:
Бессимптомный , что означает, что у человека нет симптомов и признаков болезни.Пациенты без симптомов обычно находятся под пристальным наблюдением без специального лечения, хотя иногда предлагают терапию, чтобы остановить рост или распространение болезни. Это называется активным наблюдением за тлеющей миеломой (см. Типы лечения).
Симптоматический означает, что у человека есть симптомы и признаки заболевания. Пациенты с симптомами или у которых скоро появятся симптомы, нуждаются в лечении.
Симптомы, связанные с миеломой, описываются мнемонической аббревиатурой «CRAB», где каждая буква соответствует симптому:
C Уровни алюминия повышены, что называется гиперкальциемией.Это определяется как уровень кальция в сыворотке более чем на 0,25 ммоль / л выше верхнего предела нормы или уровень, который превышает 2,75 ммоль / л.
R Проблемы с эналом или почками, определяемые как уровень креатинина выше 173 ммоль / л.
Немия определяется как наличие низкого уровня гемоглобина, который на 2 г / дл ниже нижнего предела нормы, или как уровень гемоглобина менее 10 г / дл.
B одна боль или поражения, в том числе:
Литические поражения (участки поражения костей)
Остеопороз (истончение костей)
Компрессионный перелом позвоночника
Другие симптомы включают симптоматическую повышенную вязкость (сгущение крови), амилоидоз и повторяющиеся серьезные бактериальные инфекции (более 2 эпизодов за 12 месяцев).Пациентам с признаками КРАБ требуется активное лечение.
Люди также могут проходить лечение, даже если у них нет функций CRAB, при соблюдении любого из следующих условий:
.тестов для поиска множественной миеломы
Если симптомы указывают на то, что у человека может быть множественная миелома, проводятся дополнительные анализы.
Лабораторные испытания
Анализ крови
Общий анализ крови (CBC) — это тест, который измеряет уровни эритроцитов, лейкоцитов и тромбоцитов в крови. Если в костном мозге слишком много миеломных клеток, некоторые из этих клеток крови могут быть низкими. Наиболее частая находка — низкое количество эритроцитов (анемия).
Химический анализ крови
Проверяются уровни креатинина, альбумина, кальция и других электролитов в крови.
- Уровни креатинина показывают, насколько хорошо работают ваши почки. Высокий уровень означает, что почки не функционируют должным образом. Это часто встречается у людей с миеломой.
- Альбумин — это белок, содержащийся в крови. Низкий уровень можно увидеть при миеломе.
- Уровень кальция может быть высоким у людей с развитой миеломой. Высокий уровень кальция (гиперкальциемия) может вызывать симптомы усталости, слабости и спутанности сознания.
Также может быть сделан анализ крови для измерения уровня лактодегидрогеназы (ЛДГ). Это может быть полезным индикатором прогноза (перспектив) пациента. Высокие уровни означают, что болезнь находится на более поздней стадии и может иметь худший прогноз.
Анализы мочи
Обычный образец мочи обычно берут для поиска белка миеломы, который просочился через почки. Скорее всего, вас также попросят сдать образец мочи, собранный за 24-часовой период, чтобы он мог определить, сколько присутствует миеломного белка.Эти тесты называются электрофорезом белков мочи (UPEP) и иммунофиксацией мочи.
Количественные иммуноглобулины
Этот тест измеряет уровни в крови различных антител (также называемых иммуноглобулинами). В крови есть несколько различных типов антител: IgA, IgD, IgE, IgG и IgM. Уровни этих иммуноглобулинов измеряются, чтобы определить, являются ли они ненормально высокими или низкими. При множественной миеломе уровень одного типа может быть высоким, а других — низким.
Электрофорез
Антитело, продуцируемое клетками миеломы, является ненормальным, потому что оно моноклональное (все точно так же). Электрофорез сывороточного протеина (SPEP) — это тест, который измеряет антитела в крови и может обнаружить моноклональные антитела. Другой тест, называемый иммунофиксацией или иммуноэлектрофорезом, используется для определения точного типа аномального антитела (IgG, IgA или другого типа). Обнаружение моноклональных антител в крови может быть первым шагом в диагностике множественной миеломы.Этот аномальный белок известен под несколькими разными названиями, включая моноклональный иммуноглобулин , моноклональный белок (M-белок ) , M spike или парапротеин .
Антитела состоят из белковых цепочек: 2 длинных (тяжелых) цепей и 2 более коротких (легких) цепей. Иногда кусочки аномального миеломного белка фильтруются через почки в мочу. Этот белок мочи, известный как белок Бенс-Джонса , является частью антитела, называемой легкой цепью.Тесты, используемые для обнаружения моноклональных антител в моче, называются электрофорезом белков мочи (UPEP) и иммунофиксацией мочи. Чаще всего это делается на основе мочи, собранной в течение 24 часов, а не только на обычном образце мочи.
Легкие цепи, свободные от сыворотки
Этот анализ крови позволяет измерить уровень легкой цепи в крови и проводится при поиске миеломы или амилоидоза легких цепей.
Это наиболее полезно в редких случаях миеломы, при которых М-белок не обнаруживается с помощью SPEP.Поскольку SPEP измеряет уровни интактных (целых) антител, он не может измерять количество только легких цепей.
Этот тест также вычисляет соотношение легкой цепи , которое используется, чтобы увидеть, есть ли у одного типа легкой цепи больше, чем у другого. Есть 2 вида легких цепей: каппа и лямбда. Обычно они присутствуют в крови в равных количествах, что дает соотношение 1: 1. Если одного типа легкой цепи больше, чем другого, соотношение будет другим, что может быть признаком миеломы.
Бета-2 микроглобулин
Это еще один белок, вырабатываемый клетками миеломы. Хотя сам по себе этот белок не вызывает проблем, он может быть полезным индикатором прогноза (перспектив) пациента. Высокие уровни означают, что болезнь находится на более поздней стадии и может иметь худший прогноз.
Типы биопсий
Биопсия костного мозга
У людей с множественной миеломой слишком много плазматических клеток в костном мозге. Процедура, используемая для проверки костного мозга, называется биопсией костного мозга и аспирацией .Это можно сделать как в кабинете врача, так и в больнице.
При аспирации костного мозга задняя часть тазовой кости обезболивается местным анестетиком. Затем в кость вводится игла и с помощью шприца удаляется небольшое количество жидкого костного мозга. Это вызывает кратковременную острую боль. Для биопсии используется игла, чтобы удалить крошечный осколок кости и костного мозга. Пациенты могут ощущать давление во время биопсии. Когда действует обезболивающее, в области биопсии появляется некоторая болезненность.Большинство пациентов могут пойти домой сразу после процедуры.
Ткань костного мозга исследуется в лаборатории, чтобы определить внешний вид, размер и форму клеток, расположение клеток и определить, есть ли в костном мозге миеломные клетки и, если да, то сколько. Аспират (жидкая часть костного мозга) также может быть отправлен на другие тесты, включая иммуногистохимию и проточную цитометрию, а также хромосомные анализы, включая кариотип и флуоресцентную гибридизацию in situ (также известную как FISH).
- Иммуногистохимия : Часть образца биопсии обрабатывается специальными белками, которые вызывают изменение цвета и помогают идентифицировать клетки миеломы.
- Проточная цитометрия: Образец костного мозга обрабатывают специальными белками, которые прикрепляются только к определенным клеткам. Это может помочь определить, являются ли эти клетки аномальными, и являются ли они клетками миеломы, клетками лимфомы, каким-либо другим раком или незлокачественным заболеванием.
- Cytogenetics : Тест, который оценивает хромосомы (длинные цепи ДНК) в нормальных клетках костного мозга и клетках миеломы.Некоторые клетки миеломы могут иметь слишком много хромосом, слишком мало хромосом или другие хромосомные аномалии (например, транслокации и делеции). Обнаружение этих изменений иногда может помочь в прогнозировании прогноза (мировоззрения) человека. Цитогенетическое тестирование обычно занимает от 2 до 3 недель, чтобы получить результат.
- Флуоресцентная гибридизация in situ (FISH): В нем используются специальные флуоресцентные красители, которые прикрепляются только к определенным частям хромосом. Он может обнаружить большинство хромосомных изменений (таких как транслокации и делеции), которые можно увидеть в лаборатории в стандартных цитогенетических тестах, а также некоторые изменения, слишком незначительные, чтобы их можно было увидеть с помощью обычного цитогенетического тестирования.Он очень точен, и результаты часто можно получить в течение нескольких дней.
Аспирационная биопсия тонкой иглой
При аспирации тонкой иглой (FNA) используется очень тонкая игла и шприц для забора небольшого количества ткани из опухоли или лимфатического узла. Врач может направить иглу, чувствуя увеличенный лимфатический узел у поверхности тела. Если аномальная область (опухоль) находится глубоко в теле, иглу можно направлять, наблюдая за ней на компьютерной томографии (КТ) (см. Обсуждение тестов визуализации далее в этом разделе).Главное преимущество FNA в том, что не требуется хирургического вмешательства. Недостатком является то, что в некоторых случаях тонкая игла не может удалить достаточно ткани для постановки точного диагноза.
Биопсия стержневой иглой
Этот тест аналогичен FNA, но используется игла большего размера и отбирается образец ткани большего размера.
Если область на рентгеновском снимке выглядит ненормально, может потребоваться биопсия, чтобы подтвердить, что это плазмоцитома. Чаще всего применяется игольчатая биопсия (тонкая или стержневая).
Визуальные тесты
Визуализирующие тесты используют звуковые волны, рентгеновские лучи, магнитные поля или радиоактивные вещества для создания изображений внутренней части вашего тела.Визуализационные тесты могут проводиться по ряду причин, например:
- Чтобы посмотреть на подозрительные участки, которые могут быть раковыми
- Чтобы узнать, как далеко распространился рак
- Чтобы помочь определить, работает ли лечение
Рентгенография костей
Рентген может обнаружить разрушение кости, вызванное клетками миеломы. Часто врачи делают серию рентгеновских снимков, охватывающих большую часть костей. Это называется обследованием костей или обследованием скелета .
КТ (компьютерная томография)
При компьютерной томографии используются рентгеновские снимки, полученные под разными углами, которые компьютер комбинирует для получения подробных изображений органов. Иногда этот тест может помочь определить, были ли ваши кости повреждены миеломой. Его также можно использовать для ввода иглы для биопсии в проблемную зону.
Магнитно-резонансная томография (МРТ)
Как и компьютерная томография, МРТ показывает подробные изображения мягких тканей тела.Но при МРТ вместо рентгеновских лучей используются радиоволны и сильные магниты. Перед сканированием в вену можно ввести контрастный материал под названием гадолиний, чтобы лучше рассмотреть детали.
МРТ очень полезны для изучения костей, головного и спинного мозга. Поскольку МРТ позволяет обнаружить плазмоцитомы, которые нельзя увидеть на обычных рентгеновских снимках, они могут быть полезны, если у пациента есть боль в кости, но на рентгеновском снимке не видно никаких аномалий. МРТ также можно использовать для исследования костного мозга у пациентов с множественной миеломой.
Сканы позитронно-эмиссионной томографии (ПЭТ)
Для этого теста радиоактивный сахар вводится в вену и перемещается по телу. Раковые клетки поглощают большое количество этого сахара. Затем специальная камера делает снимки, которые показывают области, где сахар собирается по всему телу. ПЭТ-сканирование часто сочетается с компьютерной томографией (известной как ПЭТ / КТ-сканирование ).
Когда у пациента обнаруживается одиночная плазмоцитома, для поиска других плазмоцитом можно использовать ПЭТ-сканирование.Как и МРТ, сканирование с помощью ПЭТ позволяет обнаружить плазмоцитомы, которые нельзя увидеть на обычных рентгеновских снимках, поэтому они полезны, если у пациента есть боль в кости, но результат рентгенографии отрицательный.
Эхокардиограмма (ЭХО)
Амилоидоз часто поражает сердце, поэтому, если ваш врач диагностирует или подозревает у вас это заболевание, может быть назначена эхокардиограмма (ЭХО). Этот тест в основном представляет собой ультразвуковое исследование сердца. Он использует звуковые волны, чтобы посмотреть на сердечную мышцу и на то, насколько хорошо она работает. На эхокардиограмме можно увидеть, нормальный ли размер сердца и нормально ли оно работает.Это также особенно полезно при подозрении на амилоид, потому что амилоид в сердечной мышце отличается от нормальной сердечной мышцы.
Диагностика множественной миеломы
Множественная миелома часто диагностируется на основании анализов, симптомов пациента и медицинского осмотра пациента. Для диагностики множественной миеломы необходимо:
1. Опухоль из плазматических клеток (подтвержденная биопсией) ИЛИ не менее 10% плазматических клеток в костном мозге И
2. Хотя бы одно из следующего:
- Повышенный уровень кальция в крови
- Нарушение функции почек
- Низкое количество эритроцитов (анемия)
- Дыры в костях от опухоли, обнаруженные при визуализирующих исследованиях (КТ, МРТ, ПЭТ)
- Увеличение одного типа легкой цепи в крови, так что один тип встречается в 100 раз чаще, чем другой
- 60% или более плазматических клеток в костном мозге
Тлеющая миелома
Этот термин используется для обозначения ранней миеломы, не вызывающей никаких симптомов.Люди с тлеющей миеломой имеют некоторые признаки множественной миеломы, например любые из следующих:
- Плазматические клетки костного мозга от 10% до 60%
- Высокий уровень моноклонального иммуноглобулина (М-протеин) в крови
- Высокий уровень легких цепей в моче (также называемый белком Бенс-Джонса)
Но у них нормальный анализ крови, нормальный уровень кальция, нормальная функция почек, отсутствие повреждений костей или органов и никаких признаков амилоидоза.
Амилоидоз легкой цепи
Диагноз амилоидоза легких цепей ставится, когда у пациента есть ВСЕ из следующего:
- Признаки и симптомы амилоидоза
- Биопсия, показывающая амилоид в любой ткани (жировой ткани, костном мозге или органе, таком как сердце)
- Положительный тест, показывающий, что амилоидный белок представляет собой легкую цепь, а не тяжелую цепь
- Аномальные плазматические клетки в костном мозге, высокий уровень М-белка в крови или высокий уровень М-белка в моче.
Амилоид может накапливаться в любой ткани, и биопсия может помочь диагностировать это заболевание. Иногда это можно увидеть на биопсии костного мозга. При биопсии, которая проводится чаще всего для поиска амилоида, используется игла для удаления жира со стенки живота (живота). Это происходит после того, как кожа над местом биопсии обезболивается лекарством. Врач использует специальное пятно на удаленном жире, чтобы найти амилоид.
Поскольку амилоид часто поражает сердце и почки, их также можно сделать биопсией для поиска амилоида.Это редко необходимо, чтобы выяснить, есть ли у пациента амилоидоз легких цепей, но иногда это делают у кого-то с амилоидом, если не ясно, что его проблемы с сердцем или почками вызваны амилоидом или какой-либо другой проблемой.
Часто проводятся и другие тесты, чтобы подтвердить, что у пациента амилоидоз легких цепей, а не какой-либо другой вид. К ним относятся биопсия костного мозга, свободные легкие цепи сыворотки и электрофорез мочи (это обсуждалось ранее в этом разделе).
.