Невус пограничный — клиника, диагностика, прогноз
Обновлено: 31.10.2022
Диагностика и дифференциация родинок — невусов эпидермального меланоцитарного происхождения
По патоморфологическим признакам (по глубине расположения невусных клеток) обычные невомеланоцитарные приобретенные невусы подразделяются на юнкциональные (пограничные), смешанные (сложные) и внутридермальные. Иногда в обычных родинках могут встречаться гистологические особенности диспластических невусов (лентигинозная меланоцитарная дисплазия, клеточная атипия меланоцитов, лимфоцитарная инфильтрация в сосочковом слое дермы и другие).
Данное обстоятельство некоторыми исследователями считается допустимым для обычных родинок и не требует их переквалификации в диспластические невусы. Чаще это возможно у невусов особых локализаций и невусов, появившихся и существующих в детском возрасте.
Основным методом диагностики обычных невомеланоцитарных приобретенных невусов является клинико-анамнестический. При подозрении о наличии у обследуемых потенциально злокачественных и злокачественных пигментных опухолей кожи применяются морфологические методы диагностики (цитологический и гистологический). При осмотре образований на коже используются лупа (с 6- или 7-кратным увеличением) и боковое освещение.
При подозрении о наличии у обследуемых потенциально злокачественных и злокачественных пигментных опухолей кожи применяются морфологические методы диагностики (цитологический и гистологический). При осмотре образований на коже используются лупа (с 6- или 7-кратным увеличением) и боковое освещение.
Диагноз основывается на знании элементов кожной сыпи, особенностей их окраски; помогают для постановки диагноза также пальпация образований и анамнестические данные. Другим методом диагностики является фотографирование очагов поражения с помощью макросъемки с последующим просмотром фотографий на экране фотоаппарата или компьютера. Перспективным методом диагностики пигментных опухолей кожи является дерматоскопия. Это неинвазивный диагностический метод визуальной оценки поражений кожного покрова.
а — невус пограничный невомеланоцитарный розовато-коричневатый
б — невусы пограничные невомеланоцитарные однородные коричневые
Дерматоскопия позволяет более тщательно изучить поверхность кожи и субэпидермальные структуры. Она дает возможность распознавать морфологические структуры, невидимые невооруженным глазом, для быстрого подтверждения диагноза. Раньше врачи удаляли все «родинки», которые вызывали минимальное подозрение, и оставляли пациенту множество ненужных шрамов. Применение дерматоскопии позволяет избежать ненужных профилактических удалений. Дерматоскопия может определять тактику хирургического лечения.
Она дает возможность распознавать морфологические структуры, невидимые невооруженным глазом, для быстрого подтверждения диагноза. Раньше врачи удаляли все «родинки», которые вызывали минимальное подозрение, и оставляли пациенту множество ненужных шрамов. Применение дерматоскопии позволяет избежать ненужных профилактических удалений. Дерматоскопия может определять тактику хирургического лечения.
Злокачественные опухоли удаляют широким иссечением. Если обнаруживается, что это на 90% доброкачественное образование, то применяется поверхностное удаление, что позволяет снизить риск образования рубцов. С помощью дерматоскопии можно проводить дифференциальную диагностику пигментной формы базалиомы, себорейного кератоза, доброкачественных меланоцитарных невусов, меланоопасных невусов (диспластический и врожденный невоклеточные невусы, злокачественное лентиго) и поверхностно распространяющейся меланомы. Совпадение дерматоскопического результата с морфологическим диагнозом составляет 92,2%.
У людей с множеством родинок необходимо определить сигнатуру невусов. У таких пациентов появляющиеся новые невусы по клиническим и морфологическим признакам похожи на предыдущие родинки. Определение количества и клинико-морфологических вариантов родинок у индивидуума называется «сигнатура невусов».
Дифференциальный диагноз прежде всего проводят с диспластическими невусами и меланомой. После идентификации сигнатуры невусов необходимо обращать внимание на появление признака «гадкого утенка». У одного человека сигнатура невусов представлена, как правило, несколькими вариантами обычных родинок. При появлении пигментного образования, которое резко отличается от предыдущих невусов, необходимо заподозрить у пациента возникновение диспластического невуса или меланомы. Кроме того, у пациентов после 30 лет начинают возникать очаги себорейного кератоза.
Данная опухоль также очень часто встречается у людей и требует проведения дифференциальной диагностики с меланоцитарными новообразованиями.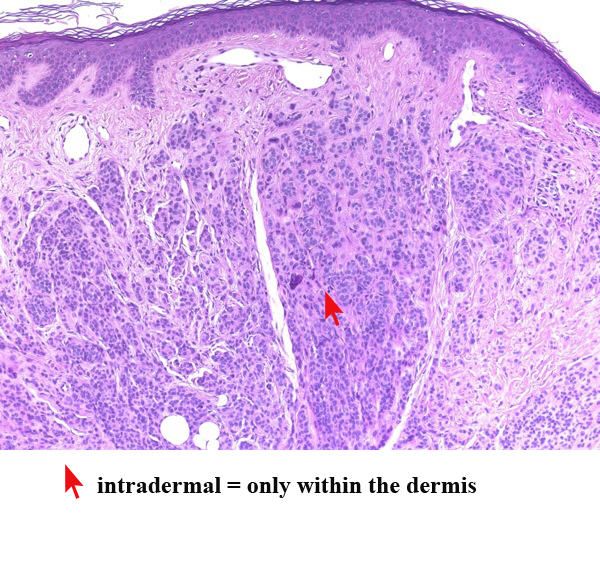
а — регрессирующий пограничный невомеланоцитарный невус у женщины 36 лет.
Со слов пациентки невус в течение нескольких месяцев стал светлее и уменьшился в размере
б — невус сложный невомеланоцитарный однородный светло-коричневый с сохраненным кожным рисунком на поверхности.
Невус слегка и равномерно приподнят над поверхностью кожи
в — невус сложный невомеланоцитарный равномерно возвышающийся однородный коричневый с ростом щетинистых волос
г — невус сложный невомеланоцитарный темной окраски
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Невус пограничный — клиника, диагностика, прогноз
Синонимы пограничных невусов: юнкциональный или переходный невус, родинка.
Определение. Приобретенный пигментный невус, невусные клетки которого расположены только на границе эпидермиса и дермы.
Возраст и пол. Появляется в раннем детском возрасте. Первые элементы возникают, как правило, с 6—12 месяцев от рождения. Половых предпочтений нет.
Половых предпочтений нет.
Элементы сыпи пограничных невусов. Круглое или овальное пятно, иногда незначительно приподнятое над уровнем кожи, размером менее 1 см, с четкими ровными границами. Очаги, как правило, множественные. Все пограничные невусы по форме являются плоскими образованиями. В третьей главе книги подробно изложены различные клинические варианты плоских обычных родинок.
Цвет однородный: различные оттенки коричневого, розового.
Локализация любая. Иногда невусы располагаются на ладонях, подошвах и в области половых органов.
Гистология невуса пограничного. Гнезда невусных клеток в нижней части эпидермиса. Верхние слои эпидермиса без особых изменений, отмечается лишь удлинение эпидермальных выростов. Невусные клетки крупнее нормальных меланоцитов, с округлыми или, значительно реже, вытянутыми ядрами, небольшими базофильными ядрышками, с обильной светлой цитоплазмой, в которой может быть большое количество пигмента.
Наблюдается ретракционный артефакт, благодаря которому меланоциты невуса не прилегают к окружающим кератиноцитам.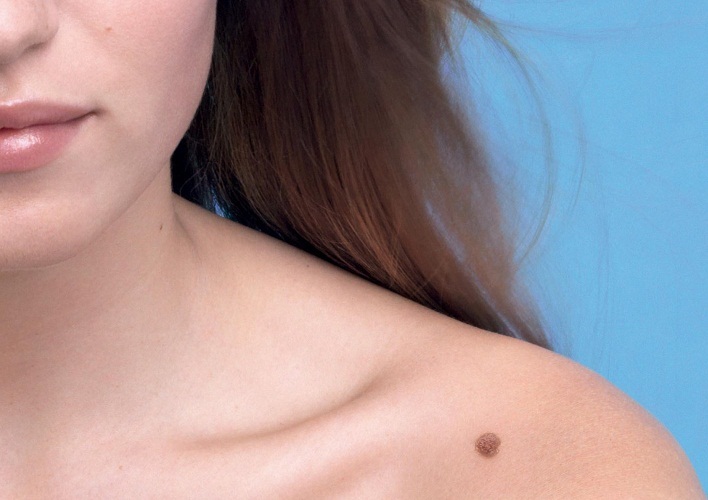 В случаях, когда невус сильно пигментирован, определяется элиминация меланина через вышележащие слои эпидермиса. Невусные клетки могут быть четко отграниченными от эпидермиса и дермы в виде гнезд («неактивный пограничный невус»).
В случаях, когда невус сильно пигментирован, определяется элиминация меланина через вышележащие слои эпидермиса. Невусные клетки могут быть четко отграниченными от эпидермиса и дермы в виде гнезд («неактивный пограничный невус»).
Однако в некоторых случаях невусные клетки интимно связаны с эпидермисом, как бы сползают с его базального слоя (феномен «скапливания») в виде нечетко контурированных групп и одиночных клеток, имеющих тенденцию к проникновению в дерму («активный пограничный невус»). При этом правильность строения слоев эпидермиса нарушается, границы его с дермой становятся нечеткими. В дерме может наблюдаться гистиоцитарная инфильтрация, обычно слабо выраженная.
В активных пограничных невусах наблюдаются изменения, напоминающие ранние признаки озлокачествления. В детском возрасте подобные изменения отмечаются нередко и не должны вызывать тревоги. Активные пограничные невусы у взрослых людей, особенно при наличии вакуолизации, значительного атипизма клеток и митозов, следует расценивать как самую начальную фазу озлокачествления.
Диагноз устанавливается клинически.
Дифференцируют пограничный невус по клиническим признакам с простым лентиго. Эти два меланоцитарных поражения клинически не отличаются друг от друга. Однако простое лентиго чаще возникает на губе (преимущественно на нижней) или на половом члене (обычно на головке). Кроме того, в настоящем атласе в третьей главе выделены различные клинико-морфологические варианты обычных родинок, в связи с этим целесообразно проводить дифференциальную диагностику в этих нозологических группах.
Течение и прогноз. Невус пограничный, который возник в раннем детстве, в результате пролиферации невусных клеток и продвижения их в дерму становится смешанным. Обычно это происходит в пубертатном периоде. После исчезновения пограничного компонента он является внутридермальным меланоцитарным невусом. Это, как правило, возникает в 10—30 лет. В некоторых случаях обычные приобретенные невусы остаются пограничными всю жизнь пациентов. Это прежде всего касается невусов особых локализаций, которые рассмотрены в пятой главе атласа.
Невусы пограничные могут разрешиться, а в некоторых случаях трансформироваться в диспластические и затем в меланому.
Пограничный пигментный невус
Пограничный пигментный невус — пигментированный узелок размером до 1 см, окраска которого может варьировать от светло-коричневого и серого цвета до черного. Пограничный невус может иметь любую локализацию. Чаще бывает единичным. Диагностика проводится путем дерматологического осмотра, дерматоскопии, сиаскопии. В целях профилактики меланомы рекомендовано удаление невуса лазером, радиоволновым аппаратом, жидким азотом, электрокоагуляцией или путем хирургического иссечения. При необходимости производится гистологическое исследование удаленного материала.
Общие сведения
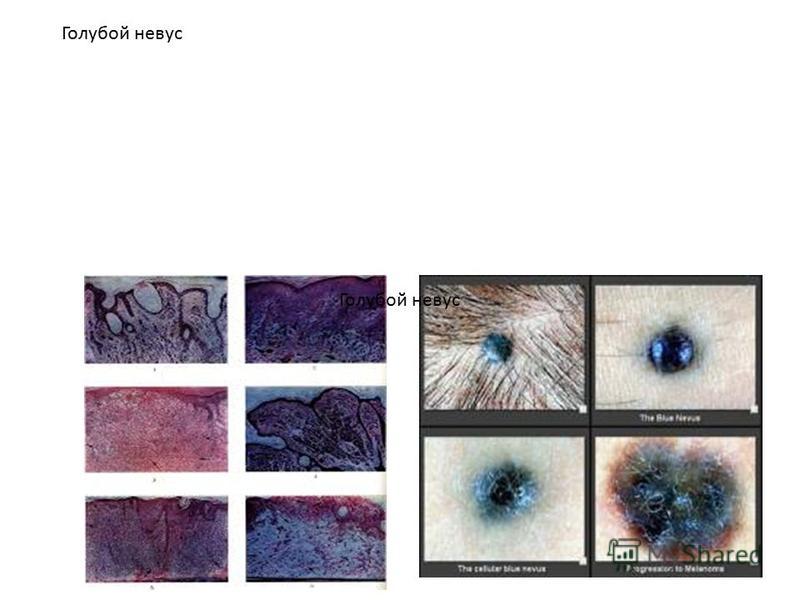
Пограничный пигментный невус чаще всего бывает врожденным новообразованием. Реже он появляется в детском возрасте, пубертатном периоде или позже. Наряду с невусом Ота, голубым невусом, меланозом Дюбрейля и гиганским пигментным невусом пограничный пигментный невус может претерпевать злокачественное перерождение. Поэтому дерматология относит его к меланомоопасным невусам.
Поэтому дерматология относит его к меланомоопасным невусам.
Симптомы пограничного пигментного невуса
Пограничный пигментный невус представляет собой уплощенный узелок серого, черного, светло- или темно-коричневого цвета. Его размеры бывают от нескольких миллиметров до 4-5 см, но чаще не превышают 1 см. Поверхность невуса гладкая и сухая, может быть немного неровной. Отличительной особенностью является отсутствие роста волос (даже пушковых) на поверхности невуса. Пограничный невус не имеет излюбленной локализации и может располагаться на любом участке тела, в том числе на ладонях и подошвах, где другие виды невусов практически не встречаются. Обычно пограничный невус является одиночным образованием, но встречаются случаи и множественного невуса.
Разновидностью пограничного невуса является кокардный невус, характеризующийся постепенным усилением пигментации по периферии образования, за счет чего с течением времени невус приобретает вид концентрических колец, отличающихся различной насыщенностью окраски.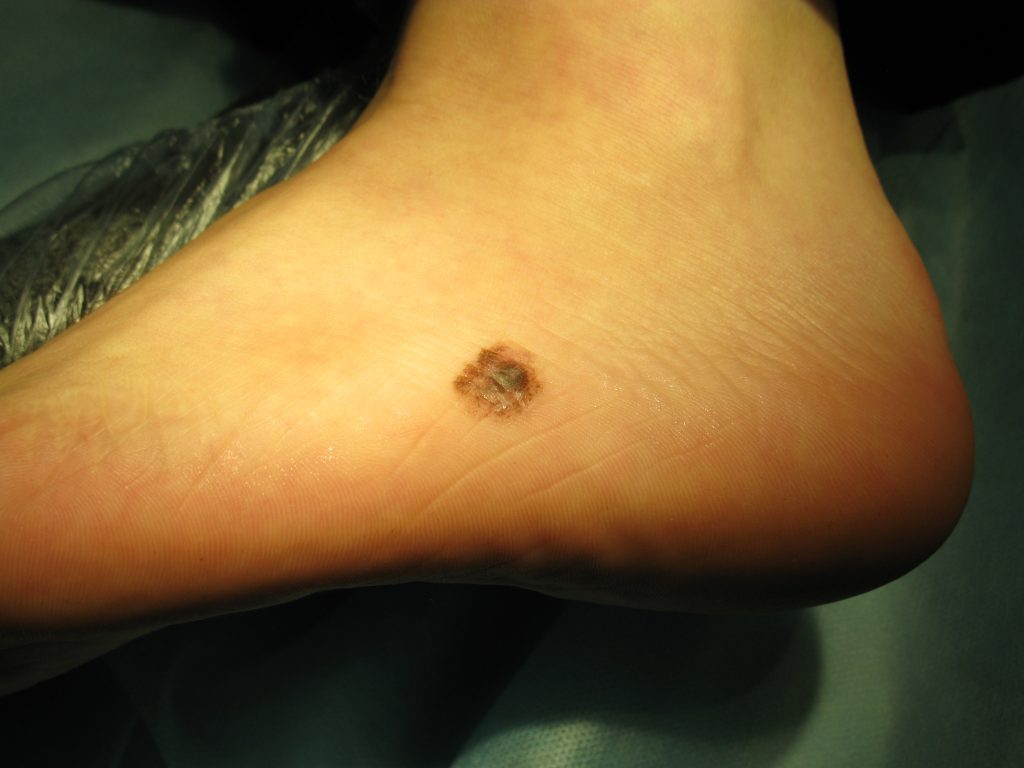 Изменение цвета пограничного пигментного невуса, его резкое увеличение, появление трещин, эрозий или бугристостей на его поверхности, возникновение покраснения вокруг невуса или расплывчатость его границ могут свидетельствовать о злокачественной трансформации и требуют безотлагательной консультации дерматолога.
Изменение цвета пограничного пигментного невуса, его резкое увеличение, появление трещин, эрозий или бугристостей на его поверхности, возникновение покраснения вокруг невуса или расплывчатость его границ могут свидетельствовать о злокачественной трансформации и требуют безотлагательной консультации дерматолога.
Диагностика пограничного пигментного невуса
Пограничный пигментный невус диагностируется в ходе дерматологического осмотра и дерматоскопии. Дополнительным методом является сиаскопия. При подозрении на малигнизацию невуса требуется консультация дерматоонколога.
Биопсия кожи из области пограничного пигментного невуса обычно не проводится, поскольку такое травмирование может дать толчок к его злокачественному перерождению. Гистологическое исследование осуществляется после удаления невуса хирургическим или радиоволновым методом.
Пограничный пигментный невус дифференцируют от других пигментных образований: веснушек, пигментных пятен, невуса Сеттона, меланоза Дюбрейля, голубого невуса.
Лечение пограничного пигментного невуса
Пациентам с пограничным пигментным невусом рекомендовано наблюдение дерматолога. Как доброкачественное новообразование кожи он не нуждается в срочном удалении. Но следует помнить, что пограничный пигментный невус относится к меланомоопасным и лучшим способом предупреждения меланомы является удаление невуса. Показанием для хирургического лечения невуса является его постоянная травматизация, особенно при расположении на подошвах или ладонях.
Удаление пограничного пигментного невуса может проводиться хирургическим скальпелем, лазером или радиоволновым аппаратом. Электрокоагуляция и криодеструкция невуса не желательна, так как по мнению некоторых специалистов эти методы удаления вызывают сильную травматизацию тканей, что может привести к развитию меланомы на месте удаленного пигментного невуса.
Удаление родинок лазером не оставляет после себя косметического дефекта. Однако оно может применяться только в тех случаях, когда гистологическое исследование удаленного материала не требуется.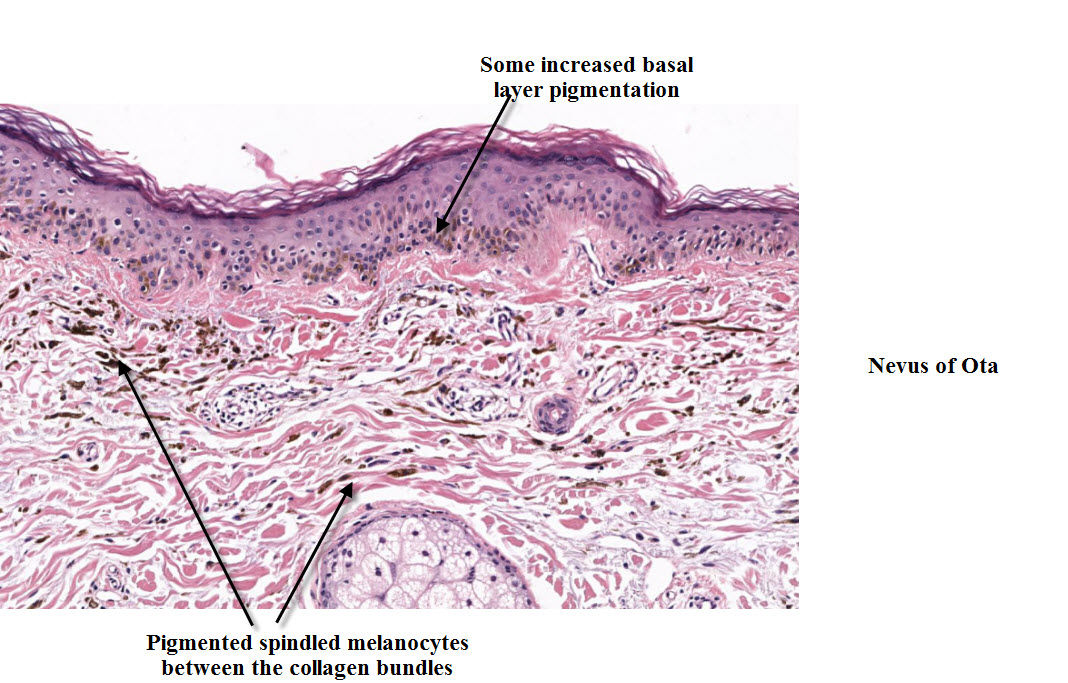 Удаление невусов радиохирургическим ножом чаще проводится при их размерах до 5 мм. Оба метода при небольших размерах образования не требуют наложения швов. При выявлении признаков злокачественной трансформации невуса проводится его срочное хирургическое иссечение с последующим гистологическим исследованием удаленного материала.
Удаление невусов радиохирургическим ножом чаще проводится при их размерах до 5 мм. Оба метода при небольших размерах образования не требуют наложения швов. При выявлении признаков злокачественной трансформации невуса проводится его срочное хирургическое иссечение с последующим гистологическим исследованием удаленного материала.
Сложный пигментный невус
Сложный пигментный невус — доброкачественное пигментное образование коричневого цвета, расположенное одновременно в эпидермальном слое кожи и дерме. Сложный невус имеет вид округлой, возвышающейся над уровнем кожи папулы или бородавки диаметром до 1 см. Его диагностика включает осмотр, дерматоскопию и сиаскопию, при необходимости — УЗИ. Гистология сложного пигментного невуса проводится после его удаления. Учитывая вероятность трансформации невуса в меланому, пациентам необходимо наблюдение дерматолога. Наиболее безопасными и оптимальными способами удаления сложного пигментного невуса является радиоволновой метод и хирургическое иссечение.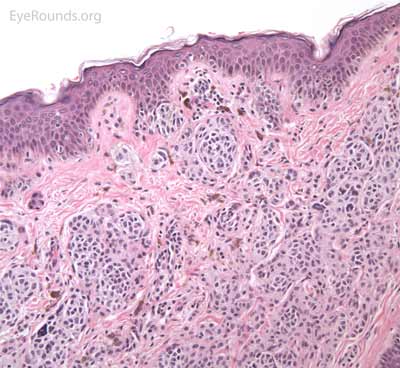
Вместе с интрадермальным и пограничным пигментным невусом сложный пигментный невус относится к основным типам меланоцитарных невусов эпидермального происхождения. Свой рост он начинает в верхнем слое кожи — эпидермисе, а затем прорастает в дерму. Таким образом, в отличие от большинства других родинок, сложный пигментный невус располагается одновременно и в эпидермисе, и в дерме. Этот факт и послужил поводом для его названия — дермоэпидермальный или сложный невус.
Сложный пигментный невус является доброкачественным новообразованием кожи. Однако по данным разных авторов трансформация в меланому может произойти в 50-80% случаев сложного пигментного невуса. Поэтому в клинической дерматологии он классифицируется как меланомоопасный и требует определенной онконастороженности.
Проявления сложного пигментного невуса
Благодаря своему расположению в обоих слоях кожи сложный пигментный невус сочетает признаки внутриэпидермального (пограничного) и внутридермального невуса.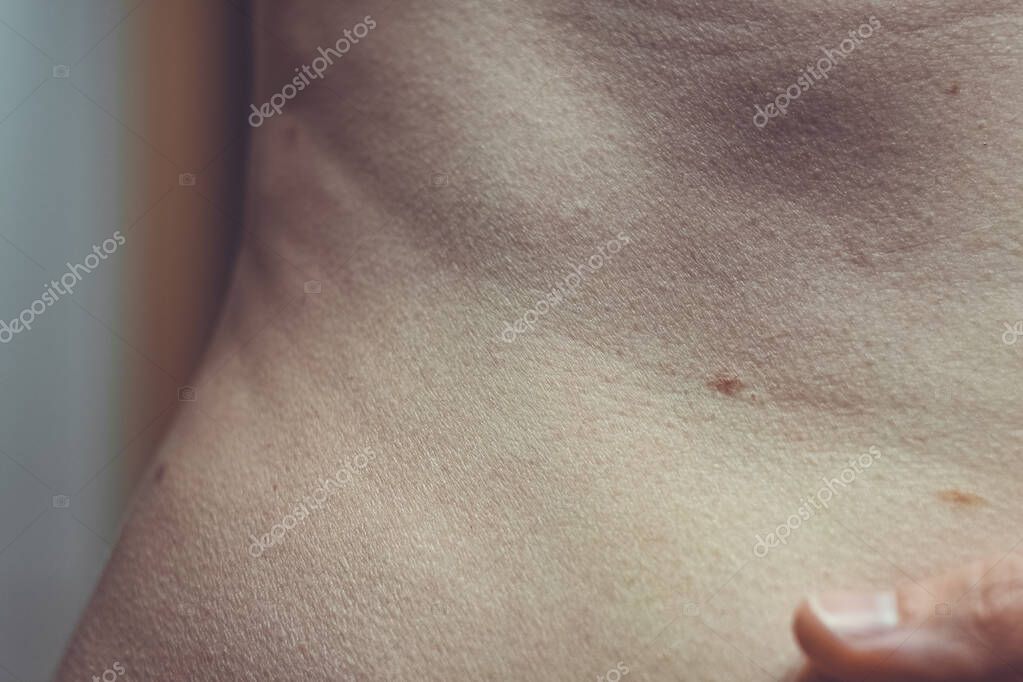 Эпидермальный компонент невуса обуславливает его интенсивную коричневую, а в некоторых случаях почти черную, окраску. Наличие внутридермального компонента способствует тому, что невус немного приподнят над общим уровнем кожи и поэтому может напоминать обыкновенную бородавку.
Эпидермальный компонент невуса обуславливает его интенсивную коричневую, а в некоторых случаях почти черную, окраску. Наличие внутридермального компонента способствует тому, что невус немного приподнят над общим уровнем кожи и поэтому может напоминать обыкновенную бородавку.
Сложный пигментный невус имеет вид папулы или узла куполообразной, круглой формы. Его поверхность чаще гладкая, на ней отмечается рост щетинистых волос. Встречаются сложные невусы с ороговевающей или бородавчатой поверхностью. В большинстве случаев невус располагается на лице или волосистой части головы, но может иметь любую локализацию. Сложный невус редко достигает значительного размера, обычно его диаметр не превышает 1 см.
Диагностика сложного пигментного невуса
Сложный пигментный невус диагностируется дерматологом на основании данных осмотра, дерматосокопии и сиаскопии пигментного образования. Для определения степени прорастания невуса в дерму может применяться УЗИ кожного образования. Подозрение на злокачественное перерождение невуса или меланому является показанием для срочной консультации дерматоонколога.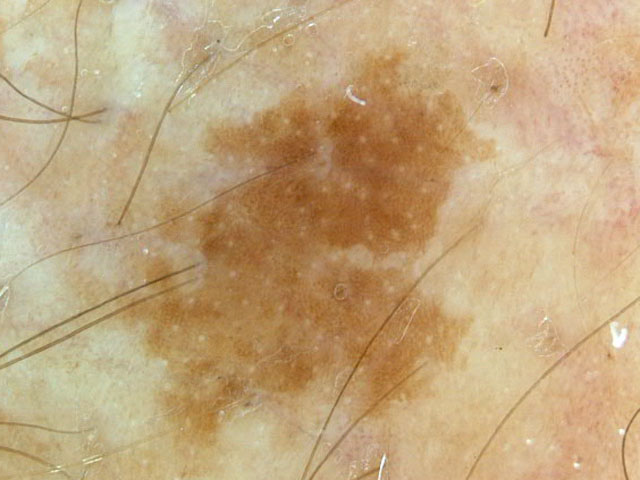
Проведение биопсии сложного невуса опасно его травмированием, которое может привести к злокачественному перерождению в меланому. По этой причине гистологическое исследование тканей невуса проводится чаще всего после его полного удаления. Оно выявляет характерное расположение гнезд невусных клеток как в эпидермисе, так и в дерме.
Дифференциальная диагностика сложного пигментного невуса проводится в первую очередь с меланомой и другими видами пигментных невусов: голубым невусом, пограничным пигментным невусом, невусом Сеттона, меланозом Дюбрейля, а также с бородавками, папилломами, старческой кератомой, дерматофибромой.
Лечение сложного пигментного невуса
Сложный пигментный невус требует наблюдения дерматолога. Абсолютным показанием к его лечению (удалению) является регулярная травматизация или появление признаков озлокачествления. Удаление невуса может быть проведено из косметических соображений. К способам удаления сложного пигментного невуса относятся: удаление лазером, радиоволновой метод и хирургическое иссечение. Электрокоагуляция и криодеструкция не применяются из-за опасности травматизации образования и неполного его удаления, что может стимулировать злокачественный рост.
Электрокоагуляция и криодеструкция не применяются из-за опасности травматизации образования и неполного его удаления, что может стимулировать злокачественный рост.
Удаление родинок лазером применимо в случае сложного невуса, если оно заключается в использовании лазера в качестве скальпеля и позволяет провести последующее гистологическое изучение удаленного образования. Наиболее целесообразно применение радиоволнового метода или хирургическое иссечение сложного невуса, так как они дают возможность полного удаления невусных клеток, что имеет большое значение в плане предупреждения меланомы.
Родинки. Невусы.
Родинка или невус – это врожденное или появившееся в течение жизни доброкачественное пигментное образование на коже. Родинки могут быть различными по форме, размеру и цвету: плоские в виде пятнышка или выпуклые, как горошина, точечные или больших размеров, от светло-телесного до темно-коричневого цвета. Под воздействием неблагоприятных внешних агентов (избыточное количество ультрафиолета, травмы невуса и т.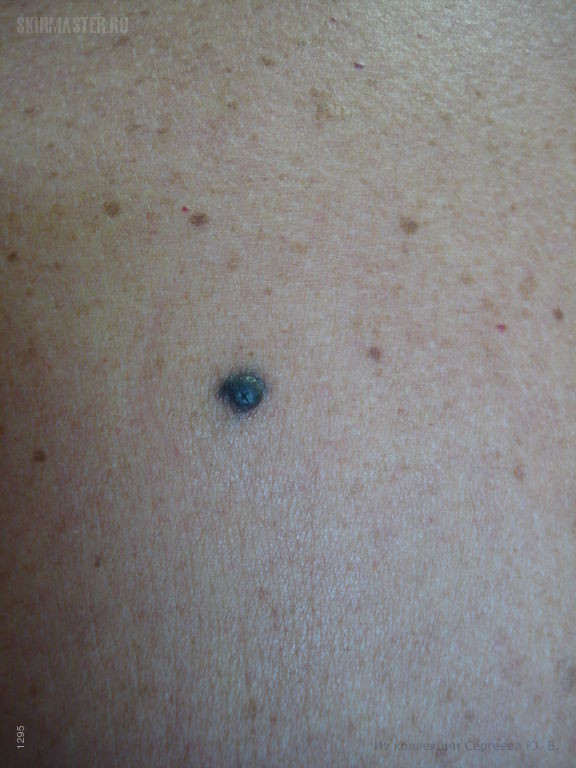 д.) из родинки может развиться злокачественное новообразование – меланома.
д.) из родинки может развиться злокачественное новообразование – меланома.
Причины появления родинок (невусов)
Врожденные невусы
Причины возникновения родинок (невусов) можно разделить на две большие группы: врожденного и приобретенного характера. Врожденные невусы являются пороком эмбрионального развития, в основе которого лежит нарушение процесса миграции клеток меланобластов (предшественников пигментных клеток меланоцитов) из нейроэктодермальной трубки в кожу. Скопление этих пигментных клеток в коже и приводит к образованию родинок (невусов).
На теле новорожденных родинки не видны, но они начинают проявляться уже на первых годах жизни. В зависимости от размера родинки делятся на мелкие (d — от 0,5 до 1,5 см), средние (d -от 1,5 до 10 см) и крупные (диаметром более 10 см). Крупные невусы, занимающие отдельные анатомические участки тела (например, ягодицу), называются гигантскими.
Мелкие родинки неопасны в плане перерождения в злокачественную опухоль, а средние, крупные и особенно гигантские значительно больше подвержены озлокачествлению. Вероятность злокачественного перерождения гигантских невусов в меланому составляет от 10 до 50%. Люди, имеющие на теле родинки больших размеров, должны находиться под наблюдением дерматолога и онколога. Такие невусы нельзя подвергать ультрафиолетовому облучению, а в некоторых случаях с профилактической целью лучше удалить.
Вероятность злокачественного перерождения гигантских невусов в меланому составляет от 10 до 50%. Люди, имеющие на теле родинки больших размеров, должны находиться под наблюдением дерматолога и онколога. Такие невусы нельзя подвергать ультрафиолетовому облучению, а в некоторых случаях с профилактической целью лучше удалить.
Приобретенные невусы
В течение жизни количество родинок постоянно изменяется. Они могут появляться на новых участках тела, изменять свои контуры, цвет, рельеф. Поэтому за родинками следует постоянно наблюдать самостоятельно и показывать их врачу.
Появление родинок в течение жизни генетически обусловлено: если родинки были у родителей, то они наверняка передадутся и ребенку.
Значительное увеличение количества родинок связано с эндокринной перестройкой организма и происходит в подростковом возрасте и во время беременности. Появление новых родинок провоцируют кожные инфекции (прыщи, раздражения, сыпь и т. д.), вызывая воспалительные изменения эпидермиса. Но самым мощным катализатором роста и увеличения числа родинок служит избыточная инсоляция кожи. Поэтому обладателям значительного количества родинок следует ограничить себя в посещении солярия и пребывании под солнцем.
Но самым мощным катализатором роста и увеличения числа родинок служит избыточная инсоляция кожи. Поэтому обладателям значительного количества родинок следует ограничить себя в посещении солярия и пребывании под солнцем.
У грудных детей невусы встречаются в 4-10% случаев, а в возрасте 15-16 лет они имеются уже более чем у 90% людей. С возрастом происходит уменьшение числа родинок. Так, в 20-25 лет их количество на теле в среднем равно 40, к 80-85 годам у большинства людей нет ни одной родинки. В зрелом возрасте на теле человека располагается 15-20 невусов.
В зависимости от локализации в коже приобретенные невусы делятся на внутридермальные (скопления меланоцитов располагаются глубоко в дермальном слое кожи), эпидермальные (скопления клеток образуются в эпидермисе — верхнем слое кожи) и смешанные или пограничные (скопления меланоцитов находятся на границе эпидермиса и дермы).
Приобретенные внутридермальные и эпидермальные родинки обычно выглядят как горошины. Пограничный невус, в большинстве случаев, имеет вид плоского, на одном уровне с кожей, коричневатого пятна.
Диагностика невусов
Жизненно важно вовремя распознать злокачественность родинки, отличить ее от доброкачественного невуса. Вовремя поставленный диагноз, точное определение стадии развития меланомы является залогом успешного лечения.
В беседе с пациентом выясняется, когда возникло пигментное образование (является оно врожденным или приобретенным), изменялся ли вид невуса, его размер, форма, цвет. Если происходили изменения, чем они были вызваны (травма, ожог, расчесывание, попытки удаления), как давно были замечены изменения. Выясняется также, проводилось ли лечение невуса и какого плана было это лечение. В ходе осмотра родинки или пятна уточняется их размер, цвет, форма, другие видимые характеристики.
Визуально невозможно с достаточной степенью достоверности различить доброкачественное и злокачественное новообразование, для более точной диагностики необходимы специальные исследования. Следует помнить, что биопсия (частичное удаление невуса) для гистологического исследования категорически недопустима.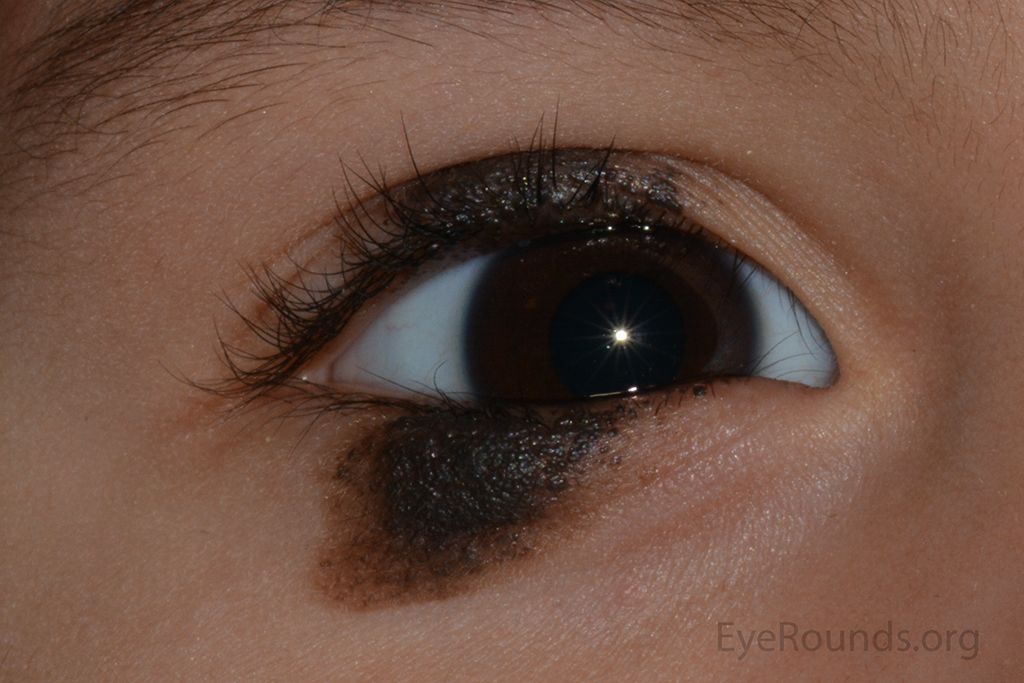
Установлено, что любое травматичное воздействие (механическое, химическое, радиационное) может вызвать перерождение некоторых видов меланомоопасных невусов, особенно пограничных, в злокачественную форму. Поэтому биопсия, а также такие виды косметического лечения как электрокоагуляция, криотерапия (криодеструкция), удаление родинок с помощью химических веществ являются угрозой развития злокачественной опухоли.
Материал для гистологического исследования невусов получают с помощью взятия мазка с поверхности новообразования, если на нем имеются трещины и кровоточивость. На следующий день можно уже иметь готовый результат исследования ткани, который проводится под микроскопом.
Подобное исследование следует проводить только в специализированных онкологических учреждениях, где возможно сразу после получения результатов под местной анестезией полностью удалить новообразование (с отступами 3-5 мм от краев) для дальнейшего гистологического исследования. Через несколько дней результат будет готов.
В настоящее время появился новый метод диагностики – эпилюминисцентная микроскопия. Исследование проводится с помощью оптического прибора с искусственным подсвечиванием (дерматоскопа) непосредственно на поверхности тела. На пигментное образование наносится несколько капель растительного масла для создания эффекта эпилюминисценции (возникает масляная среда между объектом исследования и дерматоскопом), затем к месту исследования приставляют прибор. Такой метод исследования не повреждает невус и является наиболее точным в определении структуры пигментного новообразования.
Метод компьютерной диагностики также относится к числу передовых методов исследования. С помощью цифровой видеокамеры фиксируют изображение пигментного образования и сохраняют в памяти компьютера. Специальная компьютерная программа обрабатывает полученные данные, сравнивает с базой данных и выдает точное заключение.
Недостатком компьютерной диагностики и эпилюминисцентной микроскопии является их дороговизна, что мешает их широкому распространению в нашей стране.
Способы удаления родинок
Меланоопасные невусы категорически не рекомендуется подвергать любым косметическим процедурам. Они подлежат обязательному хирургическому иссечению в пределах здоровых тканей.
Вопрос об удалении родинок встает перед пациентом в двух случаях: когда новообразования являются косметической проблемой, а также в случае онкологических показаний. От категории показаний будет зависеть и способ удаления. И в том, и в другом случае решение остается за специалистом.
Косметические показания
Для решения косметической проблемы удалить родинки и родимые пятна можно хирургическим способом, с помощью жидкого азота (криодеструкция), с помощью электрического тока высокой частоты (электрокоагуляция), с помощью лазера или методом радиохирургии.
Хирургический метод является традиционным и особенно подходящим в случае удаления глубокого или обширного невуса. Недостатком хирургического способа являются заметные следы после операции, т.к. родинку приходится удалять с прилегающей кожей, по онкологическим требованиям диаметр иссекаемой поверхности должен составлять 3-5 см в зависимости от места расположения невуса.
Криодеструкция — метод разрушения ткани холодом (жидким азотом сверхнизких температур). Родинка сморщивается, образуя сухой струп (корочку) и надежно предохраняет ранку от проникновения инфекции. Под ней со временем нарастает здоровая ткань. К криодеструкции прибегают для удаления невусов, находящихся на одном уровне с кожей. Иногда воздействие азота распространяется и на здоровые ткани или не полностью разрушает патологически измененные. В последнем случае требуется проведение повторного сеанса.
Метод электрокоагуляции предполагает термическое воздействие высокочастотным током на ткань вокруг удаляемого очага. После электрокоагуляции родинка должна быть отправлена на гистологический анализ. Ранка после удаления невуса заживает под корочкой, с формированием слабовыраженного рубца.
Лазерное удаление родинок. Наиболее результативным сегодня считается удаление образований кожи с помощью лазера. Его часто используют для удаления родинок в области лица и открытых частей тела. Преимуществами лазера являются малый диаметр и точная глубина воздействия, сохранность окружающих тканей. Небольшая корочка после лазерной операции защищает ранку от инфицирования и образования рубца. После удаления небольших родинок не остается никакого следа, при более обширных поражениях иногда возникает участок депигментации.
Преимуществами лазера являются малый диаметр и точная глубина воздействия, сохранность окружающих тканей. Небольшая корочка после лазерной операции защищает ранку от инфицирования и образования рубца. После удаления небольших родинок не остается никакого следа, при более обширных поражениях иногда возникает участок депигментации.
Радиохирургия – бесконтактный метод иссечения тканей аппаратом-сургитроном (радионожом) при помощи радиоволн. Широко используется в косметологии, применяется для удаления образований доброкачественного и злокачественного характера. Совмещает в себе рассекающее ткани, кровоостанавливающее и дезинфицирующее действие, не оставляет послеоперационных рубцов.
Онкологические показания
Подозрительные в плане злокачественного перерождения невусы подлежат полному хирургическому иссечению в пределах здоровых тканей и последующему гистологическому исследованию.
Профилактика развития меланомы
В последнее время в мире отмечается тенденция к значительному росту числа заболеваний меланомой кожи, особенно у женщин молодого возраста.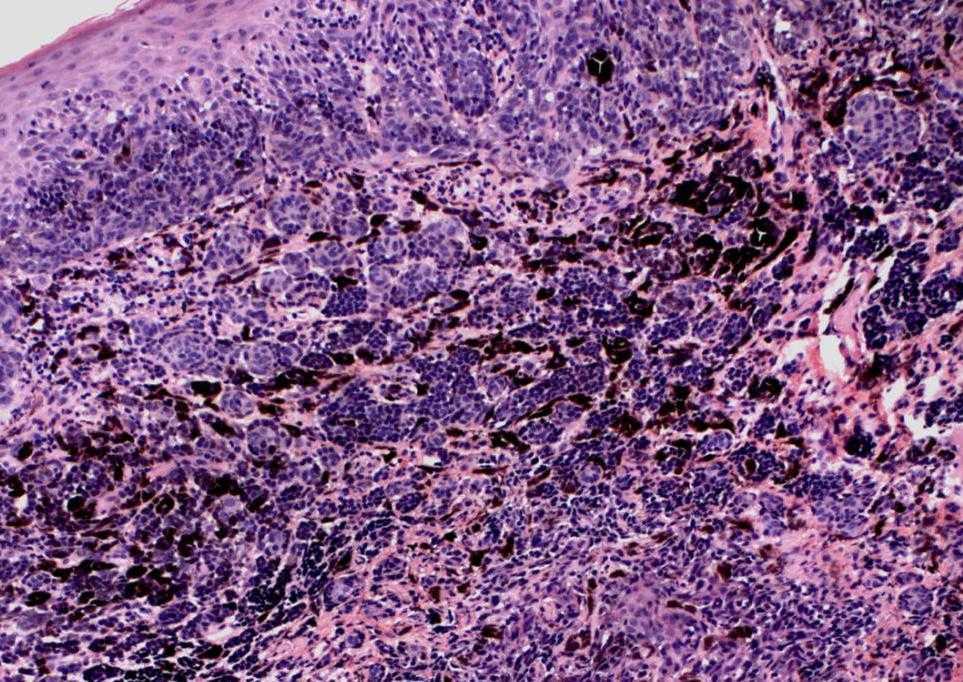 У мужчин меланома чаще локализуется на спине, а у женщин – на нижних конечностях. Статистика заболеваемости меланомой кожи в России тоже неутешительна, она составляет четверо заболевших на 100 тыс. населения. Прорастая все слои кожи, опухолевые клетки с током крови и лимфы разносятся по всему организму, образуя отдаленные метастазы (вторичные очаги опухоли) в легких, печени, головном мозге. Летальность при меланоме кожи достигает 50%. Предупредить развитие меланомы кожи можно, соблюдая следующие рекомендации:
У мужчин меланома чаще локализуется на спине, а у женщин – на нижних конечностях. Статистика заболеваемости меланомой кожи в России тоже неутешительна, она составляет четверо заболевших на 100 тыс. населения. Прорастая все слои кожи, опухолевые клетки с током крови и лимфы разносятся по всему организму, образуя отдаленные метастазы (вторичные очаги опухоли) в легких, печени, головном мозге. Летальность при меланоме кожи достигает 50%. Предупредить развитие меланомы кожи можно, соблюдая следующие рекомендации:
Читайте также:
- Костно-пластическая трепанация черепа. Показания для трепанации черепа. Методика выполнения трепанации черепа.
- Простудные заболевания. Механизмы возникновения простуды
- Признаки внутреннего импиджмента плечевого сустава
- Связки пациента. Осмотр суставов пациента
- Вероятность проаритмии. Риск возникновения тахиаритмий
Меланоцитарный невус.
 Причины, Симптомы, Лечение
Причины, Симптомы, ЛечениеМеланоцитарный невус – это пигментные родинки, которые часто диагностируются у людей различного возраста, в том числе у детей. В одинаковой степени доброкачественные образования встречаются у представителей обоих полов. Формируют новообразование меланоциты кожи – клетки, которые производят пигмент меланин. Если они по какой-то причине группируются на одном участке, на кожном покрове появляется меланоцитарный невус (МН).
Этот вид образований может присутствовать на коже младенца, то есть патология имеет врожденный характер. Также невус может появиться в первые годы жизни, в подростковом возрасте, на любом этапе жизни. В этом случае новообразования называют приобретенными меланоцитарными невусами. Для этого вида кожных образований характерно увеличение числа до 40 лет. После этого возраста новые пигментные родинки появляются реже. Если человек обнаруживает у себя новое образование, рекомендуется контролировать и проверять его, особенно, если оно растет или меняется по форме, текстуре, цвету.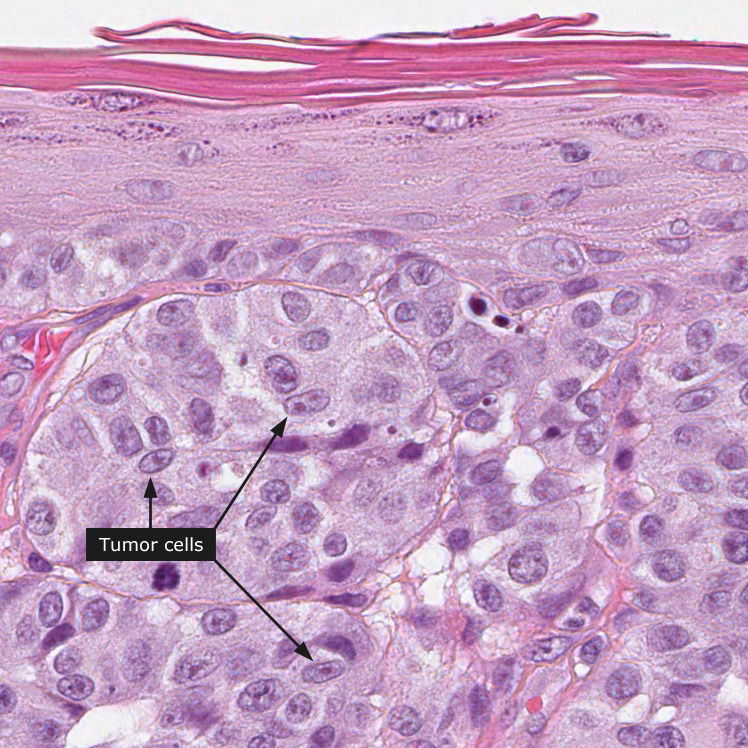
Важно: В последние годы участились случаи диагностики злокачественных заболеваний кожи. Поэтому, хоть меланоцитарный невус является доброкачественным образованием, специалисты рекомендуют с большим вниманием отнестись к родинкам, чтобы исключить риски и не пропустить момент перерождения.
Симптомы
Пигментные родинки выглядят как плоские или выступающие над поверхностью кожи пятна округлой или овальной формы с четкими границами и гладкой поверхностью. Исключение – диспластические родинки. Меланоцитарный невус с признаками дисплазии, как правило, имеет размытые контуры в структуре кожи. Несмотря на изначально доброкачественный характер, такое образование требует особого наблюдения.
Цвет всех меланоцитарных образований варьируется от светло-коричневого оттенка до насыщенного коричневого и даже черного.
По размеру выделяют:
- мелкий МН до 1,5 см в диаметре;
- средний МН до 10 см в диаметре;
- крупное образование, размеры которого превышают 10 см в диаметре.

Если родинка имеет размер более 20 см в диаметре, диагностируют гигантский меланоцитарный невус. Как правило, это лентигиозное родимое пятно, которое занимает большую область кожи на одном ее участке.
В подавляющем большинстве случаев новообразования этого типа не имеют специфических симптомов, не доставляют неприятных ощущений. Они не болят, не чешутся, но могут изменять вид. Важно правильно оценивать трансформацию. Если невус увеличивается пропорционально росту кожи, например, при наборе веса или с взрослением, это считается нормой. В других случаях лучше получить консультацию дерматолога, чтобы исключить развитие серьезной патологии.
Виды невусов
Подавляющее большинство МН – приобретенные. Специалисты разграничивают обычные и особые образования. Обычные невусы проходят три стадии развития. На разных стадийных фазах они за счет продвижения (проникновения) клеток новообразования вглубь дермы бывают:
- пограничными (эпидермальными), когда пигментные клетки находятся только в верхних слоях кожи;
- сложными (смешанными), у которых часть клеток располагаются в верхних слоях кожи, а часть распространяется в ее глубокие слои;
- внутридермальными (интрадермальными), которые проросли в глубокие слои дермы.

Среди особых невусов выделяют папилломатозный внутридермальный меланоцитарный невус, который внешне напоминает папиллому и возвышается над поверхностью кожи.
Меланоцитарный невус: причины появления
Многие дерматологи считают, что все пигментные невусы (даже приобретенные) нужно считать врожденными дефектами кожи. По их мнению, нарушения возникают в период эмбрионального развития. Однако четкого ответа на вопрос: «Почему образуются родинки на коже?» нет.
Среди врожденных причин, образующих диспластические невусы, называют:
- гормональный дисбаланс у беременной женщины;
- перенесенные будущей мамой инфекции;
- воздействие на организм беременной токсичных веществ, излучений;
- наследственная предрасположенность, при которой нарушается развитие меланоцитов.
В каждом из этих случаев меланобласты (первичные меланоциты) скапливаются в одном участке и трансформируются в невоциты, которые не имеют способности распространять пигмент в соседние клетки кожи.
Кроме других факторов, которые могут вызвать нарушение пигментации кожного покрова на отдельном участке, называют:
- Гормональные перестройки.
- Чрезмерное воздействие на кожный покров ультрафиолетовых лучей.
- Травмы кожи, воспалительные заболевания (угри, дерматиты, различные сыпи).
Диагностика
Главные задачи, которые стоят перед дерматологом, проводящим диагностику невуса, это:
- определить тип образования;
- исключить или подтвердить начало процесса перерождения;
- разработать план лечения.
Визит предусматривает беседу, в ходе которой врач уточняет:
- когда появилась родинка;
- увеличилась она в размерах или нет;
- сохранился ли первоначальный цвет, неизменен ли общий вид образования.
Далее следует осмотр. Поставить точный диагноз позволяет дерматоскопия – изучение невуса при многократном увеличении. В случае кровоточивости, трещин, шелушения пигментного пятна может быть назначена гистология. Гистологическое исследование предполагает изучение мазка с новообразования при помощи микроскопа. Способ позволяет определить тип клеток.
Гистологическое исследование предполагает изучение мазка с новообразования при помощи микроскопа. Способ позволяет определить тип клеток.
Меланоцитарный невус: лечение
Единственным эффективным способом лечения пигментных невусов является их удаление. Необходимость и целесообразность операции определяется в каждом клиническом случае. К примеру, если образование опасное из-за постоянного травматизма, из-за быстрого роста и трансформаций, от него обязательно нужно избавиться.
Оптимальный способ удаления любых кожных образований – лазерный. Этот способ имеет массу преимуществ:
- Безопасный и высокоточный метод, который позволяет не затрагивать соседние ткани. Луч «выпаривает» лишь патологические клетки.
- Бескровный способ, так как все капилляры разу прижигаются.
- Безболезненная процедура, так как лазерные импульсы очень короткие. Болевые рецепторы не успевают среагировать.
- Малотравматичное воздействие, которое приводит к быстрому восстановлению кожного покрова.

Приглашаем вас в специализированную медицинскую клинику «Лазерсвіт» на диагностику и при необходимости на лазерное лечение меланоцитарного невуса. Гарантируем высокое качество предоставляемых услуг и конкурентные цены.
Часто задаваемые вопросы
В чем опасность сложных невусов?
Опасность этого образования в том, что из-за своей формы и структуры оно часто травмируется одеждой и аксессуарами, начинает кровоточить. Возникает риск присоединения вторичной инфекции и даже перерождения.
После лазерного удаления невуса он может появиться вновь?
Это исключено, так как лазерный луч выпаривает все клетки патологического образования.
 Но успешное лечение не исключает появление родинки на другом месте.
Но успешное лечение не исключает появление родинки на другом месте.Что такое карта родинок, зачем она нужна?
Карта родинок – это выявление и обозначение на компьютерной модели тела всех кожных образований с указанием их вида и параметров. Она нужна, чтобы отслеживать изменения невусов, появление новых пигментных образований.
Какие причины для удаления родинок считаются объективными?
Опасность перерождения, постоянный травматизм одеждой и аксессуарами, эстетические факторы.
Глубоко проникающие невусоподобные пограничные опухоли: уникальная подгруппа неоднозначных меланоцитарных опухолей со злокачественным потенциалом и нормальной цитогенетикой
Сохранить цитату в файл
Формат: Резюме (текст)PubMedPMIDAbstract (текст)CSV
Добавить в коллекции
- Создать новую коллекцию
- Добавить в существующую коллекцию
Назовите свою коллекцию:
Имя должно содержать менее 100 символов
Выберите коллекцию:
Не удалось загрузить вашу коллекцию из-за ошибки
Повторите попытку
Добавить в мою библиографию
- Моя библиография
Не удалось загрузить делегатов из-за ошибки
Ваш сохраненный поиск
Название сохраненного поиска:
Условия поиска:
Тестовые условия поиска
Эл.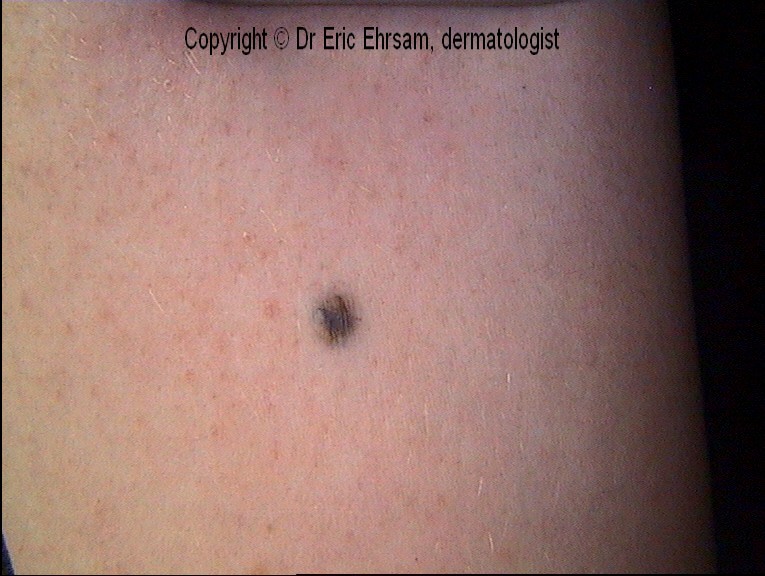 адрес:
(изменить)
адрес:
(изменить)
Который день? Первое воскресеньеПервый понедельникПервый вторникПервая средаПервый четвергПервая пятницаПервая субботаПервый деньПервый будний день
Который день? ВоскресеньеПонедельникВторникСредаЧетвергПятницаСуббота
Формат отчета: SummarySummary (text)AbstractAbstract (text)PubMed
Отправить максимум: 1 шт. 5 шт. 10 шт. 20 шт. 50 шт. 100 шт. 200 шт.
Отправить, даже если нет новых результатов
Необязательный текст в электронном письме:
Создайте файл для внешнего программного обеспечения для управления цитированием
. 2014 сен-октябрь;24(5):594-602.
doi: 10.1684/ejd.2014. 2393.
2393.
Синтия М Магро 1 , Ронни М. Абрахам 2 , Жуйфэн Го 3 , Шибо Ли 4 , Сюань Ван 1 , Стивен Пропер 5 , Нил Кроусон 6 , Мартин Михм 7
Принадлежности
- 1 Кафедра патологии и лабораторной медицины, комната F-309, 1300 York Avenue, Медицинский колледж Вейла Корнельского университета, Нью-Йорк, США.
- 2 Кафедра патологии и лабораторной медицины, кабинет F-309, 1300 York Avenue, Медицинский колледж Вейла Корнелльского университета, Нью-Йорк, штат Нью-Йорк, США, кафедра патологии, Мемориальный онкологический центр Слоуна-Кеттеринга, Нью-Йорк, США.

- 3 Отделение патологии.
- 4 Лаборатория генетики, кафедра педиатрии, Центр медицинских наук Университета Оклахомы, Оклахома-Сити, США.
- 5 Центр дерматологии и хирургии кожи, Тампа, Флорида, США.
- 6 Региональные медицинские лаборатории, Талса, Оклахома, США.
- 7 Brigham and Women’s Hospital, Гарвардская медицинская школа, Бостон, Массачусетс, США.
- PMID: 25118781
- DOI:
10.
 1684/ejd.2014.2393
1684/ejd.2014.2393
Синтия М. Магро и др. Евр Дж Дерматол. 2014 сен-окт.
. 2014 сен-октябрь;24(5):594-602.
doi: 10.1684/ejd.2014.2393.
Авторы
Синтия М Магро 1 , Ронни М. Абрахам 2 , Жуйфэн Го 3 , Шибо Ли 4 , Сюань Ван 1 , Стивен Пропер 5 , Нил Кроусон 6 , Мартин Михм 7
Принадлежности
- 1 Кафедра патологии и лабораторной медицины, комната F-309, 1300 York Avenue, Медицинский колледж Вейла Корнельского университета, Нью-Йорк, США.

- 2 Кафедра патологии и лабораторной медицины, кабинет F-309, 1300 York Avenue, Медицинский колледж Вейла Корнелльского университета, Нью-Йорк, штат Нью-Йорк, США, кафедра патологии, Мемориальный онкологический центр Слоуна-Кеттеринга, Нью-Йорк, США.
- 3 Отделение патологии.
- 4 Лаборатория генетики, кафедра педиатрии, Центр медицинских наук Университета Оклахомы, Оклахома-Сити, США.
- 5 Центр дерматологии и хирургии кожи, Тампа, Флорида, США.
- 6 Региональные медицинские лаборатории, Талса, Оклахома, США.
- 7 Brigham and Women’s Hospital, Гарвардская медицинская школа, Бостон, Массачусетс, США.

- PMID: 25118781
- DOI: 10.1684/ejd.2014.2393
Абстрактный
Фон: Глубокие пенетрирующие невусы (ДПН) являются относительно редким подтипом меланоцитарных невусов. Небольшая часть этих поражений демонстрирует атипичные черты (цитологическая и архитектурная атипия, митотическая активность), наблюдаемые при меланоме. Эти поражения мы называем глубоко проникающими невусоподобными пограничными опухолями. Однозначные меланомы могут демонстрировать перекрывающиеся морфологические признаки ДПН, которые были названы плексиформными меланомами.
Пациенты и методы: Выявлено 40 случаев ДПН-подобной пограничной опухоли и 6 случаев плексиформной меланомы. Было получено клиническое наблюдение, наряду с цитогенетическим анализом в форме флуоресцентной гибридизации in situ (FISH) и/или сравнительной геномной гибридизации (CGH).
Было получено клиническое наблюдение, наряду с цитогенетическим анализом в форме флуоресцентной гибридизации in situ (FISH) и/или сравнительной геномной гибридизации (CGH).
Полученные результаты: Среди пациентов с ДПН-подобной пограничной опухолью было 24 женщины и 16 мужчин. Из выполненных биопсий сигнальных лимфатических узлов в 1/3 случаев было выявлено поражение лимфатических узлов. Все пациенты, у которых был принят агрессивный клинический подход, остаются здоровыми. Все 6 ДПН-подобных пограничных опухолей, протестированных CGH, показали нормальную цитогенетику, как и 7 из 9 случаев.случаев, проверенных FISH. Из плексиформных меланом 4/6 пациентов умерли от болезни. В 3 случаях имело место морфологическое прогрессирование от ДПН-подобной пограничной опухоли до явной меланомы. В одном случае прогрессирования цитогенетика была нормальной при ДПН-подобной пограничной опухоли, а затем ненормальной при прогрессирующей меланоме.
Вывод: ДПН-подобные пограничные опухоли представляют собой меланоцитарные опухоли, связанные с высокой частотой поражения регионарных лимфатических узлов и демонстрирующие потенциал для прогрессирования меланомы, несмотря на нормальный цитогенетический профиль. Пациентов с такими поражениями следует лечить агрессивно, по крайней мере, с полным повторным иссечением и рассмотрением вопроса о биопсии сторожевого лимфатического узла, независимо от цитогенетических данных.
Ключевые слова: неоднозначная меланоцитарная опухоль; пограничная меланоцитарная опухоль; глубоко проникающий невус; глубоко проникающая невусоподобная пограничная опухоль; меланоцитарная опухоль неопределенного злокачественного потенциала.
Похожие статьи
Кожная пограничная меланоцитарная опухоль: категорический подход.

Магро К.М., Кроусон А.Н., Михм М.К. младший, Гупта К., Уокер М.Дж., Соломон Г. Магро С.М. и др. J Am Acad Дерматол. 2010 март; 62 (3): 469-79. doi: 10.1016/j.jaad.2009.06.042. J Am Acad Дерматол. 2010. PMID: 20159313
Корреляция стандартного 5-зондового анализа FISH с меланоцитарными опухолями с неопределенным злокачественным потенциалом.
Мюльбауэр А., Момтахен С., Михм М.С., Ван Дж., Магро С.М. Мюльбауэр А. и соавт. Энн Диагн Патол. 2017 июнь;28:30-36. doi: 10.1016/j.anndiagpath.2016.11.001. Epub 2016 10 ноября. Энн Диагн Патол. 2017. PMID: 28648937
Анализ флуоресцентной гибридизации in situ (FISH) меланоцитарных невусов и меланом: чувствительность, специфичность и отсутствие связи со статусом сигнального узла.

Фанг Ю., Душа С., Джанвар С., Бусам К.Дж. Фан Ю и др. Международный Дж. Сург Патол. 2012 окт; 20 (5): 434-40. дои: 10.1177/1066896912445923. Epub 2012 4 мая. Международный Дж. Сург Патол. 2012. PMID: 22561674
Гистологически неоднозначные («пограничные») первичные кожные меланоцитарные опухоли: подходы к ведению пациентов, включая роль молекулярного тестирования и биопсии сигнальных лимфатических узлов.
Скольер Р.А., Мурали Р., Маккарти С.В., Томпсон Дж.Ф. Сколер Р.А. и соавт. Arch Pathol Lab Med. 2010 декабрь; 134 (12): 1770-7. doi: 10.5858/2009-0612-RAR.1. Arch Pathol Lab Med. 2010. PMID: 21128774 Обзор.
Два врожденных случая пигментированной эпителиоидной меланоцитомы, изученные с помощью флуоресцентной гибридизации in situ для меланоцитарных опухолей: отчеты о случаях и обзор этих недавних тем.

Баттистелла М., Прохазкова-Карлотти М., Берреби Д., Беннасер С., Эдан С., Риффо Л., Рюттен А., Фрайтаг С. Баттистелла М. и др. Дерматология. 2010;221(2):97-106. дои: 10.1159/000314160. Epub 2010 18 июня. Дерматология. 2010. PMID: 20558976 Обзор.
Посмотреть все похожие статьи
Цитируется
Обычный и атипичный глубоко проникающий невус, глубоко проникающая меланома, похожая на невус, и родственные варианты.
Гилл П., Аунг П.П. Гилл П. и др. Биология (Базель). 2022 17 марта; 11 (3): 460. doi: 10.3390/biology11030460. Биология (Базель). 2022. PMID: 35336833 Бесплатная статья ЧВК. Обзор.
Классификация кожных меланоцитарных новообразований ВОЗ 2018 г.
 : рекомендации из повседневной практики.
: рекомендации из повседневной практики.Феррара Г., Ардженциано Г. Феррара Г. и др. Фронт Онкол. 2021 2 июля; 11:675296. doi: 10.3389/fonc.2021.675296. Электронная коллекция 2021. Фронт Онкол. 2021. PMID: 34277420 Бесплатная статья ЧВК. Обзор.
Анализ атипичных глубоко проникающих невусов на основе NGS.
Манка А., Сини М.С., Чезинаро А.М., Портелли Ф., Урсо С., Лентини М., Кардиа Р., Алос Л., Кук М., Сими С., Палиояннис П., Де Джорджи В., Коссу А., Пальмиери Г., Масси Д. Манка А. и др. Раков (Базель). 2021 19 июня; 13 (12): 3066. doi: 10.3390/раки13123066. Раков (Базель). 2021. PMID: 34205480 Бесплатная статья ЧВК.
Полногеномные вариации числа копий как инструмент молекулярной диагностики кожных промежуточных меланоцитарных поражений: систематический обзор и метаанализ данных отдельных пациентов.

Ebbelaar CF, Jansen AML, Bloem LT, Blokx WAM. Эббелар С.Ф. и соавт. Арка Вирхова. 2021 окт; 479(4):773-783. doi: 10.1007/s00428-021-03095-5. Epub 2021 13 апр. Арка Вирхова. 2021. PMID: 33851238 Бесплатная статья ЧВК.
Глубоко проникающий невус и погранично-глубоко проникающий невус: обзор литературы.
Косгареа И., Гриванк К.Г., Унгуряну Л., Тамайо А., Зипманн Т. Косгареа I и др. Фронт Онкол. 2020 20 мая; 10:837. дои: 10.3389/fonc.2020.00837. Электронная коллекция 2020. Фронт Онкол. 2020. PMID: 32509588 Бесплатная статья ЧВК. Обзор.
Просмотреть все статьи «Цитируется по»
Типы публикаций
термины MeSH
вещества
Полнотекстовые ссылки
Джон Либби Евротекст
Укажите
Формат: ААД АПА МДА НЛМ
Отправить по телефону
Глубокопроникающий невус и погранично-глубокопроникающий невус: обзор литературы
Введение
Термин «глубокий пенетрирующий невус» (ДПН) впервые был введен Seab et al.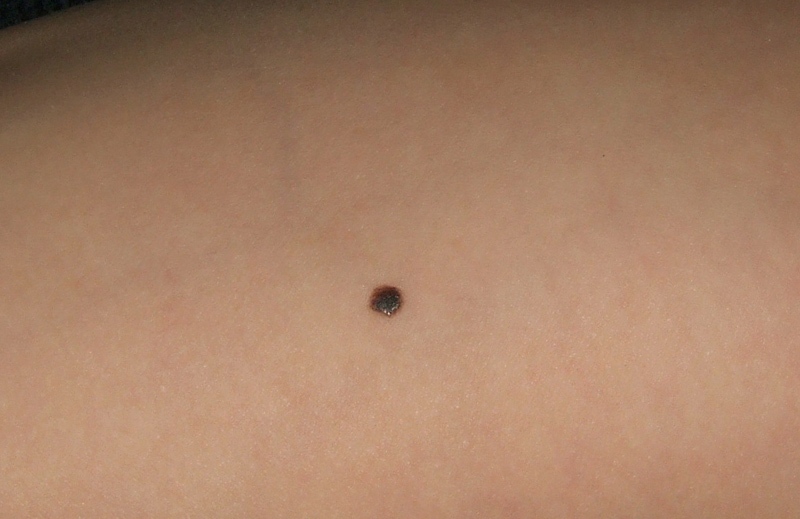 в 1989 г., когда автор описал серию случаев, которые первоначально были ошибочно диагностированы как злокачественная меланома (1). Из-за своего клинического и, в частности, гистопатологического проявления, ДПН может быть сложно дифференцировать от клеточных голубых невусов, невусов шпица и злокачественной меланомы (2). Клинически проявляясь в виде одиночных пигментированных папул или узелков, ДПН чаще встречается у молодых людей с преимущественным появлением в области головы и шеи (3, 4). Гистологически он характеризуется как четко очерченные клиновидные поражения, достигающие ретикулярной дермы/подкожной клетчатки, демонстрирующие эпителиоидные/веретеноклеточные меланоцитарные гнезда с низкой степенью цитологической атипии и возможными фигурами митоза (1, 2, 5, 6). Несмотря на заметный гистопатологический вид, ДПН имеют хороший прогноз, демонстрируя доброкачественное течение (1, 2, 5, 6). Однако было описано распространение в регионарные лимфатические узлы (7), и в литературе можно найти даже случаи метастазирования ДПН с атипичными признаками, классифицированными как «пограничные» (В-ДПН) (7–10).
в 1989 г., когда автор описал серию случаев, которые первоначально были ошибочно диагностированы как злокачественная меланома (1). Из-за своего клинического и, в частности, гистопатологического проявления, ДПН может быть сложно дифференцировать от клеточных голубых невусов, невусов шпица и злокачественной меланомы (2). Клинически проявляясь в виде одиночных пигментированных папул или узелков, ДПН чаще встречается у молодых людей с преимущественным появлением в области головы и шеи (3, 4). Гистологически он характеризуется как четко очерченные клиновидные поражения, достигающие ретикулярной дермы/подкожной клетчатки, демонстрирующие эпителиоидные/веретеноклеточные меланоцитарные гнезда с низкой степенью цитологической атипии и возможными фигурами митоза (1, 2, 5, 6). Несмотря на заметный гистопатологический вид, ДПН имеют хороший прогноз, демонстрируя доброкачественное течение (1, 2, 5, 6). Однако было описано распространение в регионарные лимфатические узлы (7), и в литературе можно найти даже случаи метастазирования ДПН с атипичными признаками, классифицированными как «пограничные» (В-ДПН) (7–10).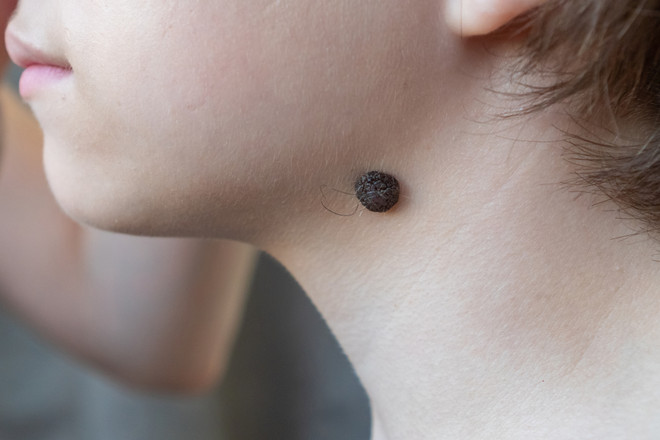 Представляя диагностическую проблему даже для специалистов в области дерматопатологии и патологии (7), правильный диагноз имеет первостепенное значение для эффективного клинического лечения и исхода. Рекомендации по терапевтическому лечению и последующему наблюдению непоследовательны и не основаны на достаточных клинических данных. Недостаточное и чрезмерное лечение, включая длительное наблюдение, часто встречается у пациентов с этими опухолями (2, 6, 8, 9)., 11, 12). Мы стремились предоставить обзор литературы по ДПН и Б-ДПН с оценкой клинического ведения, включая лечение и последующую оценку.
Представляя диагностическую проблему даже для специалистов в области дерматопатологии и патологии (7), правильный диагноз имеет первостепенное значение для эффективного клинического лечения и исхода. Рекомендации по терапевтическому лечению и последующему наблюдению непоследовательны и не основаны на достаточных клинических данных. Недостаточное и чрезмерное лечение, включая длительное наблюдение, часто встречается у пациентов с этими опухолями (2, 6, 8, 9)., 11, 12). Мы стремились предоставить обзор литературы по ДПН и Б-ДПН с оценкой клинического ведения, включая лечение и последующую оценку.
Материалы и методы
Мы провели обзор наборов данных Medline, Scopus и Embase для клинических исследований, опубликованных с 1989 г. по 30 июля 2019 г., по ДПН и Б-ДПН.
Слова «глубоко проникающий невус» и «глубокий невус» использовались для обозначения исследований пациентов с этим заболеванием, содержащих данные клинических и лабораторных исследований, которым они подвергались. Комбинации терминов MeSH (Medical Subject Heading) и логических операторов, использованных в нашем поиске в Medline, перечислены ниже: глубокий проникающий невус ИЛИ глубокий проникающий невус ИЛИ темно-синий невус ИЛИ темно-синий невус ИЛИ глубокий невус ИЛИ глубокий невус. Поиск в Scopus выполнялся с использованием следующих комбинаций терминов MeSH и логических операторов: [(невус) ИЛИ (невус) ИЛИ (невус) ИЛИ (невус)] И [(глубокий) ИЛИ (синий) ИЛИ (проникающий)]. Комбинации терминов MeSH и логических операторов, используемые в нашем поиске на Embase, включали следующее: [невус/невус И ((синий) ИЛИ (глубокий)]. Мы рассматривали только статьи, опубликованные на английском или немецком языке, для дальнейшего рассмотрения и исключали дубликаты. Чтобы восполнить ожидаемое общее отсутствие хорошо спланированных исследований в больших популяциях пациентов с ДПН и Б-ДПН, мы включили проспективные исследования любого дизайна, ретроспективный когортный анализ, а также отчеты о клинических случаях.
Комбинации терминов MeSH (Medical Subject Heading) и логических операторов, использованных в нашем поиске в Medline, перечислены ниже: глубокий проникающий невус ИЛИ глубокий проникающий невус ИЛИ темно-синий невус ИЛИ темно-синий невус ИЛИ глубокий невус ИЛИ глубокий невус. Поиск в Scopus выполнялся с использованием следующих комбинаций терминов MeSH и логических операторов: [(невус) ИЛИ (невус) ИЛИ (невус) ИЛИ (невус)] И [(глубокий) ИЛИ (синий) ИЛИ (проникающий)]. Комбинации терминов MeSH и логических операторов, используемые в нашем поиске на Embase, включали следующее: [невус/невус И ((синий) ИЛИ (глубокий)]. Мы рассматривали только статьи, опубликованные на английском или немецком языке, для дальнейшего рассмотрения и исключали дубликаты. Чтобы восполнить ожидаемое общее отсутствие хорошо спланированных исследований в больших популяциях пациентов с ДПН и Б-ДПН, мы включили проспективные исследования любого дизайна, ретроспективный когортный анализ, а также отчеты о клинических случаях.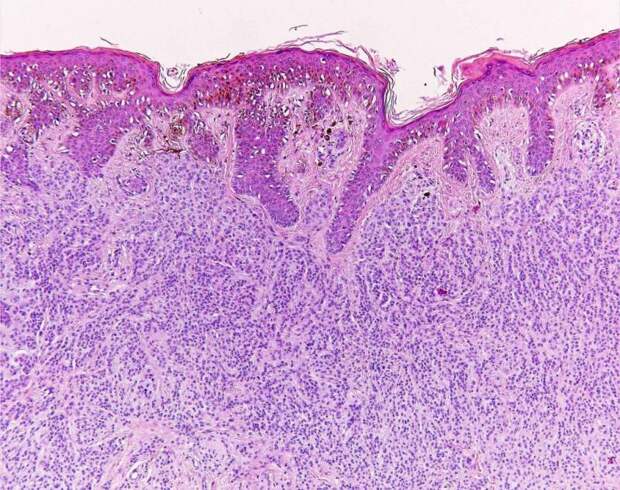 устойчивые эффекты клинического ведения и прогностические исходы, мы включили только те исследования, которые содержали данные последующего наблюдения. Статьи были проверены на основе названия и аннотации, чтобы определить соответствие критериям для нашего обзора. Были проанализированы и извлечены целые статьи для оценки приемлемости. Кроме того, мы вручную провели поиск библиографии включенных статей.
устойчивые эффекты клинического ведения и прогностические исходы, мы включили только те исследования, которые содержали данные последующего наблюдения. Статьи были проверены на основе названия и аннотации, чтобы определить соответствие критериям для нашего обзора. Были проанализированы и извлечены целые статьи для оценки приемлемости. Кроме того, мы вручную провели поиск библиографии включенных статей.
Результаты
Первоначальный поиск выявил в общей сложности 3513 исследований, а в процессе обзора еще три статьи были найдены путем ручного поиска в списках литературы. После устранения повторяющихся статей осталось 3369 статей. Статьи были сужены по названию, аннотации и полнотекстовому обзору. Всего 15 статей соответствовали критериям включения (рис. 1). Все 15 статей, которые соответствовали критериям включения, перечислены в таблицах 1A, B. Исследования были разделены на статьи, посвященные клиническому ведению ДПН, и статьи, посвященные Б-ДПН. Включенные исследования состоят из 10 когортных исследований и пяти клинических случаев, включающих в общей сложности 355 пациентов с ДПН и 48 пациентов с Б-ДПН. Клинические характеристики и данные последующего наблюдения включенных исследований показаны в таблицах 1A, B.
Клинические характеристики и данные последующего наблюдения включенных исследований показаны в таблицах 1A, B.
Рисунок 1 . Схема выбора исследования.
Таблица 1A . Клинические данные пациентов, включенных в группу ДПН.
Таблица 1B . Клинические данные пациентов, включенных в группу Б-ДПН.
Клинические характеристики
Для группы глубоко проникающих невусов возрастной диапазон в исследованиях, за исключением описания случая, варьировал от 3 месяцев до 64 лет со средним возрастом 30 лет, аналогично группе B-DPN, где возрастной диапазон составлял 4 года. –62 года, при этом средний возраст во всех исследованиях был моложе 30 лет. Распределение по полу было сходным для обеих групп с немного большим количеством женщин, 203 (57,1%) в DPN и 25 (54,1%) в B-DPN, чем мужчин, 152 (42,8%) в DPN и 22 (45,8%). ) в B-DPN. Расположение невуса было разделено на шесть категорий: голова и шея, туловище, верхняя конечность, нижняя конечность (включая ягодицы), другое и неизвестное.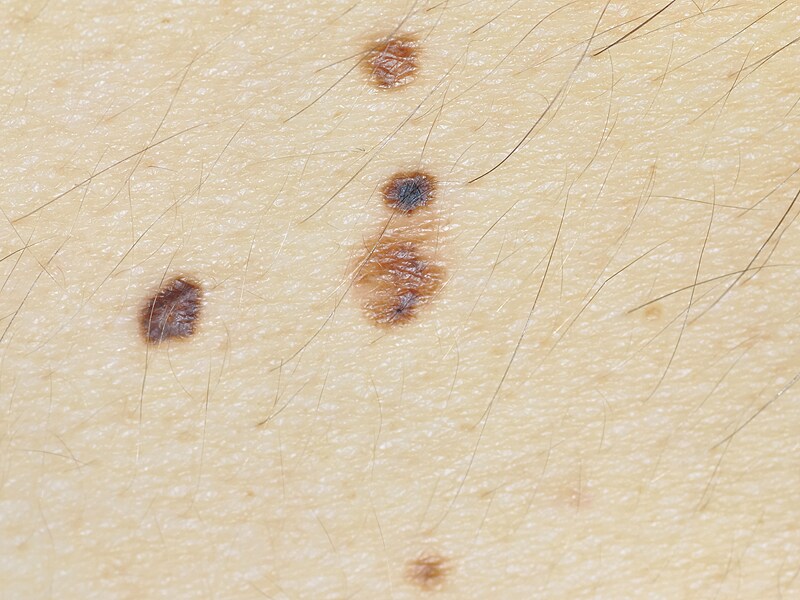 Большинство невусов в группе ДПН располагалось в области головы и шеи, 117 (32,9%), а на верхней и нижней конечности — 111 (31,2%). Из 111 невусов на конечностях диагностировано больше невусов на верхней конечности, чем на нижней, 61 против 44 соответственно. Среди необычных мест расположения невусов была конъюнктива в 34 случаях ДПН (19) и слизистая оболочка щек и мягкое небо в одном случае (17). В группе B-DPN наиболее частая локализация была аналогична группе DPN, голова и шея с 16 случаями, затем туловище и верхняя конечность, каждая с 14 случаями, а в остальных четырех случаях локализация была нижней конечностью.
Большинство невусов в группе ДПН располагалось в области головы и шеи, 117 (32,9%), а на верхней и нижней конечности — 111 (31,2%). Из 111 невусов на конечностях диагностировано больше невусов на верхней конечности, чем на нижней, 61 против 44 соответственно. Среди необычных мест расположения невусов была конъюнктива в 34 случаях ДПН (19) и слизистая оболочка щек и мягкое небо в одном случае (17). В группе B-DPN наиболее частая локализация была аналогична группе DPN, голова и шея с 16 случаями, затем туловище и верхняя конечность, каждая с 14 случаями, а в остальных четырех случаях локализация была нижней конечностью.
Ведение
Информация о тактике лечения в группе ДПН была доступна не для всех включенных исследований. Простое иссечение без каких-либо дополнительных хирургических процедур было основным методом лечения большинства пациентов. В нескольких случаях было выполнено повторное иссечение, в случаях, когда невус не был полностью удален в первый раз, а у некоторых пациентов было выполнено широкое иссечение без дополнительных уточнений по этому поводу. В группе B-DPN лечение варьировалось от иссечений/широких иссечений до биопсии сигнальных лимфатических узлов (SLNB) и системного лечения. В исследование Magro et al., проведенное в 2010 г., были включены 32 пациента с пограничными меланоцитарными опухолями, из которых у семи пациентов был диагностирован В-ДПН (9).). У четырех из этих пациентов были положительные результаты биопсии сигнальных лимфатических узлов (БСЛУ). У одного из этих пациентов был первоначально диагностирован ДПН, и поражение рецидивировало через 1,5 года, демонстрируя гистологические характеристики глубоко инвазивной меланомы. Повторная оценка первоначальной биопсии диагностировала поражение как B-DPN, что, по мнению авторов, имело бы показание для широкого иссечения и БСЛУ. У пациента развились последующие полиорганные метастазы, и он умер. Остальным пациентам с положительным SLB была проведена полная лимфаденэктомия без дальнейших признаков заболевания и проведена адъювантная терапия интерфероном. У пациентов не было выявлено каких-либо дальнейших рецидивов или метастазов в течение 4-летнего наблюдения.
В группе B-DPN лечение варьировалось от иссечений/широких иссечений до биопсии сигнальных лимфатических узлов (SLNB) и системного лечения. В исследование Magro et al., проведенное в 2010 г., были включены 32 пациента с пограничными меланоцитарными опухолями, из которых у семи пациентов был диагностирован В-ДПН (9).). У четырех из этих пациентов были положительные результаты биопсии сигнальных лимфатических узлов (БСЛУ). У одного из этих пациентов был первоначально диагностирован ДПН, и поражение рецидивировало через 1,5 года, демонстрируя гистологические характеристики глубоко инвазивной меланомы. Повторная оценка первоначальной биопсии диагностировала поражение как B-DPN, что, по мнению авторов, имело бы показание для широкого иссечения и БСЛУ. У пациента развились последующие полиорганные метастазы, и он умер. Остальным пациентам с положительным SLB была проведена полная лимфаденэктомия без дальнейших признаков заболевания и проведена адъювантная терапия интерфероном. У пациентов не было выявлено каких-либо дальнейших рецидивов или метастазов в течение 4-летнего наблюдения.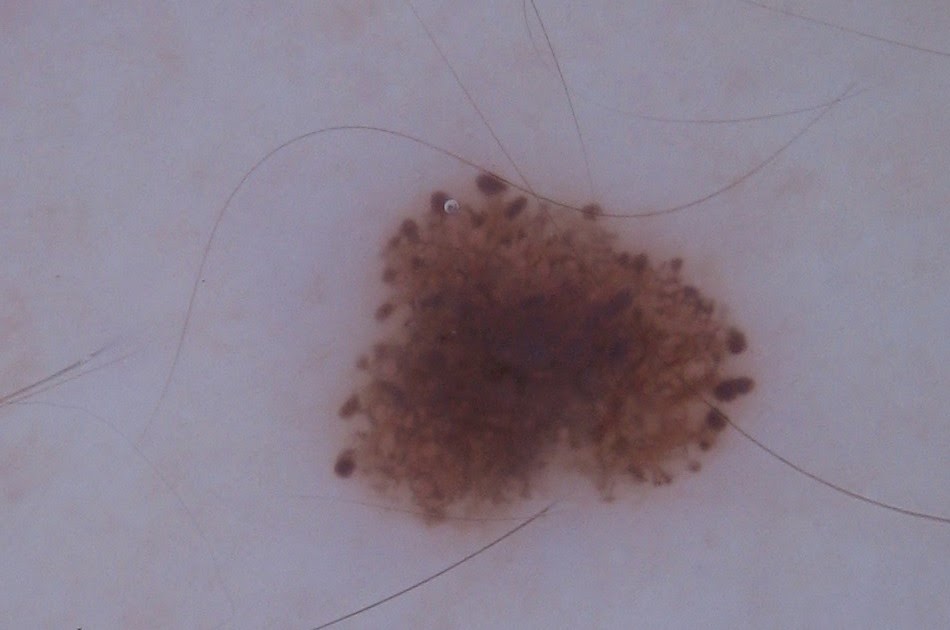 Второе исследование Magro et al. (8) включили 40 пациентов с ДПН-подобной пограничной опухолью. В 35 случаях было выполнено повторное иссечение, и в 23 из них процедура представляла собой широкое повторное иссечение, остаточная пограничная опухоль присутствовала в 11 образцах. Из 23 пациентов с широким повторным иссечением 19прошла БСЛУ, из которых 7 были положительными. Авторы сообщили, что в большинстве этих положительных случаев СЛУ опухолевые отложения были субкапсулярными и небольшими, в то время как у одного пациента, у которого возник рецидив через 1 год после лечения, были обширные паренхиматозные отложения. Полная лимфаденэктомия была выполнена у четырех пациентов с положительным SLNB без дальнейших признаков заболевания, а два пациента получили адъювантную терапию интерфероном альфа. В двух из 40 случаев первоначальным диагнозом был диспластический невус и клеточный голубой невус, пациентам проводилось небольшое консервативное повторное иссечение или не проводилось повторное иссечение соответственно.
Второе исследование Magro et al. (8) включили 40 пациентов с ДПН-подобной пограничной опухолью. В 35 случаях было выполнено повторное иссечение, и в 23 из них процедура представляла собой широкое повторное иссечение, остаточная пограничная опухоль присутствовала в 11 образцах. Из 23 пациентов с широким повторным иссечением 19прошла БСЛУ, из которых 7 были положительными. Авторы сообщили, что в большинстве этих положительных случаев СЛУ опухолевые отложения были субкапсулярными и небольшими, в то время как у одного пациента, у которого возник рецидив через 1 год после лечения, были обширные паренхиматозные отложения. Полная лимфаденэктомия была выполнена у четырех пациентов с положительным SLNB без дальнейших признаков заболевания, а два пациента получили адъювантную терапию интерфероном альфа. В двух из 40 случаев первоначальным диагнозом был диспластический невус и клеточный голубой невус, пациентам проводилось небольшое консервативное повторное иссечение или не проводилось повторное иссечение соответственно.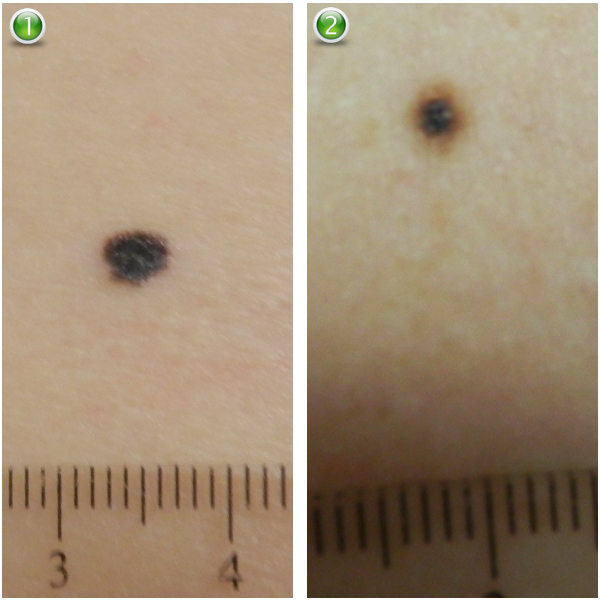 У обоих пациентов развились плексиформные меланомы вблизи предыдущего очага с метастазами, от которых оба пациента умерли. В эту группу был включен один отчет о случае 4-летнего мальчика с поражением на шее с диагнозом ДПН, у которого через 4 месяца после лечения развился видимый и пальпируемый лимфатический узел. В СЛУ были обнаружены пигментированные атипичные клетки, и мальчику была выполнена комплексная модифицированная радикальная диссекция шейки II типа с удалением 39лимфоузлы все отрицательные. Постановка не выявила дополнительных признаков метастазирования. Повторная оценка первичной биопсии привела к повторному диагнозу поражения как злокачественной меланомы.
У обоих пациентов развились плексиформные меланомы вблизи предыдущего очага с метастазами, от которых оба пациента умерли. В эту группу был включен один отчет о случае 4-летнего мальчика с поражением на шее с диагнозом ДПН, у которого через 4 месяца после лечения развился видимый и пальпируемый лимфатический узел. В СЛУ были обнаружены пигментированные атипичные клетки, и мальчику была выполнена комплексная модифицированная радикальная диссекция шейки II типа с удалением 39лимфоузлы все отрицательные. Постановка не выявила дополнительных признаков метастазирования. Повторная оценка первичной биопсии привела к повторному диагнозу поражения как злокачественной меланомы.
Последующее наблюдение
Срок наблюдения пациентов в группе ДПН варьировал от 4 месяцев до 23 лет. В пяти исследованиях некоторые пациенты наблюдались более 10 лет. Из 12 исследований местные рецидивы были зарегистрированы только у двух пациентов из двух разных исследований, и ни одного случая метастазирования не наблюдалось.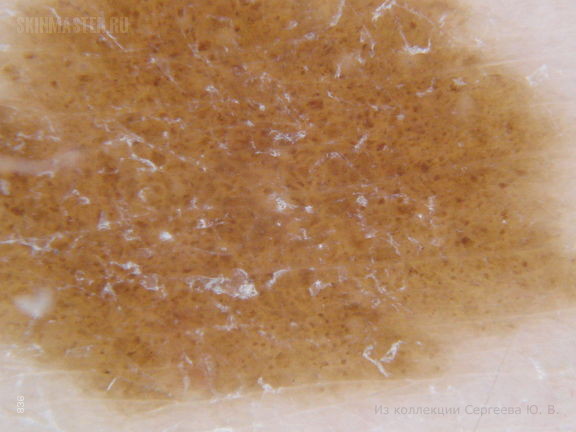 Срок наблюдения в группе Б-ДПН варьировал от 5 месяцев до 5 лет. В общей сложности наблюдалось четыре рецидива и три случая смерти, причем во всех трех случаях изначально был поставлен неправильный диагноз, что привело к недостаточному лечению пациентов.
Срок наблюдения в группе Б-ДПН варьировал от 5 месяцев до 5 лет. В общей сложности наблюдалось четыре рецидива и три случая смерти, причем во всех трех случаях изначально был поставлен неправильный диагноз, что привело к недостаточному лечению пациентов.
Обсуждение
Гистологический диагноз атипичных меланоцитарных опухолей может быть очень сложным даже для опытных дерматопатологов и патологов (7), а дифференциация между доброкачественными и злокачественными образованиями имеет терапевтические и прогностические последствия. Несмотря на то, что ДПН широко описывается как доброкачественное меланоцитарное поражение (1, 6, 11, 13, 18, 19), его злокачественный потенциал интенсивно обсуждается (5, 7) и сообщалось о случаях поражения регионарных лимфатических узлов ( 2, 5, 12). Тем не менее, 2009 г.Международная исследовательская группа по патологии меланомы согласилась с тем, что отдаленное заболевание за пределами регионарных узлов встречается редко и что при отсутствии митотической активности, ядерного плеоморфизма и экспансивного роста <2% поражений распространяются на лимфатические узлы (5). Во время «XXIX симпозиума Международного общества дерматопатологов в Граце» в 2008 г. эксперты-дерматопатологи и патологоанатомы рассмотрели 57 случаев MELTUMP (меланоцитарные опухоли с неопределенным злокачественным потенциалом), которые включали атипичные опухоли шпица (AST) и атипичные эпителиоидные/веретенообразные голубые невусы, последние категория, включая ДПН (7). Пациенты были разделены на три группы с благоприятным (отсутствие метастазов в течение 5 лет наблюдения), неблагоприятным (смерть, связанная с опухолью и/или метастазирование в лимфатические узлы и/или внутренние органы) и пограничным (узловые отложения опухолевых клеток ≤ 0,2). мм) поведение, и авторы отметили, что неблагоприятная группа чаще представляла три гистопатологических признака, а именно наличие митоза, митоза у основания и воспалительную реакцию. Кроме того, авторы отметили сложность достижения консенсуса в отношении доброкачественного или злокачественного диагноза поражений. О случаях метастатической ДПН сообщали и другие группы, в которых отмечалось, что эти поражения имели «пограничные» или «атипичные» признаки (8–10), что указывает на неопределенный злокачественный потенциал этих поражений, когда диагностика и терапевтическое лечение затруднены.
Во время «XXIX симпозиума Международного общества дерматопатологов в Граце» в 2008 г. эксперты-дерматопатологи и патологоанатомы рассмотрели 57 случаев MELTUMP (меланоцитарные опухоли с неопределенным злокачественным потенциалом), которые включали атипичные опухоли шпица (AST) и атипичные эпителиоидные/веретенообразные голубые невусы, последние категория, включая ДПН (7). Пациенты были разделены на три группы с благоприятным (отсутствие метастазов в течение 5 лет наблюдения), неблагоприятным (смерть, связанная с опухолью и/или метастазирование в лимфатические узлы и/или внутренние органы) и пограничным (узловые отложения опухолевых клеток ≤ 0,2). мм) поведение, и авторы отметили, что неблагоприятная группа чаще представляла три гистопатологических признака, а именно наличие митоза, митоза у основания и воспалительную реакцию. Кроме того, авторы отметили сложность достижения консенсуса в отношении доброкачественного или злокачественного диагноза поражений. О случаях метастатической ДПН сообщали и другие группы, в которых отмечалось, что эти поражения имели «пограничные» или «атипичные» признаки (8–10), что указывает на неопределенный злокачественный потенциал этих поражений, когда диагностика и терапевтическое лечение затруднены. В настоящем обзоре мы разделили включенные исследования на две группы: ДПН и Б-ДПН. В общей сложности 355 пациентов были включены в группу ДПН, и в течение периода наблюдения от 4 месяцев до 23 лет было зарегистрировано только два местных рецидива и ни одного метастаза. Во вторую группу, Б-ДПН, было включено 48 пациентов, из них 24 пациента перенесли СЛУ и пять блокировали лимфоузлы после положительного результата СЛУ, а некоторые пациенты даже получали после этого адъювантную терапию интерфероном альфа. В этой группе «высокого риска» частота рецидивов была низкой, у четырех пациентов развились локальные рецидивы и у трех широко распространенные метастатические заболевания. Тот факт, что ни у одного из пациентов в группе ДПН не развилось метастатическое заболевание, и что, несмотря на то, что из 12 пациентов из группы В-ДПН были положительные БСЛУ, только у трех, двое из которых изначально были неправильно диагностированы, развилось широкое метастатическое заболевание, подчеркивает доброкачественное течение этого меланоцитарного поражения.
В настоящем обзоре мы разделили включенные исследования на две группы: ДПН и Б-ДПН. В общей сложности 355 пациентов были включены в группу ДПН, и в течение периода наблюдения от 4 месяцев до 23 лет было зарегистрировано только два местных рецидива и ни одного метастаза. Во вторую группу, Б-ДПН, было включено 48 пациентов, из них 24 пациента перенесли СЛУ и пять блокировали лимфоузлы после положительного результата СЛУ, а некоторые пациенты даже получали после этого адъювантную терапию интерфероном альфа. В этой группе «высокого риска» частота рецидивов была низкой, у четырех пациентов развились локальные рецидивы и у трех широко распространенные метастатические заболевания. Тот факт, что ни у одного из пациентов в группе ДПН не развилось метастатическое заболевание, и что, несмотря на то, что из 12 пациентов из группы В-ДПН были положительные БСЛУ, только у трех, двое из которых изначально были неправильно диагностированы, развилось широкое метастатическое заболевание, подчеркивает доброкачественное течение этого меланоцитарного поражения. . Однако на основании двух исследований Magro et al. (8, 9) его следует дополнительно оценить и исследовать, если более широкий начальный хирургический подход не окажется полезным для пациентов с пограничной/атипичной ДПН.
. Однако на основании двух исследований Magro et al. (8, 9) его следует дополнительно оценить и исследовать, если более широкий начальный хирургический подход не окажется полезным для пациентов с пограничной/атипичной ДПН.
Несмотря на то, что возраст при постановке диагноза ДПН и В-ДПН варьирует от 3 месяцев до 64 лет, в нашем обзоре поражения обычно диагностировались у молодых людей в возрасте до 30 лет (1, 6, 8, 9). Ранее в литературе сообщалось о врожденной ДПН (6), но в большинстве случаев ДПН является приобретенным поражением (3). В одном случае, включенном в наш обзор, авторы сообщают о развитии ДПН во врожденном невусе правой подколенной ямки у 3-месячного мальчика (14). Первоначальное иссечение поражения показало положительные глубокие края, из-за чего пациент подвергся повторному иссечению, после чего в течение 15 месяцев последующего наблюдения не было никаких признаков рецидива или метастазов. Самый молодой обнаруженный случай B-DPN был у 4-летнего мальчика, у которого первоначально был диагностирован DPN, но повторно диагностирована как меланома после того, как 4 месяца спустя были обнаружены метастазы в лимфатических узлах.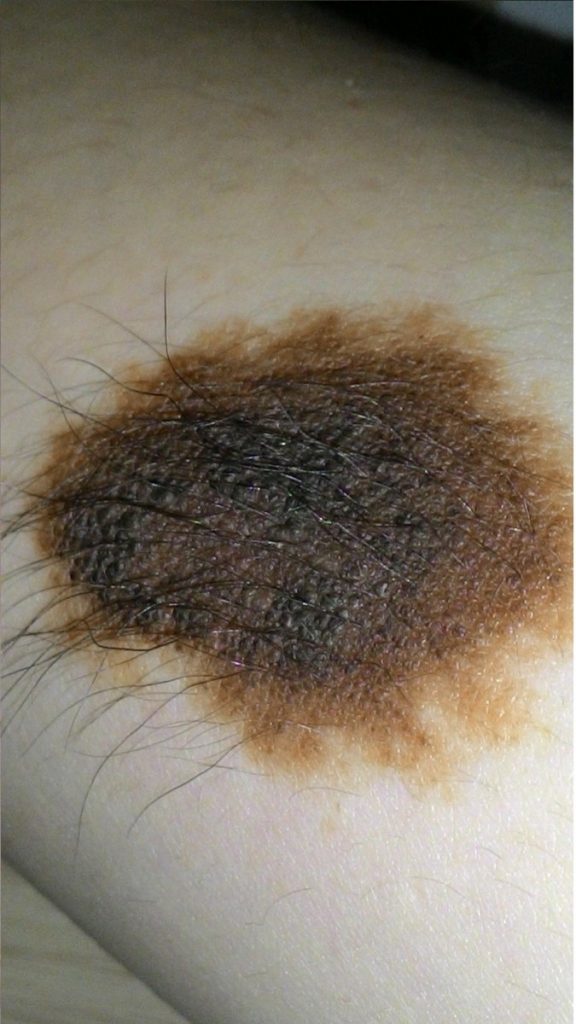 У мальчика не было никаких дальнейших метастатических заболеваний, однако ему была проведена модифицированная радикальная диссекция шеи III типа с иссечением 39лимфатические узлы, все гистологически отрицательные. Дифференциальный диагноз между ДПН и злокачественной меланомой у детей может быть затруднен, поскольку ДПН может демонстрировать цитологическую атипию и наличие митотической активности, вызывая подозрение на злокачественность (2). Авторы упомянули, что рассматривали диагноз пигментированной эпителиоидной меланоцитомы, но поскольку не все гистологические критерии были соблюдены, диагноз был изменен на меланому (20). Было бы интересно повторно оценить поражение и определить, применяются ли критерии, упомянутые в более поздних исследованиях (7–9) поражение лучше классифицировать как пограничную/атипичную ДПН.
У мальчика не было никаких дальнейших метастатических заболеваний, однако ему была проведена модифицированная радикальная диссекция шеи III типа с иссечением 39лимфатические узлы, все гистологически отрицательные. Дифференциальный диагноз между ДПН и злокачественной меланомой у детей может быть затруднен, поскольку ДПН может демонстрировать цитологическую атипию и наличие митотической активности, вызывая подозрение на злокачественность (2). Авторы упомянули, что рассматривали диагноз пигментированной эпителиоидной меланоцитомы, но поскольку не все гистологические критерии были соблюдены, диагноз был изменен на меланому (20). Было бы интересно повторно оценить поражение и определить, применяются ли критерии, упомянутые в более поздних исследованиях (7–9) поражение лучше классифицировать как пограничную/атипичную ДПН.
В недавней публикации, посвященной генетике меланоцитарных поражений с гистологическими аспектами ДПН, были сделаны наблюдения, отличающие эту нозологию от других меланоцитарных опухолей (21).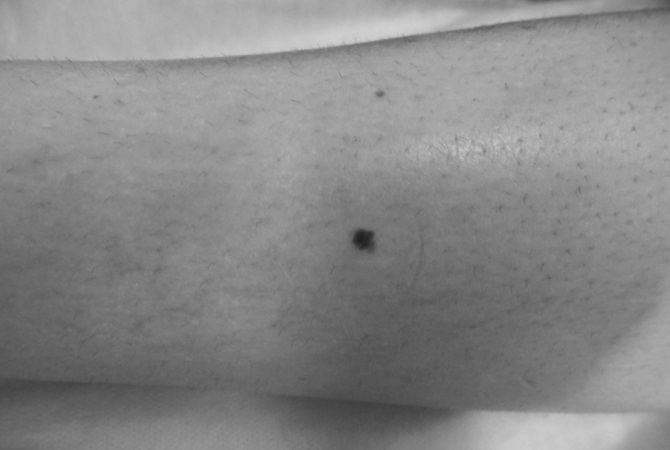 Помимо наличия мутаций, активирующих путь киназы MAP (например, MAP2K1 или BRAF ), также наблюдаемых в других невусах, стало очевидным, что ДПН имеют частые одновременные мутации CTNNB1 . Это приводит к постоянной активации сигнального пути бета-катенина. Это также наблюдалось гистологически. В обычных невусах меланоциты становятся меньше («зрелыми») и демонстрируют более низкую экспрессию CTNNB1 и CCND1 по данным иммуногистохимии в более глубоких слоях дермы. При ДПН клетки не мельчают («созревают») и сохраняют экспрессию CTNNB1 и CCND1 в нижних слоях дермы. Авторы также определили, что злокачественная ДПН (меланомы, возникающие при ДПН) демонстрируют дополнительные генетические изменения (активация MAP-киназы и CTNNB1 мутаций). Эти выводы имеют ряд важных следствий. Иммуногистохимия CTNNB1 может быть полезна для выявления поражений ДПН (19, 22). Кроме того, профиль мутаций может помочь в дифференциации голубых невусов (с мутациями GNAQ или GNA11 (23)) от ДПН, что может быть затруднено исключительно на основании гистологических критериев.
Помимо наличия мутаций, активирующих путь киназы MAP (например, MAP2K1 или BRAF ), также наблюдаемых в других невусах, стало очевидным, что ДПН имеют частые одновременные мутации CTNNB1 . Это приводит к постоянной активации сигнального пути бета-катенина. Это также наблюдалось гистологически. В обычных невусах меланоциты становятся меньше («зрелыми») и демонстрируют более низкую экспрессию CTNNB1 и CCND1 по данным иммуногистохимии в более глубоких слоях дермы. При ДПН клетки не мельчают («созревают») и сохраняют экспрессию CTNNB1 и CCND1 в нижних слоях дермы. Авторы также определили, что злокачественная ДПН (меланомы, возникающие при ДПН) демонстрируют дополнительные генетические изменения (активация MAP-киназы и CTNNB1 мутаций). Эти выводы имеют ряд важных следствий. Иммуногистохимия CTNNB1 может быть полезна для выявления поражений ДПН (19, 22). Кроме того, профиль мутаций может помочь в дифференциации голубых невусов (с мутациями GNAQ или GNA11 (23)) от ДПН, что может быть затруднено исключительно на основании гистологических критериев.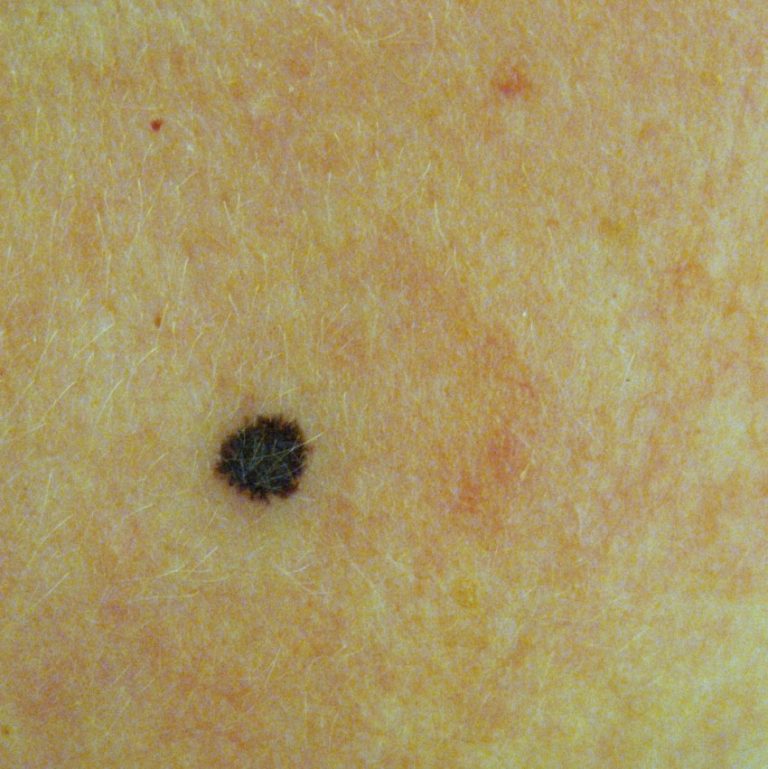 Наконец, наличие дополнительных генетических событий, таких как промотор TERT , CDKN2A, TP53 или других мутаций, свидетельствует о злокачественной опухоли и плохом прогнозе.
Наконец, наличие дополнительных генетических событий, таких как промотор TERT , CDKN2A, TP53 или других мутаций, свидетельствует о злокачественной опухоли и плохом прогнозе.
Недавно описанные генетические данные могут оказать значительную помощь в правильно диагностированных ДПН и В-ДПН. Эти генетические находки были включены в последнюю систему классификации меланоцитарных опухолей ВОЗ, в которой ДПН и В-ДПН помещались между обычными невусами и меланомами в промежуточных группах/меланоцитомах, где ДПН обозначали как дисплазию низкой степени, а В-ДПН — как дисплазию высокой степени. 24). Подробные последующие исследования, в которых применяются генетические критерии, представленные Yeh et al. в настоящее время отсутствуют. Особое значение, конечно, имело бы более крупное проспективное исследование. Эти данные потенциально могут дополнительно уточнить модель, предложенную Yeh et al. и позволяют более точно оценить поведение опухоли на генетической основе в случаях, когда их трудно классифицировать только на основе гистопатологической оценки.
Сила нашего обзора подчеркивает существенный недостаток проспективных когортных исследований, сочетающих клиническую и гистопатологическую корреляцию с генетической оценкой для определения эффективных стратегий клинического лечения ДПН и В-ДПН. В то же время малое количество включенных исследований является ограничением для надлежащего статистического анализа при лечении ДПН и пограничной/атипичной ДПН.
Вклад авторов
IC и TS внесли свой вклад в разработку концепции исследования. IC, TS, AT и LU внесли свой вклад в разработку дизайна исследования. Сбор и анализ данных осуществляли IC и KG. IC, AT, KG, LU и TS подготовили и рассмотрели рукопись.
Финансирование
Подтверждение поддержки Фондом публикаций открытого доступа SLUB/TU Dresden.
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.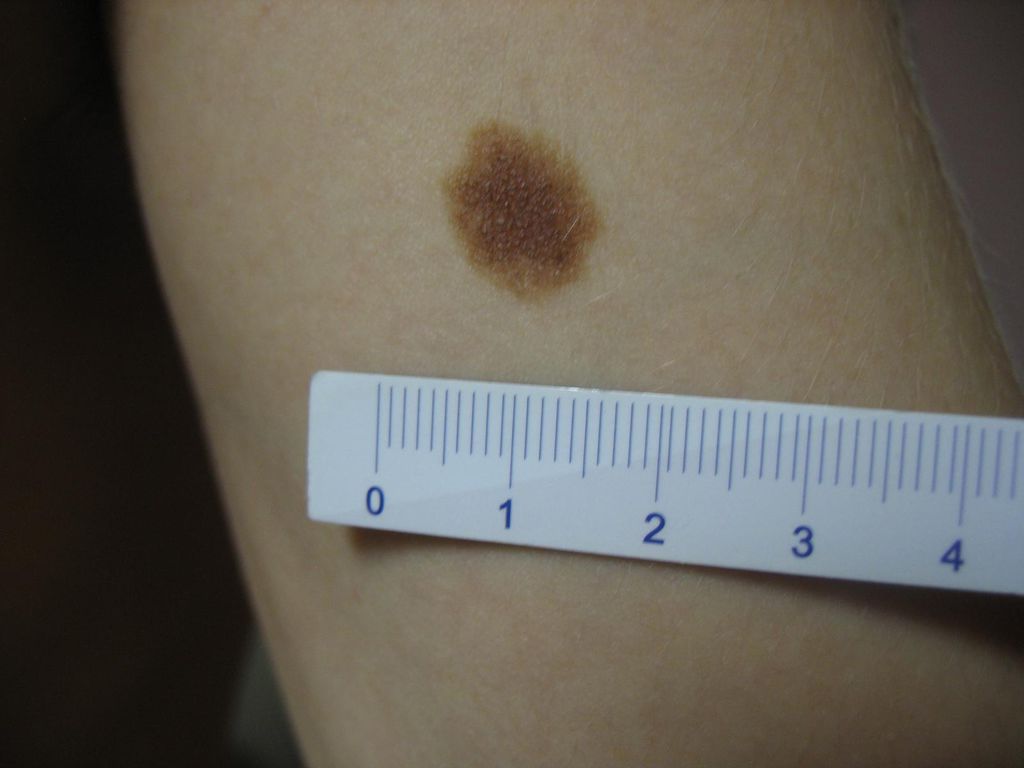
Благодарности
Эта работа является частью магистерской диссертации в рамках магистерской программы клинических исследований Центра клинических исследований и управленческого образования, Отдел медицинских наук, Дрезденский международный университет, Дрезден, Германия.
Ссылки
1. Seab JA Jr, Graham JH, Helwig EB. Глубоко проникающий невус. Am J Surg Pathol. (1989) 13:39–44. doi: 10.1097/00000478-1980-00005
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
2. Robson A, Morley-Quante M, Hempel H, McKee PH, Calonje E. Глубоко проникающий невус: клинико-патологическое исследование 31 случая с дальнейшим определением гистологических особенностей, позволяющих отличить его от других пигментированных доброкачественных меланоцитарных поражений и меланомы. Гистопатология. (2003) 43:529–37. doi: 10.1111/j.1365-2559.2003.01730.x
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
3. Страццула Л., Сенна М.М., Ясуда М., Белазарян Л. Глубоко проникающий невус. J Am Acad Dermatol. (2014) 71:1234–40. doi: 10.1016/j.jaad.2014.07.026
Страццула Л., Сенна М.М., Ясуда М., Белазарян Л. Глубоко проникающий невус. J Am Acad Dermatol. (2014) 71:1234–40. doi: 10.1016/j.jaad.2014.07.026
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
4. Luzar B, Calonje E. Глубоко проникающий невус: обзор. Arch Pathol Lab Med. (2011) 135:321–6. дои: 10.1043/2009-0493-RA.1
CrossRef Полный текст | Google Scholar
5. Barnhill RL, Cerroni L, Cook M, Elder DE, Kerl H, Leboit PE, et al. Состояние дел, номенклатура, точки консенсуса и разногласия в отношении доброкачественных меланоцитарных поражений: итоги международного семинара. Адвокат Анат Патол. (2010) 17:73–90. doi: 10.1097/PAP.0b013e3181cfe758
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
6. Cooper PH. Глубоко проникающий (плексиформный веретеноклеточный) невус: частый участник комбинированных невусов. Дж. Кутан Патол. (1992) 19:172–80. doi: 10.1111/j.1600-0560. 1992.tb01655.x
1992.tb01655.x
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
7. Cerroni L, Barnhill R, Elder D, Gottlieb G, Heenan P, Kutzner H, et al. Меланоцитарные опухоли неопределенного злокачественного потенциала: результаты учебного курса, проведенного на XXIX симпозиуме международного общества дерматопатологов в Граце, октябрь 2008 г. Am J Surg Pathol. (2010) 34:314–26. дои: 10.1097/PAS.0b013e3181cf7fa0
Реферат PubMed | Полный текст перекрестной ссылки | Google Scholar
8. Magro CM, Abraham RM, Guo R, Li S, Wang X, Proper S, et al. Глубоко проникающие невусоподобные пограничные опухоли: уникальное подмножество неоднозначных меланоцитарных опухолей со злокачественным потенциалом и нормальной цитогенетикой. Eur J Дерматол. (2014) 24:594–602. doi: 10.1684/ejd.2014.2393
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
9. Magro CM, Crowson AN, Mihm MC Jr, Gupta K, Walker MJ, Solomon G. Кожная пограничная меланоцитарная опухоль: категориальный подход.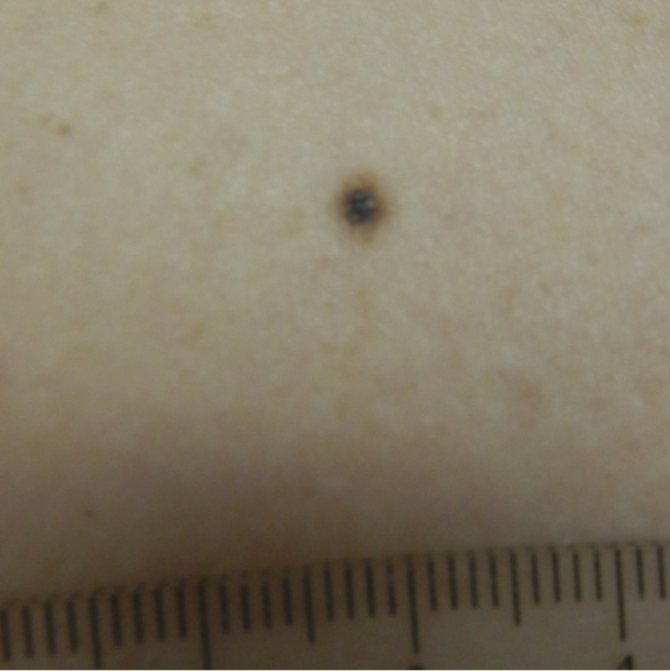 J Am Acad Dermatol. (2010) 62:469–79. doi: 10.1016/j.jaad.2009.06.042
J Am Acad Dermatol. (2010) 62:469–79. doi: 10.1016/j.jaad.2009.06.042
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
10. Abraham RM, Ming ME, Elder DE, Xu X. Атипичное меланоцитарное поражение без геномных аномалий показывает локорегиональные метастазы. Дж. Кутан Патол. (2012) 39:21–4. doi: 10.1111/j.1600-0560.2011.01849.x
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
11. Барнхилл Р.Л., Михм М.С. мл., Магро С.М. Плексиформный веретенообразный невус: характерный вариант плексиформного меланоцитарного невуса. Гистопатология. (1991) 18:243–7. doi: 10.1111/j.1365-2559.1991.tb00832.x
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
12. Хай В.А., Аланен К.В., Голиц Л.Е. Является ли меланоцитарный невус с очаговыми атипичными эпителиоидными компонентами (клональный невус) поверхностным вариантом глубоко проникающего невуса? J Am Acad Dermatol. (2006) 55:460–6. doi: 10.1016/j.jaad.2006.04.054
doi: 10.1016/j.jaad.2006.04.054
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
13. Мехреган Д.А., Мехреган А.Х. Глубоко проникающий невус. Арка Дерматол. (1993) 129:328–31. doi: 10.1001/archderm.129.3.328
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
14. Murphy MJ, Jen M, Chang MW, Grant-Kels JM, Makkar H. Молекулярная диагностика доброкачественного пролиферативного узла, развивающегося во врожденном меланоцитарном невусе у 3-месячного младенца. J Am Acad Dermatol. (2008) 59:518–23. doi: 10.1016/j.jaad.2008.05.011
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
15. Абрахам Р.М., Каракусис Г., Ас Г., Зиобер А.Ф., Черрони Л., Михм М.К. мл. и др. Лимфатическая инвазия предсказывает агрессивное поведение меланоцитарных опухолей с неопределенным злокачественным потенциалом (MELTUMP). 903:79 Am J Surg Pathol. (2013) 37:669–75. doi: 10.1097/PAS.0b013e318288ff47
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
16. Veronese F, Celasco M, Meli F, Zavattaro E, Ramponi A, Merlo E, et al. Глубоко проникающий невус подошвенной поверхности: отчет о случае с дерматоскопическими признаками. J Dtsch Dermatol Ges. (2016) 14:517–8. doi: 10.1111/ddg.12718
Veronese F, Celasco M, Meli F, Zavattaro E, Ramponi A, Merlo E, et al. Глубоко проникающий невус подошвенной поверхности: отчет о случае с дерматоскопическими признаками. J Dtsch Dermatol Ges. (2016) 14:517–8. doi: 10.1111/ddg.12718
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
17. Чо Э.С., Чо Х.М., Нам В., Ким Х.С. Множественные глубоко проникающие невусы в ротовой полости, распространяющиеся на жевательные мышцы и буккальное жировое тело. J Оральный челюстно-лицевой хирург. (2017) 75:2579–92. doi: 10.1016/j.joms.2017.05.026
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
18. Lee JJ, Vilain RE, Granter SR, Hu NR, Bresler SC, Xu S, et al. 5-гидроксиметилцитозин является ядерным биомаркером для оценки биологического потенциала гистологически неоднозначных сильно пигментированных меланоцитарных новообразований. Дж. Кутан Патол. (2017) 44: 249–55. doi: 10.1111/cup.12880
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
19. Шекоранья Д., Вергот К., Хаулина Г., Пизем Дж. Комбинированные глубокие невусы конъюнктивы — относительно распространенные поражения, характеризующиеся мутацией BRAFV600E и активацией пути бета-катенина: клинико-патологический анализ 34 поражений. Br J Офтальмол . (2019). doi: 10.1136/bjophthalmol-2019-314807. [Epub перед печатью].
Шекоранья Д., Вергот К., Хаулина Г., Пизем Дж. Комбинированные глубокие невусы конъюнктивы — относительно распространенные поражения, характеризующиеся мутацией BRAFV600E и активацией пути бета-катенина: клинико-патологический анализ 34 поражений. Br J Офтальмол . (2019). doi: 10.1136/bjophthalmol-2019-314807. [Epub перед печатью].
Реферат PubMed | Полный текст перекрестной ссылки | Google Scholar
20. Ridha H, Ahmed S, Theaker JM, Horlock N. Злокачественная меланома и глубоко проникающие родинки – трудности диагностики у детей. J Plast Reconstr Aestet Surg. (2007) 60:1252–5. doi: 10.1016/j.bjps.2006.05.002
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
21. Yeh I, Lang UE, Durieux E, Tee MK, Jorapur A, Shain AH, et al. Комбинированная активация пути MAP-киназы и передачи сигналов β-катенина вызывает глубоко проникающие невусы. Нац.коммун. (2017) 8:644. doi: 10.1038/s41467-017-00758-3
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
22.

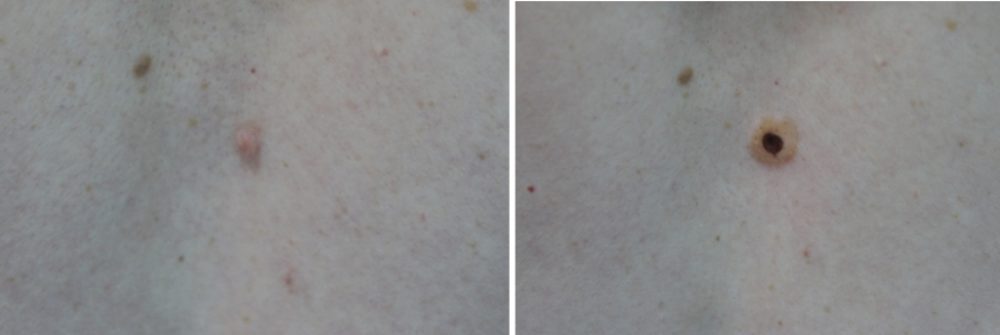

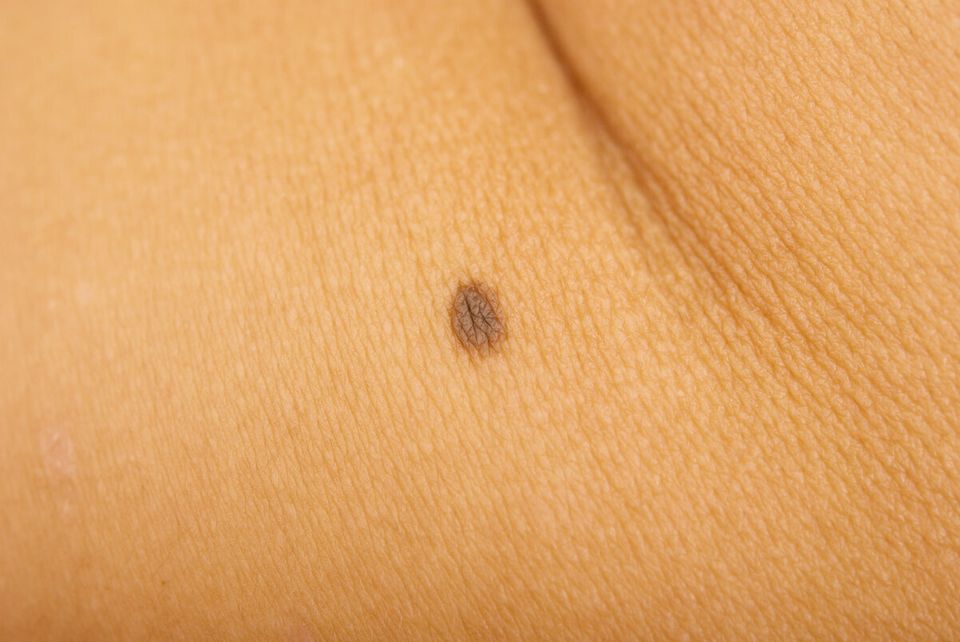
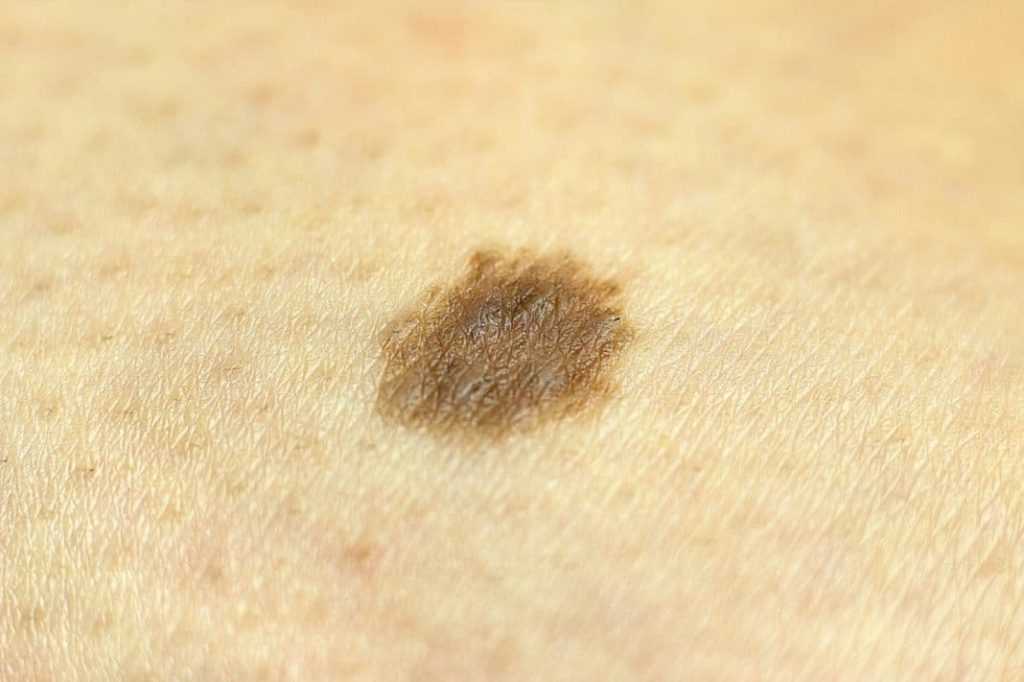 Но успешное лечение не исключает появление родинки на другом месте.
Но успешное лечение не исключает появление родинки на другом месте.
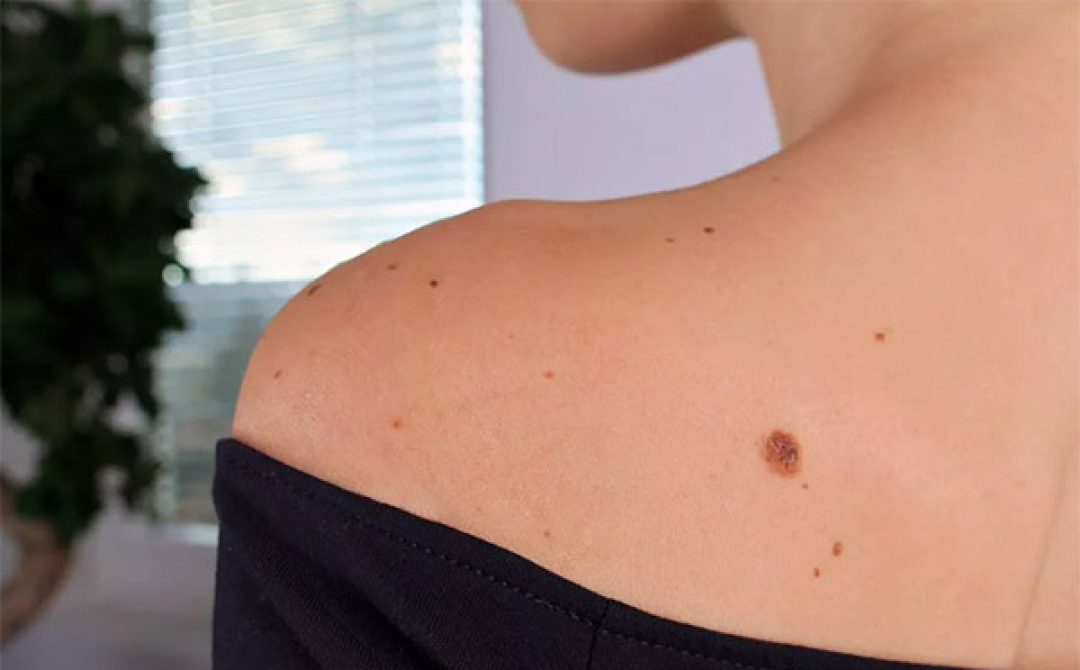 1684/ejd.2014.2393
1684/ejd.2014.2393
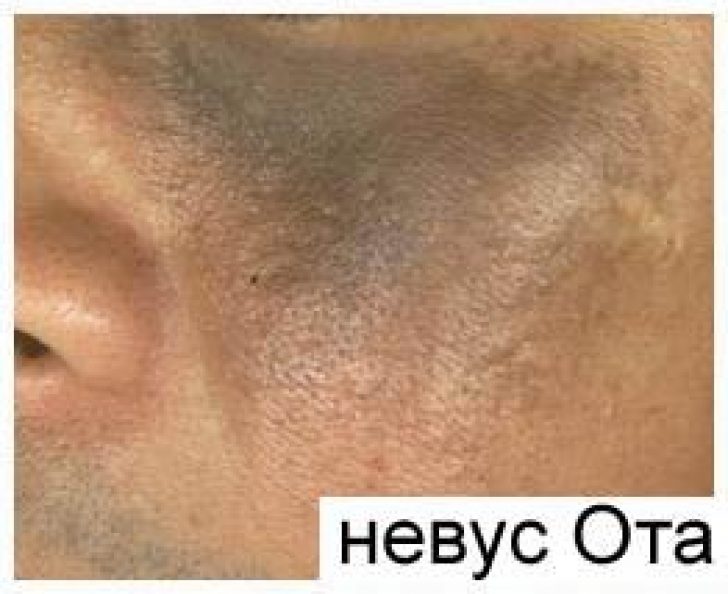
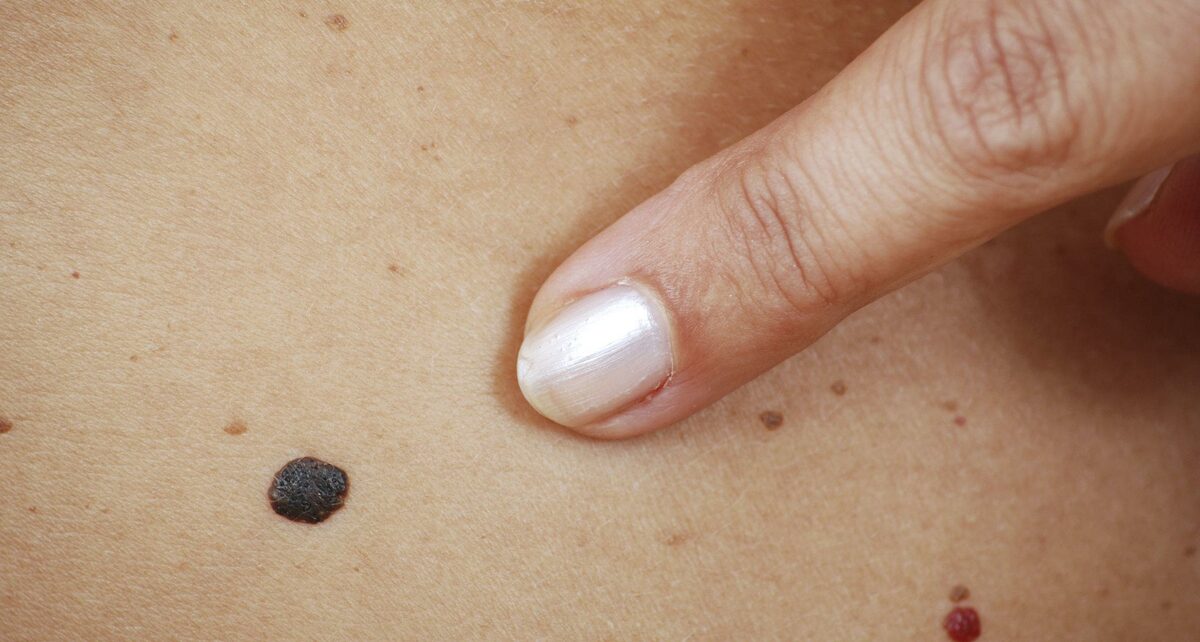


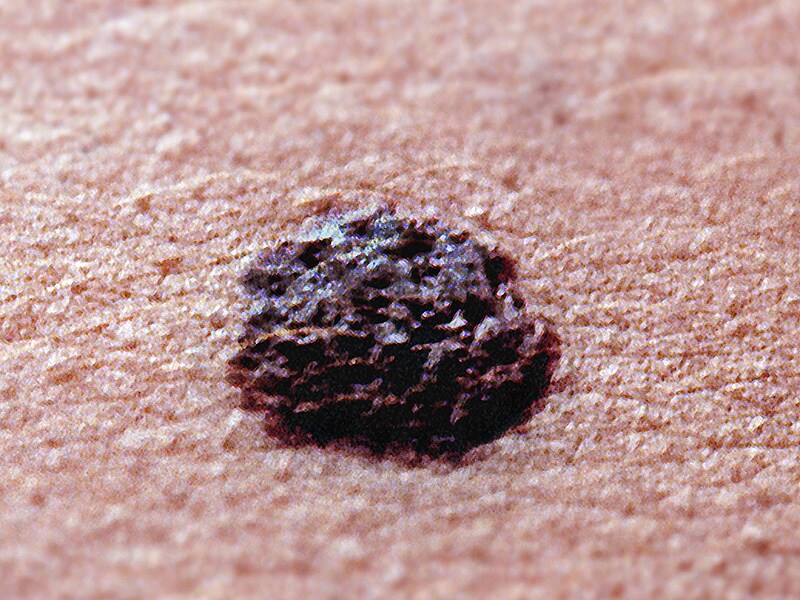 : рекомендации из повседневной практики.
: рекомендации из повседневной практики.