Устойчивость к антибиотикам Helicobacter pylori: обзор эпидемиологических тенденций и проблемы терапии | Ахметова Д.Г., Балтабекова А.Ж., Шустов А.В.
В статье представлены обзор эпидемиологических тенденций и проблемы терапии устойчивости к антибиотикам Helicobacter pylori
Введение
Бактерия H. pylori является глобально распространенным условно-патогенным микроорганизмом и колонизирует примерно 50% населения мира [1]. Данный патоген был впервые обнаружен в биопсиях желудка в 1983 г. [2]. H.pylori — это грамотрицательная бацилла, которая колонизирует слизистую оболочку желудка человека. У многих людей такая инфекция со временем приводит к хроническому гастриту, язвенной болезни желудка, лимфоме лимфоидной ткани слизистой оболочки (MALT) и карциноме желудка. Не так давно было высказано предположение, что H.pylori может быть связанаи с внекишечными заболеваниями, такими как тромбоцитопеническая пурпура, железодефицитная анемия и дефицит витамина В12 [3, 4].

резистентности будет все более возрастать с учетом того, что лечение назначается все большему количеству больных в мире [5, 6]. В последних Маастрихтских рекомендациях есть положение о том, что в регионах с высокой частотой устойчивости H. pylori к кларитромицину необходимо до назначения терапии тестировать восприимчивость возбудителя к антибиотикам [1]. Данная идея получила развитие в решениях Киотского глобального консенсусного совещания по хеликобактерной инфекции: в каждом регионе мира нужно применять только такие схемы лечения, которые обеспечивают эрадикацию не менее чем в 90% случаев.

Распространенность инфекции H. pylori
Заражение H. pylori происходит во всем мире, но при этом наблюдаются географические различия в распространенности инфекции. Многочисленные исследования показали, что низкий социально-экономический статус ассоциируется с повышенным риском инфекции
Распространенность устойчивости к антибиотикам
Распространенность антибиотикорезистентности H. py-lori разнится по географическим районам [15]. Распространенность хеликобактерной инфекции в США не изменилась с 2000 по 2010 г., но частота успешной эрадикации инфекции снизилась в этот период [1, 6, 13, 16].
Европейское многоцентровое исследование, проведенное с 2008 по 2009 г., показало частоту встречаемости резистентности случаев инфекции H. pylori к кларитромицину, метронидазолу и левофлоксацину: 17,5%, 34,9% и 14,1% соответственно [5]. Исследование, выполненное в Японии в 2002–2005 гг., выявило быстрый рост случаев инфекции, вызванных кларитромицин-устойчивым штаммом
 В исследовании консорциума SHARP (Surveillance of H. pylori Antimicrobial Resistance Partnership) выполнен метаанализ данных, собранных с 1993 по 1999 г., и показано, что уровень резистентности к кларитромицину, метронидазолу и амоксициллину составил 10,1, 36,9 и 1,4% соответственно. Проспективное многоцентровое исследование HARP (Helicobacter pylori Antimicrobial Resistance Monitoring Program) проводилось в период 1998–2002 гг. и продемонстрировало резистентность к кларитромицину, метронидазолу и амоксициллину в 12,9, 25,1 и 0,9% случаев соответственно.
В исследовании консорциума SHARP (Surveillance of H. pylori Antimicrobial Resistance Partnership) выполнен метаанализ данных, собранных с 1993 по 1999 г., и показано, что уровень резистентности к кларитромицину, метронидазолу и амоксициллину составил 10,1, 36,9 и 1,4% соответственно. Проспективное многоцентровое исследование HARP (Helicobacter pylori Antimicrobial Resistance Monitoring Program) проводилось в период 1998–2002 гг. и продемонстрировало резистентность к кларитромицину, метронидазолу и амоксициллину в 12,9, 25,1 и 0,9% случаев соответственно. pylori, и из этих пациентов 92% ранее получали лечение макролидами. Более того, наблюдался эффект зависимости от дозы: частота встречаемости резистентности к кларитромицину была тем выше, чем большее количество курсов лечения макролидами было в подгруппах обследованных. В этой популяции подобная связь была найдена между частотой резистентности к метронидазолу и объемом использования метронидазола в индивидуальной истории больных [17].
pylori, и из этих пациентов 92% ранее получали лечение макролидами. Более того, наблюдался эффект зависимости от дозы: частота встречаемости резистентности к кларитромицину была тем выше, чем большее количество курсов лечения макролидами было в подгруппах обследованных. В этой популяции подобная связь была найдена между частотой резистентности к метронидазолу и объемом использования метронидазола в индивидуальной истории больных [17]. Кларитромицин
Распространенность устойчивости к кларитромицину увеличивается во многих странах (рис. 2а) [5, 18–23]. Исследования показали, что в странах, где низок общий уровень серопозитивности к маркерам инфекции pylori сталкиваются с ростом устойчивости возбудителя
pylori сталкиваются с ростом устойчивости возбудителя к кларитромицину. Например, распространенность устойчивости к кларитромицину значительно возросла (с 1,8% в 1996 г. до 27,1% в 2008 г.) в Японии; серопозитивность за период 2000–2013 гг. выросла с 40 до 55%, а встречаемость кларитромицин-резистентных случаев достигла 31,1%. Аналогично в Китае с 2000 по 2014 г. встречаемость резистентности
Метронидазол
Во многих странах мира отмечена резистентность H. pylori к метронидазолу, и ее уровень растет (рис. 2б) [18–22, 25–28]. Распространенность резистентности H.pylori к метронидазолу в Европе в общей популяции варьирует на уровне от 20 до 40% со средней цифрой 33,1% без явных различий между Южной и Северной Европой. Зато в Центральной и Восточной Европе уровни резистентности ниже. С другой стороны, в развивающихся странах за пределами Европы резистентность H. pylori к метронидазолу встречается значительно чаще (50–80%), например в Мексике — 76,3%. В развитых странах за пределами Европы резистентность к метронидазолу в общей популяции встречается реже, чем средняя цифра по Европе: в Японии — 9–12%, в Канаде — 18–22%, в США — 21,5% [23]. Ряд авторов объясняет различия в частоте встречаемости резистентности неодинаковыми объемами предшествующего использования метронидазола в обследованных регионах. Обследование коренных народов Аляски показало статистически значимо бóльшую частоту встречаемости устойчивости среди женщин по сравнению с мужчинами, причем уровни резистентности коррелировали с количеством перенесенных курсов терапии метронидазолом.
pylori к метронидазолу, и ее уровень растет (рис. 2б) [18–22, 25–28]. Распространенность резистентности H.pylori к метронидазолу в Европе в общей популяции варьирует на уровне от 20 до 40% со средней цифрой 33,1% без явных различий между Южной и Северной Европой. Зато в Центральной и Восточной Европе уровни резистентности ниже. С другой стороны, в развивающихся странах за пределами Европы резистентность H. pylori к метронидазолу встречается значительно чаще (50–80%), например в Мексике — 76,3%. В развитых странах за пределами Европы резистентность к метронидазолу в общей популяции встречается реже, чем средняя цифра по Европе: в Японии — 9–12%, в Канаде — 18–22%, в США — 21,5% [23]. Ряд авторов объясняет различия в частоте встречаемости резистентности неодинаковыми объемами предшествующего использования метронидазола в обследованных регионах. Обследование коренных народов Аляски показало статистически значимо бóльшую частоту встречаемости устойчивости среди женщин по сравнению с мужчинами, причем уровни резистентности коррелировали с количеством перенесенных курсов терапии метронидазолом.
Другие антибиотики
Частота встречаемости устойчивости H. pylori к тетрациклину низкая: 0,7% в Испании, 0,5% в Великобритании, 0,5% в Гонконге, причем в ряде стран сообщили об отсутствии выявления случаев резистентности к тетрациклину [5]. Некоторые исследования определяли распространенность устойчивости к фторхинолонам [1].В Китае, Италии и США резистентность к левофлоксацину обнаружена в 34,5, 22,1 и 31,9% случаев соответственно [19, 21, 23]. Распространенность резистентности к левофлоксацину в Европе известна на примере Португалии — 20,9%. Эпидемиология резистентности к левофлоксацину изучена гораздо хуже, чем к другим упомянутым препаратам, однако ряд авторов указывает на тенденцию к увеличению встречаемости устойчивости
 Во Франции резистентность к фторхинолонам описана в 3,3% случаев, в странах Восточной Европы — в 3,9%. Также описано, что новый фторхинолоновый антибиотик ситафлоксацин, по-видимому, не обладает выраженной кросс-резистентностью с другими фторхинолонами (которые уже имеют историю использования в популяции) и поэтому эффективно эрадицирует H. pylori [29, 30].
Во Франции резистентность к фторхинолонам описана в 3,3% случаев, в странах Восточной Европы — в 3,9%. Также описано, что новый фторхинолоновый антибиотик ситафлоксацин, по-видимому, не обладает выраженной кросс-резистентностью с другими фторхинолонами (которые уже имеют историю использования в популяции) и поэтому эффективно эрадицирует H. pylori [29, 30].Устойчивость H. pylori к амоксициллину в европейских странах встречается редко (от 0 до
Диагностика инфекции H. pylori
Тестирование пациентов с болями в эпигастральной области и диспепсией на инфекцию H. pylori стало распространенной диагностической практикой. Важность хеликобактерной инфекции значительно возросла в связи с обнаружением статистической связи между данной инфекцией и раком желудка. Международное агентство по изучению рака (International Agency for Research on Cancer) считает H. pylori канцерогеном I группы [2].Способы обследования на инфекцию H. pylori делятся на инвазивные и неинвазивные.
 Неинвазивные методы рекомендованы для пациентов H. pylori в стуле пациента. Серологическое тестирование обнаруживает иммуноглобулины IgG к антигенам H. pylori в сыворотке; впрочем, есть и рекомендации не использовать серологический метод для диагностики данной инфекции из-за того, что уровень сероконверсии существенно ниже 100% [1]. Серологический тест не пригоден для мониторинга эффективности терапии, поскольку успешное лечение не изменяет уровня IgG в краткосрочной перспективе. Альтернативный серологический метод предусматривает обнаружение антител другого класса — IgM к антигенам H.pylori, которые появляются в период острой фазы инфекции сразу после заражения, однако период времени, в течение которого IgM присутствуют в определяемых концентрациях, слишком короткий.
Неинвазивные методы рекомендованы для пациентов H. pylori в стуле пациента. Серологическое тестирование обнаруживает иммуноглобулины IgG к антигенам H. pylori в сыворотке; впрочем, есть и рекомендации не использовать серологический метод для диагностики данной инфекции из-за того, что уровень сероконверсии существенно ниже 100% [1]. Серологический тест не пригоден для мониторинга эффективности терапии, поскольку успешное лечение не изменяет уровня IgG в краткосрочной перспективе. Альтернативный серологический метод предусматривает обнаружение антител другого класса — IgM к антигенам H.pylori, которые появляются в период острой фазы инфекции сразу после заражения, однако период времени, в течение которого IgM присутствуют в определяемых концентрациях, слишком короткий. Уреазный дыхательный тест с мочевиной, меченной 13C, в настоящее время является «золотым стандартом» для диагностирования инфекции H. pylori. Этот тест использует мочевину, в молекулу которой включен нерадиоактивный, но редкий изотоп углерода 13С, для выявления активности фермента уреазы (у человека нет эндогенной уреазы, но этот фермент производят многие бактерии, и в частности H.
 pylori). Наличие изотопа 13C в выдыхаемом воздухе статистически связано с инфекцией H. pylori. Еще один неинвазивный тест обнаруживает антиген H. pylori в стуле больного с помощью реакции с соответствующими антителами и последующей детекции образовавшихся комплексов антиген — антитело. Важное преимущество дыхательного теста с мочевиной и теста на антиген в стуле больного заключается в пригодности указанных методов для контроля полноты эрадикации патогена в результате лечения [33, 34].
pylori). Наличие изотопа 13C в выдыхаемом воздухе статистически связано с инфекцией H. pylori. Еще один неинвазивный тест обнаруживает антиген H. pylori в стуле больного с помощью реакции с соответствующими антителами и последующей детекции образовавшихся комплексов антиген — антитело. Важное преимущество дыхательного теста с мочевиной и теста на антиген в стуле больного заключается в пригодности указанных методов для контроля полноты эрадикации патогена в результате лечения [33, 34].Гастроэндоскопия (инвазивная процедура) рекомендована для пациентов с впервые выявленной диспепсией, сопровождаемой сигнальными симптомами, среди которых непреднамеренная потеря веса, желудочно-кишечные кровотечения, железодефицитная анемия или дисфагия. Для больных с впервые выявленной диспепсией в отсутствие сигнальных симптомов гастроэндоскопия показана, если возраст больного >54 лет (впрочем, граничный возраст, при котором следует назначать гастроэндоскопию, является предметом дискуссий и может варьировать в зависимости от популяционной группы, а именно от локальной частоты рака желудка в данной группе) [1].
 Если при обследовании больного можно быстро получить биопсию, рекомендовано проведение быстрого уреазного теста. В быстром уреазном тесте исследуют биоптаты антрального отдела и тела желудка для обнаружения активности уреазы. Уреазный тест быстрее гистологического исследования, но на практике если есть возможность взять биопсию, то образец также отправляется на гистологическое исследование из-за его высокой диагностической ценности — оно позволяет оценить тяжесть воспаления и обнаружить присоединяющиеся патологии, в т. ч. лимфому или карциному желудка [7]. Для микроскопического выявления H.pylori в биопсиях предложены несколько методов окрашивания (например, модифицированный метод Гимза или окрашивание по Уортину — Старри, или иммуногистохимические методы).
Если при обследовании больного можно быстро получить биопсию, рекомендовано проведение быстрого уреазного теста. В быстром уреазном тесте исследуют биоптаты антрального отдела и тела желудка для обнаружения активности уреазы. Уреазный тест быстрее гистологического исследования, но на практике если есть возможность взять биопсию, то образец также отправляется на гистологическое исследование из-за его высокой диагностической ценности — оно позволяет оценить тяжесть воспаления и обнаружить присоединяющиеся патологии, в т. ч. лимфому или карциному желудка [7]. Для микроскопического выявления H.pylori в биопсиях предложены несколько методов окрашивания (например, модифицированный метод Гимза или окрашивание по Уортину — Старри, или иммуногистохимические методы).Стратегии антибиотикотерапии
Для лечения инфекции H. pylori разработано много протоколов терапии (рис. 3). В том случае если не удается достигнуть эрадикации, предложены протоколы консервативного поддерживающего лечения.
Тройная терапия
Эффективность применения антибиотиков зависит от ряда факторов, таких как эффективность антимикробного действия выбранного препарата с учетом возможной резистентности, способа применения, продолжительности курса. При назначении лечения также следует учитывать эффекты, определяющие приверженность больного протоколу лечения, которые связаны со стоимостью препарата, его побочными действиями и переносимостью. Внастоящее время стандартный протокол лечения инфекции H. pylori в регионах, где распространенность резистентности к кларитромицину ниже 15%, представляет собой тройную терапию, которая включает ингибиторы протонной помпы (ИПП), кларитромицин и амоксициллин [35]. Эта терапевтическая схема широко используется в мире уже более 10 лет, однако ее эффективность постепенно снижается. В случае аллергии к пенициллинам у больного амоксициллин можно заменить метронидазолом без потери эффективности тройной терапии. Основной причиной неудачи эрадикации для стандартного протокола тройной терапии считается повышенная устойчивость изолята H. pylori у больного к кларитромицину. Другие факторы, которые могут повлиять на показатели эффективности лечения, включают приверженность терапии (соблюдение пациентом назначений), повышенную массу тела, генотип H. pylori, уровень бактериальной нагрузки, кислотность желудочного сока и наличие у пациента атрофического гастрита. Некоторые авторы предлагают в регионах, где высока встречаемость резистентности к кларитромицину, избегать стандартного протокола (включающего кларитромицин) для проведения терапии первой линии [16, 36]. В соответствии с Маастрихтским консенсусом рекомендуется тестирование чувствительности до назначения лечения в регионах, где уровень резистентности превышает 20% в популяционной группе (например, выделенной по полу и возрасту), к которой относится пациент [1]. Кроме этого, рекомендовано учитывать индивидуальную историю применения макролидных антибиотиков, потому что такой анамнез повышает вероятность обнаружить устойчивость к кларитромицину [17].
pylori у больного к кларитромицину. Другие факторы, которые могут повлиять на показатели эффективности лечения, включают приверженность терапии (соблюдение пациентом назначений), повышенную массу тела, генотип H. pylori, уровень бактериальной нагрузки, кислотность желудочного сока и наличие у пациента атрофического гастрита. Некоторые авторы предлагают в регионах, где высока встречаемость резистентности к кларитромицину, избегать стандартного протокола (включающего кларитромицин) для проведения терапии первой линии [16, 36]. В соответствии с Маастрихтским консенсусом рекомендуется тестирование чувствительности до назначения лечения в регионах, где уровень резистентности превышает 20% в популяционной группе (например, выделенной по полу и возрасту), к которой относится пациент [1]. Кроме этого, рекомендовано учитывать индивидуальную историю применения макролидных антибиотиков, потому что такой анамнез повышает вероятность обнаружить устойчивость к кларитромицину [17]. Европейские рекомендации предусматривают назначение тройной терапии с 7-дневным курсом в районах, где встречаемость устойчивости к кларитромицину 20% [1].
 Рандомизированное исследование, проведенное Paoluzi et al., посвящено сравнению частоты эрадикации H. pylori в группах пациентов, получавших стандартную тройную терапию (амоксициллин, кларитромицин и омепразол) в течение 7 или 14 дней. Уровень резистентности в обеих группах в данном исследовании не определяли и не сравнивали, однако результаты показали, что 14-дневный курс приводит к лучшим результатам по эрадикации по сравнению с 7-дневным (77% против 66%).
Рандомизированное исследование, проведенное Paoluzi et al., посвящено сравнению частоты эрадикации H. pylori в группах пациентов, получавших стандартную тройную терапию (амоксициллин, кларитромицин и омепразол) в течение 7 или 14 дней. Уровень резистентности в обеих группах в данном исследовании не определяли и не сравнивали, однако результаты показали, что 14-дневный курс приводит к лучшим результатам по эрадикации по сравнению с 7-дневным (77% против 66%).4-компонентная терапия, включающая соли висмута
4-компонентная терапия включает ИПП, препараты висмута и 2 антибиотика (обычно 2 из следующего перечня: тетрациклин, кларитромицин и метронидазол) [1]. Эффективность данного протокола в качестве терапии первой линии была проверена в регионах с высоким уровнем резистентности к кларитромицину или метронидазолу, а также в группах пациентов с историей недавнего или многократного предшествующего лечения указанными антибиотиками [1]. Основным преимуществом этой схемы является то, что она позволяет преодолеть устойчивость к кларитромицину или метронидазолу, и с этой целью данный протокол предусматривает одновременное применение кларитромицина и метронидазола. Метаанализ, выполненный Fisch и Evans, показал лучшую эффективность 4-компонентной терапии по сравнению со стандартной тройной терапией в регионах с повышенной частотой встречаемости резистентности к кларитромицину или метронидазолу.
Метаанализ, выполненный Fisch и Evans, показал лучшую эффективность 4-компонентной терапии по сравнению со стандартной тройной терапией в регионах с повышенной частотой встречаемости резистентности к кларитромицину или метронидазолу.Доксициклин или амоксициллин можно применять как замену для тетрациклина и солей висмута в регионах, где последние препараты недоступны. Однако данные об эффективности такой замены неоднозначны [37]. При назначении 4-компонентной терапии следует учитывать пониженную приверженность лечению у пациентов в связи с увеличением количества наименований препаратов и более частым приемом.
Последовательная терапия
Последовательная терапия была впервые проведена по протоколу, описанному Zullo et al., она состоит из 10-дневного лечения, включающего 5 дней комбинации ИПП + амоксициллин, затем 5 дней тройной терапии сочетанием ИПП + кларитромицин + метронидазол [1]. Левофлоксацин может быть использован у пациентов с аллергией на пенициллины или в районах с высоким уровнем резистентности к кларитромицину. Хотя последовательная терапия включает кларитромицин, она считается альтернативой стандартной тройной терапии, пригодной для использования в местностях с высокой встречаемостью устойчивости к кларитромицину [1]. Этот терапевтический режим использует назначение амоксициллина перед применением кларитромицина с целью преодоления устойчивости к кларитромицину. Амоксициллин разрушает клеточные стенки H. pylori и препятствует работе мембранных каналов экспорта кларитромицина из бактериальной клетки (один из механизмов устойчивости данной бактерии). Недостатком этой схемы терапии является ее сложность в отношении режима приема препаратов, которая снижает приверженность [16]. Если пациент не соблюдает протокол лечения, есть вероятность развития множественной лекарственной устойчивости. Последовательная терапия использует основные антибиотики, эффективные против H. pylori, и это означает, что неуспех последовательной терапии ограничивает возможности терапии второй линии.
Хотя последовательная терапия включает кларитромицин, она считается альтернативой стандартной тройной терапии, пригодной для использования в местностях с высокой встречаемостью устойчивости к кларитромицину [1]. Этот терапевтический режим использует назначение амоксициллина перед применением кларитромицина с целью преодоления устойчивости к кларитромицину. Амоксициллин разрушает клеточные стенки H. pylori и препятствует работе мембранных каналов экспорта кларитромицина из бактериальной клетки (один из механизмов устойчивости данной бактерии). Недостатком этой схемы терапии является ее сложность в отношении режима приема препаратов, которая снижает приверженность [16]. Если пациент не соблюдает протокол лечения, есть вероятность развития множественной лекарственной устойчивости. Последовательная терапия использует основные антибиотики, эффективные против H. pylori, и это означает, что неуспех последовательной терапии ограничивает возможности терапии второй линии.Сопутствующая терапия
Сопутствующая терапия представляет собой назначение курса лечения с использованием ИПП, кларитромицина, амоксициллина и метронидазола в течение по крайней мере 10 дней. В рандомизированных клинических испытаниях сопутствующая терапия превзошла по эффективности стандартную тройную терапию [38]. Метаанализ данных, полученных в Японии, Великобритании, Германии, Испании и Италии, показал уровень эрадикации >90%. Исследование в Тайване сравнило эффективность сопутствующей терапии и последовательной терапии с эффективностью использования одного и того же сочетания препаратов: ИПП, левофлоксацина, амоксициллина и метронидазола. Распространенность резистентности в группе больных до начала лечения была следующей: резистентность к левофлоксацину — 10,2%, к амоксициллину — 0,6%, к кларитромицину — 6,6% и к метронидазолу — 33,5%. Эффективность эрадикации с использованием 2-х терапевтических схем оказалась сравнимой: 92,2% для сопутствующей терапии и 93,3% для последовательной терапии [39].
В рандомизированных клинических испытаниях сопутствующая терапия превзошла по эффективности стандартную тройную терапию [38]. Метаанализ данных, полученных в Японии, Великобритании, Германии, Испании и Италии, показал уровень эрадикации >90%. Исследование в Тайване сравнило эффективность сопутствующей терапии и последовательной терапии с эффективностью использования одного и того же сочетания препаратов: ИПП, левофлоксацина, амоксициллина и метронидазола. Распространенность резистентности в группе больных до начала лечения была следующей: резистентность к левофлоксацину — 10,2%, к амоксициллину — 0,6%, к кларитромицину — 6,6% и к метронидазолу — 33,5%. Эффективность эрадикации с использованием 2-х терапевтических схем оказалась сравнимой: 92,2% для сопутствующей терапии и 93,3% для последовательной терапии [39].Теоретически преимуществом сопутствующей терапии может быть эффективность против штаммов с множественной лекарственной устойчивостью [40], однако на практике встречаемость даже двойной устойчивости (устойчивости клинических изолятов H.
 pylori одновременно к 2 антибиотикам разных классов) не изучена.
pylori одновременно к 2 антибиотикам разных классов) не изучена.Гибридная терапия (последовательно-сопутствующая)
В одной из работ предложена гибридная терапевтическая схема, которая представляет собой комбинацию ступенчатой и сопутствующей терапии [41]. Гибридная схема включает первоначальный курс ИПП + амоксициллин в течение 7 дней, после которого назначается 4-компонентная терапия сочетанием ИПП, амоксициллина, метронидазола и кларитромицина в течение 7 дней. Частота эрадикации была отличная — 99% (!), причем отмечена эрадикация штаммов с двойной устойчивостью (к кларитромицину и метронидазолу) [42]. Авторы указанного исследования предполагают, что высокая эффективность гибридной терапии связана с более длительным приемом амоксициллина (в течение 14 дней) по сравнению с последовательной или сопутствующей терапевтическими схемами. Действительно, одно рандомизированное клиническое испытание показало, что гибридная терапия эквивалентна по уровням эрадикации удлиненному (14-дневному) курсу сопутствующей терапии [43].
Терапия второй линии на основе хинолонов
В случаях, когда не удается эрадицировать H. pylori с использованием стандартной тройной терапии, предложено использовать терапию второй линии (salvage therapy): ИПП + левофлоксацин + амоксициллин в течение 10 дней [44]. Ряд исследований в Европе и Тайване продемонстрировал варьирующие конечные (после прохождения терапии первой и второй линии) уровни эрадикации (65–96%) что, вероятно, отражает различную встречаемость устойчивости к левофлоксацину в разных географических регионах [44].Другой режим терапии второй линии (так называемый LOAD (от Levofloxacin, Omeprazole, Nitazoxanide, Doxycycline)) включает прием комбинации левофлоксацина, омепразола, нитазоксанида и доксициклина в течение 7 или 10 дней. Исследование эффективности лечения когорты из 653 пациентов показало, что применение схемы LOAD привело к более высоким конечным уровням эрадикации (90%) по сравнению с таковым при применении стандартной тройной терапии (73%), независимо от продолжительности курса [45].
 Кроме этого, данное исследование показало, что у пациентов на фоне LOAD-терапии статистически значимо реже наблюдались рецидивы в течение 1-летнего периода наблюдения [45].
Кроме этого, данное исследование показало, что у пациентов на фоне LOAD-терапии статистически значимо реже наблюдались рецидивы в течение 1-летнего периода наблюдения [45].Терапия третьей линии: левофлоксацин, рифабутин, фуразолидон
Для пациентов, у которых не произошло эрадикации возбудителя после курсов терапии первой и второй линии, предлагается использование левофлоксацина. В одном исследовании в качестве терапии третьей линии предложено использование левофлоксацина в сочетании с рабепразолом, субцитратом висмута и амоксициллином. В данном исследовании, несмотря на наличие множественной лекарственной устойчивости, 10-дневный курс лечения привел к конечному уровню эрадикации в 84%. При этом в подгруппе пациентов, у которых была обнаружена резистентность возбудителя к амоксициллину или левофлоксацину, конечный уровень эрадикации был ниже.Выбор терапии с использованием хинолонов должен быть основан на результатах испытаний антибиотикочувствительности или хотя бы на данных о встречаемости резистентности в данном географическом регионе.
 Частота встречаемости резистентности к хинолонам возрастает по мере роста использования хинолонов для лечения инфекций дыхательных и мочеполовых путей [1]. Таким образом, описанный режим лечения на основе хинолонов не рекомендуется в качестве первой линии терапии. Иногда этот режим используется в качестве терапии второй линии в популяциях, где уровень устойчивости к кларитромицину >15–20%, к хинолонам
Частота встречаемости резистентности к хинолонам возрастает по мере роста использования хинолонов для лечения инфекций дыхательных и мочеполовых путей [1]. Таким образом, описанный режим лечения на основе хинолонов не рекомендуется в качестве первой линии терапии. Иногда этот режим используется в качестве терапии второй линии в популяциях, где уровень устойчивости к кларитромицину >15–20%, к хинолонамТерапия на основе рифабутина
На основании результатов исследований in vitro была предложена стратегия терапии на основе рифабутина (антибиотик, изначально нашедший терапевтическое применение для лечения туберкулеза), которая включает курс сочетанием ИПП + амоксициллин + рифабутин. Оптимальная продолжительность лечения по указанному протоколу не ясна (предложены курсы 7, 10 или 14 дней). Важным, но не частым осложнением при применении рифабутина является миелотоксичность [46]. В связи с потенциалом развития резистентности к рифабутину у возбудителя туберкулеза, циркулирующего в человеческой популяции, применение рифабутина не должно быть рутинным, вышеуказанная терапевтическая схема предложена только как терапия третьей линии. Кроме того, данная терапевтическая схема рекомендована для использования в случаях, когда невозможно использовать соли висмута и тетрациклин [1, 46].
Кроме того, данная терапевтическая схема рекомендована для использования в случаях, когда невозможно использовать соли висмута и тетрациклин [1, 46].Терапия на основе фуразолидона
Схема с применением фуразолидона включает недельный курс терапии сочетанием лансопразола, висмута трикалия дицитрата, тетрациклина и фуразолидона. Данная схема используется в случае неуспеха терапии второй линии. Конечная эффективность эрадикации достигает 90%. Проблемами, возникающими при применении этой схемы, являются высокая частота побочных эффектов и влияние существующей в популяции патогена перекрестной резистентности с метронидазолом.Двухкомпонентная терапия высокими дозами
Двухкомпонентная терапия высокими дозами была использована в регионах с высокой частотой встречаемости резистентности к кларитромицину. Эта схема включает применение ИПП и амоксициллина 3 р./сут в течение 14 дней [47]. Уровень эрадикации составил 78,4%, что несущественно ниже эффективности стандартной тройной терапии.
Заключение
Инфекция H. pylori повсеместно распространена в мире, однако встречаемость устойчивости к антибиотикам у изолятов H. pylori сильно варьирует между географическими регионами и, по имеющимся данным, имеет тенденцию к росту. Во многих странах встречаемость устойчивости H. pylori к антибиотикам перешагнула порог в 15–20%. В течение последних 20 лет эффективность эрадикации в ходе терапии упала ниже уровня 80–90%. Важнейшими причинами неуспеха терапии являются устойчивость к антибиотикам и несоблюдение режима приема препаратов из-за недостаточной приверженности пациентов лечению. Распространение резистентности у микроорганизмов коррелирует с объемом потребления антибиотиков, что показано и на примере хеликобактерной инфекции. С течением времени растет необходимость определения антибиотикорезистентности перед назначением терапии. По всей видимости, в будущем следует ожидать изменения парадигмы терапии — перехода от стандартной схемы лечения к индивидуально подобранной терапии.
.
Хеликобактер пилори: лечиться или нет? 👩🔬
Гастроэнтерологи всего мира уже сошлись во мнении, что бороться с хеликобактер с тем же размахом, как эпидемиологи в своё время боролись с оспой, неразумно. Чтобы полностью сжить со света эту бактерию, антибиотики придётся прописывать каждому второму.
В итоге, как полагает медицинское сообщество, мы получим множество случаев заболевания псевдомембранозным колитом — острым воспалением толстой кишки из-за приёма антибиотиков, а зловредную хеликобактер не изведём. Ведь у всех бактерий есть свойство мутировать, борясь за выживание.
В каких случаях нужно бороться с бактерией хеликобактер?
Споры от том, «лечить или не лечить», «выявлять или не выявлять», кипят так долго, что в итоге появился так называемый Маастрихтский консенсус. Это рекомендации врачей, выработанные на консилиуме по вопросам борьбы с бактерией.
Первая встреча медиков состоялась в городе Маастрихт, отсюда название свода рекомендаций на основе лабораторных исследований, которые регулярно обновляются. На сегодняшний день издано четыре консенсуса.
На сегодняшний день издано четыре консенсуса.
Выводы медиков, сделанные в свете последних научных знаний о хеликобактер пилори:
- Лечение требуется при язве двенадцатиперстной кишки или желудка.
- Антибактериальная терапия назначается ближайшим родственникам пациентов с раком желудка.
- Эрадикация или полное уничтожение рекомендована при атрофическом гастрите. Именно он считается предраковым заболеванием, а отнюдь не язва желудка.
- Нужно лечение, если выявлена железодефицитная анемия. Впрочем, сначала врачам потребуется выяснить: пациент теряет железо или оно не всасывается из-за бактерии.
Всё, что перечислено выше, относится к случаям, когда бактерия уже выявлена. Однако перед медиками стоит и ещё один вопрос: нужно ли искать хеликобактер у всех людей подряд? Ответ, который чаще всего дают гастроэнтерологи: скорее нет, чем да. Список примерных кандидатов на анализ у специалистов уже есть.
Когда следует искать бактерию хеликобактер
- От болей в желудке не помогают ингибиторы протонной помпы — препараты, снижающие агрессивность желудочного сока.

- Наряду с утомляемостью появляется железодефицит — первый признак рака желудка.
- Пациент входит в группу риска: родственники болели раком желудка.
- Во время исследования выявлены дисплазия желудка, кишечная метаплазия или атрофический гастрит.
В рамках диспансеризации, даже если нет жалоб на боли в верхней части живота, можно раз в 7 лет делать гастроскопию и биопсию с целью выявления бактерии.
Схема эрадикации хеликобактер пилори
- 1–2 недели пациент получает комплексную медикаментозную терапию: ингибиторы протонной помпы, препараты висмута, антибиотики. Врач должен назначить и препараты, которые восполнят дефицит полезных микроорганизмов в желудке и кишечнике после приёма антибиотиков. Популярные средства: «Де-Нол», амоксициллин, «Флемоксин»; кларитромицин; азитромицин; тетрациклин; левофлоксацин.
- Больной повторно сдаёт анализы. Если бактерия осталась, через 5–6 недель врач снова назначает курс лечения, но уже с другими антибиотиками.

- Если после второго этапа лечения тест на хеликобактер снова окажется положительным, методика лечения выбирается в индивидуальном порядке.
Какие продукты следует исключить из рациона, если выявлена бактерия хеликобактер
- макароны;
- картофель;
- сладости;
- выпечка.
Бактерия хеликобактер пилори: средства, препараты и лекарства
На сегодняшний день существует ряд препаратов висмута трикалия дицитрата, которые показаны при хроническом гастрите, вызванном как бактерией хеликобактер пилори, так и другими причинами.
Подробнее о препаратах…
Лучшая профилактика гастрита — формирование полезных пищевых привычек, а также устранение вредного влияния на здоровье человека факторов среды его обитания, в том числе отказ от алкоголя и курения.
Язва желудка. Можно ли предотвратить развитие…
Немногие знают, что проблемы с желудком возникают не только из-за бактерии Helicobacter pylori, но также из-за неправильного питания, стресса и вредных привычек.

Подробнее…
Эскейп® — противоязвенное средство с бактерицидной активностью в отношении Helicobacter pylori, которое также обладает противовоспалительным и вяжущим действием.Как работает Эскейп®?
Причины развития язвы желудка и двенадцатиперстной кишки долгое время оставались для ученых загадкой. Но в 1979 году был обнаружен основной подозреваемый — бактерия хеликобактер пилори, живущая в желудочно-кишечном тракте. Она может существовать там на протяжении долгого времени, не причиняя вреда здоровью, но при благоприятных — для бактерии — обстоятельствах она начинает активно размножаться и повреждать слизистые оболочки.
Бактерия хеликобактер пилори — опасный враг ЖКТ
Широко распространенный и опасный микроорганизм — бактерия хеликобактер пилори (Helicobacter pylori), которая в большинстве случаев становится причиной язвы желудка и двенадцатиперстной кишки. Ей не страшна соляная кислота, содержащаяся в желудочном соке. Бактерия может годами жить в этой среде и разрушать слизистые оболочки, провоцируя развитие гастрита, гастродуоденита, язвенной болезни желудка и двенадцатиперстной кишки. При запущенной язве не исключено и развитие онкологии.
При запущенной язве не исключено и развитие онкологии.
Заражение хеликобактер пилори обычно происходит при контакте, чаще всего, через слюну. Однако получить инфекцию можно также с загрязненной едой или водой. Заражение данной бактерией воздушно-капельным путем невозможно. Поскольку хеликобактер пилори передается преимущественно контактно-бытовым путем, врачи называют ее «семейным» микробом: если у одного из домочадцев обнаружена эта бактерия, то она, скорее всего, есть и у остальных — вероятность этого составляет 95%.
По некоторым данным, число инфицированных достигает 60%, однако далеко не в каждом случае антибактериальная терапия действительно необходима. Чаще всего концентрация бактерии мала и не может нанести вреда здоровью. Наша иммунная система держит количество бактерий под контролем, однако иногда защита ослабевает — к этому могут привести физическое и нервное перенапряжение, инфекционные болезни, вредные привычки и неправильный образ жизни. Тогда хеликобактер пилори активизируется и начинает интенсивно размножаться. Это случается примерно в 15% всех случаев заражения хеликобактер пилори. Ослабить защиту может и нездоровое питание — кислая или острая еда, маринады и копчености, которые раздражают желудочную оболочку, открывая доступ бактериям. К такому же исходу может привести и нарушение режима питания — вопреки рекомендациям врачей, советующих есть часто и понемногу, большинство горожан питается, в лучшем случае, дважды в день или перебивается фаст-фудом: выпечкой, снеками и разной другой сухомяткой.
Это случается примерно в 15% всех случаев заражения хеликобактер пилори. Ослабить защиту может и нездоровое питание — кислая или острая еда, маринады и копчености, которые раздражают желудочную оболочку, открывая доступ бактериям. К такому же исходу может привести и нарушение режима питания — вопреки рекомендациям врачей, советующих есть часто и понемногу, большинство горожан питается, в лучшем случае, дважды в день или перебивается фаст-фудом: выпечкой, снеками и разной другой сухомяткой.
Как правило, на начальной стадии развивается гастрит, затем — язва, а без должного лечения нужно быть готовым к крайне тяжелым последствиям — прободению язвы, кровотечениям и возникновению онкологической патологии. Кроме того, в таком случае определенные структурные изменения возможны не только в ЖКТ, но и в печени и поджелудочной железе.
Интересный факт
В 1970-х считалось, что гастрит и язву желудка вызывают стрессы и несбалансированный рацион. Один из первооткрывателей хеликобактер пилори, австралийский ученый Барри Маршалл, был уверен, что именно эта бактерия, а вовсе не чипсы с газировкой, провоцируют патологии. Чтобы доказать свою правоту, он, будучи совершенно здоровым, выпил концентрат культуры хеликобактер пилори. Уже через несколько дней у него возникли признаки гастрита. Страдания были не напрасны — за научную работу о Helicobacter pylori Маршалл и его коллеги получили в 2005 году Нобелевскую премию.
Чтобы доказать свою правоту, он, будучи совершенно здоровым, выпил концентрат культуры хеликобактер пилори. Уже через несколько дней у него возникли признаки гастрита. Страдания были не напрасны — за научную работу о Helicobacter pylori Маршалл и его коллеги получили в 2005 году Нобелевскую премию.
При гастрите, гастродуодените и язвенной болезни врач обязательно направит вас на анализы. Цель исследований — найти виновника, то есть бактерию хеликобактер пилори, а также оценить ущерб, причиненный инфекцией. Для этого делают общий и биохимический анализ крови, анализ желудочного сока, биопсию, а также высокоточный ПЦР-анализ, который позволяет найти ДНК хеликобактер пилори даже в том случае, если ее концентрация невелика.
Лекарства от инфекций, вызванных бактерией хеликобактер
За последние 30 лет было разработано несколько эффективных методик уничтожения хеликобактер пилори. В 2005 году в Нидерландах состоялся всемирный консенсус гастроэнтерологов, на котором были разработаны и утверждены протоколы лечения болезней, спровоцированных Helicobacter pylori.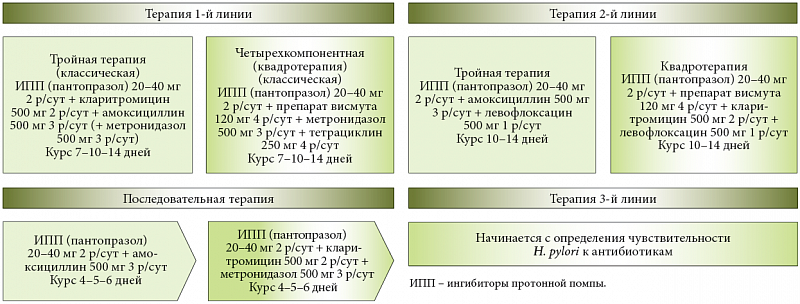 Эти схемы дают положительный эффект в 80% случаев, а частота возникновения побочных эффектов не превышает 15%.
Эти схемы дают положительный эффект в 80% случаев, а частота возникновения побочных эффектов не превышает 15%.
Обычно лечение занимает 14 дней и основывается на лекарственных средствах. Однако чтобы терапия была эффективной, необходимо также изменить образ жизни и придерживаться определенной диеты.
На заметку
Многие проблемы с кожей — акне, атопический дерматит, псориаз — могут быть связаны с деятельностью Helicobacter pylori. Абсолютно точных данных у ученых пока нет, однако уже сейчас очевидно, что эти патологии у инфицированных хеликобактер встречаются чаще.
Как уничтожить бактерию хеликобактер пилори? Лечение состоит из трех этапов. Первая линия препаратов для борьбы с этой бактерией зачастую приносит ожидаемый эффект, но если она оказывается недостаточно эффективной, врачи назначают вторую линию препаратов. Если же и вторая линия не справилась с бактерией, то используются средства третьей линии.
Препараты эрадикации первой линииЭту схему лечения называют трехкомпонентной, поскольку в ней используется сочетание трех лекарств. Она состоит из антибиотиков кларитромицина и амоксициллина, убивающих бактерии, и ингибиторов протонной помпы (действующее вещество омепразол и т.д.) — препаратов, регулирующих кислотность. Благодаря применению ингибиторов протонной помпы пациент избавляется от многих проявлений гастрита и язвенной болезни, кроме того, он может придерживаться менее строгой диеты во время лечения — хотя, конечно, питание все равно должно быть здоровым и сбалансированным. В некоторых случаях препараты на основе амоксициллина меняют на другое антибактериальное средство — метронидазол или нифурател.
Она состоит из антибиотиков кларитромицина и амоксициллина, убивающих бактерии, и ингибиторов протонной помпы (действующее вещество омепразол и т.д.) — препаратов, регулирующих кислотность. Благодаря применению ингибиторов протонной помпы пациент избавляется от многих проявлений гастрита и язвенной болезни, кроме того, он может придерживаться менее строгой диеты во время лечения — хотя, конечно, питание все равно должно быть здоровым и сбалансированным. В некоторых случаях препараты на основе амоксициллина меняют на другое антибактериальное средство — метронидазол или нифурател.
Иногда врач может добавить и четвертый компонент — препараты висмута, оказывающие гастропротекторное, противовоспалительное и вяжущее воздействие, однако обычно такие средства назначают на втором этапе. Тем не менее данные препараты оказывают положительное влияние на течение болезни: они образуют на внутренних стенках желудка своеобразную пленку, благодаря чему притупляется болевой синдром и снимается воспалительный процесс.
Для пациентов пожилого возраста используется более мягкая схема, которая включает в себя только один антибиотик (амоксициллин), препараты висмута и ингибиторы протонной помпы.
Стандартная продолжительность первого этапа — одна неделя. При недостаточной эффективности курс может быть продлен до 2 недель, но не более. Примерно для 90–95% пациентов такая терапия оказывается действенной и второй этап не требуется вообще. Однако если к окончанию первого этапа не все бактерии погибли, схема лечения требует преобразования.
Препараты эрадикации второй линииСхему лечения второго этапа называют четырехкомпонентной. Она включает в себя один ингибитор протонной помпы, препарат висмута и два антибиотика, взаимно усиливающие действие друг друга. Как правило, используются средства с действующими веществами тетрациклин и метронидазол, если они не применялись на первом этапе. Обычно выбирают такие антибиотики, которые еще не использовались в лечении, поскольку если бактерия хеликобактер пилори пережила первое воздействие определенных антибактериальных средств, то очевидно, что данный штамм к ним нечувствителен.
Второй вариант этой терапии состоит из препаратов на основе амоксициллина, антибиотика из группы нитрофуранов, ингибитора протонной помпы и препарата висмута. На этом этапе их очень часто включают в схему лечения.
Средства с трикалия дицитратом висмута оказывают бактерицидное действие, стимулируют цитопротекторные механизмы, повышают устойчивость слизистой оболочки к вредным воздействиям. Препараты восстанавливают защитные функции желудка и могут предотвратить рецидивы болезни.
Чтобы не снижать эффективность действующего вещества, рекомендуется во время приема средств на основе висмута отказаться от употребления в пищу фруктов, соков и молока.
Продолжительность терапии составляет от 10 до 14 дней.
Препараты эрадикации третьей линииВ очень редких случаях положительного эффекта не удается добиться и после применения препаратов второй линии. Тогда проводятся тесты, которые определяют чувствительность бактерий к различным типам антибиотиков, и в схему включаются самые эффективные антибактериальные препараты. В целом же этот этап мало отличается от второго — назначаются ингибиторы протонной помпы, препараты висмута и два антибиотика, показавшие во время лабораторных исследований наибольшую эффективность.
В целом же этот этап мало отличается от второго — назначаются ингибиторы протонной помпы, препараты висмута и два антибиотика, показавшие во время лабораторных исследований наибольшую эффективность.
Лекарства на основе висмута на этом этапе также играют важную роль, поскольку они обеспечивают комплексное лечение. Препараты с действующим веществом трикалия дицитрат висмута не только эффективно снимают неприятные симптомы болезни (изжогу, боль, вздутие), но и оказывают местное бактерицидное действие в отношении Helicobacter pylori, помогают активизировать регенерацию поврежденных клеток стенок желудка. Поэтому роль таких средств в эффективном лечении и уничтожении бактерии Helicobacter pylori трудно переоценить.
Следует отметить, что не всегда бактерия хеликобактер пилори является причиной язвы, к ней может привести и постоянное раздражение слизистой оболочки желудка некоторыми медикаментами (например, средствами с действующими веществами ацетилсалициловая кислота и ибупрофен, которые часто принимаются без рекомендации врача)..gif) Травмы желудка и некоторые хронические болезни (диабет, гепатит, туберкулез) также могут привести к подобным изменениям. Но в 75% случаев язва и гастрит — «дело рук» хеликобактер пилори. Чтобы обезопасить себя от заражения, нужно строго следовать правилам личной гигиены — не употреблять в пищу немытые фрукты и овощи, ни с кем не делить посуду, мыть руки перед едой, не доедать ничего из чужих тарелок. Впрочем, заражение все равно вероятно — для передачи инфекции достаточно одного поцелуя.
Травмы желудка и некоторые хронические болезни (диабет, гепатит, туберкулез) также могут привести к подобным изменениям. Но в 75% случаев язва и гастрит — «дело рук» хеликобактер пилори. Чтобы обезопасить себя от заражения, нужно строго следовать правилам личной гигиены — не употреблять в пищу немытые фрукты и овощи, ни с кем не делить посуду, мыть руки перед едой, не доедать ничего из чужих тарелок. Впрочем, заражение все равно вероятно — для передачи инфекции достаточно одного поцелуя.
Не стоит давать вредоносной бактерии шанс. Если вы не уверены, инфицированы ли вы, пройдите лабораторное исследование, например, ПЦР-тест на хеликобактер пилори. Даже если бактерия обнаружится, это еще не значит, что вам необходимо лечение. Хеликобактер не всегда является причиной гастрита, но присутствует в организме у каждого. Как было сказано выше, здоровая иммунная система может контролировать концентрацию этой бактерии. Для профилактики развития заболеваний, связанных с хеликобактер, нужно придерживаться здоровой диеты, исключающей все, что может раздражать слизистую желудка — маринады, специи и острые приправы, жареное, алкоголь, кофе и газированные напитки, кислые овощи и фрукты. Но если все-таки диагностирован гастрит, вне зависимости от причины его возникновения обязательно следует защищать желудок, и лучше всех с этим справляются препараты висмута, оказывающие гастропротекторное, противовоспалительное и вяжущее воздействие.
Но если все-таки диагностирован гастрит, вне зависимости от причины его возникновения обязательно следует защищать желудок, и лучше всех с этим справляются препараты висмута, оказывающие гастропротекторное, противовоспалительное и вяжущее воздействие.
Есть ли у Вас инфекция Хеликобактер пилори? — Гастроэнтерология — Отделения
Есть ли у Вас инфекция Хеликобактер пилори?
Хеликобактер пилори – бактерия, обитающая на слизистой оболочке желудка и двенадцатиперстной кишки и вызывающая ее воспаление и повреждение. Она является основной причиной развития хронического гастрита, язвенной болезни желудка и двенадцатиперстной кишки, а также рака желудка.
Хеликобактер пилори является одной из наиболее частых хронических инфекций человека. В России ей инфицировано до 80% взрослого населения.
Заражение обычно происходит в детском возрасте. При этом иммунитет человека не справляется с уничтожением Хеликобактер пилори. Без лечения эта бактерия практически всегда остается в желудке на протяжении всей жизни.
Вопреки частому заблуждению Хеликобактер пилори не является безвредным микроорганизмом. При его наличии всегда развивается хронический гастрит, на фоне которого в дальнейшем могут возникать язвы и рак.
Какие симптомы могут быть обусловлены хроническим воспалением слизистой желудка, ассоциированной с Хеликобактер пилори?
- Боль и дискомфорт в области желудка
- Тяжесть в области желудка после еды
- Тошнота, рвота, снижение аппетита
- Рвота с кровью и темный стул (следствия язвенного кровотечения)
В каких ситуациях важно выявить Хеликобактер пилори?
- При хроническом поверхностном и атрофическом гастрите, в том числе эрозивном
- При обострении язвенной болезни желудка и двенадцатиперстной кишки
- Если язвенная болезнь выявлялась в прошлом
- В случае длительного приема препаратов, снижающих кислотность желудочного сока (ингибиторы протонной помпы)
- При регулярном приеме болеутоляющих и противовоспалительных препаратов (нестероидных противовоспалительных препаратов)
- Если близкий родственник болел раком желудка
- Если имеются некоторые заболевания крови (идиопатическая тромбоцитопеническая пурпура, железодефицитная анемия с неясной причиной)
Как можно выявить Хеликобактер пилори?
Имеется несколько методов диагностики Хеликобактер пилори. Наличие бактерии можно определить при проведении гастроскопии, а также без нее с помощью специального дыхательного теста, анализов крови и кала.
Наличие бактерии можно определить при проведении гастроскопии, а также без нее с помощью специального дыхательного теста, анализов крови и кала.
Выбрать оптимальный метод может врач.
Как можно вылечить инфекцию Хеликобактер пилори?
Для лечения Хеликобактер пилори назначаются специальные схемы из 3-5 препаратов, содержащие в своем составе антибиотики. Длительность терапии обычно составляет 10-14 дней. Назначить лечение может только врач. При подборе схемы важно учитывать ранее проводившееся лечение Хеликобактер пилори, наличие аллергии, предшествующий прием антибиотиков, применение других лекарств.
Что может дать уничтожение инфекции Хеликобактер пилори?
- Вылечить хронический гастрит
- Остановить прогрессирование атрофии слизистой оболочки желудка
- Прекратить повторяющиеся обострения язвенной болезни желудка и двенадцатиперстной кишки
- Снизить риск развития рака желудка
- Уменьшить вероятность повреждения слизистой оболочки при приеме болеутоляющих и противовоспалительных препаратов (нестероидных противовоспалительных препаратов)
- Улучшить показатели крови при тромбоцитопенической пурпуре и железодефицитной анемии неясной этиологии
Как проконтролировать эффективность лечения инфекции Хеликобактер пилори?
Контроль эффективности лечения необходимо провести через месяц после окончания терапии. Выбрать оптимальный метод поможет врач.
Выбрать оптимальный метод поможет врач.
Надо ли Вам провериться на хеликобактер?
Чек-лист для пациентов
Мы собрали признаки, которые указывают на вероятность заражения инфекцией.
Если Вы дали положительный ответ на 3-4 признака — рекомендуем пройти обследование и обратиться к врачу.
Это про Вас?
☑ Боли в верхних отделах живота после еды
☑ Чувство раннего насыщения, тяжесть после еды
☑ Тощаковые боли в верхних отделах живота (ночью или при больших перерывах между едой)
☑ Отсутствие аппетита по утрам
☑ Изжога, отрыжка
☑ Частое посещение мест общественного питания
☑ Наличие родственников с гастритом или язвенной болезнью
Прием N-ацетилцистеина с антибиотиками для лечения инфекции Helicobacter pylori
Вопрос обзора
Безопасно ли добавление N-ацетилцистеина к антибиотикам и улучшает ли показатели излечения инфекции Helicobacter pylori?
Актуальность
Helicobacter pylori (H pylori) – это бактерия, которая живет в желудке и может вызывать ряд заболеваний, таких как рак желудка, язвенная болезнь и другие. Колонизация происходит примерно у половины населения мира и чаще встречается в странах с плохими санитарными условиями. Люди заражаются при употреблении загрязненной воды.
Колонизация происходит примерно у половины населения мира и чаще встречается в странах с плохими санитарными условиями. Люди заражаются при употреблении загрязненной воды.
Инфекция лечится с помощью антибиотиков и лекарств, которые снижают выработку кислоты в желудке. Однако устойчивость к антибиотикам во всем мире растет, что снижает показатели излечения даже при использовании лекарств. Для улучшения показателей излечения проходят испытания новые лекарства. Одно из таких лекарств – N-ацетилцистеин (NAC). NAC – это препарат, который помогает растворить слизь при заболеваниях дыхательных путей. NAC можно принимать перорально или вводить внутривенно. NAC может нарушить некоторые механизмы выживания H pylori и улучшить показатели излечения.
Характеристика исследований
Мы включили 8 исследований (рандомизированные контролируемые испытания (РКИ)) с участием 559 человек в возрасте от 17 до 76 лет. Доказательства актуальны на апрель 2018 года. Во всех исследованиях участвовали амбулаторные пациенты из центров эндоскопии (центров, которые специализируются на обследовании с использованием гибкой трубки с камерой, вводимой в желудок) в нескольких странах. Испытуемые комбинации антибиотиков во включенных исследованиях сильно отличались, как и дозы NAC (от 600 до 1 800 мг в день). NAC сравнивали с плацебо (фиктивной таблеткой) или отсутствием лечения.
Испытуемые комбинации антибиотиков во включенных исследованиях сильно отличались, как и дозы NAC (от 600 до 1 800 мг в день). NAC сравнивали с плацебо (фиктивной таблеткой) или отсутствием лечения.
Основные результаты
Мы не уверены, улучшает ли добавление NAC к антибиотикам показатели излечения инфекции H. pylori по сравнению с добавлением плацебо или отсутствием NAC. Любой возможный полезный эффект NAC следует рассматривать с осторожностью, поскольку включенные исследования были очень разными и имели низкую степень достоверности и недостатки, которые могли повлиять на их результаты и, следовательно, результаты обзора.
Мы не уверены, связан ли прием NAC с более высоким риском желудочно-кишечных или аллергических неблагоприятных событий в сравнении с плацебо или отсутствием NAC. О токсических неблагоприятных событиях во включенных исследованиях не сообщали.
Необходимы крупные рандомизированные клинические исследования с надлежащими дизайном, сбором данных по эффективности и безопасности и сообщением результатов, особенно в отношении рекомендуемых комбинаций антибиотиков.
Качество доказательств
Общая уверенность в доказательствах относительно показателей эрадикации варьировала от очень низкой до низкой. В пяти исследованиях были представлены сведения о неблагоприятных событиях (побочных эффектах), но уверенность в доказательствах была очень низкой. Включенные исследования были плохо проведены, и это уменьшило нашу уверенность в результатах.
FDA одобрило новый препарат для борьбы с H. Pylori » Медвестник
Резистентность H. Pylori к антибиотикам достигла тревожного уровня по всему миру, в частности, резистентность к кларитромицину увеличилась более чем в два раза с 2009 по 2013 год, что в значительной степени повлияло на эффективность лечения. Применение рифабутина в антихеликобактерной терапии давно рассматривалось, однако до настоящего времени так и не было зарегистрировано соответствующего препарата.
Talicia представляет собой капсулы с модифицированным высвобождением, содержащие комбинацию двух антибиотиков и ингибитора протонной помпы (ИПП): амоксициллина 250 мг, рифабутина 12,5 мг и омепразола 10 мг.
В клинических исследованиях третьей фазы приняли участие взрослые добровольцы с хеликобактерной инфекцией, которые жаловались на боль и/или дискомфорт в эпигастральной области. Четыре из 305 пациентов (1%) прекратили лечение по причине возникновения нежелательных реакций (НР). Наиболее частыми НР были тошнота, рвота, заложенность носа и назофарингит.
«Talicia предлагает новый вариант лечения хеликобактерной инфекции с отличным профилем безопасности и эффективности. Клинические исследования показали высокую эффективность препарата и нулевую резистентность к рифабутину, тогда как резистентность к кларитромицину, который в настоящее время является стандартом лечения, составила 17%, что согласуется с имеющейся информацией о неэффективности терапии с использованием кларитромицина в 25-40% случаев», – говорит профессор микробиологии и вирусологии в Медицинском колледже Бейлора, доктор Дэвид Грэхем (David Graham), руководивший третьей фазой клинических исследований.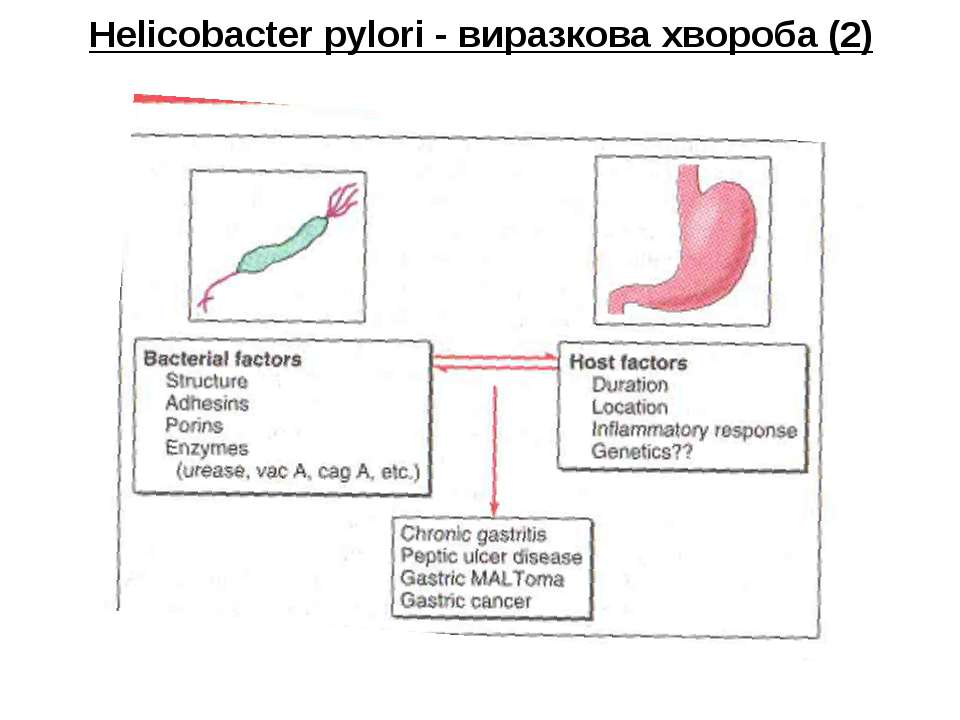
«За последнее десятилетие лечение хеликобактерной инфекции усложнилось вследствие растущей резистентности и недостатка альтернативных вариантов терапии», – отмечает глава отделения гастроэнтерологии в Научном центре здоровья Университета Теннесси (UTHSC) доктор Колин Хоуден (Colin Howden). По его мнению, со временем Talicia может стать рекомендованным препаратом первого ряда для эрадикации H. Pylori.
В данный момент рифабутин используется в терапии туберкулеза и микобактериоза в комбинации с другими препаратами и, следовательно, он должен применяться с осторожностью и строго по показаниям во избежание развития резистентности у микобактерий.
Препарат выйдет на рынок США в первом квартале 2020 года и будет представлен в течение 8 лет со статусом Qualified Infectious Disease Product (QIDP), который присваивается антибактериальным и противогрибковым препаратам для лечения серьезных или угрожающих жизни инфекций. Патентная защита будет действительна до 2034 года.
ПИЛОБАКТ НЕО: новые возможности в лечении язвенной болезни
|
Роль H. pylori в этиологии язвообразования
В настоящее время доказана ведущая роль инфекции H. pylori в развитии антрального гастрита, пептических язв желудка и двенадцатиперстной кишки, некардиальной аденокарциномы и лимфомы желудка [2].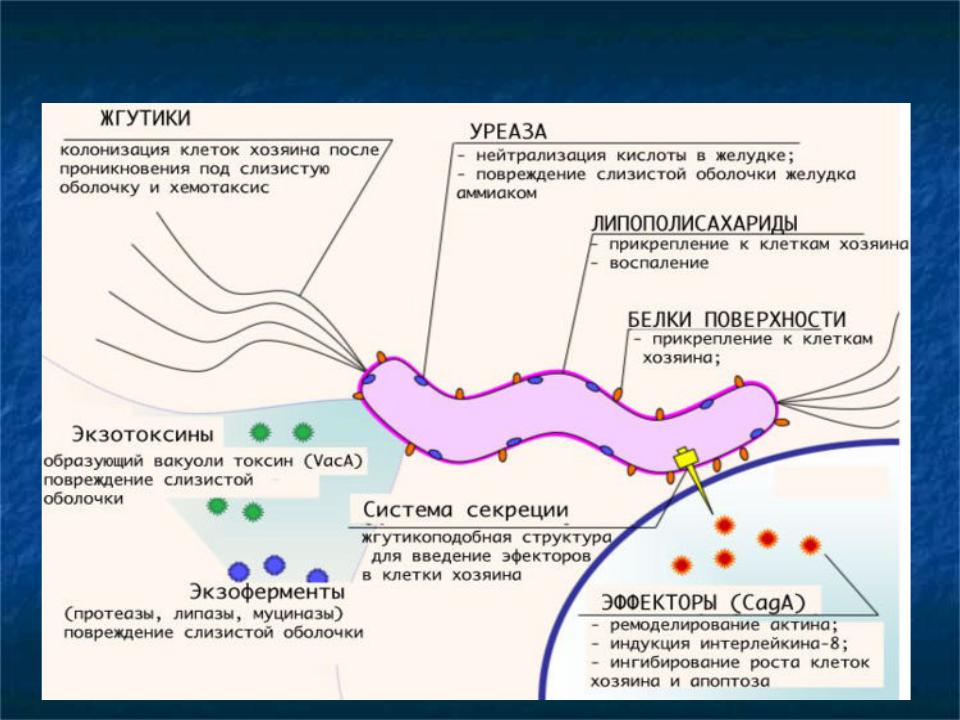 H. pylori — грамотрицательная микроаэрофильная бактерия. Спиралевидная форма и наличие жгутиков позволяют микробу хорошо передвигаться в вязкой желудочной слизи, которая покрывает слизистую оболочку желудка. H. pylori выделяет ферменты адаптации: уреазу и каталазу. Уреаза вызывает превращение мочевины в углекислый газ (СО2) и аммиак (NO2), что локально повышает рН и защищает H. pylori от бактерицидного действия соляной кислоты, то есть бактерия находится как бы «в облаке» щелочных продуктов, защищающих микроорганизм от кислой среды. Аммиак нарушает кислотопродукцию в париетальных клетках и инициирует апоптоз. Выделение каталазы и супероксиддисмутазы позволяет H. pylori подавлять клеточный иммунный ответ макроорганизма, то есть защищаться от лейкоцитов, препятствуя контакту с ними и подавляя фагоцитоз. Вследствие муколитического действия H. pylori, выработки токсических ферментов фосфолипаз А и С, а также протеинкиназы и глюкофосфатазы, повреждается мембрана поверхностного эпителия, в связи с чем воздействие кислотно-пептического фактора усиливается в местах персистенции бактерий.
H. pylori — грамотрицательная микроаэрофильная бактерия. Спиралевидная форма и наличие жгутиков позволяют микробу хорошо передвигаться в вязкой желудочной слизи, которая покрывает слизистую оболочку желудка. H. pylori выделяет ферменты адаптации: уреазу и каталазу. Уреаза вызывает превращение мочевины в углекислый газ (СО2) и аммиак (NO2), что локально повышает рН и защищает H. pylori от бактерицидного действия соляной кислоты, то есть бактерия находится как бы «в облаке» щелочных продуктов, защищающих микроорганизм от кислой среды. Аммиак нарушает кислотопродукцию в париетальных клетках и инициирует апоптоз. Выделение каталазы и супероксиддисмутазы позволяет H. pylori подавлять клеточный иммунный ответ макроорганизма, то есть защищаться от лейкоцитов, препятствуя контакту с ними и подавляя фагоцитоз. Вследствие муколитического действия H. pylori, выработки токсических ферментов фосфолипаз А и С, а также протеинкиназы и глюкофосфатазы, повреждается мембрана поверхностного эпителия, в связи с чем воздействие кислотно-пептического фактора усиливается в местах персистенции бактерий. Указанная концепция получила название «теория протекающей крыши». Определенные штаммы бактерий H. pylori продуцируют цитотоксинассоциированный белок, а также вакуолизирующий токсин, которые вызывают более интенсивное воспаление слизистой оболочки желудка. Таким образом, H. pylori хорошо защищен от неблагоприятной среды обитания и способен выделять патогенные для желудка вещества [3, 4].
Указанная концепция получила название «теория протекающей крыши». Определенные штаммы бактерий H. pylori продуцируют цитотоксинассоциированный белок, а также вакуолизирующий токсин, которые вызывают более интенсивное воспаление слизистой оболочки желудка. Таким образом, H. pylori хорошо защищен от неблагоприятной среды обитания и способен выделять патогенные для желудка вещества [3, 4].
При прогрессировании хронического хеликобактерного гастрита и распространении воспаления на тело желудка вскоре происходит атрофия слизистой оболочки, на фоне которой развиваются метаплазия и дисплазия эпителия. Тяжелая дисплазия и неполная метаплазия (толстокишечная, незрелая) являются предраковым состоянием [3]. Международным агентством по изучению рака в 1994 г. инфекция H. pylori отнесена к канцерогенам первого класса (International Agency for Research on Cancer) [5]. Несмотря на то, что за последние 50 лет распространенность рака желудка и смертность вследствие этой патологии во многих странах снизилась [6], это заболевание остается второй причиной смертности в связи с онкологическими заболеваниями в мире, составляя примерно 10% от случаев вновь диагностированного рака. Высокий уровень смертности вследствие рака желудка зафиксирован в Японии, Китае, Центральной и Южной Америке, Восточной Европе [7].
Высокий уровень смертности вследствие рака желудка зафиксирован в Японии, Китае, Центральной и Южной Америке, Восточной Европе [7].
Эрадикация H. pylori слизистой оболочки инфицированных лиц обусловливает следующие наиболее существенные эффекты [3]:
1) исчезновение воспалительного инфильтрата в слизистой оболочке желудка;
2) снижение содержания гастрина крови и максимальной кислотной продукции;
3) восстановление гидрофобных свойств слизистой оболочки желудка;
4) разрыв «порочная цепочки»: инфицирование H. pylori — воспаление — атрофия — метаплазия — дисплазия — рак.
Таким образом, инфекция H. pylori в настоящее время является важнейшим фактором язвообразования, а также относится к одной из причин возникновения рака желудка. Следует подчеркнуть, что проведение антибактериальной терапии H. pylori является трудной задачей, поскольку эти микроорганизмы приспособлены к обитанию под слоем слизи, куда доступ антибактериальных препаратов ограничен. Еще один неблагоприятный фактор — это резистентность и быстрое привыкание бактерий к антибактериальным препаратам, особенно нитроимидазолам. Причиной резистентности к имидазолам может стать предшествующее лечение этими препаратами по поводу генитальных и кишечных инфекций. Резистентность к антибиотикам возникает значительно реже [4].
Как лечить и чем лечить
Согласно положениям Маастрихтского консенсуса-2, 2000 [8], антихеликобактерная терапия настоятельно рекомендована пациентам с язвенной болезнью, в том числе при наличии осложнений, MALT-лимфомой желудка, атрофическим гастритом, после резекции желудка по поводу рака, родственникам первой степени родства пациента с раком желудка. Антихеликобактерную терапию желательно проводить инфицированным пациентам с функциональной диспепсией. В документе указано, что эрадикация H. pylori перед назначением нестероидных противовоспалительных препаратов снижает вероятность развития язв. Подчеркивается также, что проведение эрадикационной терапии в большинстве случаев не ведет к развитию гастроэзофагеальной рефлюксной болезни и не усугубляет проявления уже развившейся болезни.
Терапия первой линии должна включать ингибитор протонного насоса (омепразол в дозе 20 мг), кларитромицин 500 мг и амоксициллин 1000 мг два раза в день или метронидазол 500 мг (в течение 7 дней). Требования, предъявляемые к успешной эрадикационной терапии, следующие: лечение должно хорошо переноситься пациентами, его схема должна быть несложной, а уровень эрадикации составлять свыше 80% [9]. В результате успешной эрадикации H. pylori:
1)?происходит заживление язвенного дефекта [10]; в Маастрихтском консенсусе-2, 2000 подчеркивается, что при неосложненной язвенной болезни двенадцатиперстной кишки нет необходимости продолжать антисекреторную терапию после проведения курса эрадикации H. pylori;
2)?уменьшается число рецидивов язвенной болезни. В обзоре (проанализировано 14 исследований с участием пациентов с язвенной болезнью двенадцатиперстной кишки и 5 — с язвенной болезнью желудка) установлено, что при локализации язвы в двенадцатиперстной кишке частота рецидивов составила 6% в случае эрадикации H. pylori и 67% — в случае сохранения H. pylori. При локализации язвы в желудке рецидивы составили 4 и 59% соответственно (время наблюдения — 6–12 мес) [11];
3)?успешная эрадикация H. pylori снижает риск развития кровотечения как осложнения язвенной болезни [12].
Эффективность терапии. Установлено, что тройная терапия, включающая омепразол 20 мг, кларитромицин 500 мг и амоксициллин 1000 мг два раза в день (7 дней), позволяет достичь более высокого уровня эрадикации и меньшей частоты рецидивов заболевания по сравнению со схемой, в которую включен метронидазол: их сравнительная эффективность составила, соответственно, 90,3% и 65,6% [13]. Частота эрадиции H. pylori с использованием схемы, включающей омепразол, кларитромицин и амоксициллин по 7-дневному протоколу, по данным метаанализа, включившего 32 исследования, составила 83,2% [14]. Почему эффективность различных схем отличается? Зачастую причиной неэффективности терапии является устойчивость микроорганизма к антибактериальным препаратам. Что касается H. pylori, то по данным шведских исследователей первичная устойчивость в культуре H. pylori к метронидазолу и кларитромицину выявлена, соответственно, в 76% и 1% изолятов [15].
Кроме такого распространенного явления, как резистентность штаммов микроорганизма к препаратам, входящим в схему терапии, серьезное отрицательное влияние на результаты эрадикации H. pylori оказывает низкая комплаентность пациентов (степень приверженности больных назначенному лечению). Несоблюдение больным схемы лечения, в том числе пропуски в приеме лекарственных препаратов, прием двух препаратов вместо трех и т.п. являются одними из прогностически неблагоприятных факторов в отношении персистенции H. pylori [16].
Пациенту, которому назначена эрадикационная терапия, приходится покупать несколько упаковок разных препаратов, при этом количество купленных таблеток может превышать необходимое для курса лечения. При приеме лекарственных средств необходимо точно соблюсти назначенную дозировку, для чего может потребоваться принимать по 2, а то и 4 таблетки только лишь одного антибактериального препарата одновременно.
Этим вызвано возникновение концепции сочетания в одном блистере трех компонентов эрадикационной схемы. Указанной концепции полностью соответствует препарат производства компании «Ранбакси Лабораториз Лимитед» ПИЛОБАКТ НЕО, состав которого полностью соответствует предложенному Маастрихтским консенсусом-2, 2000?— комбинированный набор, включающий 7 блистеров. Каждый блистер содержит по две таблетки амоксициллина (1 г), кларитромицина (500 мг) и две капсулы омепразола (20 мг). Омепразол — ингибитор протонного насоса, снижает секрецию соляной кислоты в желудке, угнетая активность Na+/K+-АТФ-азы. Омепразол существенно уменьшает объем желудочного сока и таким образом повышает концентрацию амоксициллина и кларитромицина в слизистой оболочке желудка. Омепразол способствует быстрому уменьшению выраженности клинических проявлений, сокращению сроков рубцевания пептических язв. Кларитромицин — антибактериальный препарат из группы макролидов, активный в отношении многих аэробных и анаэробных микроорганизмов, включая H. pylori, устойчивый в кислой среде желудка. Одновременный прием кларитромицина и омепразола благоприятно влияет на фармакокинетику обоих препаратов. Амоксициллин — антибактериальное средство группы полусинтетических пенициллинов с широким спектром бактерицидного действия. Активен в отношении H. pylori. Ампициллинрезистентных штаммов H. pylori до настоящего времени практически не выявлено. Следует отметить, что прием пищи не влияет на биодоступность кларитромицина и амоксициллина.
Таким образом, ПИЛОБАКТ НЕО представляет собой набор, по подбору препаратов и их дозировке соответствующий схеме эрадикационной терапии первой линии, преимущества которой доказаны рядом исследований. Эта схема хорошо переносится больными, что повышает комплаентность лечения. К тому же препарат доступен по цене. Дополнительное положительное влияние на приверженность пациента лечению оказывает применение ПИЛОБАКТ НЕО: пациент каждый день принимает содержимое 1 блистера, при этом количество таблеток в одной упаковке строго рассчитано на курс лечения, что повышает его экономическую доступность. Для удобства больного три препарата расположены рядом в блистере, а на покровной фольге имеется маркировка «Утро», «Вечер». Таким образом, применение ПИЛОБАКТ НЕО обеспечивает высокую степень эрадикации H. pylori, повышает комплаентность пациентов, способствует заживлению язв, уменьшению количества рецидивов.
ЛИТЕРАТУРА | |
|
Дарья Полякова
Бактериальная инфекция H. pylori: симптомы, диагностика, лечение, профилактика
Helicobacter pylori ( H. pylori ) — это разновидность бактерий. Эти микробы могут проникнуть в ваше тело и жить в пищеварительном тракте. Спустя много лет они могут вызвать язвы, называемые язвами, на слизистой оболочке желудка или в верхней части тонкой кишки. У некоторых людей инфекция может привести к раку желудка.
Заражение H. pylori является обычным явлением. Около двух третей населения мира находится в организме.У большинства людей он не вызывает язвы или каких-либо других симптомов. Если у вас есть проблемы, существуют лекарства, которые могут убить микробы и помочь заживлению ран.
По мере того, как все больше людей в мире получает доступ к чистой воде и санитарии, все меньше людей заражаются бактериями . Имея хорошие привычки в отношении здоровья, вы можете защитить себя и своих детей от H. pylori .
Как H. pylori вызывает болезнь
На протяжении десятилетий врачи считали, что язвы у людей возникают в результате стресса, острой пищи, курения или других привычек образа жизни.Но когда в 1982 году ученые обнаружили H. pylori , они обнаружили, что микробы были причиной большинства язв желудка .
После того, как H. pylori попадает в ваше тело, он атакует слизистую оболочку желудка, которая обычно защищает вас от кислоты, которую ваше тело использует для переваривания пищи. Как только бактерии нанесут достаточно вреда, кислота может проникнуть через слизистую оболочку, что приведет к язвам. Они могут кровоточить, вызывать инфекции или препятствовать прохождению пищи через пищеварительный тракт.
Вы можете получить H. pylori из пищи, воды или посуды. Это чаще встречается в странах или сообществах, где отсутствует чистая вода или хорошая канализация. Вы также можете заразить бактерии при контакте со слюной или другими биологическими жидкостями инфицированных людей.
Многие люди заражаются H. pylori в детстве, но могут заразиться и взрослые. Микробы живут в организме годами до появления симптомов, но у большинства людей язвы никогда не появятся. Врачи не знают, почему только у некоторых людей появляются язвы после инфекции.
Симптомы
Если у вас язва, вы можете почувствовать тупую или жгучую боль в животе. Это может приходить и уходить, но вы, вероятно, почувствуете это больше всего, когда у вас пустой желудок, например, между приемами пищи или посреди ночи. Это может длиться от нескольких минут до нескольких часов. Вы можете почувствовать себя лучше после еды, питья молока или приема антацидов.
К другим признакам язвы относятся:
Язвы могут кровоточить в желудок или кишечник, что может быть опасно для вашего здоровья.Немедленно обратитесь за медицинской помощью, если у вас есть какие-либо из этих симптомов:
Это не часто, но инфекция H. pylori может вызвать рак желудка. Поначалу у болезни мало симптомов, например, изжога. Со временем вы можете заметить:
- Боль или опухоль в животе
- Тошнота
- Отсутствие чувства голода
- Чувство сытости после небольшого количества еды
- Рвота
- Беспричинная потеря веса
Диагноз
Если у вас нет симптомов язвы, ваш врач, вероятно, не будет проверять вас на H.pylori . Но если они у вас есть сейчас или были в прошлом, лучше пройти тестирование. Такие лекарства, как нестероидные противовоспалительные препараты (НПВП), также могут повредить слизистую оболочку желудка, поэтому важно выяснить, что вызывает ваши симптомы, чтобы вы могли получить правильное лечение.
Для начала ваш врач спросит вас о вашей истории болезни, симптомах и лекарствах, которые вы принимаете. Затем вам проведут медицинский осмотр, в том числе надавят на живот, чтобы проверить, нет ли отека, болезненности или боли.Вы также можете иметь:
- Анализы крови и стула, , которые могут помочь найти инфекцию.
- Дыхательный тест на мочевину. Вы выпьете особую жидкость, в которой есть мочевина. Затем вы вдохнете в сумку, которую врач отправит в лабораторию для тестирования. Если у вас H. pylori , бактерии превратят мочевину в вашем организме в углекислый газ, а лабораторные тесты покажут, что в вашем дыхании уровень газа выше нормы.
Для более внимательного изучения ваших язв ваш врач может использовать:
- Эндоскопия верхних отделов желудочно-кишечного тракта. В больнице врач с помощью трубки с маленькой камерой, называемой эндоскопом, будет смотреть вниз по горлу, в желудок и верхнюю часть тонкой кишки. Эту процедуру также можно использовать для сбора образца, который будет исследован на наличие бактерий. Вы можете спать или бодрствовать во время процедуры, но вы получите лекарство, чтобы вам было комфортнее.
- Тесты верхнего GI . В больнице вы выпьете жидкость, содержащую вещество, называемое барием, и ваш врач сделает вам рентгеновский снимок.Жидкость покрывает ваше горло и желудок, выделяя их на изображении.
- Компьютерная томография (КТ). Это мощный рентгеновский снимок, который делает подробные снимки внутренней части вашего тела.
Если у вас H. pylori , ваш врач может также проверить вас на рак желудка. Сюда входят:
- Физический осмотр
- Анализы крови для проверки на анемию, когда в вашем организме недостаточно эритроцитов. Это может произойти, если у вас кровоточащая опухоль.
- Анализ кала на скрытую кровь, который проверяет ваш стул на наличие крови, невидимой невооруженным глазом.
- Эндоскопия.
- Биопсия, когда врач берет небольшой кусочек ткани вашего желудка, чтобы найти признаки рака. Ваш врач может сделать это во время эндоскопии.
- Тесты, которые делают подробные снимки внутренних органов вашего тела, такие как компьютерная томография или магнитно-резонансная томография (МРТ)
Лечение H. pylori
Если у вас есть язвы, вызванные H.pylori , вам понадобится лечение, чтобы убить микробы, вылечить слизистую оболочку желудка и предотвратить повторное появление язв . Обычно для выздоровления требуется 1-2 недели лечения.
Ваш врач, вероятно, посоветует вам принимать несколько разных препаратов. Возможные варианты:
- Антибиотики для уничтожения бактерий в организме, такие как амоксициллин, кларитромицин (биаксин), метронидазол (флагил), тетрациклин (сумицин) или тинидазол (тиндамакс). Скорее всего, вы возьмете как минимум двоих из этой группы.
- Лекарства, которые уменьшают количество кислоты в желудке, блокируя крошечные насосы, которые ее производят. Они включают декслансопразол (Дексилант), эзомепразол (Нексиум), лансопразол (Превацид), омепразол (Прилосек), пантопразол (Протоникс) или рабепразол (Ацифекс).
- Субсалицилат висмута, который также может помочь убить H. pylori вместе с вашими антибиотиками.
- Лекарства, блокирующие химический гистамин, который заставляет желудок вырабатывать больше кислоты. Это циметидин (Тагамет), фамотидин (Флюксид, Пепцид), низатидин (Аксид) или ранитидин (Зантак).
Ваше лечение может означать, что вы будете принимать 14 или более таблеток в день в течение нескольких недель, что кажется большим количеством лекарства. Но действительно важно принимать все, что прописывает врач, и следовать его инструкциям. Если вы не принимаете антибиотики правильно, бактерии в вашем организме могут стать к ним устойчивыми, что затруднит лечение инфекций. Если ваши лекарства беспокоят вас, поговорите со своим врачом о вариантах лечения и о том, как вы можете справиться с побочными эффектами.
Примерно через 1-2 недели после окончания лечения врач может снова проверить ваше дыхание или стул, чтобы убедиться, что инфекция исчезла.
Профилактика
Вы можете защитить себя от заражения H. pylori , выполнив те же действия, что и другие микробы:
- Мойте руки после посещения туалета и перед приготовлением или приемом пищи. Учите детей делать то же самое.
- Избегайте нечистой пищи и воды.
- Не ешьте плохо приготовленные продукты.
- Избегайте еды, которую подают люди, которые не мыли руки.
Хотя стресс и острая пища не вызывают язв, они могут помешать их быстрому заживлению или усугубить вашу боль.Поговорите со своим врачом о способах борьбы со стрессом, улучшения диеты и, если вы курите, о том, как вам помочь бросить курить.
Чего мне ожидать после инфицирования H. pylori?
Большинство язв, вызванных H. pylori , заживают через несколько недель лечения. Если вы принимали один, вам следует избегать приема НПВП от боли, поскольку эти препараты могут повредить слизистую оболочку желудка. Если вам нужно обезболивающее, попросите врача порекомендовать его.
Где я могу найти информацию или поддержку?
Вы можете найти информацию о H.pylori и язвы от Американского колледжа гастроэнтерологии. Чтобы получить информацию о раке желудка, а также о группах поддержки в Интернете и на местном уровне, посетите Американское онкологическое общество.
Дыхательный тест на мочевину и результаты для H. Pylori
Дыхательный тест с мочевиной используется для обнаружения Helicobacter pylori (H. pylori), типа бактерий, которые могут инфицировать желудок и являются основной причиной язв в обоих желудках. и двенадцатиперстная кишка (первая часть тонкой кишки).
H.pylori вырабатывает фермент, называемый уреазой, который расщепляет мочевину на аммиак и углекислый газ. Во время теста проглатывается таблетка, содержащая мочевину, и измеряется количество выдыхаемого углекислого газа. Это указывает на присутствие H. pylori в желудке.
Как подготовиться к дыхательному тесту на мочевину?
Чтобы подготовиться к дыхательному тесту на мочевину, следуйте этим инструкциям:
- Сообщите своему врачу, если вы беременны, страдаете заболеванием легких или сердца или любым другим заболеванием, или если у вас аллергия на какие-либо лекарства.
- Не принимайте антибиотики как минимум за 4 недели до исследования.
- Не принимайте ингибиторы протонной помпы (Ацифекс, Нексиум, Превацид, Прилосек, Протоникс) или Пепто-Бисмол как минимум за 2 недели до теста.
- Принимайте только те лекарства, которые одобрены вашим врачом в день процедуры. Принимайте их только в течение четырех часов после процедуры, запивая небольшим глотком воды. Не прекращайте прием каких-либо лекарств, не посоветовавшись предварительно со своим основным врачом или лечащим врачом.
- Ничего не ешьте и не пейте (включая воду) за четыре часа до процедуры.
Что происходит во время теста дыхания мочевиной?
Во время дыхательного теста на мочевину:
- Медицинский работник объяснит процедуру, которая длится от 40 до 60 минут, и ответит на любые ваши вопросы.
- Будут взяты пробы дыхания.
Что происходит после теста дыхания мочевины?
После дыхательного теста с мочевиной:
- Образцы вашего дыхания отправляются в лабораторию, где они исследуются.
- Вы можете вернуться к своей обычной деятельности.
- Вы можете вернуться к своей обычной диете, если вам не назначены другие тесты, требующие диетических ограничений.
Когда я узнаю результаты теста дыхания на мочевину?
Результаты дыхательного теста на мочевину обычно доступны через два дня после его завершения.
Ск-метронидазол для приема внутрь: применение, побочные эффекты, взаимодействия, изображения, предупреждения и дозировка
Могут возникнуть головокружение, головная боль, расстройство желудка, тошнота, рвота, потеря аппетита, диарея, запор или металлический привкус во рту.Если какой-либо из этих эффектов сохраняется или ухудшается, немедленно сообщите об этом своему врачу или фармацевту.
Это лекарство может привести к потемнению вашей мочи. Этот эффект безвреден и исчезнет после прекращения приема лекарства.
Помните, что ваш врач прописал это лекарство, потому что он или она посчитали, что польза для вас больше, чем риск побочных эффектов. Многие люди, принимающие это лекарство, не имеют серьезных побочных эффектов.
Немедленно сообщите своему врачу, если у вас есть какие-либо серьезные побочные эффекты, в том числе: признаки новой инфекции (например, боль в горле, которая не проходит, лихорадка), легкие синяки / кровотечения, боли в животе / животе, болезненное мочеиспускание.
Немедленно обратитесь за медицинской помощью, если у вас есть какие-либо очень серьезные побочные эффекты, в том числе: неустойчивость, судороги, психические изменения / изменения настроения (например, спутанность сознания), проблемы с речью, онемение / покалывание в руках / ногах, боль в глазах, внезапные изменения зрения, сильная или не проходит головная боль, ригидность / болезненность шеи.
Использование этого лекарства в течение продолжительных или повторяющихся периодов может привести к молочнице полости рта или новой инфекции дрожжей. Обратитесь к врачу, если вы заметили белые пятна во рту, изменение выделений из влагалища или другие новые симптомы.
Очень серьезные аллергические реакции на этот препарат возникают редко. Однако немедленно обратитесь за медицинской помощью, если вы заметили какие-либо симптомы серьезной аллергической реакции, в том числе: сыпь, зуд / отек (особенно лица / языка / горла), сильное головокружение, затрудненное дыхание.
Это не полный список возможных побочных эффектов. Если вы заметили другие эффекты, не перечисленные выше, обратитесь к врачу или фармацевту.
В США —
Обратитесь к врачу за медицинской консультацией по поводу побочных эффектов.Вы можете сообщить о побочных эффектах в FDA по телефону 1-800-FDA-1088 или на сайте www.fda.gov/medwatch.
В Канаде — Обратитесь к врачу за медицинской консультацией по поводу побочных эффектов. Вы можете сообщить о побочных эффектах в Министерство здравоохранения Канады по телефону 1-866-234-2345.
Два основных вопроса помогают лечить H. pylori
Как одна из наиболее распространенных хронических бактериальных инфекций, Helicobacter pylori является известным врагом из-за своей способности вызывать язвенную болезнь желудка и рак желудка. Но в сегодняшнюю эпоху устойчивости к антибиотикам инфекция требует больше боеприпасов. быть побежденным.
В течение многих лет стандартным лечением H. pylori было тройное лечение кларитромицином, комбинация кларитромицина, амоксициллина или метронидазол и ингибитор протонной помпы (ИПП) в течение 14 дней. Но трехкомпонентный режим попал в немилость, сказал гастроэнтеролог Колин В. Хауден, доктор медицины, во время своего сеанса. об общих проблемах верхних отделов желудочно-кишечного тракта на встрече по внутренним болезням 2018.
По словам Колина У. Хаудена, доктора медицины, лучшие и наиболее экономически эффективные методы лечения инфекции H. pylori являются эффективными. Фото Кевина Берн«В большей части страны я бы сказал, что это больше не рекомендуется и это лечение в значительной степени устарело », — сказал он.
Итак, каковы лучшие и наиболее экономичные методы лечения H.pylori ? Проще говоря, те, которые работают, — сказал доктор Хауден, профессор медицины. в Центре медицинских наук Университета Теннесси в Мемфисе.
«Независимо от долларов и центов, самое дорогое лечение — это не работает », — сказал он. «И есть чертовски много способов лечения. там для H. pylori , которые не работают ».
Новое руководство по лечению
Хотя тестирование на чувствительность к противомикробным препаратам часто определяет лечение других бактериальных инфекции, он обычно не доступен для H.pylori , — отметил доктор Хауден. «Это дорого, трудно достать, и многие из у нас нет к нему доступа, поэтому лечение инфекции H. pylori в значительной степени эмпирическое ».
Недавнее руководство предлагает новое направление. В 2017 году Американский колледж гастроэнтерологии опубликовали обновленное клиническое руководство по лечению инфекции H. pylori .Доктор Хауден, соавтор руководства, обрисовал в общих чертах две схемы лечения. на что терапевты должны сосредоточить внимание при ведении большинства своих пациентов.
Первая четырехкратная терапия на основе висмута, включающая висмут, тетрациклин, метронидазол, и PPI от 10 до 14 дней, но предпочтительно 14 дней, сказал он. «На основе висмута четырехкратная терапия была одним из начальных методов лечения H.pylori и теперь снова в моде ».
Вторая схема, называемая сопутствующей терапией, включает кларитромицин, амоксициллин, метронидазол и ИПП в течение 10–14 дней (опять же, предпочтительно 14 дней). «Его своего рода подход к кухне-раковине. Бросьте все на жука, — сказал доктор Хауден. «По сути, сопутствующая терапия представляет собой тройную терапию кларитромицином с добавление метронидазола.”
Поскольку лечение в значительной степени эмпирическое, «Мы должны быть осторожны, когда выбираем особый режим лечения для конкретного пациента », — предупредил он.
Доктор Хауден сказал, что при выборе схемы лечения следует учитывать два ключевых вопроса. индивидуальный пациент:
- 1. Были ли контакты с макролидными антибиотиками в прошлом (например,г., кларитромицин, азитромицин, эритромицин) по любой причине, и
- 2. Есть ли у пациента аллергия на пенициллин?
Дополнительным соображением является местная картина устойчивости к антибиотикам, хотя это «информация не всегда доступна», — отметил он.
«Если пациент по какой-либо причине подвергся воздействию макролидов, вам следует вероятно, следует избегать кларитромицина для лечения H.pylori , — сказал доктор Хауден. Почему? Потому что жук наверняка помнит, как противостоять это, сказал он, отметив, что практически все взрослые с H. pylori заразились инфекцией в детстве.
«Этот жук живет в их желудке большую часть жизни», — сказал доктор Хауден. «Каждая таблетка антибиотика, которую когда-либо проглотил этот пациент, был обнаружен H.pylori , и если пациент ранее получал макролиды, от респираторной инфекции например, вы должны предположить, что жук устойчив к кларитромицину ».
Что касается аллергии на пенициллин, ожидайте, что это большая редкость. «До 10% взрослого Население США утверждает, что у него аллергия на пенициллин, но это просто неправда. Из из них около 90% имеют отрицательные кожные пробы, указывающие на отсутствие настоящей аллергии », — сказал он. отметил, подчеркнув, что ненужный отказ от пенициллина является проблемой общественного здравоохранения потому что это приводит к чрезмерному использованию небета-лактамных антибиотиков.
Это важно при лечении инфекции H. pylori , потому что амоксициллин остается важнейшим лекарством, сказал доктор Хауден. « H. pylori практически никогда не становится устойчивым к амоксициллину. Просто нужно понюхать кларитромицин. и он устойчив к нему, но по неясным, по крайней мере мне, причинам, амоксициллин устойчивость среди H. pylori чрезвычайно редка », — сказал он.
При отсутствии в анамнезе применения макролидов или аллергии на пенициллин, четырехкратная терапия висмутом и сопутствующая терапия — хороший выбор, сказал доктор Хауден, добавив, что кларитромицин тройную терапию также можно использовать, если уровень местной резистентности к кларитромицину у штаммов H. pylori составляет менее 15%. «Я готов поспорить, что большая часть Соединенных Штатов не будет соответствуют этому критерию », — сказал он.
Если нет аллергии на пенициллин, но пациент ранее получал макролид, тогда четырехкратная терапия висмутом была бы идеальной, — сказал доктор Хауден. Если пациент аллергия на пенициллин, но никогда не получал макролиды, четырехкратная терапия висмутом по-прежнему является хорошим вариантом, хотя также можно использовать тройную терапию кларитромицином если амоксициллин заменить метронидазолом, сказал он.Для тех, кто страдает аллергией для пенициллина и предыдущих пользователей макролидов четырехкратная терапия висмутом по существу — единственный вариант, — сказал доктор Хауден.
«Я говорю стипендиатам, где я работаю, [что] четырехкратная висмутовая терапия никогда не неправильный ответ »при лечении инфекции H. pylori , — сказал он.
После лечения
Несмотря на эффективность 14-дневного курса четырех разных лекарств, схема пациентам сложно принимать.Доктор Хауден советует обсудить обе причины. схемы и любых нежелательных явлений, которые можно ожидать.
Во-первых, важно, чтобы пациенты придерживались полного режима. Неспособность принять на По крайней мере, 80% прописанных лекарств позволяют предсказать неэффективность эрадикации, и неудача эрадикации часто приводит к появлению устойчивых к антибиотикам штаммов бактерий, он сказал.
«Я бы предпочел, чтобы вы проигнорировали инфекцию H. pylori и не лечили ее, чем лечили ее неадекватно или назначили неэффективную схему лечения. потому что это только способствует появлению устойчивых штаммов », — сказал доктор Хауден. сказал.
Что касается побочных эффектов, диарея очень распространена при применении этих комбинаций антибиотиков, Он отметил, что кларитромицин и метронидазол также могут вызывать нарушение вкуса.В Кроме того, существует взаимодействие алкоголя с метронидазолом. «Это не серьезно, но это не особенно приятно, поэтому пациентам следует рекомендовать избегать употребления алкоголя когда они принимают метронидазол, — сказал доктор Хауден.
Хотя диагностика и лечение H. pylori важны, поскольку инфекция может быть связана с серьезными долгосрочными последствиями, «Есть не менее веский аргумент в пользу того, что инфекция прошла успешно. вылечили, потому что уровень повторного заражения очень, очень низкий, менее 1% в течение года », он сказал.«Как только эта инфекция излечена, она, как правило, остается излеченной».
Кроме того, общий уровень эрадикации составляет всего от 70% до 80% (даже при полном соблюдении режима лечения), и такие симптомы, как диспепсия, не указывают на успех или неудачу лечения. — сказал Хауден. «Мы считаем, что есть веские основания для рутинного пост-лечения. тестирование ».
Следовательно, управление H.pylori включает тестирование, лечение и повторное тестирование. Доктор Хауден подчеркнул, что после лечения Тестирование должно проводиться с тестом на активную инфекцию H. pylori , например, дыхательный тест на мочевину, тест на фекальный антиген или тест на основе биопсии если пациенту проводят эндоскопию. Серология после лечения — большой запрет.
«Я говорю своим пациентам:« Если кто-нибудь предложит анализ крови на H.pylori , будьте вежливы, вспомните Нэнси Рейган, просто скажите «нет». «… Вы можете вылечить инфекцию H. pylori , и серологические исследования будут оставаться положительными в течение многих лет, если не до бесконечности», он сказал. «Я видел пациентов с излеченной инфекцией H. pylori , которых отправляли обратно ко мне из-за положительного анализа крови».
Тестирование для подтверждения ликвидации должно быть проведено не ранее, чем через четыре недели после его окончания. лечения, и пациент не должен был принимать ИПП, антибиотики или висмут. за две недели до теста Dr.- сказал Хауден.
Два главных предиктора неудачи эрадикации — плохое соблюдение схем лечения. и устойчивость к антибиотикам (особенно к кларитромицину), сказал он.
«Повторное лечение по первоначальной неудачной схеме — это то, что я вижу неоднократно. в клинической практике, особенно с кларитромицином », — сказал д-р Хауден. «Если Терапия на основе кларитромицина однажды не удалась, она снова потерпит неудачу.Так что просто не делай Это.» Четырехкратная терапия висмутом особенно подходит, когда пациенты не — ответил он на схему, содержащую кларитромицин.
В общем, избегайте повторного использования тех же антибиотиков снова, если терапия первой линии не дает результатов. — сказал доктор Хауден. «Двумя исключениями являются амоксициллин и тетрациклин. … Устойчивость к этим антибиотикам практически равна нулю.”
И когда лечение не помогает: «Думаю, тебе следует проконсультироваться со своим гастроэнтеролог, и схемы спасения нужно подбирать тщательно », — сказал он. сказал. «Рекомендации Американского колледжа гастроэнтерологии дают несколько советов. об этом.»
Если лечение не помогло три раза или более, доктор Хауден сказал, что, возможно, пришло время отказаться от лечения. сейчас.Он посоветовал лечить симптомы диспепсии в меру ваших возможностей и успокоить пациенты, которые могут стать доступными для лечения инфекции.
«Когда ничего не помогает, как, например, при лечении инфекции H. pylori , я напоминаю пациентам, что есть вещи похуже, с которыми можно жить, чем H. pylori », — сказал он.
Helicobacter pylori (H.pylori) инфекция — Диагностика и лечение
Диагноз
Чтобы определить, есть ли у вас инфекция H. pylori , используются несколько тестов и процедур. Тестирование важно для обнаружения H. pylori , но также для тестирования после лечения, чтобы убедиться, что он был устранен.
Тесты стула. Самый распространенный тест стула для обнаружения H. pylori называется тестом на антиген стула, который ищет чужеродные белки (антигены), связанные с H.pylori в вашем стуле. Антибиотики, препараты, подавляющие кислотность, известные как ингибиторы протонной помпы (ИПП) и субсалицилат висмута (пепто-бисмол), могут повлиять на точность этих тестов. Если вам ранее был поставлен диагноз и лечили от H. pylori , ваш врач обычно подождет не менее четырех недель после завершения лечения антибиотиками, чтобы проверить ваш стул. Если вы принимаете PPI , ваш врач попросит вас прекратить прием лекарств PPI за одну или две недели до теста.Этот тест доступен для взрослых и детей старше 3.
Лабораторный тест, называемый тестом полимеразной цепной реакции стула (ПЦР), может выявить инфекцию H. pylori в стуле и мутации, которые могут быть устойчивыми к антибиотикам, используемым для ее лечения. Этот тест более дорогой и может быть недоступен во всех медицинских центрах. Этот тест доступен для взрослых и детей.
Дыхательный тест. Во время проверки дыхания вы проглатываете таблетку, жидкость или пудинг, содержащие меченые молекулы углерода.Если у вас инфекция H. pylori , углерод выделяется, когда раствор распадается в желудке.
Ваше тело поглощает углерод и выводит его на выдохе. Вы выдыхаете в мешок, и ваш врач с помощью специального устройства обнаруживает молекулы углерода.
Как и в тестах на стул, ИПП, , субсалицилат висмута (пепто-бисмол) и антибиотики могут повлиять на точность этого теста. Если вы принимаете PPI , ваш врач попросит вас прекратить прием лекарств PPI за одну или две недели до теста.Если у вас ранее был диагностирован и лечился от H. pylori , ваш врач обычно подождет не менее четырех недель после завершения лечения антибиотиками, чтобы выполнить тест дыхания. Этот тест доступен для взрослых и детей.
Проверка объема. Во время этого теста, известного как верхняя эндоскопия, вы получите успокоительное. Во время обследования врач вводит длинную гибкую трубку, снабженную крошечной камерой (эндоскопом), через горло и пищевод в желудок и двенадцатиперстную кишку.Этот инструмент позволяет вашему врачу увидеть любые нарушения в верхних отделах пищеварительного тракта и взять образцы тканей (биопсия). Эти образцы анализируются на предмет инфицирования H. pylori .
Этот тест проводится для изучения симптомов, которые могут быть вызваны другими состояниями, такими как язва желудка или гастрит, причиной которых может быть H. pylori . Тест может быть повторен после лечения в зависимости от того, что было обнаружено при первой эндоскопии, или если симптомы сохраняются после H.pylori лечение. На этом втором обследовании можно выполнить биопсию, чтобы убедиться в удалении H. pylori . Если у вас ранее был диагностирован и лечился от H. pylori , ваш врач обычно подождет не менее четырех недель после завершения лечения антибиотиками, чтобы выполнить тест дыхания. Если вы принимаете PPI , ваш врач попросит вас прекратить прием лекарств PPI за одну или две недели до теста.
Этот тест не всегда рекомендуется исключительно для диагностики H.pylori , потому что это более инвазивно, чем анализ дыхания или стула. Но его можно использовать для проведения подробных анализов, чтобы врачи могли точно определить, какой антибиотик назначить для лечения H. pylori , особенно если антибиотики неэффективны или для исключения других пищеварительных заболеваний.
Лечение
Инфекции H. pylori обычно лечат как минимум двумя разными антибиотиками одновременно, чтобы помочь предотвратить развитие устойчивости бактерий к одному конкретному антибиотику.Ваш врач также пропишет или порекомендует препараты, подавляющие кислоту, чтобы помочь заживлению слизистой оболочки желудка.
Лекарства, подавляющие кислотность, включают:
- Ингибиторы протонной помпы (ИПП). Эти препараты препятствуют выработке кислоты в желудке. Некоторыми примерами ИПП являются омепразол (Прилосек), эзомепразол (Нексиум), лансопразол (Превацид) и пантопразол (Протоникс).
- Блокаторы гистамина (H-2). Эти лекарства блокируют вещество, называемое гистамином, которое вызывает выработку кислоты.Одним из примеров является циметидин (Tagamet HB).
- Субсалицилат висмута. Этот препарат, более известный под торговой маркой «Пепто-Бисмол», действует, покрывая язву и защищая ее от желудочной кислоты.
Ваш врач может порекомендовать вам пройти тестирование на H. pylori как минимум через четыре недели после лечения. Если тесты показывают, что лечение было безуспешным, вы можете пройти еще один курс лечения с другой комбинацией антибиотиков.
Подготовка к приему
Обратитесь к лечащему врачу, если у вас есть признаки или симптомы, указывающие на осложнение инфекции H. pylori . Ваш врач может проверить и вылечить вас от инфекции H. pylori или направить вас к специалисту, который лечит заболевания пищеварительной системы (гастроэнтерологу).
Поскольку встречи могут быть короткими и часто есть что обсудить, хорошо подготовиться к встрече.Вот некоторая информация, которая поможет вам подготовиться к приему и чего ожидать от врача.
Что вы можете сделать
Во время записи на прием обязательно спросите, есть ли что-нибудь, что вам нужно сделать заранее, например, ограничить свой рацион. Перед встречей вы можете составить список, который отвечает на следующие вопросы:
- Когда у вас появились симптомы?
- Что-нибудь делает их лучше или хуже?
- Испытывали ли когда-нибудь подобные проблемы у ваших родителей, братьев и сестер?
- Какие лекарства или добавки вы принимаете регулярно?
Ваше время с врачом ограничено.Если вы подготовите список вопросов, это поможет вам максимально эффективно проводить время вместе. В случае инфекции H. pylori врачу следует задать несколько основных вопросов:
- Как инфекция H. pylori вызвала те осложнения, которые у меня возникают?
- Может ли H. pylori вызывать другие осложнения?
- Какие тесты мне нужны?
- Требуют ли эти тесты специальной подготовки?
- Какие методы лечения доступны?
- Как я узнаю, сработало ли лечение?
Во время разговора задавайте дополнительные вопросы, которые возникают у вас на приеме.
Чего ожидать от врача
Ваш врач, скорее всего, задаст вам ряд вопросов. Если вы будете готовы ответить на них, у вас будет больше времени, чтобы обсудить другие вопросы, которые вы хотите затронуть. Ваш врач может спросить:
- Ваши симптомы были постоянными или случайными?
- Насколько серьезны ваши симптомы?
- Принимаете ли вы какие-либо безрецептурные болеутоляющие, такие как аспирин, ибупрофен (Адвил, Мотрин IB и др.) Или напроксен натрия (Алив)?
18 мая 2021 г.
Показать ссылки- Пептические язвы (язвы желудка).Национальный институт диабета, болезней органов пищеварения и почек. https://www.niddk.nih.gov/health-information/digestive-diseases/peptic-ulcers-stomach-ulcers/all-content. По состоянию на 9 января 2017 г.
- Papadakis MA, et al., Eds. Желудочно-кишечные расстройства. В: Текущая медицинская диагностика и лечение, 2017. 56-е изд. Нью-Йорк, штат Нью-Йорк: компании McGraw-Hill; 2017. http://www.accessmedicine.com. По состоянию на 9 января 2017 г.
- Инфекция Helicobacter pylori. Руководство Merck Professional Version.https://www.merckmanuals.com/professional/gastrointestinal-disorders/gastritis-and-peptic-ulcer-disease/helicobacter-pylori-infection. По состоянию на 6 мая 2021 г.
- Helicobacter pylori и рак. Национальный институт рака. https://www.cancer.gov/about-cancer/causes-prevention/risk/infectious-agents/h-pylori-fact-sheet. По состоянию на 9 января 2017 г.
- Руководство Американского колледжа гастроэнтерологии по лечению инфекции Helicobacter pylori. Американский колледж гастроэнтерологии.http://gi.org/guideline/management-of-helicobacter-pylori-infection/. По состоянию на 9 января 2017 г.
- Crowe SE. Бактериология и эпидемиология инфекции Helicobacter pylori. http://www.uptodate.com/home. По состоянию на 9 января 2017 г.
- Crowe SE. Показания и диагностические тесты при инфекции Helicobacter pylori. http://www.uptodate.com/home. По состоянию на 6 мая 2021 г.
- AskMayoExpert. Helicobacter pylori (взрослый). Клиника Майо; 2020.
Helicobacter pylori (H.pylori) инфекция
Рекомендации по подходу, медицинское обслуживание, профилактика
[Рекомендации] Sugano K, Tack J, Kuipers EJ и др. Для преподавателей Киотской конференции по глобальному консенсусу. Киотский глобальный консенсусный отчет по гастриту Helicobacter pylori. Кишка . 2015 Сентябрь 64 (9): 1353-67. [Медлайн].
Младенова И., Дураццо М. Передача Helicobacter pylori. Минерва Гастроэнтерол Диетол . 2018 сентябрь 64 (3): 251-4.[Медлайн].
Хорики Н., Омата Ф, Уэмура М. и др. Ежегодное изменение первичной устойчивости к кларитромицину среди изолятов Helicobacter pylori с 1996 по 2008 гг. В Японии. Хеликобактер . 2009 14 октября (5): 86-90. [Медлайн].
Fallone CA. Эпидемиология устойчивости Helicobacter pylori к антибиотикам в Канаде. Банка Дж Гастроэнтерол . 2000 14 ноября (10): 879-82. [Медлайн].
Hage N, Renshaw JG, Winkler GS, Gellert P, Stolnik S, Falcone FH.Улучшенная экспрессия и очистка адгезина BabA Helicobacter pylori за счет включения гекса-лизиновой метки. Протеин Expr Purif . 2015 фев. 106: 25-30. [Медлайн]. [Полный текст].
Tomb JF, White O, Kerlavage AR и др. Полная последовательность генома возбудителя желудочного сока Helicobacter pylori. Природа . 1997, 7 августа. 388 (6642): 539-47. [Медлайн].
Lowenthal AC, Hill M, Sycuro LK, et al. Функциональный анализ белков переключателей жгутиков Helicobacter pylori. Дж Бактериол . 2009 декабрь 191 (23): 7147-56. [Медлайн]. [Полный текст].
Гианнакис М., Чен С.Л., Карам С.М. и др. Эволюция Helicobacter pylori при прогрессировании от хронического атрофического гастрита до рака желудка и ее влияние на стволовые клетки желудка. Proc Natl Acad Sci U S A . Март 2008 г., 105 (11): 4358-63. [Медлайн].
Lehours P. Фактический диагноз инфекции Helicobacter pylori. Минерва Гастроэнтерол Диетол .2018 Сентябрь 64 (3): 267-79. [Медлайн].
Pullen LC. Объясняет ли эрадикация H.pylori рост ожирения? Медицинские новости Medscape от WebMD. 9 июня 2014 г. Доступно по адресу http://www.medscape.com/viewarticle/826406. Доступ: 19 июня 2014 г.
Кредитор Н., Талли, штат Нью-Джерси, Энк П. и др. Обзорная статья: связь между Helicobacter pylori и ожирением — экологическое исследование. Алимент Фармакол Тер . 2014 июл. 40 (1): 24-31. [Медлайн].
[Рекомендации] Shah SC, Iyer PG, Moss SF.Обновление клинической практики AGA по ведению рефрактерной инфекции Helicobacter pylori: экспертный обзор. Гастроэнтерология . 2021 Апрель 160 (5): 1831-41. [Медлайн]. [Полный текст].
Koletzko L, Macke L, Schulz C, Malfertheiner P. Эрадикация Helicobacter pylori при диспепсии: новые доказательства симптоматической пользы. Лучший Практик Рес Клин Гастроэнтерол . 2019 июн — август 40–1: 101637. [Медлайн].
Лютер Дж., Дэйв М., Хиггинс П.П., Као Дж.Связь между инфекцией Helicobacter pylori и воспалительным заболеванием кишечника: метаанализ и систематический обзор литературы. Воспаление кишечника . 2010 июн.16 (6): 1077-84. [Медлайн].
Джексон Л., Бриттон Дж., Льюис С.А. и др. Популяционное эпидемиологическое исследование инфекции Helicobacter pylori и ее связи с системным воспалением. Хеликобактер . 2009 октября, 14 (5): 108-13. [Медлайн].
[Рекомендации] Tarasconi A, Coccolini F, Biffl WL, et al.Перфорированная и кровоточащая язвенная болезнь: рекомендации WSES. Мир J Emerg Surg . 2020. 15: 3. [Медлайн]. [Полный текст].
Hsu PI, Wu DC, Chen WC, et al. Рандомизированное контролируемое исследование, сравнивающее 7-дневную тройную, 10-дневную последовательную и 7-дневную сопутствующую терапию инфекции Helicobacter pylori. Противомикробные агенты Chemother . 2014 Октябрь 58 (10): 5936-42. [Медлайн].
Pellicano R, Zagari RM, Zhang S, Saracco GM, Moss SF. Фармакологические соображения и пошаговое предложение по лечению инфекции Helicobacter pylori в 2018 году. Минерва Гастроэнтерол Диетол . 2018 Сентябрь 64 (3): 310-21. [Медлайн].
Papastergiou V, Georgopoulos SD, Karatapanis S. Лечение инфекции Helicobacter pylori: решение проблемы устойчивости к противомикробным препаратам. Мир J Гастроэнтерол . 2014 7 августа. 20 (29): 9898-911. [Медлайн].
Gisbert JP, Castro-Fernandez M, Perez-Aisa A, et al. Спасательная терапия четвертой линии с рифабутином у пациентов с тремя неудачными попытками эрадикации Helicobacter pylori. Алимент Фармакол Тер . 2012 апр. 35 (8): 941-7. [Медлайн]. [Полный текст].
Лю X, Ван Х, Lv Z, и др. Спасательная терапия с ингибитором протонной помпы плюс амоксициллин и рифабутин для инфекции Helicobacter pylori: систематический обзор и метаанализ. Гастроэнтерол Рес Прак . 2015. 2015: 415648. [Медлайн]. [Полный текст].
Сафаров Т., Киран Б., Багирова М., Аллахвердиев А.М., Абамор Э.С. Обзор основанных на нанотехнологиях подходов к лечению Helicobacter Pylori. Expert Rev Anti Infect Ther . 2019 8 октября [Medline].
Ниаз Т., Ихсан А., Аббаси Р., Шаббир С., Нур Т., Имран М. Основанные на хитозане-альбумине нано-антимикробные вещества оболочки и короны для уничтожения резистентных желудочных патогенов. Инт Дж Биол Макромол . 1 октября 2019 г. 138: 1006-18. [Медлайн].
Zhi X, Liu Y, Lin L и др. Устные pH-чувствительные нанозонды GNS @ ab для таргетной терапии Helicobacter pylori без нарушения микробиома кишечника. Наномедицина . 20 августа 2019: 10 [Медлайн].
de Avila BE, Angsantikul P, Li J, et al. Активная доставка лекарств с помощью микромотора для лечения желудочной инфекции in vivo. Нац Коммуна . 2017 16 августа. 8 (1): 272. [Медлайн]. [Полный текст].
Гринберг Э. Р., Андерсон Г. Л., Морган Д. Р. и др. 14-дневная тройная, 5-дневная сопутствующая и 10-дневная последовательная терапия инфекции Helicobacter pylori в семи странах Латинской Америки: рандомизированное исследование. Ланцет . 2011 6 августа. 378 (9790): 507-14. [Медлайн].
Liou JM, Lin JT, Chang CY, et al. Тройная терапия на основе левофлоксацина и кларитромицина в качестве терапии первого и второго ряда при инфекции Helicobacter pylori: рандомизированное сравнительное исследование с перекрестным дизайном. Кишка . 2010 май. 59 (5): 572-8. [Медлайн].
Apostolopoulos P, Koumoutsos I, Ekmektzoglou K, et al. Сопутствующая терапия по сравнению с последовательной терапией для лечения инфекции Helicobacter pylori: греческое рандомизированное проспективное исследование. Сканд Дж Гастроэнтерол . 2016 Февраль 51 (2): 145-51. [Медлайн].
Юн Х., Ким Н., Ли Б.Х. и др. Тройная терапия, содержащая моксифлоксацин, в качестве лечения второй линии при инфекции Helicobacter pylori: влияние продолжительности лечения и устойчивости к антибиотикам на скорость эрадикации. Хеликобактер . 2009 октября, 14 (5): 77-85. [Медлайн].
Malfertheiner P, Bazzoli F, Delchier JC, et al. Эрадикация Helicobacter pylori с помощью капсулы, содержащей субцитрат висмута калия, метронидазол и тетрациклин, с омепразолом по сравнению с тройной терапией на основе кларитромицина: рандомизированное открытое исследование не меньшей эффективности, фаза 3. Ланцет . 2011 12 марта. 377 (9769): 905-13. [Медлайн].
Ли С.Б., Ян Дж.В., Ким С.С. Связь между MALT-лимфомой конъюнктивы и Helicobacter pylori. Br J Офтальмол . 2008 апр. 92 (4): 534-6. [Медлайн].
Aanpreung P. Предполагаемые параметры эрадикационной терапии у детей с гастритом Helicobacter pylori. J Med Assoc Thai . 2005 г., ноябрь 88, приложение 8: S21-6. [Медлайн].
Adachi K, Hashimoto T, Komazawa Y, et al.Инфекция Helicobacter pylori влияет на симптоматический ответ на антисекреторную терапию у пациентов с ГЭРБ — перекрестное сравнительное исследование с фамотидином и низкими дозами лансопразола. Dig Liver Dis . 2005 июл. 37 (7): 485-90. [Медлайн].
Александр Г.А., Броули О.В. Связь инфекции Helicobacter pylori с раком желудка. Мил Мед . 2000, январь, 165 (1): 21-7. [Медлайн].
Ceponis PJ, Jones NL. Модуляция путей передачи сигнала клетки-хозяина инфекцией Helicobacter pylori. Банка Дж Гастроэнтерол . 2005 июля 19 (7): 415-20. [Медлайн].
Chelimsky G, Czinn SJ. Инфекция Helicobacter pylori у детей: обновленная информация. Curr Opin Pediatr . 2000 октября, 12 (5): 460-2. [Медлайн].
Cheng TY, Lin JT, Chen LT и др. Ассоциация полиморфизмов регуляторных генов Т-клеток с предрасположенностью к лимфоме лимфоидной ткани, ассоциированной со слизистой оболочкой желудка. Дж. Клин Онкол . 20 июля 2006 г. 24 (21): 3483-9. [Медлайн].
Chitsazi MT, Fattahi E, Farahani RM и др. Helicobacter pylori в зубном налете: имеет ли это значение для диагностики желудочной инфекции ?. Med Oral Patol Oral Cir Bucal . 1 июля 2006 г. 11 (4): E325-8. [Медлайн].
Краанен М.Э., Блок П., Деккер В. и др. Helicobacter pylori и ранний рак желудка. Кишка . 1994 окт. 35 (10): 1372-4. [Медлайн].
Давыдов Л, Ченг Ж. Связь инфекции и ишемической болезни сердца: обновленная информация. Заключение эксперта по расследованию наркотиков . 2000 ноября, 9 (11): 2505-17. [Медлайн].
Demirel A, Oncel S, Caydere M, et al. Инфекция Helicobacter pylori в образцах гастрэктомии. Интернет-журнал гастроэнтерологии 2000; 1 (1) . [Полный текст].
Данн Б.Е., Коэн Х., Блазер М.Дж. Helicobacter pylori. Clin Microbiol Ред. . 1997.10.10 (4): 720-41. [Медлайн].
Eaton KA, Benson LH, Haeger J и др.Роль экспрессии фактора транскрипции T-bet клетками CD4 + при гастрите, вызванном Helicobacter pylori у мышей. Заражение иммунной . 2006 август 74 (8): 4673-84. [Медлайн].
El-Omar EM, Carrington M, Chow WH, et al. Полиморфизм интерлейкина-1, связанный с повышенным риском рака желудка. Природа . 2000 23 марта. 404 (6776): 398-402. [Медлайн].
Эрджан I, Чакир Б.О., Узел Т.С. и др. Роль желудочной инфекции Helicobacter pylori в ларингофарингеальной рефлюксной болезни. Otolaryngol Head Neck Surg . 2006 июль 135 (1): 52-5. [Медлайн].
Fallone CA, Barkun AN, Friedman G, et al. Связана ли эрадикация Helicobacter pylori с гастроэзофагеальной рефлюксной болезнью? Ам Дж. Гастроэнтерол . 2000 апр. 95 (4): 914-20. [Медлайн].
Farag TH, Stoltzfus RJ, Khalfan SS, et al. Инфекция Helicobacter pylori связана с тяжелой анемией беременных на острове Пемба, Занзибар. Am J Trop Med Hyg .2007 Март 76 (3): 541-8. [Медлайн].
Fiorini G, Vakil N, Zullo A, et al. Селекционная терапия на основе культур для пациентов, которые не ответили на предыдущее лечение инфекции Helicobacter pylori. Клин Гастроэнтерол Гепатол . 2013 май. 11 (5): 507-10. [Медлайн].
Fischbach W. Первичная лимфома желудка MALT: соображения патогенеза, диагностики и лечения. Банка Дж Гастроэнтерол . 2000 14 ноября Дополнение D: 44D-50D.[Медлайн].
Фок К.М., Кателарис П., Сугано К. и др. Второе Азиатско-Тихоокеанское согласованное руководство по инфекции Helicobacter pylori. Дж Гастроэнтерол Гепатол . 2009 24 октября (10): 1587-600. [Медлайн].
Фрестон JW. Лечение язвенной болезни: новые вопросы. Мир J Surg . 2000 марта, 24 (3): 250-5. [Медлайн].
Гарсия-Альтес А., Рота Р., Баренис М. и др. Экономическая эффективность стратегии «оценка и масштаб» для лечения диспепсии. Eur J Gastroenterol Hepatol . 2005 июл.17 (7): 709-19. [Медлайн].
Gatopoulou A, Mimidis K, Giatromanolaki A, et al. Влияние инфекции Helicobacter pylori на гистологические изменения при неэрозивной рефлюксной болезни. Мир J Гастроэнтерол . 2004 15 апреля. 10 (8): 1180-2. [Медлайн].
Грэм Д.Ю. Терапия Helicobacter pylori: текущее состояние и проблемы. Гастроэнтерология . 2000, февраль 118 (2 приложение 1): S2-8.[Медлайн].
Graham DY, Lew GM, Lechago J. Количество антральных G-клеток и D-клеток при инфекции Helicobacter pylori: эффект эрадикации H. pylori. Гастроэнтерология . 1993 июн.104 (6): 1655-60. [Медлайн].
Graham DY, Lew GM, Malaty HM, et al. Факторы, влияющие на эрадикацию Helicobacter pylori при тройной терапии. Гастроэнтерология . 1992 февраль 102 (2): 493-6. [Медлайн].
Graham DY, Malaty HM, Evans DG, et al.Эпидемиология Helicobacter pylori у бессимптомной популяции в США. Влияние возраста, расы и социально-экономического статуса. Гастроэнтерология . 1991 июн.100 (6): 1495-501. [Медлайн].
Guslandi M. Иммуноанализ кала на Helicobacter pylori недостаточно специфичен. BMJ . 2000 г., 3 июня. 320 (7248): 1541. [Медлайн].
Howden CW, Hunt RH. Руководство по лечению инфекции Helicobacter pylori. Специальный комитет по параметрам практики Американского колледжа гастроэнтерологии. Ам Дж. Гастроэнтерол . 1998 декабрь 93 (12): 2330-8. [Медлайн].
Джеймисон Г.Г. Современное состояние показаний к операции при язвенной болезни. Мир J Surg . 2000 марта, 24 (3): 256-8. [Медлайн].
Jia CL, Jiang GS, Li CH, Li CR. Влияние контроля зубного налета на инфекцию Helicobacter pylori в слизистой оболочке желудка. Дж Периодонтол . 2009 Октябрь 80 (10): 1606-9. [Медлайн].
Kusters JG, van Vliet AH, Kuipers EJ.Патогенез инфекции Helicobacter pylori. Clin Microbiol Ред. . 2006 июл.19 (3): 449-90. [Медлайн].
Leinonen M, Saikku P. Инфекции и атеросклероз. Сканд Кардиоваск J . 2000. 34 (1): 12-20. [Медлайн].
Льюис Дж. Д. Популяционный скрининг и лечение Helicobacter pylori. Гастроэнтерология . 2000 Декабрь 119 (6): 1795-7. [Медлайн].
Логан Р. Эпидемиология может дать новые способы борьбы с H.pylori. Ланцет . 1999 18 сентября. 354 (9183): 1006. [Медлайн].
Лопес А.И., Викторино Р.М., Пальха А.М. и др. Субпопуляции лимфоцитов слизистой оболочки и экспрессия антигена HLA-DR при педиатрическом гастрите, ассоциированном с Helicobacter pylori. Клин Эксперимент Иммунол . 2006 июл.145 (1): 13-20. [Медлайн].
Мескита М.А., Лорена С.Л., Алмейда Дж. Р. и др. Однонедельная двойная терапия ранитидином цитратом висмута и кларитромицином для лечения инфекции Helicobacter pylori у бразильских пациентов с язвенной болезнью. Мир J Гастроэнтерол . 2005 21 июня. 11 (23): 3566-9. [Медлайн].
Мюллер А., Сайи А., Хитцлер И. Защитные и патогенные функции Т-клеток неотделимы во время взаимодействия Helicobacter-хозяин. Дисков Мед . 2009 8 августа (41): 68-73. [Медлайн].
Накадзима С., Кришнан Б., Ота Н. и др. Участие тучных клеток в гастрите с инфекцией Helicobacter pylori или без нее. Гастроэнтерология . 1997 сен.113 (3): 746-54. [Медлайн].
О’Морайн С., Монтегю С. Проблемы терапии в будущем. Хеликобактер . 2000. 5 Suppl 1: S23-6; обсуждение S27-31. [Медлайн].
Padol S, Yuan Y, Thabane M, et al. Влияние полиморфизмов CYP2C19 на скорость эрадикации H. pylori при терапии двойной и тройной ИПП первой линии: метаанализ. Ам Дж. Гастроэнтерол . 2006 июль 101 (7): 1467-75. [Медлайн].
Персик HG, Барнетт, NE.Детерминанты базального уровня гастрина в плазме в общей популяции. Дж Гастроэнтерол Гепатол . 2000 15 ноября (11): 1267-71. [Медлайн].
Pratt JS, Sachen KL, Wood HD и др. Модуляция иммунных ответов хозяина цитотоксическим токсином Helicobacter hepaticus. Заражение иммунной . 2006 г., август 74 (8): 4496-504. [Медлайн].
Рейрат Дж. М., Раппуоли Р., Телфорд Дж. Л. Обзор структуры цитотоксина Helicobacter. Int J Med Microbiol . 2000 Октябрь 290 (4-5): 375-9. [Медлайн].
Rodrigues MN, Queiroz DM, Bezerra Filho JG, et al. Распространенность инфекции Helicobacter pylori у детей из городских поселений на северо-востоке Бразилии и факторы риска инфицирования. Eur J Gastroenterol Hepatol . 2004 Февраль 16 (2): 201-5. [Медлайн].
Santacroce L, Bufo P, Latorre V и др. [Роль тучных клеток в физиопатологии поражений желудка, вызванных Helicobacter pylori]. Чир Итал . 2000 сен-окт. 52 (5): 527-31. [Медлайн].
Smoot DT, Mobley HL, Chippendale GR и др. Активность уреазы Helicobacter pylori токсична для эпителиальных клеток желудка человека. Заражение иммунной . 1990 июн. 58 (6): 1992-4. [Медлайн].
Stahler FN, Odenbreit S, Haas R и др. Новый насос для оттока металла Helicobacter pylori CznABC необходим для обеспечения устойчивости к кадмию, цинку и никелю, модуляции уреазы и колонизации желудка. Заражение иммунной . 2006 июль 74 (7): 3845-52. [Медлайн].
Цай С.Дж., Перри С., Санчес Л. и др. Инфекция Helicobacter pylori у разных поколений латиноамериканцев в районе залива Сан-Франциско. Am J Epidemiol . 2005 15 августа. 162 (4): 351-7. [Медлайн].
Tytgat GN. Обзорная статья: Helicobacter pylori: где мы и куда идем ?. Алимент Фармакол Тер . 2000, 14 октября, Дополнение 3: 55-8. [Медлайн].
Неопознанные изогнутые бациллы на эпителии желудка при активном хроническом гастрите. Ланцет . 4 июня 1983 г., 1 (8336): 1273-5. [Медлайн].
Вайра Д., Гатта Л., Риччи С. и др. Язвенная болезнь и Helicobacter pylori: обновленная информация о тестировании и лечении. Постградская медицина . 2005 июн. 117 (6): 17-22, 46. [Medline].
Wang X, Wattiez R, Paggliacia C, et al. Топология мембраны цитотоксина VacA из H.пилори. FEBS Lett . 2000, 15 сентября. 481 (2): 96-100. [Медлайн].
Вт TL. Курение, Helicobacter pylori и пародонтит. BMJ . 2006 г. 24 июня. 332 (7556): 1513. [Медлайн].
Wotherspoon AC. Критический обзор влияния эрадикации Helicobacter pylori на MALT-лимфому желудка. Curr Gastroenterol Rep . 2000 Декабрь 2 (6): 494-8. [Медлайн].
Чао CY, Ван Ч., Че YJ, Као CY, Wu JJ, Lee GB.Интегрированная микрофлюидная система для диагностики устойчивости Helicobacter pylori к антибиотикам на основе хинолонов. Biosens Bioelectron . 2016 15 апреля. 78: 281-9. [Медлайн].
Ли Ю.К., Чианг Т.Х., Лиу Дж. М., Чен Х. Х., Ву М. С., Грэм Д. Ю.. Массовая ликвидация Helicobacter pylori для предотвращения рака желудка: теоретические и практические соображения. Печень кишечника . 2016 23 января 10 (1): 12-26. [Медлайн].
Kono Y, Okada H, Takenaka R, et al.Усиливает ли Helicobacter pylori повреждение слизистой оболочки желудка у пользователей нестероидных противовоспалительных препаратов? Многоцентровое ретроспективное исследование случай-контроль. Печень кишечника . 2016 23 января 10 (1): 69-75. [Медлайн].
Исаева Г.С., Фагуни С. Биологические свойства и факторы патогенности Helicobacter pylori. Минерва Гастроэнтерол Диетол . 2018 Сентябрь 64 (3): 255-66. [Медлайн].
Лечение инфекции Helicobacter pylori
US Pharm. 2018; 43 (4): 27-32.
РЕФЕРАТ: Инфекция Helicobacter pylori распространена примерно у половины населения мира. Заражение H pylori связано с развитием язвенной болезни, рака желудка и лимфомы лимфоидной ткани слизистой оболочки. Значительный научный прогресс был достигнут в лечении инфекции H. pylori у взрослых; эти достижения рассматриваются в обновленных рекомендациях Американского колледжа гастроэнтерологии и Торонтского консенсуса.Растущая распространенность H pylori , устойчивого к традиционным методам лечения на основе кларитромицина, является глобальной проблемой, требующей обзора доказательств для включения дополнительных схем лечения.
Helicobacter pylori — грамотрицательная бактерия, колонизирующая желудок человека. Обычно он приобретается в детстве и передается от человека к человеку. 1,2 Факторы риска заражения H. pylori включают низкий социально-экономический статус, увеличение числа братьев и сестер и наличие инфицированного родителя. 1
Почти половина населения мира инфицирована H. pylori . Значительная глобальная распространенность и растущая устойчивость к антибиотикам привели к тому, что Всемирная организация здравоохранения признала H. pylori в качестве высокоприоритетного патогена в 2017 году. Распространенность H. pylori варьируется в зависимости от географического региона, и, по оценкам, 30% территории США население заражено. 1,3,4 H pylori является основным патогеном, вызывающим желудочно-кишечные заболевания, такие как язвенная болезнь (ЯБ), рак желудка и лимфома, ассоциированная со слизистой оболочкой лимфоидной ткани (MALT), и он связан с нежесточными заболеваниями, включая железодефицитная анемия (ЖДА) и идиопатическая тромбоцитопеническая пурпура (ИТП). 5,6 Обновленные рекомендации США и Канады включают последние данные по лечению инфекций H pylori .
ДиагнозИсторически, тестирование H. pylori было показано пациентам с клиническими проявлениями инфекции H. pylori , включая анамнез или активную ЯБ-лимфому или MALT-лимфому. 1,2,5 Последние данные способствовали расширению тестирования и включили в него группы пациентов, которые ранее считались спорными.Помимо желудочно-кишечных проявлений инфекции H pylori , данные также подтверждают использование теста H pylori при негастральных заболеваниях, таких как необъяснимая ЖДА и ИТП. 1,2,5 См. ТАБЛИЦА 1 .
Тесты на H. pylori делятся на неэндоскопические и эндоскопические ( ТАБЛИЦА 2 ). При выборе диагностического теста следует учитывать возможность его проведения, клиническую ситуацию и стоимость.Хотя не существует стандартного теста для определения H pylori , дыхательный тест с мочевиной (UBT) предпочтительнее у пациентов без тревожных симптомов, поскольку он неинвазивный, недорогой, высокочувствительный и специфичный. 2 Культура, еще один метод диагностики H pylori , позволяет проводить тесты на чувствительность; однако он не широко доступен в культуре США, и тестирование на чувствительность следует рассматривать в областях с высокой резистентностью к кларитромицину или при неудачной терапии, потому что неудача схемы первого ряда указывает на вероятность развития резистентности от 60% до 70%.
Фармацевты должны знать о лекарствах, которые могут повлиять на различные типы тестов. 2,5 Чтобы избежать ложноотрицательных результатов экспресс-теста на уреазу, UBT или теста на антиген стула (SAT), прием ингибиторов протонной помпы (ИПП) следует прекратить как минимум за 2 недели до тестирования, а также следует прекратить прием висмута и антибиотиков отказано по крайней мере за 4 недели до этого. Антагонисты рецептора H 2 оказывают минимальное влияние на чувствительность диагностических тестов для H pylori , и нет рекомендаций по отмене их до тестирования.Антациды не влияют на диагностические тесты и могут использоваться для облегчения симптомов, пока не назначают терапию ИПП. 2
ЛечениеЛечение H. pylori следует назначать всем пациентам с положительным результатом теста на активную инфекцию, а выбранная схема лечения должна обеспечивать уровень эрадикации не менее 90%. H pylori Схемы включают тройную терапию, последовательную терапию (пациенту назначают одно лечение, затем другое), четырехкратную терапию и тройную терапию на основе левофлоксацина ( ТАБЛИЦА 3 ). 7 При выборе наиболее подходящей эмпирической схемы лечения H pylori необходимо учитывать предыдущее воздействие антибиотиков, региональные особенности устойчивости к антибиотикам и уровень эрадикации, поскольку эти факторы могут повлиять на успешное лечение. Успешное лечение также зависит от факторов хозяина, таких как аллергия и приверженность. 8-10
Две схемы тройной терапии, которые считаются первой линией, содержат кларитромицин, ИПП и амоксициллин или метронидазол. 1,7-9,11 Терапия на основе кларитромицина считалась наиболее переносимой и безопасной; однако рост устойчивости к антибиотикам привел к снижению эффективности. 12,13 Показатели эрадикации при терапии на основе кларитромицина ниже 80%; Таким образом, эту терапию следует применять только в тех географических регионах, где устойчивость к кларитромицину составляет менее 15%, а также для пациентов, ранее не подвергавшихся воздействию макролидов. 1,7-9,12
Механизм устойчивости H pylori к кларитромицину изучается, но предполагается, что он связан с двумя основными мутациями (A2142G и A2143G) в области пептидилтрансферазы, кодируемой в домене V 23S рРНК. 6,13 Текущие результаты также предполагают, что по крайней мере четыре семейства эффлюкс-помпы кластеров генов в штаммах H pylori могут иметь синергетические эффекты, вызывающие устойчивость к антибиотикам. 13 Дополнительные схемы становятся терапией первой линии для ликвидации инфекций H. pylori , чтобы вылечить нынешний кризис резистентности к кларитромицину.
Четырехкратная терапия висмутом обеспечивает скорость эрадикации, аналогичную таковой при терапии на основе кларитромицина. 1,2,9 Этот режим первого ряда рекомендуется в областях с высокой резистентностью, в случаях предшествующего воздействия макролидов и в случаях, когда терапия на основе кларитромицина не принесла результатов. Недостатком этого режима является большое количество таблеток; однако приверженность и переносимость аналогичны таковым для терапии на основе кларитромицина. FDA одобрило комбинированный продукт (Pylera), который содержит субцитрат висмута, тетрациклин и метронидазол в сочетании с ИПП; Эти агенты не одобрены FDA для терапии, если они назначаются отдельно. 1,2,9
Невисмутовая четырехкомпонентная терапия (т. Е. Сопутствующая) в течение 10–14 дней (Торонтский консенсус настоятельно рекомендует 14 дней) — еще одна схема первой линии. 1,2,9 Этот режим также может использоваться в качестве терапии спасения у пациентов с персистирующей инфекцией H. pylori , когда первичная или предпочтительная терапия не дает результатов. Хотя никакие рандомизированные контролируемые исследования в Северной Америке не оценивали сопутствующую терапию, Американский колледж гастроэнтерологии (ACG) рекомендует ее использование на основе метаанализа 19 исследований, включающих более 2000 пациентов, которые продемонстрировали высокие показатели эрадикации (в среднем 88%) даже в регионах с высокой устойчивостью к кларитромицину и метронидазолу. 1,8,14 Примечательно, что, как и в случае с кларитромицином, уровень резистентности к метронидазолу также вызывает тревогу (> 20%). 1,6
Аллергия на пенициллинКакая схема лечения H pylori лучше всего подходит для пациентов с заявленной аллергией на пенициллин? Литература предполагает, что большинство пациентов с задокументированной историей аллергии на пенициллин не имеют истинной гиперчувствительности, которая исключала бы использование схем, содержащих амоксициллин. 1 Амоксициллин является ключевым компонентом нескольких методов лечения H pylori , поскольку показатели устойчивости остаются относительно низкими.Четырехкратная терапия висмутом не содержит амоксициллина и может применяться у пациентов с истинной аллергией на пенициллин. Если у пациента с аллергией на пенициллин не удалось добиться эрадикации после одной или двух схем, следует рассмотреть возможность тестирования на аллергию, чтобы определить, можно ли безопасно использовать схемы спасения, содержащие амоксициллин. Кроме того, метаанализ подтвердил, что тройная и четверная схемы, содержащие доксициклин, эффективны в уничтожении H. pylori и могут быть рассмотрены для использования у пациентов, которые не могут принимать амоксициллин. 1,15
Альтернативные схемы первого рядаACG условно рекомендует использовать последовательные, гибридные схемы и схемы на основе фторхинолонов в качестве лечения первого ряда, тогда как Консенсус Торонто не рекомендует их использование на основании недостаточных доказательств . 1,9 В настоящее время терапия на основе левофлоксацина является вариантом лечения спасения, но ACG считает, что она предлагает наиболее надежные данные об эффективности первой линии, основанные на международных исследованиях. 1
Эффективность последовательной терапии зависит от географического региона. 1,2,9 Мета-анализ глобальных данных показал, что уровень искоренения составляет 84%; однако последовательная терапия не превосходит тройную терапию (в течение 14 дней) или терапию на основе висмута и невисмута. 8,14 Североамериканские исследования, оценивающие эффективность последовательной терапии, не обнаружили разницы в эффективности по сравнению с терапией на основе кларитромицина и предложили ее в качестве жизнеспособной альтернативы.Последовательная терапия может быть эффективным вариантом первой линии, если используется в течение 14 дней, но необходимы дальнейшие исследования. Кроме того, последовательный режим сложен, что может увеличить частоту неудач. 1,7,8,16
Гибридная терапия сочетает в себе последовательную и сопутствующую терапию и признана ACG многообещающей, поскольку в международных исследованиях она показала высокие показатели излечения. 1,9 Терапия на основе левофлоксацина сравнима с тройной терапией кларитромицином, но в Северной Америке нет достаточных указаний по уровням резистентности к фторхинолонам, и данные свидетельствуют о том, что резистентность может быть выше по сравнению с кларитромицином.(Показатели устойчивости к антибиотикам штаммов H. pylori в США с 2009 по 2011 г. показали, что более 30% штаммов устойчивы к левофлоксацину. 1 ) Тройной режим рифабутина с ИПП и амоксициллином и двойная терапия высокими дозами с ИПП и амоксициллин не имеют достаточных доказательств и не рекомендуются. 1,9
В целом, Торонтский консенсус и ACG пришли к согласию в отношении искоренения H. pylori и рекомендуют более длительную продолжительность лечения (14 дней), ограничивая терапию на основе кларитромицина и применяя в первую очередь четырехкратный препарат висмута. терапия и сопутствующая терапия. 1,9 Учитывая ограниченные режимы антибиотиков для лечения H pylori и повышенный уровень устойчивости к противомикробным препаратам к этим антибиотикам, существует потребность в лучших долгосрочных решениях для предотвращения и контроля этого патогена человека.
Фармацевты могут выполнять важную функцию в лечении инфекций H. pylori , собирая анамнез предыдущего воздействия антибиотиков и аллергии на лекарства, а также будучи знакомыми с рекомендованными схемами первого и альтернативного первого или вспомогательного лечения, а также факторами, влияющими на эмпирический режим. выбор, например модели сопротивления в их географической области.Фармацевты также могут обучать пациентов их режиму лечения, подчеркивая важность приема назначенных лекарств для повышения вероятности успешного искоренения.
ПробиотикиИспользование пробиотиков для лечения H. pylori является спорным из-за противоречивых данных, а также из-за того, что составы, оптимальная доза, время (до, во время или после эрадикации) и продолжительность терапии не соответствуют друг другу. стандартизированный. 1,9 Хотя ACG предполагает, что пробиотическая терапия может быть многообещающей, Торонтский консенсус рекомендует не добавлять пробиотики.В некоторых литературных источниках предлагается добавлять пробиотики, такие как виды Saccharomyces boulardii и Lactobacillus , в тройные схемы для увеличения показателей эрадикации (абсолютное увеличение на 9% и 5% соответственно) и для уменьшения побочных эффектов, в первую очередь диареи (абсолютное снижение на 14% и 5% соответственно). 7% соответственно). 8,17,18 Однако добавление пробиотиков увеличивает стоимость и нагрузку на таблетки и без того сложного режима.
МониторингВ идеале все пациенты должны пройти тестирование на эрадикацию H. pylori для подтверждения успешного лечения, а также для отслеживания показателей H. pylori ; однако подтверждение эрадикации во всех группах лечения не является рентабельным.Показания для подтверждающего исследования H pylori — эрадикация включают H pylori — ассоциированную язву, стойкие диспепсические симптомы, H pylori — ассоциированную лимфому MALT и удаление раннего рака желудка. Подтверждающие тесты следует проводить через 4-8 недель после терапии. 5 UBT — лучший вариант для подтверждения эрадикации H. pylori ; SAT — альтернатива. 2,5 Серология может выявить инфекций H. pylori в прошлом и не должна использоваться для контроля эффективности. 2,9
ЗаключениеH. pylori является глобально распространенным патогеном высокого риска. Рекомендуемое тестирование для H pylori было расширено, и все пациенты с положительным результатом должны получить лечение. UBT лучше всего подходит для обнаружения и искоренения. Антибиотики и висмут следует проводить не менее 4 недель, а ИПП следует проводить не менее 2 недель до всех диагностических тестов H pylori , кроме серологических. Успешное искоренение H. pylori основано на бактериальных факторах и факторах хозяина.Тройная терапия кларитромицином исторически была лечением первой линии; однако увеличение резистентности к кларитромицину требует дополнительных терапий первой линии. Чтобы выбрать наиболее эффективный эмпирический режим, пациентов следует спросить о предыдущем приеме макролидов и об аллергии на лекарства. Доказательства относительно пробиотиков для лечения H pylori противоречивы. Фармацевты должны быть знакомы со схемами лечения H pylori и разъяснять пациентам важность соблюдения режима лечения.Тестирование на эрадикацию рекомендуется в определенных группах пациентов через 4-8 недель после завершения лечения.
ССЫЛКИ 1. Chey WD, Leontiadis GI, Howden CW, Moss SF. Клинические рекомендации ACG: лечение инфекции Helicobacter pylori . Ам Дж. Гастроэнтерол . 2017; 112: 212-239.
2. Мальфертхайнер П., Мегро Ф., О’Мораин Калифорния и др. Управление инфекцией Helicobacter pylori — Маастрихтский отчет V / Флорентийский консенсус. Кишечник . 2017; 66: 6-30.
3. Глобальное руководство Всемирной гастроэнтерологической организации: Helicobacter pylori в развивающихся странах. Дж Клин Гастроэнтерол . 2011; 45: 383-388.
4. Хант Р.Х., Сяо С.Д., Меграуд Ф. и др. Helicobacter pylori в развивающихся странах. Глобальное руководство Всемирной гастроэнтерологической организации. J Gastrointestin Liver Dis. 2011; 20: 299-304.
5. Chey WD, Wong BCY. Руководство Американского колледжа гастроэнтерологии по ведению инфекции Helicobacter pylori . Ам Дж. Гастроэнтерол . 2007; 102: 1808-1825.
6. Альба С., Бланко А., Аларкон Т. Устойчивость к антибиотикам в Helicobacter pylori . Curr Opin Infect Dis . 2017; 30: 489-497.
7. Де Франческо В., Беллезиа А., Ридола Л. и др. Терапия первой линии для ликвидации Helicobacter pylori : критическая переоценка обновленных руководств. Энн Гастроэнтерол . 2017; 30: 373-379.
8. Fashner J, Gitu AC. Диагностика и лечение язвенной болезни H.pylori инфекция. Am Fam Врач . 2015; 91: 236-242.
9. Fallone CA, Chiba N, van Zanten SV, et al. Торонтский консенсус по лечению инфекции Helicobacter pylori у взрослых. Гастроэнтерология . 2016; 151: 51-69.e14.
10. Грэм Д.Ю., Фишбах Л. Лечение Helicobacter pylori в эпоху повышения устойчивости к антибиотикам. Кишечник . 2010; 59: 1143-1153.
11. Дак В.М., Собел Дж., Пруклер Дж. М. и др. Частота возникновения устойчивости к противомикробным препаратам и факторы риска среди человек, инфицированных Helicobacter pylori, , США. Emerg Infect Dis . 2004; 10: 1088-1094.
12. McNulty CA, Lasseter G, Shaw I., et al. Необходим ли эпиднадзор за устойчивостью к антибиотикам Helicobacter pylori и как его проводить? Алимент Фармакол Тер . 2012; 35: 1221-1230.
13. Abadi ATB. Устойчивость к кларитромицину и роль гастроэнтеролога в номинации Helicobacter pylori как высокоприоритетный патоген Всемирной организацией здравоохранения. Мир Дж. Гастроэнтерол .2017; 23: 6379-6384.
14. Гисберт Дж. П., Кальвет X. Обновленная информация о четырехкратной (сопутствующей) терапии без висмута для искоренения Helicobacter pylori . Клин Эксп Гастроэнтерол . 2012; 5: 23-34.
15. Niv Y. Доксициклин в эрадикационной терапии Helicobacter pylori — систематический обзор и метаанализ. Пищеварение . 2016; 93: 167-173.
16. Георгопулос С.Д., Ксироучакис Э., Мартинес-Гонсалес Б. и др. Рандомизированное клиническое испытание, сравнивающее десятидневную сопутствующую и последовательную терапию для эрадикации Helicobacter pylori в зоне с высокой резистентностью к кларитромицину. Eur J Intern Med . 2016; 32: 84-90.
17. Вильгельм С.М., Джонсон Дж. Л., Кале-Прадхан ПБ. Лечение клопов с помощью клопов: роль пробиотиков в качестве дополнительной терапии для Helicobacter pylori . Энн Фармакотер . 2011; 45: 960-966.
18. Szajewska H, Horvath A, Piwowarczyk A. Мета-анализ: влияние добавок Saccharomyces boulardii на скорость эрадикации Helicobacter pylori и побочные эффекты во время лечения. Алимент Фармакол Тер .2010; 32: 1069-1079.
19. Moayyedi PM, Lacy BE, Andrews CN, et al. Клинические рекомендации ACG и CAG: лечение диспепсии. Ам Дж. Гастроэнтерол . 2017; 112: 988-1013.
20. Кац П.О., Герсон Л.Б., Вела М.Ф. Рекомендации по диагностике и лечению гастроэзофагеальной рефлюксной болезни. Ам Дж. Гастроэнтерол . 2013; 108: 308-328.
Чтобы прокомментировать эту статью, свяжитесь с [email protected].
.