симптомы, лечение, что это такое, мелких ветвей, признаки, причины, классификация, диагностика
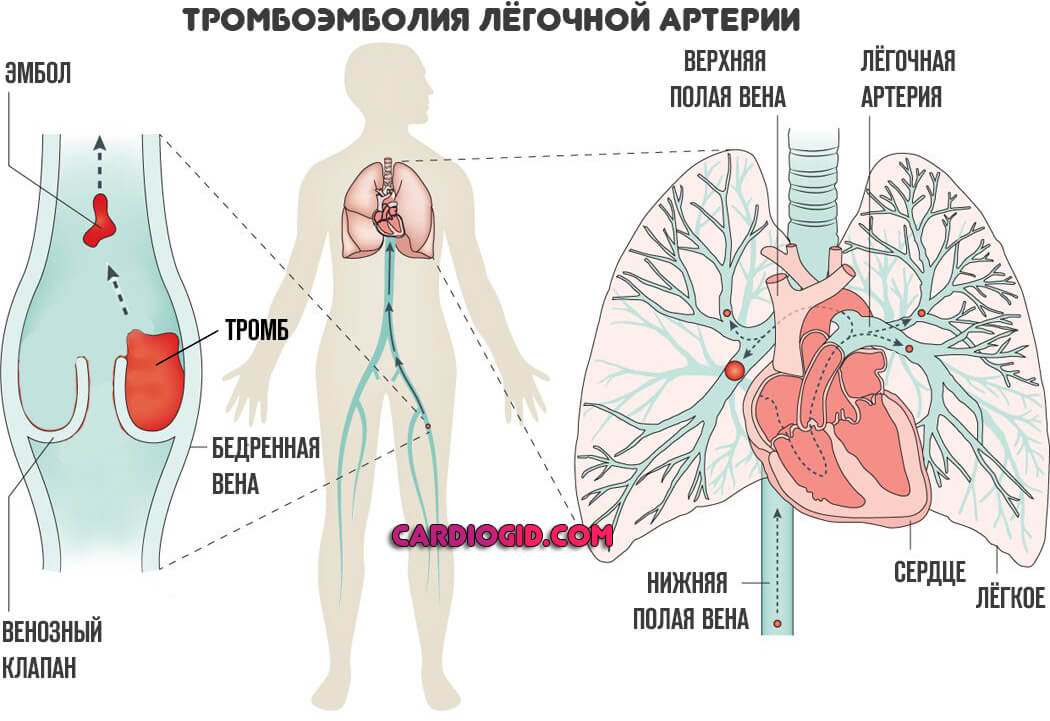
Тромбоэмболия легочной артерии (ТЭЛА) — это осложнение тромбоза вен, создающееся в результате перекрытия тромбом магистрального ствола кровеносного сосуда или его ветвей, доставляющих кровь из сердца в легкие. Указанное состояние часто становится причиной смерти больных, страдающих тяжелыми патологиями, связанными с тромбообразованием. Согласно медицинской статистике, в последние десятилетия частота развития тромболегочной болезни многократно увеличилась.


Причины развития
При развитии легочной тромбоэмболии венозная кровь не поступает в легкие для газообмена. Это негативно отражается на всем организме человека, он испытывает кислородное голодание. Давление в артерии повышается, создавая дополнительную нагрузку на правый желудочек сердца, что может привести к острой сердечной недостаточности.
Часто закупорка сосудов происходит тромбом, сформированным в нижних конечностях в результате тромбоза. С током крови эмбол переносится в легкое и осуществляет блокировку сосудов. Могут спровоцировать ТЭЛА тромбы из верхних конечностей, полости живота, сердца.
Главной причиной тромбоэмболии легочной артерии надо считать тромбоз глубоких вен ног. Данное заболевание может быть связано:
- с нарушением кровотока из-за малоподвижности человека;
- с повышением свертываемости крови, чему способствуют заболевания — онкология, тромбофилия, сердечная недостаточность и др.;
- с повреждением стенки сосуда, происходящих из-за травм, во время операций, воспалительных процессов и пр.
Другими причинами появления эмболии легочной артерии являются наличие таких тяжелых патологий, как ишемическая болезнь сердца, инфаркт миокарда, инфекционный эндокардит, ревматизм и др.
Факторами, способствующими возникновению ТЭЛА, надо считать:
- пожилой и старческий возраст;
- беременность и осложненные роды;
- лишний вес;
- курение;
- прием гормональных противозачаточных средств;
- наличие родственника с тромбозом вен;
- любое хирургическое вмешательство.
В редких случаях при формировании ТЭЛА причины могут быть связаны с длительным нахождением в обездвиженном положении.
Классификация
Для постановки правильного диагноза, установления степени тяжести патологии и выбора эффективной тактики лечения используется развернутая классификация ТЭЛА, отражающая все стороны проявления патологии.
В зависимости от локализации, легочная эмболия подразделяется на левостороннюю, правостороннюю, двухстороннюю.


Закупорка может происходить на уровне мелких, крупных или промежуточных кровеносных сосудов.
Течение легочной тромбоэмболии носит хронический, острый или рецидивирующий характер.
Медики, опираясь на клиническую картину развития болезни, выделяют:
- Инфарктную пневмонию, представляющую тромбоэмболию мелких ветвей легочной артерии.
- Острое легочное сердце, при котором болезнь поражает крупные ветви кровеносных сосудов легких.
- Рецидивирующую ТЭЛА мелких ветвей.
В зависимости от объема пораженных легочных кровеносных сосудов, заболевание может принимать массивную или не массивную форму. Указанная характеристика напрямую влияет на степень тяжести патологии.
Симптомы и внешние проявления
Легочная эмболия не имеет специфических симптомов заболевания. Ее клиническая картина многообразна, может зависеть от следующих факторов:
- степени тяжести болезни;
- скорости развития патологических процессов в легких;
- проявлений патологии, спровоцировавшей данное осложнение.
При поражении 25% сосудов легких, функции главных органов сохраняются, клиника не выражена. У больного наблюдается только одышка.
При увеличении объема исключенных из общего кровотока проблемных кровеносных сосудов можно наблюдать следующие симптомы тромбоэмболии легочной артерии:
- загрудинные острые или сдавливающие боли;
- одышку;
- увеличение ЧСС;
- кашель с кровянистой мокротой;
- грудные хрипы;
- посинение или бледность кожи;
- лихорадку.
ТЭЛА часто маскируется под тяжелые заболевания — воспаление легких, инфаркт миокарда и др. Патология может быть не выявлена при жизни больного.
Легочная эмболия в большинстве случаев характеризуется наличием синдромов, связанных с мозговыми, дыхательными, кардиальными нарушениями.
Мозговые нарушения
Симптомы ТЭЛА при нарушении мозгового кровообращения наблюдаются при тяжелой массивной форме заболевания. К ним можно отнести:
- гипоксию;
- головокружение;
- обмороки;
- шум в ушах;
- судороги;
- слабость;
- нарушение сознания;
- коматозное состояние.
Кардиальная симптоматика
Закупорка легочного сосуда ведет к снижению насосной функции сердца. В результате резко понижается артериальное давление в системе. Могут наблюдаться признаки ателектаза, инфаркта миокарда.
Для компенсации данного состояния увеличивается частота сердечных сокращений (ЧСС) до 100 и выше ударов в минуту. Симптомы легочной эмболии кардиальной направленности:
- сильная тахикардия;
- сжимающая боль в груди;
- шум в сердце;
- гипотензия;
- пульсирующее набухание вен шеи и солнечного сплетения из-за переполнения их кровью;
- шок.
Дыхательные нарушения
Неизменным признаком эмболии легких является постоянная одышка, свидетельствующая о легочной недостаточности. Происходит увеличение частоты дыхания. У больных наблюдается посинение кожных покровов.


С развитием бронхоспастического синдрома и формирования очагов инфаркта легких возникают свистящие хрипы, непродуктивный кашель, боль в груди, повышается температура тела.
Диагностика
Диагностика ТЭЛА включает:
- детальную беседу с больным по поводу жалоб на состояние здоровья, наличия патологии у близких родственников и пр.
- физикальное обследование с выявлением повышенной температуры тела, пониженного АД, выявления одышки, прослушивание хрипов, шума в сердце;
- ЭКГ;
- эхокардиоскопию;
- рентгенографию органов грудной клетки;
- ангиографию легочных сосудов с применением контрастного вещества;
- МРТ;
- КТ;
- вентиляционно-перфузионное сканирование;
- УЗИ вен нижних конечностей;
- биохимический анализ крови.
Медики при диагностике тромбоэмболии часто испытывают затруднения, т. к. клиника указанной патологии может возникать при других тяжелых заболеваниях.
Для подтверждения правильного диагноза существуют специальные шкалы для оценки вероятности и степени тяжести ТЭЛА.
В ходе полного обследования выявляются тромбы и участки поврежденных артерий в легких, патологические изменения сердца и другие признаки болезни.
Как лечить
Лечение ТЭЛА может быть:
- консервативное;
- малоинвазивное;
- оперативное.
Оно преследует цели:
- экстренное выведение больного из состояния, угрожающего его жизни;
- устранение тромбов в артериях;
- снятие симптоматики заболевания;
- восстановление функциональности легких и сердца.
Тактика и вид лечения подбирается врачом с учетом степени тяжести болезни, сопутствующих заболеваний, индивидуальных особенностей больного.
Медикаментозное лечение
Медикаментозное лечение тромбоэмболии легочной артерии производится при помощи антикоагулянтов — медицинских препаратов, активно влияющих на факторы сворачиваемости крови. Данные средства растворяют имеющиеся тромбы, снижают риск их образования.
Распространенными антикоагулянтами считаются препараты — Варфарин и Гепарин. Последний вводится больному подкожно или внутривенно. Варфарин применяется перорально. Но их длительное применение может вызвать тяжелые последствия — кровотечения, кровоизлияние в мозг, тошноту, рвоту и др. При приеме данных препаратов следует контролировать сворачиваемость крови при помощи коагулограммы.


Сегодня лечить ТЭЛА можно более безопасными эффективными препаратами. К ним относятся — Апиксабан, Дабигатран, Ривароксабан.
Хирургическое вмешательство
При тяжелых формах легочной эмболии лечение консервативное становится неэффективным. Для спасения жизни больного требуется применение радикальных мер. Показаниями для операционного вмешательства при ТЭЛА следует считать:
- массивную форму заболевания;
- неэффективность терапии;
- нарушение общего кровообращения;
- рецидив и др.
Эмболия легких устраняется при помощи следующих видов хирургических вмешательств:
- эмболэктомия, при которой производится удаление тромба;
- тромбэндартерэктомия, когда вместе с бляшкой удаляется внутренняя стенка кровеносного сосуда.
Операции сложные, происходящие со вскрытием грудной клетки больного и переходом на временное искусственное кровоснабжение организма.
Указанные вмешательства продолжительны по времени, требуют участия специалистов высокого класса — торакальных хирургов и кардиохирургов.
Сегодня для устранения тромба часто применяются щадящие хирургические вмешательства:
- катетерная эмболэктомия;
- катетерный тромболизис при помощи медикаментов — стрептокиназы, альтеплазы, урокиназы.
Манипуляции проводятся при помощи специального катетера через небольшие проколы кожи. По магистральным венам катетер подводится к месту тромба, где под постоянным компьютерным наблюдением производится его удаление.
Установка кава-фильтра
Кава-фильтр представляет собой специальную ловушку в виде сетки, предназначенную для оторвавшихся тромбов. Приспособление устанавливается в нижней полой вене и служит в профилактических целях для защиты от эмболов легочной артерии и сердца.
При установке кава-фильтра применяются малоинвазивные методы лечения в виде эндоваскулярного вмешательства. Специалист через небольшой прокол на коже с использованием катетера по венам доставляет в требуемое место сетку, где расправляет и закрепляет ее. Катетер выводится наружу. Магистральными венами при установке ловушки считаются большая подкожная, яремная или подключичная вены.
Манипуляции проводятся под небольшим наркозом и продолжаются не более часа. После этого больному прописывается на 2 суток постельный режим.
Осложнения и прогнозы врачей
Легочная эмболия имеет неблагоприятный прогноз течения, который зависит от своевременности выявления, грамотного лечения, наличия других тяжелых патологий. При неблагоприятном развитии ТЭЛА смертность составляет более 60%. Больные умирают из-за развившихся осложнений со стороны дыхательной и сердечно-сосудистой систем.
Частыми осложнениями указанного заболевания надо считать:
- инфаркт легкого;
- пневмонию;
- пневмоторакс;
- абсцесс легочной ткани;
- эмпиему;
- плеврит;
- рецидив;
- остановку сердца и др.
Профилактика
Снизить риск возникновения эмболии легочной артерии у людей, склонных к тромбообразованию, поможет:
- сбалансированное питание;
- использование компрессионного белья;
- применение антикоагулянтов;
- избавление от вредных привычек — курения, злоупотребления алкоголем;
- ведение активного образа жизни;
- избавление от лишнего веса.
Состояние больных, страдающих тяжелыми хроническими патологиями (сердечной недостаточностью, сахарным диабетом, варикозным расширением вен и др.), находящихся длительное время после оперативного вмешательства на постельном режиме должны строго контролироваться специалистами.
симптомы, лечение, профилактика в домашних условиях
Антикоагулянтные препараты. В большинстве случаев лечение состоит из антикоагулянтных препаратов (также называемых разжижителей крови). Антикоагулянты снижают способность крови к свертыванию и предотвращают образование тромбов в будущем. Антикоагулянтные препараты включают Варфарин, Гепарин, низкомолекулярный Гепарин и Фондапаринукс.Варфарин выпускается в форме таблеток и принимается внутрь (перорально).
Гепарин является жидким лекарственным средством и вводится либо внутривенно, либо подкожно, чтобы медленнее высвобождаться в кровь.
Низкомолекулярный гепарин вводится подкожно. Его применяют один или два раза в день даже дома.
Фондапаринукс – это новое лекарство, которое вводится подкожно, один раз в день.
Как и в случае с любыми лекарствами, важно, чтобы вы понимали, как и когда принимать антикоагулянты, и следовали рекомендациям врача. Тип назначенного вам лекарства, продолжительность приема и последующий мониторинг зависят от диагноза. Обязательно соблюдайте все рекомендации, приходите на запланированные последующие посещения врача и сдавайте анализы, чтобы можно было внимательно следить за реакцией на лекарство.
На фоне приема антикоагулянтов, врач будет часто проводить анализы крови, такие как:
- оценка протромбинового времени – он поможет врачу определить, как быстро сворачивается ваша кровь и нужно ли менять дозу лекарства: этот тест используется для контроля вашего состояния, если вы принимаете антикоагулянты дома;
- активированный частичный тромбопластин (АЧТВ) – измеряет время, необходимое для свертывания крови: этот тест используется для контроля состояния, если вы принимаете Гепарин;
- анализ анти-Ха или уровень гепарина – измеряет уровень низкомолекулярного гепарина в крови – обычно нет необходимости использовать этот тест, если у вас нет лишнего веса, заболеваний почек или беременности.
Тромбоэмболия легочной артерии и ее ветвей. Лечение
Лечение ТЭЛА является сложной задачей. Болезнь возникает неожиданно, быстро прогрессирует, вследствие чего врач имеет в своем распоряжении минимум времени, чтобы определить тактику и метод лечения больного. Во-первых, не может быть стандартных схем лечения ТЭЛА. Выбор метода определяется локализацией эмбола, степенью нарушения легочной перфузии, характером и выраженностью гемодинамических нарушений в большом и малом круге кровообращения. Во-вторых, лечение ТЭЛА не может быть ограничено только ликвидацией эмбола в легочной артерии. Не следует упускать из виду и источник эмболизации.
Неотложная помощь
Мероприятия неотложной помощи при ТЭЛА можно условно разделить на три группы:
1) поддержание жизни больного в первые минуты ТЭЛА;
2) устранение смертельных рефлекторных реакций;
3) ликвидация эмбола.
Поддержание жизни в случаях клинической смерти больных осуществляется прежде всего проведением реанимации. К первоочередным мероприятиям относятся борьба с коллапсом при помощи прессорных аминов, коррекция кислотно-щелочного состояния, эффективная оксигенобаротерапия. Одновременно необходимо начать тромболитическую терапию нативными препаратами стрептокиназы (стрептодеказа, стрептаза, авелизин, целеаза и др.).
Находящийся в артерии эмбол вызывает рефлекторные реакции, в силу чего тяжелые расстройства гемодинамики наступают нередко и при немассивной ТЭЛА. Для устранения болевого синдрома внутривенно вводятся 4-5 мл 50%-ного раствора анальгина и 2 мл дроперидола или седуксена. При необходимости применяются наркотики. При выраженном болевом синдроме аналгезия начинается с введения наркотиков в комбинации с дроперидолом или седуксеном. Помимо обезболивающего эффекта при этом подавляется чувство страха смерти, уменьшаются катехоламинемия, потребность миокарда в кислороде и электрическая нестабильность сердца, улучшаются реологические свойства крови и микроциркуляция. С целью уменьшения артериолоспазма и бронхоспазма применяются эуфиллин, папаверин, но-шпа, преднизолон в обычных дозах. Ликвидация эмбола (основа патогенетического лечения) достигается тромболитической терапией, начатой сразу же после установления диагноза ТЭЛА. Относительные противопоказания к тромболитической терапии, имеющиеся у многих больных, не являются препятствием для ее применения. Высокая вероятность летального исхода оправдывает риск лечения.
При отсутствии тромболитических препаратов показано постоянное внутривенное введение гепарина в дозе 1000 ЕД в час. Суточная доза составит 24 000 ЕД. При таком способе введения значительно реже наступают рецидивы ТЭЛА, надежнее предупреждается ре-тромбоз.
При уточнении диагноза тромбоэмболии легочной артерии, степени окклюзии легочного кровотока, локализации эмбола выбирается консервативный или хирургический метод лечения.
Консервативное лечение
Консервативный метод лечения тромбоэмболии легочной артерии в настоящее время является основным и включает в себя следующие мероприятия:
1. Обеспечение тромболизиса и остановка дальнейшего тромбообразования.
2. Снижение легочной артериальной гипертензии.
3. Компенсация легочной и правосердечной недостаточности.
4. Устранение артериальной гипотонии и выведение больного из коллапса.
5. Лечение инфаркта легкого и его осложнений.
6. Адекватное обезболивание и десенсибилизирующая терапия.
Схема консервативного лечения тромбоэмболии легочной артерии в наиболее типичном виде может быть представлена следующим образом:
1. Полный покой больного, лежачее положение больного с приподнятым головным концом при отсутствии коллапса.
2. При болях в груди и сильном кашле введение анальгетиков и спазмолитиков.
3. Кислородные ингаляции.
4. При коллапсе проводится весь комплекс лечебных мероприятий острой сосудистой недостаточности.
5. При сердечной слабости назначаются гликозиды (строфантин, коргликон).
6. Антигистаминные средства: димедрол, пипольфен, супрастин и др.
7. Тромболитическая и антикоагулянтная терапия. Действующим началом тромболитических препаратов (стрептазы, авелизина, стрептодеказы) является продукт обмена веществ гемолитического стрептококка — стрептокиназа, которая, активизируя плазминоген, образует с ним комплекс, способствующий появлению плазмина, растворяющего фибрин непосредственно в тромбе. Введение тромболитических препаратов, как правило, производится в одну из периферических вен верхних конечностей или в подключичную вену. Но при массивных и субмассивных тромбоэмболиях наиболее оптимальным является введение их непосредственно в зону тромба, окклюзирущего легочную артерию, что достигается зондированием легочной артерии и подведением катетера под контролем рентгеновского аппарата к тромбу. Введение тромболитических препаратов непосредственно в легочную артерию быстрее создает их оптимальную концентрацию в области тромбоэмбола. Кроме того, при зондировании одновременно производится попытка фрагментации или туннелирования тромбоэмболов с целью быстрейшего восстановления легочного кровотока. Перед введением стрептазы в качестве исходных данных определяются следующие показатели крови: фибриноген, плазминоген, протромбин, тромбиновое время, время свертывания крови, длительность кровотечения. Последовательность введения лекарственных средств:
1. Внутривенно струйно вводится 5000 ЕД гепарина и 120 мг преднизолона.
2. Внутривенно капельно в течение 30 мин вводится 250 000 ЕД стрептазы (пробная доза), разведенной в 150 мл физиологического раствора, после чего вновь исследуются перечисленные выше показатели крови.
3. При отсутствии аллергической реакции, что свидетельствует о хорошей переносимости препарата, и умеренном изменении контрольных показателей начинается введение лечебной дозы стрептазы из расчета 75 000-100 000 ЕД/ч, гепарина 1000 ЕД/ч, нитроглицерина 30 мкг/мин. Примерный состав раствора для инфузии:
|
I %-ный раствор нитроглицерина |
4,0 мл |
|
гепарин |
20 000 ЕД |
|
стрептаза |
1 500 000 ЕД |
|
0,9%-ный раствор хлористого натрия |
400,0 мл |
Раствор вводится внутривенно капельно со скоростью 20 мл/ч.
4. Во время введения стрептазы внутривенно струйно каждые 6 ч вводится 120 мг преднизолона. Продолжительность введения стрептазы (24-96 ч), определяется индивидуально.
По окончании лечения тромболитиками больной переводится на лечение поддерживающими дозами гепарина по 25 000-45 000 ЕД в сутки внутривенно или подкожно в течение 3-5 суток под контролем показателей времени свертывания и длительности кровотечения.
В последний день введения гепарина назначаются непрямые антикоагулянты (пелентан, варфарин), суточная доза которых подбирается таким образом, чтобы протромбиновый индекс удерживался в пределах (40-60%), международное нормализованное отношение (MHO) — 2,5. Лечение непрямыми антикоагулянтами может при необходимости продолжаться в течение длительного времени (до трех-шести месяцев и более ).
Абсолютные противопоказания к тромболитической терапии:
1. Нарушенное сознание.
2. Внутричерепные и спинномозговые образования, артериовенозные аневризмы.
3. Тяжелые формы артериальной гипертонии с явлениями нарушения мозгового кровообращения.
4. Кровотечения любой локализации, исключая кровохарканье, обусловленное инфарктом легкого.
5. Беременность.
6. Наличие потенциальных источников кровотечения (язва желудка или кишечника, оперативные вмешательства в сроки от 5 до 7 дней, состояние после аортографии).
7. Недавно перенесенные стрептококковые инфекции (острый ревматизм, острый гломерулонефрит, сепсис, затяжной эндокардит).
8. Недавняя черепно-мозговая травма.
9. Предшествующий геморрагический инсульт.
10. Известные нарушения свертывающей системы крови.
11. Необъяснимая головная боль или нарушение зрения на протяжении последних 6 недель.
12. Черепно-мозговые или спинномозговые операции на протяжении последних двух месяцев.
13. Острый панкреатит.
14. Активный туберкулез.
15. Подозрение на расслаивающую аневризму аорты.
16. Острые инфекционные заболевания на момент поступления.
Относительные противопоказания к тромболитической терапии:
1. Обострение язвенной болезни желудка и 12-перстной кишки.
2. Ишемические или эмболические инсульты в анамнезе.
3. Прием непрямых антикоагулянтов на момент поступления.
4. Серьезные травмы или хирургические вмешательства более двух недель назад, но не более двух месяцев;
5. Хроническая неконтролируемая артериальная гипертензия (диастолическое АД более 100 мм рт. ст.).
6. Тяжелая почечная или печеночная недостаточность.
7. Катетеризация подключичной или внутренней яремной вены.
8. Внутрисердечные тромбы или клапанные вегетации.
При витальных показаниях следует выбирать между риском заболевания и риском терапии.
Наиболее частыми осложнениями при применении тромболитических и антикоагулянтных препаратов являются кровотечения и аллергические реакции. Их профилактика сводится к тщательному выполнению правил применения этих препаратов. При наличии признаков кровотечения, связанных с применением тромболитиков, внутривенно капельно вводятся:
- эпсилон-аминокапроновая кислота — 150-200 мл 50%-ного раствора;
- фибриноген — 1-2 г на 200 мл физиологического раствора;
- хлористый кальций — 10 мл 10%-ного раствора;
- свежезамороженная плазма. Внутримышечно вводятся:
- гемофобин — 5-10 мл;
- викасол — 2-4 мл 1%-ного раствора.
При необходимости показано переливание свежецитратной крови. При аллергической реакции вводится преднизолон, промедол, димедрол. Антидотом гепарина является протамин-сульфат, который вводится в количестве 5-10 мл 10%-ного раствора.
Среди препаратов последнего поколения необходимо отметить группу тканевых активаторов плазминогена (альтеплаза, актилизе, retavase), которые активируются, связываясь с фибрином, и способствуют переходу плазминогена в плазмин. При использовании этих препаратов фибринолиз повышается только в тромбе. Альтеплазу вводят в дозе 100 мг по схеме: болюсное введение 10 мг в течение 1-2 мин, затем в течение первого часа — 50 мг, в последующие два часа — оставшиеся 40 мг. Еще более выраженным литическим действием обладает retavase, которую применяют в клинической практике с конца 1990-х годов. Максимальный литический эффект при ее применении достигается в течение первых 30 мин после введения (10 ЕД + 10 ЕД внутривенно). Частота кровотечений при использовании тканевых активаторов плазминогена значительно меньше, чем при применении тромболитиков.
Проведение консервативного лечения возможно лишь тогда, когда у больного сохраняется возможность обеспечения относительно устойчивого кровообращения в течение нескольких часов или суток (субмассивная эмболия или эмболия мелких ветвей). При эмболии ствола и крупных ветвей легочной артерии эффективность консервативного лечения составляет лишь 20-25%. В этих случаях методом выбора является хирургическое лечение — эмболотромбэктомия из легочной артерии.
Хирургическое лечение
Первую успешную операцию при тромбоэмболии легочной артерии провел ученик Ф. Тренделенбурга М. Киршнер в 1924 г. Многие хирурги делали попытки эмболотромбэктомии из легочной артерии, но число больных, умерших во время операции, было значительно больше, чем ее перенесших. В 1959 г. К. Vossschulte и Н. Stiller предложили выполнить эту операцию в условиях временной окклюзии полых вен трансстернальным доступом. Методика обеспечивала широкий свободный доступ, быстрый подход к сердцу и устранение опасной дилатации правого желудочка. Поиск более безопасных способов эмболэктомии привел к использованию общей гипотермии (P. Allison et al., 1960 г.), а затем и искусственного кровообращения (Е. Sharp, 1961 г.; D. Cooley et al., 1961 г.). Общая гипотермия не получила распространения из-за дефицита времени, зато использование искусственного кровообращения открыло новые горизонты в лечении этого заболевания.
В нашей стране методику эмболэктомии в условиях окклюзии полых вен разработали и успешно применяют B.C. Савельев и соавт. (1979 г.). Авторы считают, что легочная эмболэктомия показана тем, кому угрожает смерть от острой сердечно-легочной недостаточности или развития тяжелой постэмболической гипертензии малого круга кровообращения.
В настоящее время оптимальными методами эмболэктомии при массивной тромбоэмболии легочной артерии являются:
1 Операция в условиях временной окклюзии полых вен.
2. Эмболэктомия через главную ветвь легочной артерии.
3. Оперативное вмешательство в условиях искусственного кровообращения.
Применение первой методики показано при массивной эмболии ствола или обеих ветвей легочной артерии. В случае преимущественного одностороннего поражения более оправдана эмболэктомия через соответствующую ветвь легочной артерии. Основным показанием к проведению операции в условиях искусственного кровообращения при массивной эмболии легочной артерии является распространенная дистальная окклюзия сосудистого русла легких.
B.C. Савельев и соавт. (1979 и 1990 гг.) выделяют абсолютные и относительные показания к эмболотромбэктомии. К абсолютным показаниям они относят:
- тромбоэмболию ствола и главных ветвей легочной артерии;
- тромбоэмболию главных ветвей легочной артерии при стойкой гипотензии (при давлении в легочной артерии ниже 50 мм рт. ст.)
Относительными показаниями служат тромбоэмболия главных ветвей легочной артерии при стабильной гемодинамике и выраженной гипертензии в легочной артерии и правых отделах сердца.
Противопоказаниями к эмболэктомии они считают:
- тяжелые сопутствующие заболевания с неблагоприятным прогнозом, например рак;
- заболевания сердечно-сосудистой системы, при которых успех операции сомнителен, а риск ее не оправдан.
Ретроспективный анализ возможностей эмболэктомии у больных, умерших от массивной эмболии, показал, что на успех можно рассчитывать лишь в 10-11% случаев и даже при удачно выполненной эмболэктомии не исключена возможность повторной эмболии. Следовательно, основным направлением в решении проблемы должна быть профилактика. ТЭЛА — не фатальное состояние. Современные методы диагностики венозных тромбозов позволяют прогнозировать опасность возникновения тромбоэмболии и осуществить ее профилактику.
Перспективным следует считать метод эндоваскулярной роторной дезобструкции легочной артерии (ЭРДЛА), предложенный Т. Schmitz-Rode, U. Janssens, Н.Н. Schild и соавт. (1998 г.) и примененный у достаточно большого числа больных Б.Ю. Бобровым (2004 г.). Эндоваскулярная роторная дезобструкция главных и долевых ветвей легочной артерии показана больным с массивной тромбоэмболией, особенно при ее окклюзивной форме. Выполняется ЭРДЛА во время ангиопульмонографии с помошью специального устройства, разработанного Т. Schmitz-Rode (1998 г.). Принцип метода заключается в механическом разрушении массивных тромбоэмболов в легочных артериях. Он может быть самостоятельным способом лечения при противопоказаниях или неэффективности тромболитической терапии или предшествовать тромболизису, что значительно увеличивает его эффективность, сокращает время его проведения, позволяет снизить дозировку тромболитических препаратов и способствует снижению количества осложнений. Выполнение ЭРДЛА противопоказано при наличии эмбола-наездника в легочном стволе из-за риска окклюзии главных ветвей легочной артерии за счет миграции фрагментов, а также у больных с неокклюзивной и периферической формой эмболии ветвей легочной артерии.
Профилактика тромбоэмболии легочной артерии
Профилактика тромбоэмболии легочной артерии должна проводиться в двух направлениях:
1) предупреждение возникновения периферических венозных тромбозов в послеоперационном периоде;
2) при уже сформировавшемся венозном тромбозе необходимо проводить лечение для предотвращения отрыва тромботических масс и их забрасывания в легочную артерию.
Для предупреждения послеоперационных тромбозов вен нижних конечностей и таза применяют два вида профилактических мероприятий: неспецифическую и специфическую профилактику. Неспецифическая профилактика включает в себя борьбу с гиподинамией в кровати и улучшение венозного кровообращения в системе нижней полой вены. Специфическая профилактика периферических венозных тромбозов подразумевает применение антиагрегантов и антикоагулянтов. Специфическая профилактика показана тромбоопасным больным, неспецифическая — всем без исключения. Подробно профилактика венозных тромбозов и тромбоэмболических осложнений изложена в следующей лекции.
При уже сформировавшемся венозном тромбозе применяются хирургические методы противоэмболической профилактики: тромбэктомия из илиокавального сегмента, пликация нижней полой вены, перевязка магистральных вен и имплантация кава-фильтра. Наиболее эффективной профилактичекой мерой, получившей в последние три десятка лет широкое применение в клинической практике, является имплантация кава-фильтра. Наибольшее распространение получил зонтичный фильтр, предложенный К. Mobin-Uddin в 1967 г. На протяжении всех лет применения фильтра предложены различные модификации последних: «песочные часы», нитиноловый фильтр Саймона, «птичье гнездо», стальной фильтр Гринфилда. Каждый из фильтров имеет свои достоинства и недостатки, однако ни один из них не отвечает полностью всем предъявляемым к ним требованиям, что и определяет необходимость дальнейших поисков. Преимуществом фильтра «песочные часы», применяемого в клинической практике с 1994 г., являются высокая эмболоулавливающая активность и низкая способность к перфорации нижней полой вены. Основные показания к имплантации кава-фильтра:
- эмболоопасные (флотирующие) тромбы в нижней полой вене, подвздошных и бедренных венах, осложненные или неосложненные ТЭЛА;
- массивная тромбоэмболия легочной артерии;
- повторные ТЭЛА, источник которых не установлен.
Во многих случаях имплантация кава-фильтраов более предпочтительна, чем оперативные вмешательства на венах:
- у больных пожилого и старческого возраста при тяжелых сопутствующих заболеваниях и высокой степени риска операции;
- у больных, недавно перенесших оперативное вмешательство на органах брюшной полости, малого таза и забрюшинного пространства;
- при рецидиве тромбоза после тромбэктомии из илиокавального и подвздошно-бедренного сегментов;
- у больных с гнойными процессами в брюшной полости и в за-брюшинном пространстве;
- при резко выраженном ожирении;
- при беременности сроком более 3 мес;
- при старых неокклюзивных тромбозах илиокавального и подвздошно-бедренного сегментов, осложненных ТЭЛА;
- при наличии осложнений со стороны ранее установленного кава-фильтра (слабая фиксация, угроза миграции, неправильный выбор размера).
Наиболее серьезным осложнением установки кава-фильтров является тромбоз нижней полой вены с развитием хронической венозной недостаточности нижних конечностей, которая наблюдается, по данным разных авторов, в 10-15% случаев. Однако, это невысокая цена за риск возможной ТЭЛА. Кава-фильтр сам по себе может быть причиной тромбоза нижней полой вены (НПВ) при нарушении свертывающих свойств крови. Возникновение тромбоза в поздние после имплантации фильтра сроки (спустя 3 мес) может быть обусловлено и захватом эмболов, и тромбогенным воздействием фильтра на сосудистую стенку и протекающую кровь. Поэтому в настоящее время в ряде случаев предусматривается установка временного кава-фильтра. Имплантация постоянного кава-фильтра целесообразна при выявлении нарушений свертывающей системы крови, создающих опасность рецидива ТЭЛА в течение жизни пациента. В других случаях возможна установка временного кава-фильтра сроком до 3 мес.
Имплантация кава-фильтра не решает полностью процесс тромбообразования и тромбоэмболических осложнений, поэтому постоянная медикаментозная профилактика должна проводиться на протяжении всей жизни пациента.
Серьезным последствием перенесенной тромбоэмболии легочной артерии, несмотря на проводимое лечение, является хроническая окклюзия или стеноз главного ствола или главных ветвей легочной артерии с развитием тяжелой гипертензии малого круга кровообращения. Это состояние называется «хроническая постэмболическая легочная гипертензия» (ХПЭЛГ). Частота развития данного состояния после тромбоэмболии артерий крупного калибра составляет 17%. Ведущим симптомом ХПЭЛГ является одышка, которая может наблюдаться даже в покое. Больных часто беспокоит сухой кашель, кровохарканье, боли в сердце. Как результат гемодинамической недостаточности правых отделов сердца наблюдаются увеличение печени, расширение и пульсация яремных вен, асцит, желтуха. По мнению большинства клиницистов, прогноз при ХПЭЛГ крайне неблагоприятный. Продолжительность жизни таких больных, как правило, не превышает трех-четырех лет. При выраженной клинической картине постэмболических поражений легочных артерий показано оперативное вмешательство — интимотромбэктомия. Исход вмешательства определяется длительностью заболевания (срок окклюзии не более 3 лет), уровнем гипертензии в малом круге (систолическое давление до 100 мм рт. ст.) и состоянием дистального легочно-артериального русла. Адекватным оперативным вмешательством можно достигнуть регрессии тяжелой ХПЭЛГ.
* * *
Тромбоэмболия легочной артерии является одной из наиболее важных проблем медицинской науки и практического здравоохранения. В настоящее время имеются все возможности для того, чтобы снизить летальность от этого заболевания. Нельзя мириться с мнением, что ТЭЛА есть нечто фатальное и непредотвратимое. Накопленный опыт говорит об обратном. Современные методы диагностики позволяют прогнозировать исход, а своевременное и адекватное лечение дает успешные результаты.
Необходимо совершенствовать методы диагностики и лечения флеботромбозов как основного источника эмболии, повышать уровень активной профилактики и лечения пациентов хронической венозной недостаточностью, выявлять больных с факторами риска и своевременно их санировать.
Избранные лекции по ангиологии. Е.П. Кохан, И.К. Заварина
Опубликовал Константин Моканов
Тромбоэмболия лёгочной артерии — Инновационный сосудистый центр
Кратко о заболевании
Тромбоэмболия легочной артерии (ТЭЛА) — критическое состояние, вызываемое закупоркой лёгочной артерии или её ветвей тромбами, которые образуются чаще в крупных венах нижних конечностей или таза и переносятся током крови через правые отделы сердца в легочные артерии, вызывая тяжелое нарушение кровообращения. Тромбоэмболия является одной из основных причин смерти в современном мире, уступая лишь болезням сердца, онкологии и травмам.
Основным способом снижения смертности от тромбоэмболии легких является ее предупреждение. Для этого пациенты перед хирургическими операциями, при отеках ног и после длительного вынужденного сидячего положения должны быть обследованы с помощью ультразвукового сканирования вен на предмет развития скрытого венозного тромбоза.
Лечение массивной ТЭЛА эффективно только в случае, если больной пережил 6 часов после начала заболевания. Основу лечения составляет тромболитическая терапия, которую лучше всего проводить локально с помощью ангиографического катетера непосредственно в тромб. Если пациент переносит тромбэмболию, то в последствии у него может развиться хроническое повышение давления в легочной артерии — легочная гипертензия, которая приводит к развитию хронической сердечной недостаточности.
Методы лечения в ИСЦ
Наш Центр занимается лечением тромбоэмболии по технологии Aspirex. Зонд, вставляемый через крупную вену, позволяет быстро и эффективно удалить эмбол и обладает высокой аспирационной (то есть всасывающей) способностью.Кроме того, мы устанавливаем через нижнюю полую вену специальные кава-фильтры, улавливающие и останавливающие тромбы.
Причины возникновения и факторы риска
Основным источником эмболии при ТЭЛА является тромбоз в системе нижней полой вены. Самым частым источником тромбоэмболов становится тромбоз глубоких вен (ТГВ) нижних конечностей. Он встречается у 84-93% случаев. В 3-7% имеет место тромбоз в полостях правой половины сердца и системе верхней полой вены. Иногда источник ТЭЛА установить не удается. Частота легочной эмболии при тромбозе крупных вен голеней составляет 46%, бедренных — 67%, подвздошных вен -77%. Чаще всего ТЭЛА развивается через 3-7 дней после ТГВ. Очень часто тромбоз и эмболия протекают бессимптомно. В 75% случаев при венозных тромбозах нижних конечностей обнаруживают скрытую ТЭЛА, а в 80% случаев лёгочной эмболии находят не проявившиеся клинически венозные тромбозы. Имеющиеся данные позволяют утверждать, что почти у 25% населения мира в тот или иной период жизни возникают венозные тромбоэмболические осложнения.
В России венозный тромбоз ежегодно возникает у 240 тысяч человек, у 100 тысяч из которых развивается ТЭЛА. При инсультах и ортопедических вмешательствах тромбозы глубоких вен развиваются более чем у половины пациентов. В условиях многопрофильного стационара ТЭЛА наблюдается у 15-20 из 1000 лечившихся пациентов; с ней связано 10% госпитальной летальности. При абдоминальных хирургических вмешательствах и операциях на грудной клетке ТГВ встречается у каждого третьего пациента. В терапевтических стационарах тромбозы вен возникают у 17% больных, а при инфаркте миокарда они выявляются в 22% случаев. ТЭЛА является причиной смерти у 2-5 женщин на каждые 1000 родов.
Наиболее частой причиной тромбоэмболии становится отрыв тромба и закупорка им части или всего русла легочной артерии. Тромб, чаще всего, образуется в венах таза или ног, поэтому основную причину развития заболевания составляют тромбоз, варикоз или воспаление глубоких вен нижних конечностей. Риск ТЭЛА сильно возрастает при тромбофлебите. Иногда сгустки крови образуются в венах рук или в правой части сердца.
Факторами риска являются:
- беременность и первые 6 недель после родов,
- прием гормональных препаратов (влияющих на свёртываемость крови),
- рак и некоторые виды лечения рака, такие как химиотерапия,
- повреждение сосудистой стенки вследствие травм и переломов,
- хирургия, особенно абдоминальная или ортопедическая хирургия, такая как хирургия бедра или колена,
- сердечно-сосудистые заболевания, такие как фибрилляция предсердий, сердечная недостаточность, сердечный приступ или инсульт,
- прием гормональных препаратов,
- унаследованные нарушения свёртывания крови, например, тромбофилия,
- воспалительное заболевание кишечника,
- аутоиммунные заболевания, такие как волчанка или антифосфолипидный синдром,
- размещение венозных катетеров, кардиостимуляторов или имплантируемых дефибрилляторов,
- жир, который может вырваться из костного мозга, когда кость ломается (хотя это случается относительно редко).
- Семейная история тромбозов,
- Ожирение,
- Пожилой возраст,
- Использование оральных контрацептивов, особенно курильщиками после 35 лет,
- Длительный период постельного режима или сидения в течение длительного времени, например, в самолете или автомобиле.
Клинические формы заболевания
В зависимости от клинической симптоматики выделяют несколько форм тромбоэмболии легочной артерии.
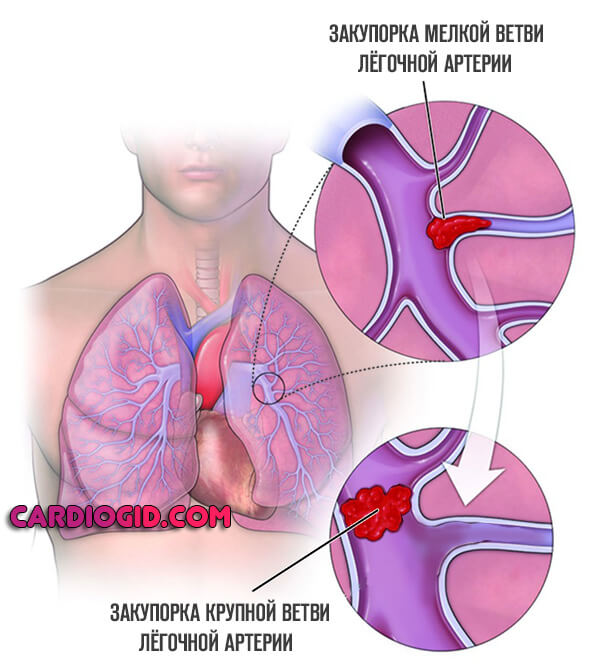
Тромбоэмболия мелких ветвей (немассивная) — может проявляться как послеоперационная пневмония, с небольшой одышкой, болью в грудной клетки. Непосредственно жизни не угрожает, но требует тщательного обследования и профилактики повторных эмболий.
Субмассивная ТЭЛА — возникает при закупорке долевых ветвей легочной артерий, проявляется признаками выраженной сердечно-сосудистой недостаточности, которая может нарастать или на фоне лечения уменьшаться, приводя в итоге к развитию хронической легочной гипертензии.
Массивная тромбоэмболия легочной артерии характеризуется крайне-тяжелым состоянием пациента, с низким артериальным давление, одышкой, нарастанием явлений острой сердечно-сосудистой недостаточности. При массивной ТЭЛА чаще всего наступает смерть в ближайшее время после первых признаков заболевания.
Симптомы
Легочная эмболия требует неотложной медицинской помощи. Симптомы зависят от того, насколько заблокирована легочная артерия и от общего состояния человека. Они тяжелее и ярче выраженнее, если есть серьезное заболевание, такое как хроническая обструктивная болезнь легких или болезнь коронарных артерий.Симптомы ТЭЛА могут напоминать инфаркт миокарда или воспаление лёгких.
Основными симптомами лёгкой формы болезни, с которыми пациенты обращаются к врачу, являются отдышки, боли в грудной клетке и кашель. В более серьёзных случаях наблюдается частый слабый пульс, повышенная температура тела, бледность и потери сознания.
Симптомы обычно начинаются внезапно и могут включать:
- Внезапная одышка.
- Резкая боль в груди, часто усугубляется кашлем или движением.
- Боль в спине.
- Кашель с или без кровавой мокроты.
- Чрезмерное потоотделение.
- Быстрый пульс или дыхание.
- Посинение губ.
- Синеватая кожа (цианоз).
При физическом осмотре легкие обычно нормальные. Иногда шум трения плевры может слышаться на пораженные участки легких (в основном в ЧП с инфаркт). Плевральный выпот иногда представить, что это экссудативный, выявляемого специалистами компании перкуссионный звук, слышно дыхание и вокального резонанса. Нагрузку на правый желудочек могут быть обнаружены в левой парастернальной тя, громкий легочный компонент второго сердечного звука, и/или повышение давления в яремной Вене.[2] Низкосортная лихорадка может присутствовать, в частности если связанные легочные кровоизлияния или инфаркт.[17]
А мелкие легочные эмболы, как правило, селят в более отдаленных районах без коллатеральное кровообращение они чаще всего становятся причиной инфаркта легких и небольших выпотов (оба из которых являются болезненные), но не гипоксии, одышки или нестабильности гемодинамики, таких как тахикардия. Больше пес, который, как правило, селят в центре, как правило, причиной диспноэ, гипоксия, пониженное давление, быстрое сердцебиение и обмороки, но часто безболезненно, потому что нет инфаркта легких за счет коллатерального кровообращения. Классическая презентация для PE с плевритной боли, одышка и тахикардия, скорее всего, вызвана большой фрагментированный эмболия в результате большой и малый пес. Таким образом, малый пес часто пропускал, потому что они вызывают только плевритной боли без каких-либо других выводов и большой пес часто пропускала, потому что они безболезненны и имитировать другие условия часто вызывает изменений на ЭКГ и небольшие подъемы уровней тропонина и БНП.[18]
Осложнения
В некоторых случаях, не выявленная своевременно тромбоэмболия развивается в хроническую тромбоэмболическую лёгочную гипертензию. Она проявляется в виде слабости, повышенной утомляемости и отдышек после физических нагрузок.Более серьёзными осложнениями ТЭЛА являются остановка сердца, инфаркт лёгкого с развитием пневмонии или плеврит.
Внезапная смерть.
Профилактика и прогноз
Во избежание тромбоэмболии необходимо предотвратить факторы риска: ожирение, курение, варикоз. Людям, принимающим препараты со стероидными гормонами, следует регулярно проверять свертываемость крови.Если в семье есть родственники с факторами риска, необходимо наблюдаться у терапевта на предмет возможного возникновения тромбов. Летальность ТЭЛА без лечения составляет 18-33%, при диагностике и оказании медицинской помощи – 8%,а 75-90% пациентов умирают в течение первых нескольких часов после эмболии.
После истечения периода повышенного риска (примерно одна неделя) потребуются месяцы или годы, чтобы полностью решить проблему. У вас может развиться легочная гипертензия со значительными последствиями для жизни, включая одышку и непереносимость физической нагрузки.
ТЭЛА — это не самостоятельное заболевание, а осложнение большинства болезней с образованием тромбов и занимает третье место по смертности среди всех заболеваний.
Тромбоэмболия легочной артерии (ТЭЛА): симптомы, лечение, неотложная помощь
Острые нарушения нормального кровотока на общем, генерализованном уровне встречаются в кардиологической практике в 10-15% случаев от всех опасных процессов.
В зависимости от тяжести расстройства, риски гибели больного отличаются. Прогноз можно дать только после оценки и диагностики, иногда позже, по окончании первичных терапевтических мероприятий.
Тромбоэмболия легочной артерии — это острое нарушение кровотока, движения жидкой соединительной ткани от сердца в малый круг для обогащения ее кислородом и дальнейшего выброса в аорту.
Отклонение от нормы провоцирует катастрофические последствия.
Непосредственная причина патологического процесса — закупорка легочной артерии каким-либо объектом. Таковым выступает сгусток крови (подавляющее большинство случаев), пузырек воздуха (обычно в результате неудачного ятрогенного, врачебного вмешательства).
Самостоятельный регресс состояния невозможен. При неполной закупорке отмечают общее нарушение гемодинамики (кровотока), и острые проблемы с кардиальной деятельностью.
Обнаруживается гипоксия всех структур (кислородное голодание), что в краткосрочной перспективе приводит к смерти больного. Полная закупорка заканчивается стремительным летальным исходом, в течение нескольких секунд.
Симптомы неспецифичны. Диагностика больших трудностей не представляет, если знать, что искать и куда смотреть. Терапия срочная, в условиях стационара.
Механизм развития
Как было сказано, непосредственная причина ТЭЛА — закупорка легочной артерии инородной структурой. Здесь возможны варианты. Чаще всего встречаются тромбы (кровяные сгустки).
Подобные образования формируются в верхних, нижних конечностях, самом сердце (несколько реже). Они не всегда жестко прикреплены к месту собственного формирования.
При воздействии негативного фактора: надавливания, удара, сгусток может оторваться и двинуться по кровеносному руслу. Далее все зависит от его размеров и от воли случая.
Тромб остановится в той или иной части сосудистой сети, вполне вероятно, что именно в легочной артерии.
Далее схема стандартная. Образуется механическое препятствие для тока крови по малому кругу.
Изначально она бедна кислородом (венозная), и недостаточно насыщается O2, а значит такое же скудное количество поступает в сердце, выбрасывается в аорту и циркулирует по организму.
По понятным причинам, обеспечить потребности клеток в кислороде такая кровь не может. Потому наступает выраженное голодание на фоне расстройства клеточного дыхания.
В краткосрочной перспективе это приводит к ишемии головного мозга, полиорганной недостаточности. Возможно наступление гибели в течение считанных дней. Если же происходит тотальная закупорка легочной артерии, смерть наступает почти мгновенно.
Закупорка пузырьком воздуха
Помимо тромбов, возможно проникновение в кровеносное русло пузырька воздуха. Спонтанно такое происходит редко. Намного чаще в результате врачебного вмешательства.
Вопреки распространенному заблуждению, капельница после того, как излилось лекарство, не способна спровоцировать проникновения воздуха в кровеносное русло из-за перепада артериального давления и показателя в системе.
Потому и используются специальные стойки и высоким расположением стеклянной тары с лекарством.
Более того, для развития эмболии требуется не менее 5 кубиков газа или свыше. Такое количество может проникнуть только при проведении открытых операций или катетеризации артерий. Встречается подобный вариант много реже.
Далее все развивается по идентичному пути. Закупорка, нарушение клеточного дыхания, возможная гибель больного без проведения качественного и срочного лечения. В некоторых случаях кардинальным образом повлиять на ситуацию невозможно вообще.
Симптомы
Клиническая картина зависит от массы факторов: точной локализации очага непроходимости, размеров блокирующего агента, давности патологического процесса.
Речь не идет о тотальной закупорке. Потому как последнее, что успевает почувствовать человек — острая боль в грудной клетке, нехватка воздуха. Затем наступает обморок и смерть.
В остальных ситуациях обнаруживаются четкие симптомы легочной тромбоэмболии. Верификация диагноза проводится срочно, инструментальными методами.
Клиника ТЭЛА включает в себя такие проявления:
- Болевой синдром в грудной клетке. Тянущий, давящий. Мучительный для пациента, поскольку отличается стойкость. Хотя и при средней интенсивности. Продолжительность дискомфорта неопределенно высокая.
Спонтанного регресса почти нет. На вдохе, особенно глубоком, сила боли резко возрастает. Потому пациент старается контролировать естественный процесс, что приводит гипоксии и усугублению.
- Кашель. Непродуктивный в том плане, что отсутствует мокрота. Зато обильно отходит кровь в виде пенистых сгустков алого цвета.
Это указание на возросшее давление в малом круге, разрывы сосудов. Неблагоприятный признак. Почти во всех случаях указывает на тромбоэмболию легочных артерий.
Исключить прочие заболевания, вроде туберкулеза, рака не сложно — признаки при ТЭЛА развиваются внезапно, дополняются нетипичными для онкологии или инфекции моментами.
- Повышение температуры тела. До фебрильных отметок (38-39 градусов), встречаются и другие уровни.
Купирование симптома антипиретическими медикаментами не дает выраженной эффективности, потому как процесс имеет центральное происхождение. Провокаторы — не инфекционные агенты. Это рефлекторная реакция тела.
- Одышка в состоянии покоя. При физической активности доходит до критических отметок, делая невозможным даже передвижения медленным шагом, перемену положения тела.
Снижение толерантности к физической нагрузке развивается стремительно, что характерно для легочной тромбоэмболии и нетипично для прочих сердечнососудистых заболеваний.
- Тахикардия. Организм увеличивает число сердечных сокращений, чтобы обеспечить все ткани кислородом.
Качество подменяется количеством: кровь двигается быстрее, чтобы хоть как то малыми частями обогащаться кислородом.
Система работает на износ. Очень скоро процесс сменяется обратным. ЧСС снижается. Сначала незначительно, обнаруживается легкая брадикардия (около 70 ударов) затем переходит в критическую фазу.
- Падение уровня артериального давления. Также постепенное, но выраженное. Обнаруживается по мерее прогрессирования декомпенсации.
- Головная боль. Тревожное проявление. Указывает на постепенное нарушение питания церебральных структур. Может в краткосрочной перспективе закончиться обширным инсультом и смертью больного.
- Вертиго. Невозможность ориентироваться в пространстве. Человек занимает вынужденное положение лежа, меньше двигается, чтобы не провоцировать усиления симптома. Также называется головокружением.
- Тошнота, рвота. Встречаются сравнительно редко
- Бледность кожных покровов, слизистых оболочек.
- Цианоз носогубного треугольника. Образование синеватого кольца вокруг рта. Типичный симптом кардиальной дисфункции и кислородного голодания организма.
Если смотреть на проблему во временном аспекте и отслеживать прогрессирование, средние сроки от возникновения первых симптомов тромбоэмболии легочной артерии до летального исхода, составляет от 3 до 12 дней. Редко больше. Возможно меньше.
Стадии тромбоэмболии
Процесс претерпевает три фазы.
- Первая — компенсация. Возникают минимальные проявления, который трудно увязать со столь опасным неотложным состоянием. Кашель, небольшая одышка, тошнота, боли в грудной клетке и некоторые другие моменты.
- Вторая — частичная компенсация. Организм все еще может нормализовать состояние, но полного восстановления функций добиться не получается. Отсюда выраженная клиника, с кровохарканием, церебральными проявлениями, нарушениями кардиальной активности.
- Третья — полная декомпенсация. Тело не в состоянии скорректировать работу основных систем. Без медицинской помощи летальный исход в перспективе ближайших часов, максимум суток гарантирован.
ТЭЛА мелких ветвей легочной артерии протекает менее активно в субъективном плане, самочувствии.
Исход идентичен, но сроки развития такового больше вдвое. Диагностика сложна, потому как клиника минимальна.
Первая помощь
Проводится в срочном порядке. На фоне острого периода сделать нельзя ничего. Смерть наступит в любом случае. В течение считанных секунд человек умрет, даже если находится в условиях полностью оборудованной реанимации. Это аксиома.
То же касается декомпенсированной фазы, когда шансы «вытащить человека» еще имеются. Главное действие — вызов скорой медицинской помощи. Самостоятельно скорректировать нарушение невозможно.
До приезда бригады нужно уложить больного. Голова должна находиться в чуть приподнятом состоянии. Этого можно добиться, поставив подушку или использовав импровизированный валик.
Сильного анатомического перегиба быть не должно, чтобы не спровоцировать инсульт. Все в меру.
Препараты использовать нельзя. Не известно, как организм среагирует на пероральное введение медикаментов. Возможно усугубление состояния.
Обеспечивается полный покой. Неотложная помощь при ТЭЛА предполагает размещение рук и ног на уровне ниже сердца. То есть не стоит подкладывать под конечности валики и именно поэтому положение лежа самое предпочтительное.
Рекомендуется каждые 10 минут измерять артериальное давление, частоту сердечных сокращений. Фиксировать динамику. По прибытии специалистов сообщить о состоянии пострадавшего, рассказать об объективных показателях.
Дальше можно только сопроводить больного в стационар, чтобы по надобности помочь с перемещением, передать необходимые сведения.
Причины
Легочная эмболия — полифакторное состояние. Моментов развития огромное количество: от избыточной массы тела и переизбытка холестерина в организме (хотя формой атеросклероза ТЭЛА и не является, связь здесь косвенная), до патологий сердечнососудистой системы.
Чаще всего имеют место такие причины:
- Артериальная гипертензия. Может спровоцировать разрыв сосуда, образование тромба. А в дальнейшем его перемещение по организму.
- Колоссальные риски создают инфаркт, инсульт (геморрагического типа).
- Травмы, крупные гематомы. Вероятность мала, но она присутствует. Особенно, если нарушены реологические свойства крови.
- Чрезмерная густота жидкой соединительной ткани.
Повышают вероятность процесса возраст от 55 лет, принадлежность к мужскому полу, пристрастие к курению, спиртному, наркотическим веществам, бесконтрольное применение препаратов различных групп (особенно опасны оральные контрацептивы и противовоспалительные).
Сказывается недостаток сна, неправильное питание. Определенную роль играет семейный анамнез, склонность к гематологическим заболеваниям (изменение свойств крови).
Диагностика
У врачей не так много времени, если речь идет об «остром» пациенте. Заболевание определяется первичными методами: визуальной оценкой состояния пострадавшего, данными, которые сообщили родственники или люди, оказавшие помощь.
Более тщательное обследование возможно после стабилизации состояния или на фоне начальных стадий нарушения.
Перечень мероприятий:
- Устный опрос. Проводится для объективизации жалоб, выстраивания понятной, однозначной клинической картины.
- Сбор анамнеза. Перенесенные, текущие патологии, семейная история. Используется для выявления вероятного происхождения лёгочной эмболии.
- Исследование сатурации кислорода, Д-димера (показатель всегда повышается при наличии рассматриваемого состояния, это надежный дифференциальный и верифицирующий уровень).
- Ангиография легочной артерии. Посредством стандартного рентгена или МРТ (предпочтительно).
- Возможно проведение вентиляционно-перфузионного сканирования для оценки характера газообмена в организме. Это довольно редкая методика, которая требует оборудования и квалификации докторов и среднего медицинского персонала.
- Эхокардиография. Используется для срочного сканирования кардиальных структур, обнаружения органических расстройств, функциональных нарушений, таких как рост давления в сосудах.
Независимо от того, какая форма тромбоза легочной артерии имеет место, времени на долгие раздумья нет. В лучшем случае, присутствует 12-20 часов, а полноценную диагностику и верификацию заболевания. Потому альтернатив госпитализации не существует.
Лечение
Методик не так много. Однако и те, что имеются, дают неплохие шансы на успех.
На ранних этапах проводится медикаментозное воздействие. Используются средства – антикоагулянты. Они разжижают кровь (говоря условно, на самом же деле эффект от этих медикаментов косвенный, не вдаваясь в подробности).
В первые 6 дней проводятся внутривенные инъекции Гепарина. Это опасный препарат с большим количеством побочных эффектов. Потому нужен постоянный контроль над состоянием пациента.
При положительной динамике, уже после выхода из стен кардиологического отделения прописываются более мягкие аналоги в таблетированной форме. Например, Варфарин, Мареван, Варфарекс. На усмотрение специалиста.
Продолжительность курса терапии после острого состояния — 3-12 месяцев. Сроки определяются доктором. Самовольно корректировать длительность нельзя.
При благоприятном сценарии, удается добиться стойкой редукции симптомов в первые же дни. Тотальное восстановление наблюдается спустя несколько месяцев. Больной считается условно выздоровевшим.
Неотложные состояния или тяжелые формы эмболии легочной артерии требуют применения тромболитиков. Например, Урокиназы, Стрептокиназы в ударных дозировках. Они растворяют кровяные сгустки, способствуют нормализации тока жидкой соединительной ткани.
Крайняя методика предполагает проведение полостной операции по механическому устранению тромба (эмболэктомии). Это опасный, тяжелый способ. Но вариантов нет, к тому же риски оправданы. Пациенту и так грозит гибель, хуже точно не будет.
В дальнейшем рекомендуется тщательно провериться на предмет сердечнососудистых, гормональных патологий, чтобы устранить первопричину тромбоэмболии. Это позволит свести к минимуму вероятность рецидива.
Прогноз и последствия
При раннем обнаружении патологического процесса, исход условно благоприятный в 70% случаев. Поздняя диагностика снижает процент до 20 и менее. Полная закупорка сосуда летальна всегда, шансов на выживание нет.
Основные последствия, они же причины гибели — обширный инфаркт, инсульт. При медленном прогрессировании помимо описанных осложнений встречается полиорганная дисфункция, в результате недостаточного снабжения кислородом.
Профилактика
Специфических мер нет. Достаточно придерживаться правил здравого смысла.
- Отказаться от курения. Спиртного и наркотиков. Также не принимать никакие препараты без назначения специалиста. Они могут оказать влияние на свертываемость крови, ее текучесть.
- Избегать тяжелых травм. Гематомы требуют обязательного лечения.
- При наличии соматических заболеваний, особенно влияющих на реологические свойства жидкой соединительной ткани, обращаться к врачу для назначения лечения.
- Пить достаточное количество воды в сутки: не менее 1.5 литров. При отсутствии противопоказаний — 1.8-2. Это не жесткий показатель. Важно исходить из массы тела.
- Придерживаться оптимального уровня физической активности. Хотя бы 1-2 часа гулять на свежем воздухе.
Тромбоэмболия лёгочной артерии — летальное во многих случаях состояние. Оно требует срочной диагностики и стремительного лечения. Иначе последствия будут плачевными.
что это такое, описание симптомов, признаки, лечение и профилактика, прогноз
Тромбоэмболия легочной артерии (ТЭЛА) – это блокировка просвета ствола или мелких ветвей сосуда тромбами, что приводит к гипертензии малого круга кровообращения, легочному сердцу (часто декомпенсированному).

Общие сведения
Тромбоэмболия легочной артерии составляет около 117 случаев на 100 000 населения в год, что обусловливает развитие около 350 000 случаев заболевания (как минимум, 100000 в США) и 85 000 летальных исходов в год. Она развивается преимущественно у взрослых. В результате ТЭЛА прекращается кровоснабжение легочной ткани. Развитие ТЭЛА происходит часто стремительно и может привести к гибели больного.
От ТЭЛА умирает 0,1% населения земного шара ежегодно. Около 90% больным, умершим от ТЭЛА, во время не был установлен правильный диагноз, и не было проведено необходимое лечение. Среди причин смерти населения от сердечно-сосудистой заболеваний ТЭЛА стоит на третьем месте после ИБС и инсульта.
ТЭЛА может приводить к летальному исходу при некардиологической патологии, возникая после операций, полученных травм, родов. При своевременном оптимальном лечении ТЭЛА наблюдается высокий показатель снижения уровня смертности до 2 – 8%.
Этиология и патогенез
Почти все легочные эмболы возникают по причине тромбов в венах ног или таза (тромбоз глубоких вен). Риск эмболизации увеличивается, если тромбы расположены проксимальнее вен голени. Тромбоэмболы могут также образоваться в венах рук или центральных венах грудной полости (они возникают при применении центральных венозных катетеров или в результате компрессионного синдрома верхней апертуры грудной клетки).
Факторы риска тромбоза глубоких вен и легочной тромбоэмболии сходны у детей и взрослых и включают:
- Условия, ухудшающие венозный отток, в том числе постельный режим и госпитализацию с отсутствием прогулок;
- Условия, вызывающие повреждение эндотелия или его дисфункцию;
- Нарушения, обуславливающие гиперкоагуляцию (тромбофилия)
Факторы риска развития тромбоза глубоких вен и тромбоэмболии легочной артерии:
Возраст >60 лет.
Рак.
Гормональную модуляцию:
- Модуляторы эстрогеновых рецепторов (например, ралоксифен, тамоксифен).
- Экзогенные эстрогены и прогестины, включая оральные контрацептивы и терапию эстрогенами.
- Экзогенный тестостерон.
Сердечная недостаточность.
Иммобилизация.
Постоянные венозные катетеры.
Миелопролиферативные заболевания (повышенная вязкость крови).
Нефротический синдром.
Ожирение.
Беременность/послеродовой период.
Тромбоэмболия в анамнезе.
Серповидноклеточная анемия.
Курение.
Инсульт.
Тромботические нарушения (тромбофилии):
- Антифосфолипидный синдром
- Недостаточность антитромбина III
- Лейденская мутация V фактора (резистентность к активированному протеину С)
- Гепарин-индуцированная тромбоцитопения
- Наследственные фибринолитические дефекты
- Гипергомоцистинемия
- Увеличение уровня фактора VIII
- Увеличение уровня фактора XI
- Увеличение уровня фактора Виллебранда
- Пароксизмальная ночная гемоглобинурия
- Недостаточность протеина С
- Недостаточность протеина S
- Вариант гена протромбина G20210A
- Недостаточность или нарушение функции ингибитора пути тканевого фактора
Травма и/или хирургическое вмешательство.
Другие заболевания, связанные с ограниченнием подвижности, повреждением вены или гиперкоагуляцией.
Патофизиология
После развития тромбоз глубоких вен тромбы могут отделяться и перемещаться по венозной системе, попадая в правые отделы сердца, а затем – в легочные артерии, где они частично или полностью окклюзируют один или более сосудов. Последствия будут зависеть от размера и количества эмболов, исходного состояния легких, способности тромболитической системы организма растворять тромбы и от того, насколько хорошо функционирует правый желудочек (ПЖ). Смерть, наступающая вследствие правожелудочковой недостаточности.
Небольшие эмболы не оказывают немедленного воздействия; многие из них моментально начинают лизироваться и через несколько часов или дней растворяются. Большие эмболы могут привести к рефлекторному увеличению вентиляции легких (тахипноэ), гипоксемии в результате вентиляционно-перфузионного несоответствия, и низкому содержанию кислорода в венозной крови за счет снижения сердечного выброса, ателектазам вследствие альвеолярной гиперкапнии и патологическому изменению сурфактанта, а также к увеличению резистентности легочных сосудов, обусловленному механической обструкцией и вазоконстрикцией. Большинство тромбов, даже средних размеров, растворяется за счет эндогенного лизиса, данный физиологический эффект постепенно затухает в течение часов или дней. Некоторые эмболы резистентны к лизису и могут группироваться и персистировать.
Классификация
В зависимости от локализации тромбоэмболического процесса различают следующие варианты ТЭЛА:
- массивная (тромб локализуется в главном стволе или основных ветвях легочной артерии)
- эмболия сегментарных или долевых ветвей легочной артерии
- эмболия мелких ветвей легочной артерии (чаще двусторонняя).
В зависимости от объема отключенного артериального кровотока при ТЭЛА выделяют формы:
- малую (поражены менее 25% легочных сосудов) — сопровождается одышкой, правый желудочек функционирует нормально
- субмассивную (субмаксимальную — объем пораженных сосудов легких от 30 до 50%), при которой у пациента отмечается одышка, нормальное артериальное давление, правожелудочковая недостаточность мало выражена
- массивную (объем отключенного легочного кровотока более 50%) — наблюдается потеря сознания, гипотония, тахикардия, кардиогенный шок, легочная гипертензия, острая правожелудочковая недостаточность
- смертельную (объем отключенного кровотока в легких более 75%).
ТЭЛА может протекать в тяжелой, среднетяжелой или легкой форме.
Клиническое течение ТЭЛА может быть:
- острейшим (молниеносным), когда наблюдается моментальная и полная закупорка тромбом главного ствола или обеих основных ветвей легочной артерии. Развивается острая дыхательная недостаточность, остановка дыхания, коллапс, фибрилляция желудочков. Летальный исход наступает за несколько минут, инфаркт легких не успевает развиться.
- острым, при котором отмечается быстро нарастающая обтурация основных ветвей легочной артерии и части долевых или сегментарных. Начинается внезапно, бурно прогрессирует, развиваются симптомы дыхательной, сердечной и церебральной недостаточности. Продолжается максимально 3 – 5 дней, осложняется развитием инфаркта легких.
- подострым (затяжным) с тромбозом крупных и средних ветвей легочной артерии и развитием множественных инфарктов легких. Продолжается несколько недель, медленно прогрессирует, сопровождаясь нарастанием дыхательной и правожелудочковой недостаточности. Могут возникать повторные тромбоэмболии с обострением симптомов, при которых нередко наступает смертельный исход.
- хроническим (рецидивирующим), сопровождающимся рецидивирующими тромбозами долевых, сегментарных ветвей легочной артерии. Проявляется повторными инфарктами легких или повторными плевритами (чаще двусторонними), а также постепенно нарастающей гипертензией малого круга кровообращения и развитием правожелудочковой недостаточности. Часто развивается в послеоперационном периоде, на фоне уже имеющихся онкологических заболеваний, сердечно-сосудистых патологий.
ТЭЛА также может иметь и нетромбогенный генез.
Симптомы ТЭЛА
Клиническая картина зависит от массы факторов: точной локализации очага непроходимости, размеров блокирующего агента, давности патологического процесса. Речь не идет о тотальной закупорке. Потому как последнее, что успевает почувствовать человек — острая боль в грудной клетке, нехватка воздуха. Затем наступает обморок и смерть. В остальных ситуациях обнаруживаются четкие симптомы легочной тромбоэмболии. Верификация диагноза проводится срочно, инструментальными методами.

Клиника ТЭЛА включает в себя такие проявления:
- Болевой синдром в грудной клетке. Тянущий, давящий. Мучительный для пациента, поскольку отличается стойкость. Хотя и при средней интенсивности. Продолжительность дискомфорта неопределенно высокая. Спонтанного регресса почти нет. На вдохе, особенно глубоком, сила боли резко возрастает. Потому пациент старается контролировать естественный процесс, что приводит гипоксии и усугублению.
- Кашель. Непродуктивный в том плане, что отсутствует мокрота. Зато обильно отходит кровь в виде пенистых сгустков алого цвета. Это указание на возросшее давление в малом круге, разрывы сосудов. Неблагоприятный признак. Почти во всех случаях указывает на тромбоэмболию легочных артерий. Исключить прочие заболевания, вроде туберкулеза, рака не сложно — признаки при ТЭЛА развиваются внезапно, дополняются нетипичными для онкологии или инфекции моментами.
- Повышение температуры тела. До фебрильных отметок (38-39 градусов), встречаются и другие уровни. Купирование симптома антипиретическими медикаментами не дает выраженной эффективности, потому как процесс имеет центральное происхождение. Провокаторы — не инфекционные агенты. Это рефлекторная реакция тела.
- Одышка в состоянии покоя. При физической активности доходит до критических отметок, делая невозможным даже передвижения медленным шагом, перемену положения тела. Снижение толерантности к физической нагрузке развивается стремительно, что характерно для легочной тромбоэмболии и нетипично для прочих сердечнососудистых заболеваний.
- Тахикардия. Организм увеличивает число сердечных сокращений, чтобы обеспечить все ткани кислородом. Качество подменяется количеством: кровь двигается быстрее, чтобы хоть как то малыми частями обогащаться кислородом. Система работает на износ. Очень скоро процесс сменяется обратным. ЧСС снижается. Сначала незначительно, обнаруживается легкая брадикардия (около 70 ударов) затем переходит в критическую фазу.
- Падение уровня артериального давления. Также постепенное, но выраженное. Обнаруживается по мерее прогрессирования декомпенсации.
- Головная боль. Тревожное проявление. Указывает на постепенное нарушение питания церебральных структур. Может в краткосрочной перспективе закончиться обширным инсультом и смертью больного.
- Вертиго. Невозможность ориентироваться в пространстве. Человек занимает вынужденное положение лежа, меньше двигается, чтобы не провоцировать усиления симптома. Также называется головокружением.
- Тошнота, рвота. Встречаются сравнительно редко
- Бледность кожных покровов, слизистых оболочек.
- Цианоз носогубного треугольника. Образование синеватого кольца вокруг рта. Типичный симптом кардиальной дисфункции и кислородного голодания организма.
Если смотреть на проблему во временном аспекте и отслеживать прогрессирование, средние сроки от возникновения первых симптомов тромбоэмболии легочной артерии до летального исхода, составляет от 3 до 12 дней. Редко больше. Возможно меньше.
Стадии тромбоэмболии
Процесс претерпевает три фазы.
- Первая — компенсация. Возникают минимальные проявления, который трудно увязать со столь опасным неотложным состоянием. Кашель, небольшая одышка, тошнота, боли в грудной клетке и некоторые другие моменты.
- Вторая — частичная компенсация. Организм все еще может нормализовать состояние, но полного восстановления функций добиться не получается. Отсюда выраженная клиника, с кровохарканием, церебральными проявлениями, нарушениями кардиальной активности.
- Третья — полная декомпенсация. Тело не в состоянии скорректировать работу основных систем. Без медицинской помощи летальный исход в перспективе ближайших часов, максимум суток гарантирован.
ТЭЛА мелких ветвей легочной артерии протекает менее активно в субъективном плане, самочувствии. Исход идентичен, но сроки развития такового больше вдвое. Диагностика сложна, потому как клиника минимальна.
Диагностика
Диагноз тромбоэмболии устанавливают на основании жалоб пациента, врачебного осмотра и с помощью дополнительных методов обследования. Иногда легочную эмболию очень трудно диагностировать, так как ее клиническая картина может быть очень разнообразной и подобной другим заболеваниям.
Для уточнения диагноза проводят:
- Электрокардиографию.
- Анализ крови на Д-димер – вещество, уровень которого увеличивается при наличии тромбоза в организме. При нормальном уровне Д-димера тромбоэмболия легочной артерии отсутствует.
- Определение уровня кислорода и углекислого газа в крови.
- Рентгенографию органов грудной полости.
- Вентиляционно-перфузионное сканирование – используется для изучения газообмена и кровотока в легких.
- Ангиографию легочной артерии – рентгенологическое обследование сосудов легких с помощью контрастирования. С помощью этого обследования можно выявить эмболы в легочной артерии.
- Ангиографию легочной артерии с помощью компьютерной или магнитно-резонансной томографии.
- Ультразвуковое обследование вен нижних конечностей.
- Эхокардиоскопию – ультразвуковое исследование сердца.
- Определение сердечных маркеров рассматривается как полезный метод для стратификации риска смерти для пациентов с острой ТЭЛА. Если ТЭЛА является подозреваемой или доказанной, дополнительно может использоваться анализатор сердечных маркеров. Повышенный уровень тропонина является признаком ишемии правого желудочка (или иногда левого желудочка). Повышенные уровни мозгового натрийуретического пептида (BNP) и pro-BNP могут означать дисфункцию правого желудочка, однако эти тесты не являются специфичными для напряжения правого желудочка или ТЭЛА.
- Исследование тромботических расстройств (тромбофилии) должно проводиться для пациентов с ТЭЛА, у которых отсутствуют известные факторы риска, особенно если их возраст < 35 лет, имеющих рецидивирующую ТЭЛА или положительный семейный анамнез.
Диагноз затруднен, поскольку жалобы и симптомы неспецифичны, а диагностические анализы не являются на 100% чувствительными и специфичными. Необходимо учитывать ТЭЛА при дифференциальной диагностике, если имеют место такие неспецифичные симптомы, как одышка, плевритическая боль, кровохарканье, головокружение или обморок. Таким образом, ТЭЛА следует рассматривать в дифференциальной диагностике пациентов с подозрением на:
- Ишемию миокарда
- Сердечная недостаточность
- Обострение ХОБЛ
- Пневмоторакс
- Пневмонию
- Сепсис
- Острый грудной синдром (у пациентов с серповидно-клеточной анемией)
- Острое состояние беспокойства с гипервентиляцией.
Диагностическим ключом может являться клинически значимая тахикардия неизвестной этиологии. ТЭЛА следует подозревать у любого пожилого человека с тахипноэ и нарушением психического статуса.
В качестве начальных диагностических методик используют пульсоксиметрию, рентгеновские снимки и ЭКГ, газовый состав артериальной крови, или оба этих исследования могут помочь исключить другие диагнозы (например, острый инфаркт миокарда).
Рентгенография органов грудной клетки чаще всего не дает специфической информации, но может выявить ателектазы, локальные инфильтраты, подъем половины купола диафрагмы или плевральный выпот. Такие классические симптомы, как локальное отсутствие легочного рисунка (симптом Вестермарка), периферическая клиновидная тень (горб Хэмптона) или расширение правой нисходящей легочной артерии (признак Палла), предполагают наличие ТЭЛА, однако они встречаются редко, поэтому имеют низкую чувствительность и неустановленную специфичность. При рентгенографии грудной клетки также можно исключить пневмонию. Инфаркт легкого по причине ТЭЛА может быть ошибочно принят за пневмонию.
Пульсоксиметрия является удобным и быстрым способом определения оксигенации; гипоксемия часто обнаруживается при ТЭЛА и требует дальнейшего обследования. Определение газового состава артериальной крови может выявить увеличение альвеолярно-артериального градиента по кислороду (А-а) (иногда, так называемый «A-градиент») или гипокапнию; каждый по отдельности или оба признака вместе обладают умеренной чувствительностью в отношении ТЭЛА, но неспецифичны. Газовый анализ крови следует проводить пациентам с одышкой или тахипноэ, у которых при пульсоксиметрии не было выявлено гипоксемии. Показатели насыщения кислородом могут быть нормальными по причине небольших тромбовых бляшек или компенсаторной гипервентиляции; очень низкое парциальное давление CO2 наблюдаемое при определении газового состава артериальной крови, может подтвердить гипервентиляцию.
На ЭКГ часто обнаруживают тахикардию и различные изменения конечной части желудочкового комплекса ST-T, которые не являются специфичными для ТЭЛА ( ЭКГ при ТЭЛА). S1Q3T3 или появление блокады правой ножки пучка Гиса могут свидетельствовать о резком повышении давления в правом желудочке. Эти данные сравнительно специфичны, но малочувствительны и проявляются только у 5% пациентов. Может обнаруживаться отклонение электрической оси вправо (R >S в V1). Также может присутствовать инверсия зубца Т в отведениях V1-V4.
Клиническая вероятность
Клиническая вероятность ТЭЛА может быть оценена при анализе данных ЭКГ и рентгенографии грудной клетки в совокупности с анамнестическими данными и результатами объективного обследования. Клинические шкалы прогнозирования, такие как шкала Уэллса, пересмотренная Женевская шкала, или шкала критериев дифференциальной диагностики легочной эмболии (PERC), могут помочь врачам-консультантам в оценке шансов развития острой ЛЭ. Эти системы присвоения баллов для различных клинических факторов, с совокупными балльными показателями, соответствуют обозначениям вероятности ТЭЛА до тестирования (предтестовой вероятности).
Например, результат шкалы Уэллса классифицируется для ТЭЛА как вероятный или маловероятный. Однако, предположение о том, что ТЭЛА более вероятна, чем другое заболевание, довольно субъективно. Кроме этого, клиническая оценка опытных клиницистов может быть чувствительна, или даже более чувствительна, чем результаты таких шкал. ТЭЛА может быть установлена с большей вероятностью, если как минимум 1 жалоба или симптом, в частности одышка, кровохарканье, тахикардия или гипоксемия, не имеют видимой причины по клиническим или рентгенографическим данным.
Показатели клинической вероятности подсказывают стратегии исследования и интерпретацию результатов исследования. Для пациентов, у которых вероятность возникновения ТЭЛА считается малой, требуются только минимальные дополнительные исследования (такие, как определение D-димера). В таких случаях негативный результат определения D-димера (< 0,4 мкг/мл) является весьма показательным для о отсутствия ТЭЛА. Если существует высокая клиническая настороженность для ТЭЛА, и риск кровотечений низкий, пациентам сразу назначают антикоагулянты, пока диагноз не подтверждается при помощи дополнительных исследований.
Особенности лечения ТЭЛА
Терапию больных с ТЭЛА следует проводить в соответствии с клиническим статусом пациента, объемом эмболизации, наличием сопутствующей сердечно-легочной патологии, уровнем маркеров некроза миокарда (тропонин), а также со степенью дисфункции правых отделов сердца, которую оценивают на основании физикального обследования, ЭКГ и эхоКГ. Пациентам с высоким риском развития неблагоприятных событий необходимо проводить тромболитическую терапию или эмболэктомию для восстановления проходимости магистральных ЛА на фоне введения гепарина для профилактики повторной эмболизации. В то же время пациенты с низким риском нуждаются только в проведении адекватной антикоагулянтной терапии. Чрескожные катетерные вмешательства (интервенционные процедуры) могут стать альтернативой хирургической эмболэктомии у пациентов с высоким риском развития осложнений или у больных с противопоказаниями для тромболитической терапии.
Тромболитическая терапия
Тромболитическая терапия позволяет спасти жизнь больным с кардиогенным шоком на фоне ТЭЛА. Физическое растворение тромба, закрывающего просвет магистральной ЛА, приводит к предотвращению быстропрогрессирующего развития правожелудочковой недостаточности и уменьшению высвобождения серотонина и других нейрогуморальных факторов, способствующих усилению легочной гипертензии.
У больных с легочной гипертензией и низким сердечным выбросом на фоне ТЭЛА проведение тромболитической терапии сопровождается снижением среднего давления в ЛА на 30% и повышением сердечного индекса на 15% уже через 2 ч от ее начала. Через 72 ч повышение сердечного индекса достигает уже 80%, а снижение среднего давления в ЛА — 40%. Отмечено также значительное уменьшение конечно-диастолического размера ПЖ через 3 ч после начала тромболитической терапии. В то же время назначение только гепарина не приводит к изменению вышеуказанных параметров. Системная тромболитическая терапия также способствует растворению тромбов в малом тазу и/или глубоких венах нижних конечностей, которые могут быть источниками рецидивирования ТЭЛА.
Идеальное лекарственное средство прежде всего должно обеспечивать максимальную клиническую эффективность при минимальном риске побочных эффектов. Идеальный фибринолитический препарат для применения у больных с ТЭЛА должен иметь четко определенные показания для применения, отличаться быстротой развития терапевтического эффекта в сочетании с низкой частотой побочных реакций, среди которых наиболее значимыми являются кровотечения, а также оказывать положительное влияние на дальнейший прогноз заболевания. Кроме того, важно, чтобы препарат был удобен и прост в применении, в том числе при подборе режима дозирования, а также обеспечивал разумное соотношение эффективность/стоимость. Такого фибринолитического агента в нашем арсенале сегодня нет.
В клинических исследованиях проведено тестирование нескольких фибринолитических препаратов (альтеплаза, стрептокиназа, урокиназа) для лечения больных с ТЭЛА. Несмотря на некоторые отличия между различными препаратами и режимами их введения в отношении влияния на показатели центральной гемодинамики в ранние сроки, не было установлено достоверных различий между отдельными режимами по влиянию на смертность. По данным последних исследований, введение альтеплазы (100 мг в течение 2 ч) позволяет быстрее достичь тромболитического и гемодинамического эффекта, чем введение урокиназы (4400 МЕ кг/ч в течение 12–24 ч), стрептокиназы (1,5 млн МЕ в течение 2 ч) или альтеплазы (0,6 мг/кг в течение 15 мин). При этом различия между режимами достоверны только в течение первого часа после начала терапии.
В отличие от ИМ терапевтическое окно для эффективного проведения тромболитической терапии у больных с ТЭЛА намного шире и составляет до 14 дней от развития симптомов заболевания. Такая эффективность, вероятно, обусловлена существованием коллатерального бронхиального кровообращения. Таким образом, больных с подозрением на ТЭЛА следует рассматривать в качестве потенциальных кандидатов для проведения тромболитической терапии при развитии новых симптомов заболевания в течение 2 нед, предшествующих госпитализации.
Проведено несколько рандомизированных контролируемых клинических исследований, в которых оценивали эффективность и безопасность тромболитической терапии на фоне назначения гепарина по сравнению с введением гепарина в режиме монотерапии у больных с острой ТЭЛА. Метаанализ 9 из них (суммарно включен 461 больной) не выявил достоверного снижения смертности или повторной эмболизации ЛА при применении фибринолитических средств. Однако снижение частоты развития каждого из неблагоприятных событий практически на 40% при применении тромболитической терапии позволяет предположить необходимость включения большего количества больных для достижения статистически достоверных отличий. Хотя показания к проведению тромболитической терапии при ТЭЛА до сих пор строго не определены, пациенты c массивной ТЭЛА (гемодинамическая нестабильность и дисфункция ПЖ) теоретически должны иметь максимальные преимущества от ее проведения.
До настоящего времени ни один из тромболитических препаратов не продемонстрировал преимуществ перед остальными в плане эффективности лечения больных с ТЭЛА. Однако риск прогрессирования артериальной гипотензии при применении стрептокиназы у больных с массивной ТЭЛА делает назначение альтеплазы и урокиназы более предпочтительным.
Таким образом:
- Терапевтическое «окно» для проведения тромболитической терапии у больных с ТЭЛА составляет до 14 дней от развития симптомов
- Тромболитическая терапия показана всем больным с массивной ТЭЛА
- Большинство противопоказаний для проведения тромболитической терапии при массивной ТЭЛА являются относительными
- С учетом эффективности и безопасности предпочтительным режимом тромболитической терапии при ТЭЛА является системное введение 100 мг альтеплазы в течение 2 ч
- Эффективность тромболитических препаратов у больных с субмассивной ТЭЛА (гипокинезия ПЖ) не доказана, однако ввиду клинической целесообразности может проводиться по усмотрению лечащего врача
- Тромболитическая терапия не показана гемодинамически стабильным больным без признаков перегрузки/дисфункции ПЖ.
Катетер-направленная терапия
При терапии ТЭЛА с использованием управляемого катетера (тромболитики, эмболэктомия) используется катетер, размещенный в легочной артерии для разрушения и/или лизиса тромба. Применяется для лечения массивной ТЭЛА. Показания для лечения субмассивной ТЭЛА в настоящее время разрабатываются. К настоящему времени, исследования, в том числе проспективные рандомизированные клинические испытания, продемонстрировали, что подобный подход ведет к улучшению соотношения ПЖ/ЛЖ за 24 ч по сравнению с только антикоагулянтной терапией. Другие исходы и безопасность катетерной терапии по сравнению с системным тромболизисом в настоящее время исследуются.
Тромболитическая терапия ТЭЛА с использованием катетера, осуществляется посредством стандартной процедуры катетеризации правых отделов сердца/легочной артериографии легочной артерии, и тромболитики доставляются непосредственно в крупные проксимальные эмболы через катетер. Наиболее полно изучен метод с использованием высокочастотного маломощного УЗИ для облегчения доставки тромболитиков. УЗИ ускоряет тромболитический процесс путем разделения нитей фибрина и увеличения проницаемости тромба для литического препарата.
Другие методы включают эмболэктомию с использованием катетер-направленного вихревого всасывания, иногда в сочетании с экстракорпоральным шунтированием. Эмболэктомия с использованием катетер-направленного вихревого всасывания отличается от системного тромболизиса и тромболитической терапии ТЭЛА на основе катетера тем, что не требует большего отверстия катетера, и отсасываемая кровь должна быть перенаправлена обратно в вену (обычно в бедренную). Лучшими кандидатами на процедуру являются пациенты с венозным кавальным фильтром, или транзитным тромбом правого предсердия или правого желудочка, и очень острой проксимальной ТЭЛА. Венозно-артериальная экстракорпоральная мембранная оксигенация (ECMO) может быть использована в качестве процедуры спасения для тяжело больных пациентов с острой ТЭЛА, независимо от того, какие еще методы лечения используются.
Хирургическая эмболэктомия
Хирургическая эмболэктомия показана пациентам с ТЭЛА, у которых, несмотря на симптоматическую терапию, сохраняется артериальная гипотензия (стойкое снижение систолического АД ≤ 90 мм рт.ст. после инфузионной терапии и кислородотерапии или назначения вазопрессоров) или существует угроза остановки сердца или дыхания. Хирургическая эмболэктомия должна рассматриваться в случаях, когда противопоказано использование тромболизиса; в этих случаях может быть также рассмотрена катетер-направленная вихревая эмболэктомия, и, в зависимости от местных ресурсов и клинического опыта, применена перед хирургической эмболэктомии. Хирургическая эмболэктомия по всей вероятности увеличивает выживаемость пациентов с массивной ТЭЛА, но не имеет широкой распространенности. Как и в случае с катетер-опосредованной экстракцией тромба/сгустка, решение о проведении эмболэктомии и выбор техники зависит от наличия местных ресурсов и опыта работы в данном учреждении.
Осложнения
Острая ТЭЛА может служить причиной остановки сердца и внезапной смерти. При срабатывании компенсаторных механизмов пациент сразу не погибает, но при отсутствии лечения очень быстро прогрессируют вторичные гемодинамические нарушения. Имеющиеся у пациента кардиоваскулярные заболевания значительно снижают компенсаторные возможности сердечно-сосудистой системы и ухудшают прогноз.
Прогноз и профилактика
При раннем оказании полного объема помощи пациентам прогноз для жизни благоприятный. При выраженных сердечно-сосудистых и дыхательных нарушениях на фоне обширной ТЭЛА летальность превышает 30%. Половина рецидивов ТЭЛА развивается у пациентов, не получавших антикоагулянты. Своевременная, правильно проведенная антикоагулянтная терапия вдвое снижает риск рецидивов ТЭЛА. Для предупреждения тромбоэмболии необходимы ранняя диагностика и лечение тромбофлебита, назначение непрямых антикоагулянтов пациентам из групп риска.
Источники: krasotaimedicina.ru, msdmanuals.com, cardiogid.com, compendium.com.ua

Редакция сайта
Коллектив авторов с высшим и средним медицинским образованием, имеющих многолетний опыт работы в практической медицине, узкопрофильные специалисты и врачи общей практики.
Тромбоэмболия легочной артерии (ТЭЛА) — симптомы, лечение, профилактика, причины, первые признаки
Что такое тромбоэмболия легочной артерии (ТЭЛА)?
Тромбоэмболия легочной артерии (ТЭЛА) — внезапная остановка кровотока в ветви легочной артерии вследствие закупорки ее кровяным сгустком (тромбом), влекущая за собой прекращение поступления крови в кровоснабжаемый этой ветвью участок легочной ткани. Следует уточнить, что упомянутый тромб является фрагментом другого тромба, образовавшегося и расположенного вне легочной артерии. Состояние же, при котором происходит распространение тромбов по сосудам организма, называют тромбоэмболией.
Новости по теме
ТЭЛА — одно из наиболее распространенных и грозных осложнений многих заболеваний послеоперационного и послеродового периодов, неблагоприятно влияющее на их течение и исход. Внезапная смерть в 1/3 случаев объясняется тромбоэмболией легочной артерии. Умирают около 20% больных с ТЭЛА, причем более половины из них в первые 2 часа после возникновения эмболии.
Причины, приводящие к тромбоэмболии, и что при этом происходит?
Для возможности своего существования организм человека нуждается в кислороде, причем поступление кислорода в организм должно осуществляться непрерывно. Для этого в легких постоянно происходит газообмен. С ветвями легочной артерии в мельчайшие образования легочной ткани, называемые альвеолами, доставляется отработанная организмом венозная кровь. Здесь эта кровь освобождается от углекислого газа, который удаляется из организма во время выдоха, и насыщается кислородом атмосферного воздуха, поступающего в легкие при вдохе. В результате газообмена кровь становится артериальной, насыщенной кислородом и доставляется ко всем органам и тканям организма.
В результате тромбоэмболии участок пораженного легкого практически не кровоснабжается, выключается из газообмена, соответственно через легкие проходит меньшее количество крови, проходящая кровь хуже насыщается кислородом, а это может привести к тому, что к органам дойдет недостаточное количество крови, насыщенной кислородом, в худшем случае к резкому падению артериального давления и шоку. Все это может сопровождаться инфарктом миокарда, ателектазом (спадением части легочной ткани) в легких.
Чаще всего причиной ТЭЛА бывают тромбы, возникшие в глубоких венах и чаще всего в глубоких венах нижних конечностей.
Для образования тромба необходимо наличие трех условий:
- повреждение стенки сосуда;
- замедление тока крови в этом месте;
- повышение свертываемости крови.
Стенка вены может повреждаться при воспалительных заболеваниях, внутривенных инъекциях, травмах.
Условия для замедления кровотока возникают вследствие сердечной недостаточности, длительном вынужденном положении: постельный режим, особенно у больных с заболеваниями легких, инфарктом миокарда, операциями по поводу перелома бедра. И чаще всего у больных с повреждениями спинного мозга. Изредка тромбоэмболия легочных артерий может возникнуть и у здоровых людей, которые долго находятся в вынужденном положении. Например, при перелете на самолете.
Причинами повышения свертываемости крови являются некоторые наследственные нарушения в свертывающей системе крови, прием противозачаточных средств, СПИД.
Также факторами риска возникновения тромбоза глубоких вен, помимо указанных выше, являются: пожилой и старческий возраст; хирургические операции; злокачественные новообразования; варикозное расширение вен ног; беременность и роды; травмы; ожирение; некоторые заболевания (болезнь Крона, эритремия, нефротический синдром, системная красная волчанка, пароксизмальная ночная гемоглобинурия).
Симптомы ТЭЛА
Проявления ТЭЛА зависят от массивности процесса, состояния сердечно-сосудистой системы и легких.
В зависимости от объема поражения сосудов легких ТЭЛА может быть:
- массивная: более 50% сосудов легких;
- субмассивная: от 30 до 50% сосудов легких;
- немассивная: менее 30% сосудов легких.
Самое частое проявление тромбоэмболии легочной артерии — одышка и учащенное дыхание. Одышка возникает внезапно. Больной лучше чувствует себя в положении лежа. Боль в грудной клетке имеет различный характер. У больного могут быть сильные болевые ощущения или дискомфорт в грудной клетке. Изредка возникает кровохарканье. Может появиться цианоз бледность или синюшная окраска носа, губ, ушей вплоть до чугунного оттенка.
Также может наблюдаться учащенное сердцебиение, кашель, холодный пот, сонливость, заторможенность, головокружение, кратковременная или длительная потеря сознания, судороги в конечностях.
Что можете сделать вы?
Если в вашей семье есть родственники с факторами риска, нужно наблюдаться у вашего терапевта на предмет возможного возникновения тромбов.
В случае если вы сталкиваетесь с ситуацией, сопровождающейся перечисленными симптомами необходимо незамедлительно обратиться за медицинской помощью, либо позвонив в скорую помощь, либо, если вы находитесь в стационаре, к доктору.
Даже своевременное распознавание массивной ТЭЛА не всегда обеспечивает эффективную ее терапию. Во избежание летального исхода нужно обратиться за помощью как можно раньше.
Что может сделать врач?
Доктор проведет необходимый осмотр, исследования, включающие ЭКГ, рентгенографию грудной клетки, вентиляционно-перфузионную сцинтиграфию легких (исследование сосудов легких с помощью контрастных веществ), и на этом основании определит объем поражения. В зависимости от объема поражения назначит лечение. В любом случае при подтверждении диагноза пациент должен находиться под наблюдением врача в стационаре.
Обнаружили ошибку? Выделите ее и нажмите Ctrl+Enter.
Легочный фиброз — Диагностика и лечение
Диагностика
Чтобы диагностировать ваше состояние, ваш врач может изучить ваш медицинский и семейный анамнез, обсудить ваши признаки и симптомы, проанализировать любое воздействие пыли, газов и химикатов, а также провести физический осмотр. Во время медицинского осмотра врач с помощью стетоскопа внимательно выслушает ваши легкие, пока вы дышите. Он или она может также предложить один или несколько из следующих тестов.
Визуальные исследования
- Рентген грудной клетки. Рентген грудной клетки показывает изображения вашей грудной клетки. Это может показать типичную для легочного фиброза рубцовую ткань, и это может быть полезно для наблюдения за течением болезни и лечения. Однако иногда рентген грудной клетки может быть нормальным, и могут потребоваться дополнительные тесты, чтобы объяснить вашу одышку.
- Компьютерная томография (КТ). КТ-сканеры используют компьютер для объединения рентгеновских изображений, полученных под разными углами, для получения изображений поперечного сечения внутренних структур тела.Компьютерная томография с высоким разрешением может быть особенно полезна при определении степени повреждения легких, вызванного легочным фиброзом. Кроме того, некоторые виды фиброза имеют характерные особенности.
- Эхокардиограмма. Эхокардиограмма использует звуковые волны для визуализации сердца. Он может создавать неподвижные изображения структур вашего сердца, а также видео, которые показывают, как работает ваше сердце. Этот тест позволяет оценить давление в правой части сердца.
Тестирование функции легких
- Тестирование функции легких. Могут быть проведены несколько типов тестов функции легких. В тесте под названием спирометрия вы быстро и с силой выдыхаете через трубку, подключенную к аппарату. Аппарат измеряет, сколько воздуха могут удерживать ваши легкие и как быстро вы можете вводить и выводить воздух из легких. Для измерения объема легких и диффузионной способности могут проводиться другие тесты.
- Пульсоксиметрия. В этом простом тесте используется небольшое устройство, помещенное на один из ваших пальцев, для измерения насыщения крови кислородом.Оксиметрия может служить способом наблюдения за течением болезни.
- Нагрузочный тест. Тест с физической нагрузкой на беговой дорожке или велотренажере можно использовать для контроля функции легких, когда вы активны.
- Анализ газов артериальной крови. В этом тесте ваш врач исследует образец крови, обычно взятой из артерии на запястье. Затем измеряются уровни кислорода и углекислого газа в образце.
Образец ткани (биопсия)
Если другие тесты не диагностировали состояние, врачам может потребоваться удалить небольшое количество легочной ткани (биопсия).Затем биопсия исследуется в лаборатории, чтобы диагностировать фиброз легких или исключить другие состояния. Образец ткани можно получить одним из следующих способов:
Бронхоскопия. В этой процедуре ваш врач берет очень маленькие образцы тканей — обычно не больше, чем острие булавки — с помощью небольшой гибкой трубки (бронхоскопа), которая проходит через ваш рот или нос в легкие. Образцы тканей иногда слишком малы для точного диагноза.Биопсия также может использоваться для исключения других состояний.
Риски бронхоскопии обычно незначительны и могут включать временную боль в горле или дискомфорт в носу из-за прохождения бронхоскопа. Однако серьезные осложнения могут включать кровотечение или сдутое легкое.
Во время бронхоскопии врач может провести дополнительную процедуру, называемую бронхоальвеолярным лаважем. В этой процедуре ваш врач вводит соленую воду через бронхоскоп в часть вашего легкого, а затем сразу же отсасывает ее.Извлеченный раствор содержит клетки из ваших воздушных мешков.
Хотя при бронхоальвеолярном лаваже исследуется большая площадь легких, чем при других процедурах, он может не предоставить достаточно информации для диагностики легочного фиброза. Его также можно использовать для исключения других условий.
Хирургическая биопсия. Хотя хирургическая биопсия более инвазивна и имеет потенциальные осложнения, она может быть единственным способом получить достаточно большой образец ткани для постановки точного диагноза.Эта процедура может выполняться как минимально инвазивная операция, называемая торакоскопической хирургией с использованием видео (VATS), или как открытая операция (торакотомия).
Во время VATS ваш хирург вводит хирургические инструменты и небольшую камеру через два или три небольших разреза между ребрами. Камера позволяет вашему хирургу наблюдать за вашими легкими на видеомониторе, одновременно отбирая образцы тканей из легких. Эта процедура выполняется после того, как вам сделали общий наркоз, поэтому во время процедуры вы будете спать.
Во время открытой операции (торакотомии) хирург извлекает образец легкого через разрез в груди между ребрами. Процедура проводится после того, как вам сделают общий наркоз.
Анализы крови
Врачи также могут назначить анализы крови для оценки вашей функции печени и почек, а также для проверки и исключения других заболеваний.
Дополнительная информация
Показать дополнительную информациюЛечение
Рубцевание легких, возникающее при фиброзе легких, не может быть обращено вспять, и ни одно текущее лечение не доказало свою эффективность в остановке прогрессирования заболевания.Некоторые виды лечения могут временно улучшить симптомы или замедлить прогрессирование заболевания. Другие могут помочь улучшить качество жизни. Врачи оценит тяжесть вашего состояния, чтобы определить наиболее подходящее лечение.
Лекарства
Ваш врач может порекомендовать более новые лекарства, в том числе пирфенидон (Эсбриет) и нинтеданиб (Офев). Эти лекарства могут помочь замедлить прогрессирование идиопатического фиброза легких. Оба препарата были одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA).Дополнительные лекарства и новые формы этих лекарств разрабатываются, но еще не одобрены FDA.
Нинтеданиб может вызывать такие побочные эффекты, как диарея и тошнота. Побочные эффекты пирфенидона включают сыпь, тошноту и диарею.
Исследователи продолжают изучать препараты для лечения фиброза легких.
Врачи могут порекомендовать антикислотные препараты для лечения гастроэзофагеальной рефлюксной болезни (ГЭРБ), состояния пищеварения, которое обычно возникает у людей с идиопатическим фиброзом легких.
Кислородная терапия
Использование кислорода не может остановить повреждение легких, но может:
- Облегчить дыхание и упражнения
- Предотвратить или уменьшить осложнения, связанные с низким уровнем кислорода в крови
- Снизьте артериальное давление в правой части сердца
- Улучшает сон и улучшает самочувствие
Вы можете получать кислород во время сна или физических упражнений, хотя некоторые люди могут использовать его все время.Некоторые люди носят с собой баллончик с кислородом, что делает их более мобильными.
Легочная реабилитация
Легочная реабилитация может помочь вам справиться с симптомами и улучшить ваше повседневное функционирование. В программах легочной реабилитации основное внимание уделяется:
- Физические упражнения для повышения выносливости
- Дыхательные техники, повышающие эффективность легких
- Консультации по питанию
- Консультации и поддержка
- Информация о вашем состоянии
Трансплантация легких
Трансплантация легких может быть вариантом для людей с легочным фиброзом.Пересадка легкого может улучшить качество вашей жизни и продлить жизнь. Однако трансплантация легкого может вызвать такие осложнения, как отторжение и инфекция. Ваш врач может обсудить с вами, подходит ли трансплантация легких для вашего состояния.
Клинические испытания
Изучите исследования клиники Mayo Clinic, в которых тестируются новые методы лечения, вмешательства и тесты как средства предотвращения, обнаружения, лечения или управления этим заболеванием.
Образ жизни и домашние средства
Активное участие в собственном лечении и поддержание как можно более здорового состояния необходимы для жизни с фиброзом легких. По этой причине важно:
Бросьте курить. Очень важно бросить курить, если у вас заболевание легких. Поговорите со своим врачом о вариантах отказа от курения, включая программы отказа от курения, в которых используются различные проверенные методы, помогающие людям бросить курить.А поскольку пассивное курение может нанести вред вашим легким, избегайте присутствия курящих людей.
Ешьте хорошо. Люди с заболеваниями легких могут похудеть как из-за неудобства в еде, так и из-за дополнительной энергии, необходимой для дыхания. Тем не менее, необходима диета, богатая питательными веществами и содержащая достаточное количество калорий. Старайтесь чаще есть небольшими порциями в течение дня.
Старайтесь есть разнообразные фрукты и овощи, цельнозерновые продукты, нежирные или обезжиренные молочные продукты и нежирное мясо.Избегайте трансжиров и насыщенных жиров, слишком большого количества соли и добавленных сахаров. Диетолог может дать вам дополнительные рекомендации по здоровому питанию.
- Двигайтесь. Регулярные упражнения помогут вам сохранить функцию легких и справиться со стрессом. Старайтесь включить в свой распорядок дня физическую активность, например ходьбу или езду на велосипеде. Поговорите со своим врачом о том, какие виды деятельности могут вам подойти. Если вам со временем требуется помощь в передвижении, например, инвалидная коляска, поищите занятия или хобби, которые не требуют ходьбы.
- Найдите время для отдыха. Обязательно достаточно отдыхайте. Выделив время для отдыха, вы получите больше энергии и сможете справиться со стрессом, связанным с вашим состоянием.
- Сделайте прививку. Респираторные инфекции могут усугубить симптомы легочного фиброза. Убедитесь, что вы получили вакцину от пневмонии и ежегодную прививку от гриппа. Важно, чтобы члены вашей семьи также были вакцинированы. Старайтесь избегать скопления людей во время сезона гриппа.
- Следуйте своему плану лечения. Вам потребуется постоянное лечение у врача.Следуйте инструкциям врача, принимайте лекарства в соответствии с предписаниями и при необходимости корректируйте диету и упражнения. Ходите на все приемы к врачу.
Помощь и поддержка
Фиброз легких — хроническое прогрессирующее заболевание, что означает, что оно со временем ухудшается. Узнав больше о болезни, вы и ваша семья сможете справиться с ней. Посещение легочной реабилитации может помочь вам справиться с симптомами и улучшить повседневное функционирование.
Легочный фиброз может вызывать страх и стресс.Проводите время с семьей и друзьями и расскажите им, как они могут поддержать вас и помочь вам. Поговорите со своим врачом о своем состоянии и о том, как вы себя чувствуете. Если вы в депрессии, врач может порекомендовать вам обратиться к специалисту по психическому здоровью.
Может оказаться полезным участие в группе поддержки людей с фиброзом легких. Это может помочь поговорить с другими людьми, у которых были похожие симптомы или лечение, и обсудить стратегии выживания.
По мере того, как ваше состояние прогрессирует, ваш врач может посоветовать вам и вашей семье обсудить вопросы, связанные с окончанием жизни, и спланировать предварительные указания.
Подготовка к приему
Если ваш лечащий врач подозревает серьезную проблему с легкими, вас, скорее всего, направят к пульмонологу, врачу, который специализируется на заболеваниях легких.
Что вы можете сделать
Перед встречей вы можете написать список, который отвечает на следующие вопросы:
- Какие у вас симптомы и когда они появились?
- Получаете ли вы лечение от других заболеваний?
- Какие лекарства и добавки вы принимали за последние пять лет?
- Вы курите? Если да, то сколько и как долго?
- Какими занятиями вы когда-либо занимались, пусть даже всего на несколько месяцев?
- Есть ли у кого-либо из членов вашей семьи какое-либо хроническое заболевание легких?
- Получали ли вы когда-нибудь химиотерапию или лучевую терапию от рака?
- Есть ли у вас какие-либо другие заболевания, особенно артрит?
Вы также можете попросить друга или члена семьи сопровождать вас на прием.Легочный фиброз — серьезное и сложное заболевание. Друг или член семьи могут оказать эмоциональную поддержку и помочь запомнить информацию, которую вы могли забыть или упустить. Можно делать заметки.
.Новая модель бандажирования легочной артерии, ведущего к правожелудочковой недостаточности у крыс
Предпосылки . Врожденные пороки сердца часто связаны с хронической перегрузкой правого желудочка давлением (ПЖ), которая является основной причиной дисфункции ПЖ. Бандажирование легочной артерии (PA) использовалось для создания животных моделей дисфункции правого желудочка. Мы разработали новый и более простой метод сужения ЛА и сравнили его напрямую с методом частичного лигирования. Методы . Восьминедельные самцы крыс Sprague-Dawley (240–260 г) были разделены на три группы: имитационная операция, процедура частичного лигирования легочной артерии (PAL) и процедура полузакрытого зажима легочной артерии (PAC).Функцию и ремоделирование правого желудочка определяли с помощью эхокардиографии и гистоморфометрии. Результаты . Хирургическая смертность была значительно ниже в группе PAC, в то время как эхокардиография выявила значительно больше признаков дисфункции правого желудочка. На 8-й неделе после операции частота фиброза ПЖ была значительно выше в группе PAC. Выводы . Эта процедура перевязки легочной артерии у крыс проще и эффективнее частичной перевязки.
1. Введение
Точная распространенность детской сердечной недостаточности в значительной степени неизвестна, но она увеличивается.Последние достижения в диагностических методах, новых хирургических методах и улучшенном периоперационном ведении способствовали увеличению выживаемости пациентов со сложными врожденными пороками сердца, которые сегодня часто доживают до зрелого возраста [1].
Однако даже после успешного восстановления у некоторых пациентов сохраняется давление в правом желудочке (ПЖ), которое в конечном итоге ухудшает функцию ПЖ и влияет на долгосрочную смертность и заболеваемость [2–4].
Хотя компенсированная гипертрофия развивается первоначально, в конечном итоге происходит отказ ПЖ.Механизмы, лежащие в основе прогрессирования от компенсированной гипертрофии правого желудочка к декомпенсированной, не определены [5].
Клинически необходимо рассмотреть взаимосвязь между прогрессирующим фиброзом и функцией ПЖ [6, 7]. Но изучение механизмов, лежащих в основе перехода от компенсированного состояния гипертрофии к декомпенсированному состоянию, затруднено у пациентов, поскольку инвазивные данные не могут быть легко получены. Для этой цели могут быть полезны модели на животных. Маленькие экспериментальные животные, такие как крысы, широко используются в исследованиях сердечно-сосудистой системы, поскольку они могут предоставить ряд моделей заболеваний, включая гипертрофию сердца и сердечную недостаточность.Основным преимуществом этих моделей заболеваний является то, что сердечный материал может быть легко взят для изучения патологии рассматриваемого заболевания.
Процедура частичной перевязки легочной артерии широко использовалась для развития правожелудочковой недостаточности, вызванной перегрузкой давлением, но эта процедура может иметь важные недостатки, включая высокую хирургическую смертность, вызванную кровотечением, внезапной остановкой сердца или легочным тромбом.
Перегрузка давлением также может быть вызвана с помощью полузакрытых канцелярских скрепок, которые легко накладываются стопором.Мы могли регулировать размер закрытия, перемещая стопор. Целью этого исследования было создание модели недостаточности ПЖ на крысах с использованием процедуры полузакрытого зажима легочной артерии по сравнению с процедурой частичного лигирования.
2. Материалы и методы
2.1. Уход за животными
Все экспериментальные процедуры и протоколы, использованные в этом исследовании, были рассмотрены и одобрены институциональным комитетом по уходу и использованию животных и соответствовали «руководству по уходу и использованию лабораторных животных» Национального института здравоохранения (Национальные институты Публикация по вопросам здравоохранения № 85-23, редакция 1996 г.).
2.2. Модель на животных
Модель на крысах с перевязкой легочной артерии (PAB) была создана для создания хронической перегрузки ПЖ давлением. Восеминедельных самцов крыс Sprague-Dawley (240–260 г) анестезировали пентобарбиталом (50 мг / кг массы тела) и ксилазином (5 мг / кг) внутрибрюшинно и вентилировали 100% O 2 с использованием объема управляемый респиратор (2 мл, 60 циклов / мин). Левая торакотомия была выполнена в четвертом межреберье, и была осторожно обнажена главная легочная артерия (mPA) (рис. 1).
2.2.1. Модель частичного лигирования легочной артерии (PAL) ()
Проленовую нить 7-0 плотно завязывали вокруг иглы 18 калибра рядом с mPA. После последующего быстрого удаления иглы в просвете образовывалось фиксированное суженное отверстие, равное диаметру иглы [5, 8, 9].
2.2.2. Модель полузакрытого зажима (PAC) ()
Небольшой зажим (LT100 ETHICON) был наполовину закрыт вокруг мПА с помощью приспособления для наложения зажимов (LX107 ETHICON) со стопором (рис. 1).Кровоток через mPA был ограничен, чтобы равняться внутреннему сегменту полузакрытого зажима. Мы выбрали зажим типа (B), потому что этот внутренний размер был почти равен внешнему размеру иглы 18 G (Рисунок 2).
После этого грудную клетку закрыли послойно и изменили настройку вентилятора (90 циклов / мин) на полчаса, чтобы снизить респираторную нагрузку.
2.2.3. Ложная операция ()
Левую торакотомию выполняли в четвертом межреберье, после чего осторожно обнажали мПА.Грудная клетка была закрыта послойно, и настройки вентилятора были изменены (90 циклов мин. –1 ) на полчаса для уменьшения респираторной нагрузки.
2.3. Эхокардиографические измерения
Эхокардиограммы были записаны в предоперационный день, а также на 4-ю и 8-ю неделю после процедуры. Крыс подвергали анестезии для получения эхо-сигнала (пентобарбитал 50 мг кг -1 массы тела), но они дышали спонтанно и располагались на левом боку.
При измерении эхокардиограммы доза анестетиков была снижена до 50% только в тот день, когда у крысы появились клинические признаки, потеря активности, отек тела и плевральный выпот, недостаточность ПЖ.Трансторакальный 2-мерный режим, М-режим (в соответствии со стандартами Американского общества эхокардиографии) и доплеровское сканирование выполнялись с помощью датчика 6,5 МГц (Xario TOSHIBA, ЯПОНИЯ).
На рис. 3 показаны схемы измерений эхокардиограмм соответственно.
Морфология правого желудочка оценивалась по толщине свободной стенки правого желудочка (RVWT), конечному диастолическому диаметру правого желудочка (RVDd) и размеру выходного тракта правого желудочка (RVOTD). RVWT измеряли в M-режиме либо в двухмерном парастернальном виде по короткой оси ниже трикуспидального клапана, либо в парастернальном виде по длинной оси, в зависимости от качества визуализации свободной стенки правого желудочка.RVDd измеряли как максимальное расстояние от свободной стенки ПЖ до перегородки с апикальной четырехкамерной проекции.
RVOTD и размер аорты (AoD) были измерены на уровне аортального клапана в виде короткой оси. Отношение RVOTD к AoD (RVOTD / AoD) было рассчитано как репрезентативное для дилатации правого желудочка. Положение датчика было выровнено для визуализации верхушки правого желудочка.
Максимальный размер полости ПЖ перед рамкой с началом систолического закрытия створок трикуспидального клапана использовался для измерения RVDd.Чтобы оценить функцию правого желудочка, измеряли систолическую экскурсию плоскости трикуспидального кольца (TAPSE) латеральной части плоскости трикуспидального кольца по укорочению от основания до верхушки во время систолы. Это было записано в формате M-режима под двумерным эхокардиографическим контролем с апикальной четырехкамерной проекции.
Кроме того, скорость PAv (PAv) регистрировалась на уровне аортального клапана на короткой оси. Это использовалось как эхокардиографический индикатор перегрузки ПЖ давлением [10, 11].
Эхокардиограммы левого желудочка (ЛЖ) в M-режиме были записаны для оценки функции ЛЖ, как описано ранее. Конечный диастолический размер ЛЖ (LVDd), конечно-систолический размер LV (LVD), толщина стенки межжелудочковой перегородки (IVST) и толщина задней стенки LV (LVPW) измерялись на уровне папиллярных мышц, а фракционное укорочение LV (LVFS) было измерено. рассчитывается следующим образом:
.Диагностика и лечение легочной гипертензии
ТРЕНТОН Д. НАУЗЕР, доктор медицины, и СТИВЕН СТИТС, доктор медицины, Медицинский центр Канзасского университета, Канзас-Сити, Канзас
Am Fam Physician. 2001 1 мая; 63 (9): 1789-1799.
 См. Информационный бюллетень для пациентов о легочной гипертензии, написанный авторами этой статьи.
См. Информационный бюллетень для пациентов о легочной гипертензии, написанный авторами этой статьи.
Первичная легочная гипертензия — редкое заболевание неизвестной этиологии, тогда как вторичная легочная гипертензия является осложнением многих легочных, сердечных и внегрудных заболеваний.Хроническая обструктивная болезнь легких, дисфункция левого желудочка и нарушения, связанные с гипоксемией, часто приводят к легочной гипертензии. Независимо от этиологии нелегальная легочная гипертензия может привести к правосторонней сердечной недостаточности. Признаки и симптомы легочной гипертензии часто незаметны и неспецифичны. Диагноз следует подозревать у пациентов с нарастающей одышкой при физической нагрузке и известной причиной легочной гипертензии. Двумерная эхокардиография с исследованиями допплеровского кровотока является наиболее полезным методом визуализации у пациентов с подозрением на легочную гипертензию.При наличии легочной гипертензии дальнейшая оценка может включать оценку оксигенации, исследование функции легких, компьютерную томографию грудной клетки с высоким разрешением, вентиляционно-перфузионное сканирование легких и катетеризацию сердца. Лечение с помощью непрерывной внутривенной инфузии простациклина улучшает переносимость физической нагрузки, качество жизни, гемодинамику и долгосрочную выживаемость у пациентов с первичной легочной гипертензией. Лечение вторичной легочной гипертензии включает устранение первопричины и устранение гипоксемии.Трансплантация легких остается вариантом для отдельных пациентов с легочной гипертензией, которые не поддаются лечению.
Легочная гипертензия — сложная проблема, характеризующаяся неспецифическими признаками и симптомами и имеющая множество потенциальных причин. Его можно определить как систолическое давление в легочной артерии более 30 мм рт. Ст. Или среднее давление в легочной артерии более 20 мм рт.
Этиология первичной легочной гипертензии неизвестна. Вторичная легочная гипертензия может быть осложнением многих легочных, сердечных и внегрудных заболеваний.Легочное сердце — это увеличение правого желудочка вследствие нарушений дыхательной системы. Легочная гипертензия неизменно предшествует легочному сердцу. Нелегированная легочная гипертензия, независимо от первопричины, приводит к правожелудочковой недостаточности.
Эпидемиология
По оценкам, заболеваемость первичной легочной гипертензией составляет 1-2 случая на 1 миллион человек в общей популяции. В детстве это заболевание одинаково влияет на обоих полов; после полового созревания чаще встречается у женщин, чем у мужчин (соотношение: 1.7 к 1). Первичная легочная гипертензия чаще всего встречается у людей в возрасте от 20 до 40 лет. Заболевание не имеет расовой принадлежности.1
Вторичная легочная гипертензия встречается относительно часто, но не диагностируется. Трудно получить надежные оценки распространенности этого состояния из-за разнообразия идентифицируемых причин.
У лиц старше 50 лет легочное сердце, являющееся следствием нелеченой легочной гипертензии, является третьим по распространенности сердечным заболеванием (после ишемической болезни сердца и гипертонической болезни).2
Патофизиология
Нормальное систолическое давление в легочной артерии в состоянии покоя составляет от 18 до 25 мм рт. Ст., При среднем давлении в легочной артерии от 12 до 16 мм рт. Это низкое давление происходит из-за большой площади поперечного сечения малого круга кровообращения, что приводит к низкому сопротивлению. Повышение легочного сосудистого сопротивления или легочного кровотока приводит к легочной гипертензии.
Всемирная организация здравоохранения (ВОЗ) предложила систему классификации легочной гипертензии, основанную на общих клинических характеристиках (таблица 1).3 Пациенты с легочной гипертензией также могут быть классифицированы в соответствии с их функциональной способностью (Таблица 2).
Первичная легочная гипертензия
Спорадическое расстройство
Семейное расстройство
Связанные состояния
0202 9003 Сосудистые заболевания
Врожденный системно-легочный шунт
Портальная гипертензия
Инфекция, вызванная вирусом иммунодефицита человека
Наркотики и токсины
Аноректические средства (подавляющие аппетит)
Прочие
Стойкая легочная гипертензия
Другое
Легочная венозная гипертензия
Левопредсердная или желудочковая болезнь сердца
Левосторонняя клапанная болезнь сердца
Внешняя компрессия легочных вен
Фиброзирующий медиастинит
Аденопатия и / или опухоли
Легочные веноокклюзионные заболевания
3 3
Сосудистые заболевания
Врожденный системно-легочный шунт
Портальная гипертензия
Инфекция, вызванная вирусом иммунодефицита человека
Наркотики и токсины
Аноректические средства (подавляющие аппетит)
Прочие
Стойкая легочная гипертензия
Другое
Легочная венозная гипертензия
Левопредсердная или желудочковая болезнь сердца
Левосторонняя клапанная болезнь сердца
Внешняя компрессия легочных вен
Фиброзирующий медиастинит
Аденопатия и / или опухоли
Легочные веноокклюзионные заболевания
Легочная гипертензия, связанная с нарушениями дыхательной системы и / или гипоксемией
Хроническая обструктивная болезнь легких
Интерстициальная болезнь легких
Нарушение дыхания во сне
Расстройства альвеолярной гиповентиляции
Хроническое пребывание на большой высоте
Заболевание легких у новорожденных
Альвеолярно-капиллярная дисплазия
от хронической тромботической и / или эмболической болезни
Тромбоэмболическая обструкция проксимальных легочных артерий
Обструкция дистальных легочных артерий
Тромбоэмболия легочной артерии (тромб, опухоль, яйцеклетки и / или паразиты, инородный материал)
Тромбоз in-situ
Серповидно-клеточная анемия
Легочная гипертензия в результате заболеваний, непосредственно влияющих на легочная сосудистая сеть
Воспалительные состояния
Шистосомоз
Саркоидоз
0 ТАБЛИЦА 1 Диагностическая классификация легочной гипертензии Всемирной организации здравоохранения
Легочная артериальная гипертензия
Первичная легочная гипертензия
Спорадическое расстройство
Семейное расстройство
Сопутствующие состояния
Коллагеновые сосудистые заболевания
Врожденный системный шунт
– Портальная гипертензия
Инфекция, вызванная вирусом иммунодефицита человека
Наркотики и токсины
Анорексические агенты
03 Прочие
Стойкая легочная гипертензия новорожденного
Прочие
Легочная венозная гипертензия
900 42 Левостороннее предсердие или желудочковая болезнь сердца
Левосторонняя клапанная болезнь сердца
Внешняя компрессия центральных легочных вен
Фиброзирующий средостение
Аденопатия и / или опухоли
Легочная веноокклюзионная болезнь
Прочие
Легочная гипертензия, связанная с нарушениями дыхательной системы и / или гипоксемией
03
Хроническая обструктивная болезнь легких
Интерстициальная болезнь легких
Нарушение дыхания во сне
Нарушения альвеолярной гиповентиляции
Хроническая экспозиция обязательно на больших высотах
Заболевания легких у новорожденных
Альвеолярно-капиллярная дисплазия
Прочие
Легочная гипертензия в результате хронической тромботической болезни 43
Тромбоэмболическая обструкция проксимальных легочных артерий
Обструкция дистальных легочных артерий
Легочная эмболия (тромб, опухоль, яйцеклетки и / или паразиты, инородный материал)
Серповидно-клеточная анемия
Легочная гипертензия, возникающая в результате заболеваний, непосредственно влияющих на легочную сосудистую систему
Воспалительные состояния
Шистосомоз
Саркоидоз
Другие
Легочный капиллярный гемангиоматоз
935 Просмотр / функция Легочная гипертензия *
Класс I:
Пациенты с легочной гипертензией, но без ограничения физической активности.Обычная физическая активность не вызывает чрезмерной одышки или усталости, боли в груди или предобморочного состояния.
Класс II:
Пациенты с легочной гипертензией, приводящей к небольшому ограничению физической активности. Эти пациенты чувствуют себя комфортно в покое, но обычная физическая активность вызывает чрезмерную одышку или усталость, боль в груди или близость к обморокам.
Класс III:
Пациенты с легочной гипертензией, приводящей к значительному ограничению физической активности.Эти пациенты чувствуют себя комфортно в покое, но меньшая, чем обычная физическая активность, вызывает чрезмерную одышку или усталость, боль в груди или близость к обмороку.
Класс IV:
Пациенты с легочной гипертензией, приводящей к неспособности выполнять какие-либо физические нагрузки без симптомов. У этих пациентов проявляются признаки правожелудочковой недостаточности. Одышка и / или утомляемость могут присутствовать в покое, а дискомфорт усиливается при любой физической активности.
ТАБЛИЦА 2 Функциональная оценка пациентов с легочной гипертензией *
Класс I:
Пациенты с легочной гипертензией, но без ограничения физической активности.Обычная физическая активность не вызывает чрезмерной одышки или усталости, боли в груди или предобморочного состояния.
Класс II:
Пациенты с легочной гипертензией, приводящей к небольшому ограничению физической активности. Эти пациенты чувствуют себя комфортно в покое, но обычная физическая активность вызывает чрезмерную одышку или усталость, боль в груди или близость к обморокам.
Класс III:
Пациенты с легочной гипертензией, приводящей к значительному ограничению физической активности.Эти пациенты чувствуют себя комфортно в покое, но меньшая, чем обычная физическая активность, вызывает чрезмерную одышку или усталость, боль в груди или близость к обмороку.
Класс IV:
Пациенты с легочной гипертензией, приводящей к неспособности выполнять какие-либо физические нагрузки без симптомов. У этих пациентов проявляются признаки правожелудочковой недостаточности. Одышка и / или утомляемость могут присутствовать в покое, а дискомфорт усиливается при любой физической активности.
При первичной легочной гипертензии легочная сосудистая сеть является исключительной мишенью заболевания, хотя патогенез остается спекулятивным.Наиболее широко распространенная теория предполагает, что некоторые люди могут быть предрасположены к первичной легочной гипертензии. У этих людей различные раздражители могут инициировать развитие легочной артериопатии. Ремоделирование сосудистой стенки, сужение сосудов и тромбоз in situ — все это играет роль1.
Коллагеновая сосудистая болезнь, 4 портальная гипертензия, 5 инфекция, вызванная вирусом иммунодефицита человека (ВИЧ) 6, и аноректические агенты7 могут вызвать клиническую картину, аналогичную первичной легочной гипертензии.Применение препаратов, подавляющих аппетит, в течение более трех месяцев связано с более чем 30-кратным повышением риска развития легочной гипертензии.8 В Соединенных Штатах анорексические препараты фенфлурамин и дексфенфлурамин были отозваны в сентябре 1997 года, всего через 18 месяцев после того, как они начали действовать. были выпущены. ВОЗ считает, что другие подавители аппетита, такие как амфетамины, имеют «весьма вероятную» причинную роль в легочной гипертензии (Таблица 3) .3
Посмотреть / распечатать таблицу
ТАБЛИЦА 3 Факторы риска первичной легочной гипертензии
Наркотики и токсины
Определенная причинно-следственная связь
Аминорекс
Фенфлурамин
Дефлурамин
2
рапсовое масло Очень вероятная причинно-следственная связь
Амфетамины
л-триптофан
Возможная причинно-следственная связь
038
Кокаин
Химиотерапевтические препараты
Маловероятная причинно-следственная связь
Антидепрессанты
03
Эстрогеновая терапия
Курение сигарет
Демографические факторы и медицинские условия
Определенная причинно-следственная связь
Возможная причинно-следственная связь
Беременность
Системная гипертензия
Маловероятная причинная связь tionship
Ожирение
Заболевания
Определенная причинно-следственная связь
Инфекция вируса иммунодефицита человека
03 Портальная гипертензия и / или заболевание печени
Коллагеновые сосудистые заболевания
Врожденное системное легочное шунтирование сердца
9 Возможная причинная связь
Заболевания щитовидной железы
ТАБЛИЦА 3 Факторы риска первичной легочной гипертензии
Наркотики и токсины
Определенная причинно-следственная связь
Aminorex
Фенфлурамин
Dexfenfluramine
Токсичное рапсовое масло
Амфетамины
l-Триптофан
Возможная причинно-следственная связь
Мета-амфетамины
Химиотерапевтические препараты
Маловероятная причинно-следственная связь
Антидепрессанты
Пероральные контрацептивы
Эстрогеновая терапия
Курение сигарет
Демографические факторы и медицинские условия
Определенная причинно-следственная связь
Пол
Возможная причинно-следственная связь
Беременность
Системная гипертензия
Маловероятная причинно-следственная связь
2
038302 Ожирение 43830
Определенная причинно-следственная связь
Инфекция, вызванная вирусом иммунодефицита человека
Очень вероятная причинная связь
Портальная гипертензия и / или заболевание печени
Коллагеновые сосудистые заболевания
Врожденные системные шунты из легочной артерии
Возможная причинная связь
Заболевания щитовидной железы
Легочная гипертензия может быть связана с чрезмерным легочным кровотоком, например, при врожденных пороках сердца, связанных с шунтами слева направо.Когда легочный кровоток заметно увеличивается и достигается емкость легочных сосудов, любое дальнейшее увеличение кровотока вызывает повышение давления.
Повышенное давление в легких также является потенциальным следствием любого состояния, затрудняющего отток легочной вены. Легочная гипертензия, которая возникает при дисфункции левого желудочка и заболевании митрального клапана, является результатом увеличения сопротивления легочному венозному оттоку и обратной передачи повышенного давления в левом предсердии.Более прямая обструкция оттока легочных вен происходит в сочетании с необычными состояниями, такими как фиброз средостения и веноокклюзионное заболевание легких.
Легочная гипертензия часто возникает в ответ на альвеолярную гипоксию. Снижение давления кислорода вызывает сужение легочных сосудов за счет различных воздействий на эндотелий и гладкие мышцы. Хроническая горная болезнь и апноэ во сне9 являются частой этиологией легочной гипертензии, связанной с гипоксемией. Ацидоз, который также вызывает сужение сосудов легких, может усугублять последствия гипоксии.10
Вызванные гипоксией сужение сосудов и облитерация капилляров возникают при интерстициальной болезни легких и хронической обструктивной болезни легких (ХОБЛ), которая является наиболее частой причиной легочной гипертензии. Во время обострения ХОБЛ гипоксия и некомпенсированная гиперкарбия могут повышать легочное артериальное давление.
Легочная гипертензия может возникать, когда кровоток через большие легочные артерии затруднен. Классическая причина — тромбоэмболия легочной артерии. Острая тромбоэмболия легочной артерии вызывает лишь незначительное или умеренное повышение давления в легочной артерии.В острой форме правый желудочек неспособен создавать систолическое давление выше 50 мм рт. более высокое систолическое значение указывает на хронический процесс с гипертрофией правого желудочка. Следовательно, массивная тромбоэмболия легочной артерии может вызвать правожелудочковую недостаточность, но не тяжелую легочную гипертензию. Хроническая тромбоэмболия может спровоцировать тяжелую легочную гипертензию, но это состояние встречается менее чем у 1 процента пациентов с тромбоэмболической болезнью11
. Легочная гипертензия и легочное сердце — знания для студентов-медиков и врачей
Легочная гипертензия (ЛГ) — это повышенное давление в легочных артериях ≥ 20 мм рт. Ст. В покое. Он может быть идиопатическим или быть вызванным хроническим легочным (например, ХОБЛ, хроническое апноэ во сне) и / или сердечным заболеванием (например, заболеванием митрального клапана). Со временем повышение давления может привести к структурным изменениям (например, дилатации или гипертрофии) или нарушению функции правого желудочка. Если эти изменения являются вторичными по отношению к заболеваниям легких или системы легочной артерии, такое состояние называют легочным сердцем.В то время как ЛГ и легочное сердце часто протекают бессимптомно на ранних стадиях, такие симптомы, как одышка при физической нагрузке, утомляемость, цианоз и обморок, появляются на более поздних стадиях. При декомпенсированном легочном сердце риск аритмий и смерти высок. Эхокардиограммы используются в качестве начального неинвазивного теста для оценки давления в легочной артерии и демонстрации измененной структуры правого желудочка. Катетеризация правых отделов сердца позволяет поставить точный диагноз и определить точное среднее легочное артериальное давление (mPAP).Лечение в основном заключается в устранении основных причин ЛГ и легочного сердца. Для снижения гипертензии легочной артерии и улучшения оксигенации крови можно назначать дополнительный кислород, легочные вазодилататоры и диуретики. Трансплантация легких — это последнее средство лечения в рефрактерных случаях.
.Симптомы при повышенном холестерине в крови: Что делать при повышенном холестерине у мужчин?
Уплотнение на ноге под кожей с покраснением: шишка или опухоль болит при нажатии
Похожие записи
Детский массаж в Минске: польза, виды, техники и рекомендации специалистов
Каковы основные преимущества детского массажа для здоровья и развития ребенка. Какие виды детского массажа наиболее эффективны для разных возрастов. Как […]
Почему ребенок постоянно просит грудь: причины и решения
Почему грудничок часто требует грудь. Какие причины заставляют ребенка постоянно висеть на груди. Как определить, достаточно ли малышу молока. Что […]
Алфавит для иммунитета: укрепление защитных сил организма в сезон простуд
Как витаминно-минеральный комплекс Алфавит помогает укрепить иммунитет. Какие компоненты входят в состав Алфавита. Для кого предназначен Алфавит в сезон простуд. […]
Легочная артериальная гипертензия
Первичная легочная гипертензия
Спорадическое расстройство
Семейное расстройство
Сопутствующие состояния
Коллагеновые сосудистые заболевания
Врожденный системный шунт
Портальная гипертензия
Инфекция, вызванная вирусом иммунодефицита человека
Наркотики и токсины
Анорексические агенты
03 Прочие
Прочие
Стойкая легочная гипертензия новорожденного
Прочие
Легочная венозная гипертензия
900 42Левостороннее предсердие или желудочковая болезнь сердца
Левосторонняя клапанная болезнь сердца
Внешняя компрессия центральных легочных вен
Фиброзирующий средостение
Аденопатия и / или опухоли
Легочная веноокклюзионная болезнь
Прочие
Легочная гипертензия, связанная с нарушениями дыхательной системы и / или гипоксемией
03
Хроническая обструктивная болезнь легких
Интерстициальная болезнь легких
Нарушение дыхания во сне
Нарушения альвеолярной гиповентиляции
Хроническая экспозиция обязательно на больших высотах
Заболевания легких у новорожденных
Альвеолярно-капиллярная дисплазия
Прочие
Легочная гипертензия в результате хронической тромботической болезни 43
Тромбоэмболическая обструкция проксимальных легочных артерий
Обструкция дистальных легочных артерий
Легочная эмболия (тромб, опухоль, яйцеклетки и / или паразиты, инородный материал)
Серповидно-клеточная анемия
Легочная гипертензия, возникающая в результате заболеваний, непосредственно влияющих на легочную сосудистую систему
Воспалительные состояния
Шистосомоз
Саркоидоз
Другие
Легочный капиллярный гемангиоматоз
Класс I:
Пациенты с легочной гипертензией, но без ограничения физической активности.Обычная физическая активность не вызывает чрезмерной одышки или усталости, боли в груди или предобморочного состояния.
Класс II:
Пациенты с легочной гипертензией, приводящей к небольшому ограничению физической активности. Эти пациенты чувствуют себя комфортно в покое, но обычная физическая активность вызывает чрезмерную одышку или усталость, боль в груди или близость к обморокам.
Класс III:
Пациенты с легочной гипертензией, приводящей к значительному ограничению физической активности.Эти пациенты чувствуют себя комфортно в покое, но меньшая, чем обычная физическая активность, вызывает чрезмерную одышку или усталость, боль в груди или близость к обмороку.
Класс IV:
Пациенты с легочной гипертензией, приводящей к неспособности выполнять какие-либо физические нагрузки без симптомов. У этих пациентов проявляются признаки правожелудочковой недостаточности. Одышка и / или утомляемость могут присутствовать в покое, а дискомфорт усиливается при любой физической активности.
Класс I:
Пациенты с легочной гипертензией, но без ограничения физической активности.Обычная физическая активность не вызывает чрезмерной одышки или усталости, боли в груди или предобморочного состояния.
Класс II:
Пациенты с легочной гипертензией, приводящей к небольшому ограничению физической активности. Эти пациенты чувствуют себя комфортно в покое, но обычная физическая активность вызывает чрезмерную одышку или усталость, боль в груди или близость к обморокам.
Класс III:
Пациенты с легочной гипертензией, приводящей к значительному ограничению физической активности.Эти пациенты чувствуют себя комфортно в покое, но меньшая, чем обычная физическая активность, вызывает чрезмерную одышку или усталость, боль в груди или близость к обмороку.
Класс IV:
Пациенты с легочной гипертензией, приводящей к неспособности выполнять какие-либо физические нагрузки без симптомов. У этих пациентов проявляются признаки правожелудочковой недостаточности. Одышка и / или утомляемость могут присутствовать в покое, а дискомфорт усиливается при любой физической активности.
Наркотики и токсины
Определенная причинно-следственная связь
Аминорекс
Фенфлурамин
Дефлурамин
2
Очень вероятная причинно-следственная связь
Амфетамины
л-триптофан
Возможная причинно-следственная связь
038
Кокаин
Химиотерапевтические препараты
Маловероятная причинно-следственная связь
Антидепрессанты
03
Эстрогеновая терапия
Курение сигарет
Демографические факторы и медицинские условия
Определенная причинно-следственная связь
Возможная причинно-следственная связь
Беременность
Системная гипертензия
Маловероятная причинная связь tionship
Ожирение
Заболевания
Определенная причинно-следственная связь
Инфекция вируса иммунодефицита человека
03 Портальная гипертензия и / или заболевание печени
Коллагеновые сосудистые заболевания
Врожденное системное легочное шунтирование сердца
9 Возможная причинная связь
Заболевания щитовидной железы
Портальная гипертензия и / или заболевание печени
Коллагеновые сосудистые заболевания
Врожденное системное легочное шунтирование сердца
9 Возможная причинная связь
Заболевания щитовидной железы
Наркотики и токсины
Определенная причинно-следственная связь
Aminorex
Фенфлурамин
Dexfenfluramine
Токсичное рапсовое масло
Амфетамины
l-Триптофан
Возможная причинно-следственная связь
Мета-амфетамины
Химиотерапевтические препараты
Маловероятная причинно-следственная связь
Антидепрессанты
Пероральные контрацептивы
Эстрогеновая терапия
Курение сигарет
Демографические факторы и медицинские условия
Определенная причинно-следственная связь
Пол
Возможная причинно-следственная связь
Беременность
Системная гипертензия
Маловероятная причинно-следственная связь
2
038302 Ожирение 43830
0
Определенная причинно-следственная связь
Инфекция, вызванная вирусом иммунодефицита человека
Очень вероятная причинная связь
Портальная гипертензия и / или заболевание печени
Коллагеновые сосудистые заболевания
Врожденные системные шунты из легочной артерии
Возможная причинная связь
Заболевания щитовидной железы
Симптомы при повышенном холестерине в крови: Что делать при повышенном холестерине у мужчин?
Уплотнение на ноге под кожей с покраснением: шишка или опухоль болит при нажатии
Детский массаж в Минске: польза, виды, техники и рекомендации специалистов
Каковы основные преимущества детского массажа для здоровья и развития ребенка. Какие виды детского массажа наиболее эффективны для разных возрастов. Как […]
Почему ребенок постоянно просит грудь: причины и решения
Почему грудничок часто требует грудь. Какие причины заставляют ребенка постоянно висеть на груди. Как определить, достаточно ли малышу молока. Что […]
Алфавит для иммунитета: укрепление защитных сил организма в сезон простуд
Как витаминно-минеральный комплекс Алфавит помогает укрепить иммунитет. Какие компоненты входят в состав Алфавита. Для кого предназначен Алфавит в сезон простуд. […]
