Пациентам
Что такое микробиота?
Микробиота – совокупность всех живых микроорганизмов, населяющих кожу и слизистые оболочки человека. Мы часто используем и другой термин – микробиом, который подразумевает совокупность генетического материала всех микроорганизмов, обитающих в организме человека. Оба термина близки друг другу по смыслу и часто используются как синонимы. Понятие микрофлора все реже применяется в настоящее время и считается устаревшим, так как дает ложное представление о принадлежности микробиоты к царству растений.
Микробиота человека рассматривается, как самостоятельный, чрезвычайно сложный и динамически изменяющийся орган, регулирующий множество метаболических процессов нашего организма.
Основными представителями микробиоты человека являются бактериальные клетки, грибы, вирусы и простейшие, которые заселяют поверхность кожи, слизистых оболочек легких, желудочно-кишечного тракта и органов мочеполовой системы. Доминирующей считается кишечная микробиота — в её составе насчитывается около 1000 триллионов бактериальных клеток, которые составляют до 3% массы тела человека, а общее количество их генов превышает таковое у человека более чем в 100 раз. Среди всего многообразия выделяют 4 наиболее распространенных типа бактерий:
Что определяет состав кишечной микробиоты?
Исходно состав кишечной микробиоты определяется генетическими факторами, зрелостью плода при рождении, способом родоразрешения (естественные роды или роды путём кесарева сечения) и продолжительностью грудного вскармливания.
Активное формирование микробиоты происходит в течение первых 3 лет жизни, после этого ее состав остается относительно стабильным, претерпевая медленные и менее заметные изменения в юности, зрелом возрасте, старости. Вне зависимости от возраста большое значение для формирования микробиоты имеет образ жизни и внешние факторы, такие как:
- особенности питания
- прием лекарственных препаратов
- уровень физической активности
- регион проживания
- индекс массы тела
- психоэмоциональное состояние
- употребление алкоголя, курение
Как состав микробиоты влияет на здоровье человека?
Микробиота обеспечивает гомеостаз и адаптацию к условиям среды не только колонизированной области, но и всего организма.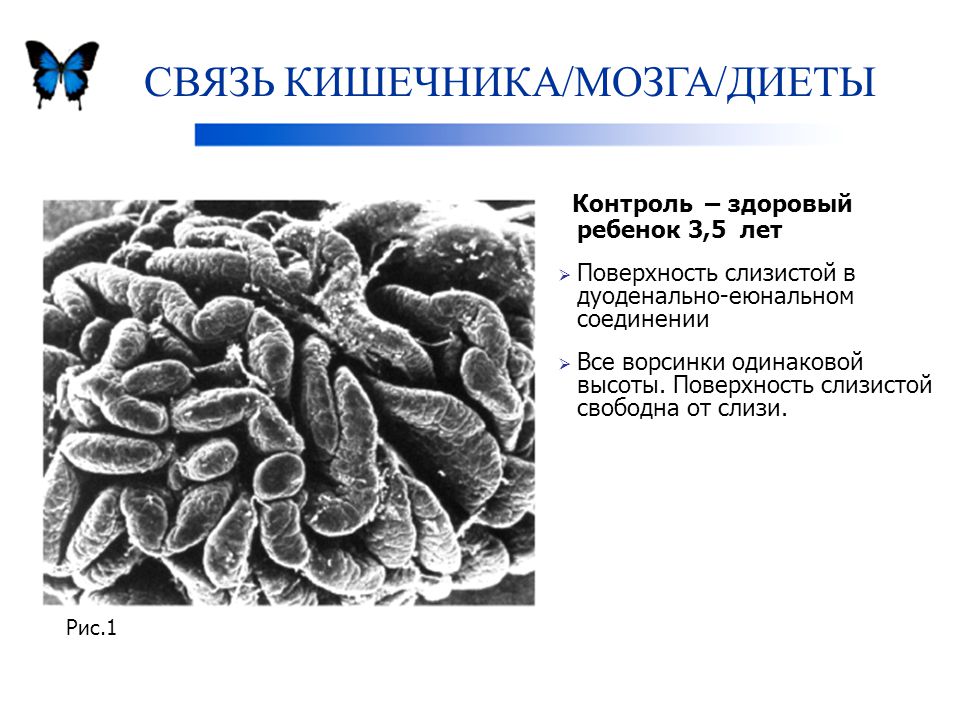 За счет большего разнообразия именно микробиота ЖКТ имеет самый широкий спектр функций:
За счет большего разнообразия именно микробиота ЖКТ имеет самый широкий спектр функций:
- защита от патогенных микроорганизмов
- участие в развитии иммунной системы
- усиление кишечного барьера
- расщепление неперевариваемых компонентов пищи, например целлюлозы, пектина
- синтез целого ряда молекул (короткоцепочечные жирные кислоты)
- метаболизм лекарств и биологически активных веществ
- Контроль пролиферации и дифференцировки эпителиальных клеток.
- взаимодействие с нервной системой и участие в регуляции деятельности кишечника (ось микробиота-кишка-головной мозг)
При нарушении микробного состава возникает вероятность развития следующих заболеваний:
- ишемическая болезнь сердца, гипертоническая болезнь, хроническая сердечная недостаточность;
- язвенная болезнь желудка и двенадцатиперстной кишки, C.difficile-ассоциированная болезнь, воспалительные заболевания ЖКТ (болезнь Крона, язвенный колит), функциональные заболевания ЖКТ, целиакия;
- НАЖБ, цирроз печени, аутоиммунные заболевания печени;
- ХОБЛ, бронхиальная астма, интерстициальные заболевания легких;
- мочекаменная болезнь, хроническая почечная недостаточность, воспалительные заболевания мочеполовой системы;
- тревожно-депрессивные и когнитивные расстройства, аутизм;
- болезнь Альцгеймера, болезнь Паркинсона, рассеянный склероз;
- псориаз, артриты, алопеция, акне, дерматозы, экзема;
- сахарный диабет, ожирение, атеросклероз, аллергические реакции;
- онкологические заболевания
Анализ на микробиоту — Сдать анализ на микробиоту кишечника в Москве
| Анализ микробных маркеров методом газовой хромато-масс-спектрометрии (Микробиота по Осипову / ХМС) | 3850 руб | до 9 суток |
Микробиотой называют совокупность микроорганизмов и бактерий, обитающих в кишечнике. Состояние и состав микробиоты влияет практически на все процессы, проходящие в кишечнике, – всасывание питательных веществ, инактивацию токсинов и так далее. Также микроорганизмы могут вырабатывать пептиды или белки, которые проникают в кровь и влияют, например, на аппетит человека.
Состояние и состав микробиоты влияет практически на все процессы, проходящие в кишечнике, – всасывание питательных веществ, инактивацию токсинов и так далее. Также микроорганизмы могут вырабатывать пептиды или белки, которые проникают в кровь и влияют, например, на аппетит человека.
В каких случаях назначают анализ на микробиоту кишечника?
Можно выделить ряд случаев, в которых необходимо получить информацию о микробиоте кишечника пациента:
- дисбактериоз, склонность к запорам или диарее, синдром раздраженного кишечника, болезнь Крона;
- вагинит, цистит, кандидоз и другие воспалительные и инфекционные заболевания женской половой системы;
- уретрит, простатит, пиелонефрит и другие урологические заболевания;
- мужское и женское бесплодие, неоднократное невынашивание беременности.
- туберкулез, пневмония, бронхит, плеврит;
- различные ЛОР-заболевания: отит, гайморит и др.;
- различные высыпания на лице, коже спины, груди.
Анализ микробиоты помогает поставить верный диагноз и выявить действительную причину проблем пациента, а также в дальнейшем осуществлять мониторинг его состояния, контроль и корректировку лечения.
Назначать исследование микробиоты могут специалисты разных направлений медицины: хирурги, гастроэнтерологи, урологи, гинекологи, косметологи, дерматологи. Также часто к вопросам микробиоты и ее состояния обращаются врачи-иммунологи, поскольку доказано, что толстая кишка – это своеобразный центр иммунитета, и от нее во многом зависит общее состояние человека, его восприимчивость к различным негативным факторам (начиная от простых респираторных заболеваний и заканчивая тяжелыми патологиями, требующими хирургического вмешательства).
В нашей клинике постоянно проходят Акции
Что показывает анализ крови на микробиоту кишечника по Осипову?
Анализ крови на микробиоту по Осипову заключается в выявлении микробных маркеров, которые могут говорить о наличии в организме воспалительных, инфекционных и других заболеваний. В процессе исследования во внимание принимаются все группы микроорганизмов: вирусы, анаэробные микроорганизмы, бактерии, грибы и др.
В процессе исследования во внимание принимаются все группы микроорганизмов: вирусы, анаэробные микроорганизмы, бактерии, грибы и др.
Результат анализа выглядит как список микроорганизмов, которые были обнаружены, с указанием количества каждого из них, а также нормативного значения.
Где в Москве сдать анализ крови на микробиоту кишечника по Осипову
В Москве в районе ЗАО сдать анализ крови на микробиоту кишечника по приемлемой цене с быстрым получением результатавам предлагает лечебно-диагностический центр «Медицина». У нас вы найдете:
- Качественный сервис – современный процедурный кабинет, где медицинский персонал быстро и безболезненно осуществит забор крови в условиях полной стерильности.
- Профессиональных специалистов в области диагностики и лечения заболеваний различной этиологии.
- Доступные цены на медицинские услуги. Все цены указаны в прайсе на сайте клиники. Также на сайте размещена информация об акциях снижения цен на наши услуги, которые мы часто проводим.
Чтобы сдать анализ, вы можете предварительно записаться по телефону или онлайн. Когда результат будет готов, наши специалисты свяжутся с вами, и вы получите результат удобным для вас способом.
Кишечная микробиота — Клиника ВАЛМЕД
Микроорганизмы внутри и вне нас. Сегодня в продолжение темы кишечника — о наших кишечных микроорганизмах более детально. Немного о понятиях:
Раньше мы, говоря о кишечнике, упоминали микрофлору.
Сейчас термин «МИКРОФЛОРА» считается несколько устаревшим, поскольку в буквальном смысле «флора» представляет собой растительный мир.
В настоящее время актуально говорить о МИКРОБИОМЕ — мире бактерий, грибов, вирусов, обитающих внутри и снаружи человека. Но часто в зарубежных статьях встречается термин «кишечный микробиом».
КИШЕЧНАЯ МИКРОБИОТА — (ещё один популярный термин 😉) — представляет собой совокупность микроорганизмов, населяющих желудочно-кишечный тракт.
Функции кишечной микробиоты:главная — участие в пищеварении, ответственны за наш комфорт или «дискомфорт» в животе, урчание, боли и другие диспепсии;
синтезирует витамины группы В, Витамин К, C, никотиновую и пантотеновую кислоты.
 А это влияет на наши суставы, сосуды, кроветворение, нервную систему.
А это влияет на наши суставы, сосуды, кроветворение, нервную систему.участвует в процессах всасывания и обмена кальция, железа и витаминов D и E. Не буду повторяться.
принимает участие в образовании белков, аминокислот, гормонов; регулирует синтез гистамина, снижая и профилактируя аллергические проявления;
участвует в формировании иммунокомпетентных клеток, синтезе цитокинов, иммуноглобулинов. В настоящее время существует много научных данных о роли микробиоты в развитии аутоиммунных заболеваний (ревматоидного артрита, рассеянного склероза, сахарного диабета 1 типа, и др), состоянии иммунитета в целом.
сдерживает рост условно-патогенных и патогенных бактерий, грибов, являясь их антагонистом.
участвует в выработке нейромедиаторов, которые влияют на структуры центральной нервной системы и организма в целом. Отсюда теория действующей оси «кишечник — головной мозг — кишечник».
принимает участие в детоксикации организма, в выведении шлаков и токсинов, азотистых соединений, холестерина и др.
влияет на микробиоту мочеполовой системы, кожи.
Таким образом, от состояния кишечника зависит наше здоровье, настроение, внешность.
Думаю, понимают это все. Но восстанавливать флору не просто. Поговорим об этом?
Определённые бактерии в кишечнике связали с развитием диабета второго типа
Группа российских учёных, включая руководителя Лаборатории постгеномных исследований НИИ Физико-химической медицины и сотрудника МФТИ Елену Кострюкову и аспирантку МФТИ Марию Вахитову обнаружила, что наличие определённых бактерий в кишечнике может быть связано с развитием диабета второго типа.
Сахарный диабет второго типа, он же инсулиннезависимый диабет, является серьёзным нарушением обмена веществ. При этом заболевании клетки организма утрачивают способность реагировать на инсулин — гормон, управляющий усвоением глюкозы.
По оценкам ВОЗ, в мире насчитывается около 285 миллионов больных диабетом второго типа. Распространённость болезни и тяжесть её осложнений (например, у больных в 20 раз возрастает риск гангрены нижних конечностей) заставляет врачей и учёных искать как причины нарушений, так и новые способы борьбы с ними.
В последнее время исследователи стали располагать серьёзными аргументами в пользу того, что диабет может быть связан в том числе и с составом микробного сообщества внутри кишечника человека, с так называемой кишечной микробиотой. Именно изменения микробиоты толстого кишечника изучали специалисты четырёх российских научных центров, чья работа была опубликована в журнале Endocrinology Connections.
Микробиотой кишечника называют совокупность всех живых микроорганизмов, обитающих в нём (включая даже некоторых одноклеточных грибов и архей). Ещё часто можно услышать, что жители кишечника зовутся микрофлорой — это исторический термин, сложившийся во времена, когда бактерий считали растениями.
Учёные проанализировали состав кишечной микробиоты у 92 человек, включая 20 пациентов с сахарным диабетом и 48 здоровых людей без каких-то хронических болезней; ещё у 24 наблюдались признаки нарушения обмена веществ, которые медики отнесли к предиабету — состоянию, способному привести к развитию диабета второго типа с течением времени. Уровень глюкозы, как важнейший индикатор обмена веществ, также был проконтролирован у участников исследования при помощи анализа крови.
«Главными героями» этого исследования были бактерии. Чтобы определить, с какими именно микроорганизмами исследователи имеют дело, они анализировали ДНК, выделенную из образцов кала. Получив генетический материал, учёные секвенировали его (считали и расшифровали последовательность «букв» в ДНК). Затем по этим данным они определили, с какими бактериями имеют дело в том или ином случае.
Затем по этим данным они определили, с какими бактериями имеют дело в том или ином случае.
Сопоставив состав микробиома с диагнозом (диабет/предиабет/отсутствие нарушений) и диетой участвовавших в исследовании добровольцев, исследователи сделали несколько выводов.
Прежде всего, они смогли связать уровень непереносимости глюкозы с наличием трёх специфических представителей микробиоты: бактерий родов Blautia, Serratia и Akkermansia. Все они есть и у здоровых людей, но при предиабете и диабете их доля значительно увеличивается.
А вот повышение уровней бифидобактерий (их больше всего в кишечнике детей, питающихся материнским молоком, и их принято считать одним из важнейших компонентов микробиоты) удалось связать с высоким потреблением пищевых волокон, то есть клетчатки. Это перекликается с результатами более раннего исследования микробиоты кишечника городов и сёл России, проведенного с участием той же группы учёных.
Тогда исследователи выяснили, что у жителей сёл Тувинской области бифидобактерий значительно больше, чем у жителей других регионов: предположительно, это связано с тем, что в диете сельского населения преобладают натуральные продукты, а доля «промышленной» пищи с пониженным содержанием клетчатки, напротив, невелика.
Полученные данные приближают учёных и медиков к пониманию сложных причинно-следственных связей между изменением доли определённых видов бактерий, нарушениями обмена веществ и диетой. Как указывают авторы исследования, одним из возможных механизмов влияния микроорганизмов на диабет может быть провоцирование реакции иммунитета — такая теория ранее высказывалась финскими специалистами.
Микробиота кишечника | Biocodex Microbiote Institut
Микроорганизмы в вашем кишечнике, в первую очередь бактерии, образуют с ним «партнерство», которое начинается с самого рождения. Для полноценного формирования микробиоты желудочно-кишечного тракта требуется около трех лет – с рождения до периода относительной стабильности, который затем продолжается до старости, когда микробиота снова претерпевает глубокие изменения.

Пищеварительная система новорожденного быстро колонизируется «простой» микробиотой, происходящей из вагинальных и фекальных бактерий его матери. Развитие полезных бактерий, таких как бифидобактерии, быстрее осуществляется при грудном вскармливании, но стабилизация микробиоты кишечника длится около трех лет. Эта стабилизация зависит от множества факторов. Например, анаэробные бактерии, которые не нуждаются в кислороде для выживания, находятся в меньшинстве у младенцев, но доминируют у взрослых. Развитие этих анаэробных бактерий происходит медленнее в случае родоразрешения путем кесарева сечения или в случае преждевременных родов, при этом микробиота у таких детей менее разнообразна, чем у младенцев, рожденных естественным путем и в срок. Разнообразие микробиоты также зависит от окружающей среды в раннем детстве: у детей, живущих в западных странах, наблюдается меньшее разнообразие, которое может быть связано с чрезмерной гигиеной. Желудочно-кишечная микробиота наращивается с годами, при этом она всегда сохраняет отпечаток профиля раннего детства. Меньшее микробиологическое разнообразие может привести в дальнейшем к развитию заболеваний.
Утрата разнообразия в пожилом возрасте
В зрелом возрасте немногие факторы могут радикально изменить доминантную микробиоту в отличие от гормональных изменений во время полового созревания, беременности и менопаузы. Но именно в старости изменения становятся более выраженными. Микробиота становится менее разнообразной из-за физиологических изменений, таких как снижение иммунитета, скудный рацион питания, прием многочисленных лекарств, включая антибиотики, и особенно образ жизни, когда люди становятся более зависимыми. Действительно, у пожилых людей, живущих в домах престарелых, микробиота беднее, чем у тех, кто живет дома и соблюдает свой обычный рацион. Это глубокое изменение равновесия микробиоты может привести к заболеваниям, таким как воспаление кишечника и повышенная восприимчивость к инфекции.
Источники
Yatsunenko T, Rey FE, Manary MJ, et al. Human gut microbiome viewed across age and geography. Nature 2012 ; 486 : 222-7.
Human gut microbiome viewed across age and geography. Nature 2012 ; 486 : 222-7.
Guaraldi F, Salvatori G. Effect of breast and formula feeding on gut microbiota shaping in newborns. Front Cell Infect Microbiol 2012 ; 2 : 94.
Campeotto F, Waligora-Dupriet AJ, Doucet-Populaire F, et al. Establishment of the intestinal microflora in neonates. Gastroenterol Clin Biol 2007 ; 31 : 533-42.
Biasucci G, Rubini M, RiboniS et al. Mode of delivery affects the bacterial community in the newborn gut. Early Hum Dev 2010 ; 86 (Suppl 1) : 13-5.
Okada H, Kuhn C, Feillet H, Bach JF. The ‘hygiene hypothesis’ for autoimmune and allergic diseases: an update. Clin Exp Immunol. 2010;160(1):1-9.
Koren O, Goodrich JK, Cullender TC, et al. Host remodeling of the gut microbiome and metabolic changes during pregnancy. Cell 2012 ; 150 : 470-80
Biagi E, Candela M, Turroni S, et al. Ageing and gut microbes : perspectives for health maintenance and longevity. Pharmacol Res 2013 ; 69 : 11-20.
Claesson MJ, Jeffery IB, Conde S, et al. Gut microbiota composition correlates with diet and health in the elderly. Nature 2012 ; 488 : 178-84.
Живущим в вашей толстой кишке тоже нужно здоровое питание
- Адам Резерфорд
- BBC Future
Автор фото, iStock
Чтобы сохранить здоровье и необходимое количество полезных бактерий в организме, мало просто есть йогурт с пробиотиками. Обозреватель BBC Future выяснил это, сдав один не очень приятный анализ.
Все началось с того, что не назовешь иначе как хитроумным изобретением. Это раскладывающийся лист с клейкими бумажками спереди и сзади, похожий на плоскую морскую звезду.
Бумажки приклеиваются к сидению унитаза. Закрепленный должным образом лист превращается в своеобразный гамак, на который и попадает образец для взятия пробы.
Готовясь к процедуре, я надел резиновые перчатки. Оставив свой биоматериал в «гамаке», я взял его пробу при помощи небольшой ложечки, закрепленной на внутренней стороне синей крышки от пробирки.
Затем я плотно завинтил крышку и завернул пластиковую пробирку в пакет со льдом, приготовленный мной заранее. Теперь ценный груз был готов к доставке.
А везти я его собрался в компанию Map My Gut, которая пообещала мне определить, какие именно микроорганизмы затаились в глубинах моего кишечника.
Результаты различных исследований, проведенных в последние годы, свидетельствуют о том, что микроорганизмы, живущие в нашей пищеварительной системе, намного более важны для нашего здоровья и самочувствия, чем считалось ранее.
Но вскоре я обнаружил, что мои собственные бактерии не слишком-то процветают, и что определенный рацион может полностью изменить нашу с ними общую жизнь.
Автор фото, SPL
Подпись к фото,Methanobrevibacter помогает повысить усвояемость пищи
В кишечнике среднестатистического человека живет около тысячи различных видов бактерий.
Общее их количество определить затруднительно, но счет идет на триллионы, и почти все они выполняют полезную для нас работу.
Геном человека насчитывает около 20 000 генов, однако у живущих в нашем организме микроорганизмов в совокупности их примерно в 500 раз больше.
Это позволяет им справляться с довольно непростыми задачами: помогать переваривать пищу, вырабатывать витамины и минералы и даже предотвращать болезни, объединяясь в группы и уничтожая патогенные бактерии.
Но это лишь малая часть их работы; на самом деле от них зависит, кем мы являемся внутри и снаружи.
Как сказал мне Эд Янг, автор книги «Множества во мне» (I Contain Multitudes), «микробы помогают строить тело человека, они формируют и обновляют наши органы по мере того как мы стареем».
«Возможно, они даже могут влиять на наше поведение и образ мыслей. Многочисленные эксперименты на животных показали, что микроорганизмы в их кишечнике могут оказывать влияние на настроение, характер и устойчивость к тревоге и стрессу», — отмечает он.
Однако насколько эти результаты применимы к человеку, нам еще предстоит понять.
Наверняка известно лишь то, что микробиомы двух человек различаются намного больше, чем их геномы.
Состав микроорганизмов в организме человека зависит от истории его болезней, места жительства и рациона.
У каждого человека он индивидуален и может сильно отличаться даже у ближайших родственников.
Автор фото, Getty Images
Подпись к фото,Некоторые продукты гораздо лучше стимулируют рост полезных бактерий в организме, чем йогурт
Именно поэтому мне пришлось опорожниться на бумажку и отнести кусочек биоматериала на анализ.
Признаюсь, что, входя в офис Тима Спектора, профессора генетики из больницы Святого Фомы, чтобы узнать результаты, я слегка нервничал.
Что я узнаю о таинственном внутреннем мире своих бактерий? Что именно прячется в моей толстой кишке?
Если честно, мой анализ был хуже некуда.
«Ваш результат намного ниже среднего. По разнообразию вы попадаете в 10% населения с самыми худшими результатами», — сказал мне Спектор с еле заметной ноткой радости в голосе. Радости, которую испытывает ученый, обнаружив какое-либо отклонение от нормы.
Он объяснил, что разнообразие — это один из главных факторов, влияющих на здоровье кишечника.
Дело в том, что разные микробы выполняют разные задачи, и чем более разнообразна эта рабочая сила, тем больше пользы мы получаем.
Но мало того, что мне недоставало разнообразия, так еще и группы бактерий, поселившиеся в моем кишечнике, были не самыми доброжелательными.
Анализ показал, что у меня в 65 раз больше Clostridium perfringens, чем у среднестатистического человека, и в 211 раз больше E.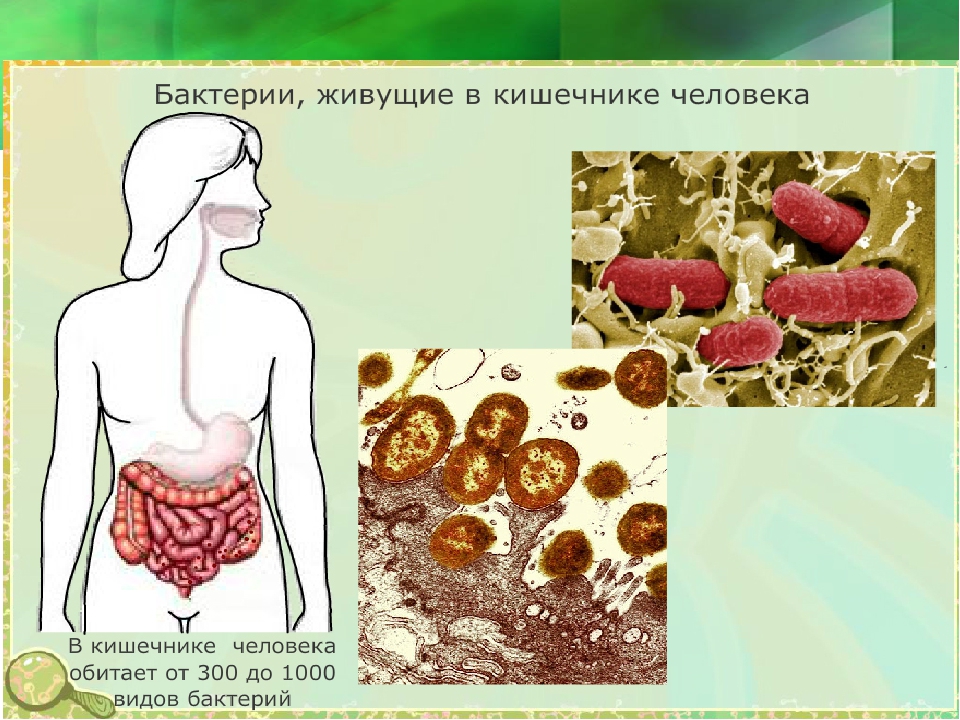 coli. Обе эти бактерии способны вызвать заболевания желудочно-кишечного тракта.
coli. Обе эти бактерии способны вызвать заболевания желудочно-кишечного тракта.
«Эти результаты указывают на то, что у вас очень нездоровый микробиом», — говорилось в выданном мне документе с результатами анализов.
Я, конечно же, мог бы попытаться оправдать себя тем, что был в командировке и, возможно, съел что-то сомнительное.
Однако Спектор заявил, что однократная инфекция вряд ли способна сильно сместить баланс в худшую сторону.
А как насчет полезных бактерий? Менее 100 видов бактерий способны вызвать инфекционные заболевания, в то время как тысячи видов микроорганизмов, живущих в кишечнике человека, как сказал бы писатель Дуглас Адамс, «практически безвредны».
Так как же у меня обстоят дела с теми, кто на моей стороне?
В самом начале списка «наиболее желательных» микроорганизмов находятся такие бактерии, как Akkermansia и труднопроизносимая Christensenellaceae. Обе помогают предотвратить набор веса.
Methanobrevibacter способствует лучшей усвояемости пищи, в результате чего вы можете есть меньше. Oxalobacter обеспечивает профилактику появления камней в почках.
Сколько этих полезных бактерий обнаружилось у меня? Ноль.
Итак, меня не просто причислили к самой худшей группе, но и прописали моему кишечнику строгий режим питания, пообещав отменить его только в том случае, если он хорошенько подумает о своем поведении и решит измениться.
Автор фото, SPL
Подпись к фото,Clostridium perfringens связывают с возникновением заболеваний желудочно-кишечного тракта
Что же я могу предпринять, чтобы улучшить свой микробиом? По-видимому, самое главное — это разнообразие.
Чем разнообразнее ваше питание, тем больше видов бактерий поселится в вашем кишечнике.
Особенно полезны для поддержания здорового микробиома ферментированные пищевые продукты.
«Люди знают о живых йогуртах, но восточный кисломолочный напиток под названием кефир — это совершенно другой уровень: в нем в пять раз больше микроорганизмов», — сказал мне Спектор.
Население наших внутренностей также будет очень радо другим ферментированным продуктам, в том числе супу мисо и кимчхи (квашеной капусте).
Если для вас все это звучит слишком экзотично, то имейте в виду, что полезные продукты с высоким содержанием пищевых волокон — это чеснок, артишоки, бананы и цельные злаки.
А полифенолы, содержащиеся в красном винограде — излюбленная пища бактерий Akkermansia. Я считаю это неплохим поводом выпить бокал вина.
В рекламе пробиотиков говорится, что они помогают повысить содержание бактерий в кишечнике, но на самом деле тратить на них деньги вряд ли стоит.
Доказательств того, что эти бактерии задерживаются в организме достаточно долго для того, чтобы изменить микробиом, слишком мало.
Однако было доказано, что они полезны как для очень маленьких, так и для пожилых пациентов и могут использоваться для профилактики расстройства желудка при приеме антибиотиков.
Но моему кишечнику они уже вряд ли помогут.
С тех пор, как я сделал это шокирующее открытие, я полностью изменил свое питание. С момента получения результатов анализа прошло больше месяца, и в течение всего этого времени я не ел мяса.
Суп мисо заменил мне фрикадельки, а кимчхи — рыбу с картошкой. Несмотря на то, что банка с кимчхи пахнет, гм… прикольно, моя жена заставляет меня держать ее в сарае.
Только время покажет, смогут ли эти перемены оказать долговременное влияние на мой микробиом.
Но я знаю, что сейчас я ем не только для себя, но и для триллионов микроорганизмов, населяющих мое тело.
Надеюсь, этот строгий режим не продлится слишком долго.
Прочитать оригинал этой статьи на английском языке можно на сайте BBC Future.
Совокупность микроорганизмов, обитающих в определенной среде — почве, воде, воздухе, пищевых продуктах, в организмах человека, животных и растений, 10 букв
Энциклопедический словарь, 1998 г.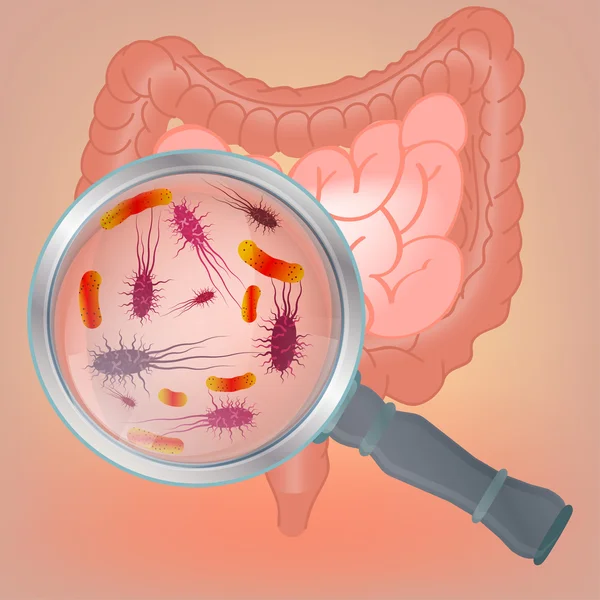 Значение слова в словаре Энциклопедический словарь, 1998 г.
Значение слова в словаре Энциклопедический словарь, 1998 г.
МИКРОФЛОРА (микробная флора) совокупность микроорганизмов, обитающих в определенной среде — почве, воде, воздухе, пищевых продуктах, в организмах человека, животных и растений. В 1 мл воды может содержаться от 5 до 100 тыс. клеток, в 1 г почвы — 2-3 млрд….
Википедия Значение слова в словаре Википедия
Микрофлора — совокупность разных типов микроорганизмов , населяющих какую-либо среду обитания . Микрофлора водоёмов , воздуха , горных пород , почвы очень разнообразна, микрофлора рубца жвачных , поровых растворов разных видов почв и т. п. более специфична…
Новый толково-словообразовательный словарь русского языка, Т. Ф. Ефремова. Значение слова в словаре Новый толково-словообразовательный словарь русского языка, Т. Ф. Ефремова.
ж. Совокупность микроорганизмов, обитающих в почве, воде, воздухе, пищевых продуктах, в организмах человека, животных и растений. Микроскопически мелкие ископаемые остатки вымерших растений (в палеонтологии).
Словарь медицинских терминов Значение слова в словаре Словарь медицинских терминов
сложившаяся в процессе эволюции устойчивая совокупность различных видов микроорганизмов, характерная для данного вида животного или растения, для определенной экологической ниши; совокупность видов микроорганизмов, обнаруженных на поверхности или в глубине. ..
..
Большая Советская Энциклопедия Значение слова в словаре Большая Советская Энциклопедия
(от микро… и флора ), совокупность микроорганизмов, находящихся в той или иной среде: почве, воде, воздухе, пищевых продуктах, в организмах человека, животных и растений и т. п. Обычно в естественных субстратах обитают разнообразные микроорганизмы: бактерии…
Микробиом кишечника
Кредит: Антуан Доре
Мы не одни в своем теле. Внутри каждого человека живут триллионы микроорганизмов — бактерий, вирусов, грибов и других форм жизни, которые вместе известны как микробиом. Различные органы имеют различных микробных обитателей, но группа, которая привлекла наибольшее внимание в биомедицинских исследованиях, — это кишечник.
Чтобы лучше понять роль, которую микробы кишечника играют в здоровье и болезнях, исследователи со всего мира исследуют, что делает микробиом кишечника «хорошим».В конце концов, в кишечнике существуют сотни различных видов бактерий — некоторые патогенные, а некоторые полезные. Компьютерный биолог Эран Сигал утверждает, что сбор данных о микробиоме позволит применить подход «глубокого фенотипирования», который может изменить открытие лекарств. А изучение некоторых видов пробиотиков, способствующих укреплению здоровья, дает биологические открытия, которые могут способствовать разработке лекарств.
В настоящее время считается, что на некоторые заболевания влияют процессы микробиома кишечника. К ним относятся рак, аутоиммунные заболевания, такие как рассеянный склероз и расстройство аутистического спектра.Микробиом кишечника также сильно взаимодействует с некоторыми лекарствами, в том числе с некоторыми терапевтическими средствами для психического здоровья, и влияет на их эффекты.
С ростом доказательств важности микробиома кишечника для здоровья биологи-синтетики стремятся создать микробиом — как на уровне отдельных видов, так и на уровне экосистемы — чтобы предотвратить развитие болезней. Также растет общественный интерес к тому, как можно повлиять на микробиом кишечника, часто сосредоточенный на личном диетическом выборе.Микробиолог Питер Тернбо рассматривает это как вопрос не о том, какие продукты принесут пользу нашему здоровью, а скорее о том, какие медицинские выводы можно почерпнуть из взаимодействия между нашими кишечными микробами и тем, что мы едим.
В настоящее время проводится гораздо больше исследований микробиома кишечника, чем может быть описано в этом обзоре, но эта добавка дает представление о широте этой надежной области.
Мы рады поблагодарить компанию Danone Nutricia Research за финансовую поддержку в подготовке настоящего обзора.Как всегда, Nature оставляет за собой исключительную ответственность за все редакционные материалы.
Что такое «карта» микробиома человека?
Что делает человеческое тело? По мнению исследователей, человеческие клетки рассказывают только половину истории. Другая половина связана с бесчисленным множеством микроорганизмов, составляющих микробиоту — «чужеродной» средой по всему нашему телу, которая, пока существует здоровый баланс, помогает нам процветать.
Поделиться на Pinterest Исследователи продолжают изучать роль кишечных бактерий в здоровье мозга и других частей тела.Чтобы получить дополнительную подтвержденную исследованиями информацию о микробиоме и его влиянии на ваше здоровье, посетите наш специализированный центр.
Человеческое тело содержит триллионы специализированных клеток — крошечных строительных блоков, которые собраны вместе, чтобы поддерживать развитие и функционирование тела.
Но человеческие клетки — не единственный «материал», из которого состоят наши тела. Фактически, мы тоже живем в симбиозе с триллионами микроорганизмов.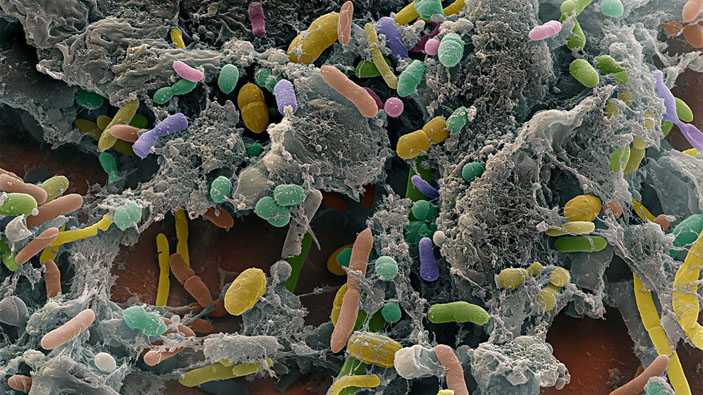
Исследователи давно спорят об истинном соотношении человеческих клеток и микроорганизмов в среднем организме.Оценки колебались, но последнее исследование, посвященное этому вопросу, появившееся в журнале PLOS Biology в 2016 году, предполагает, что в нашем теле и на нем, вероятно, столько же микроорганизмов, сколько в человеческих клетках.
Помимо бактерий и вирусов, к этим микроорганизмам относятся археи, примитивные организмы без ядра и эукариотические микроорганизмы, или эукарии, тип с ядром, которое защищает его хромосомы. К последней группе относятся грибы и простейшие, крошечные организмы на «границе» между растением и грибком.
Все они вместе составляют различную микробиоту: сообщества микроорганизмов, присутствующие в разных местах на теле человека или внутри него.
Микробиом человека состоит из разнообразной микробиоты: совокупности сообществ микроорганизмов, распространяющихся по всему человеческому телу.
Коллекции микроорганизмов в различных областях играют решающую роль в поддержании нашего здоровья — хотя для этого необходимо, чтобы количество различных типов бактерий, грибов и других микроорганизмов оставалось в идеальном равновесии.
Когда этот баланс нарушается и, например, происходит перенаселение одного вида бактерий, это может привести к инфекциям и другим проблемам со здоровьем.
Эта функция описывает различные организмы, обитающие в кишечнике, рту, влагалище и матке, половом члене, коже, глазах и легких.
Наиболее обсуждаемой средой для колонизации микроорганизмов, особенно бактерий, является кишечник человека.
Исследования показывают, что в желудочно-кишечном тракте человека находится обширная «коллекция бактерий, архей и эукариев», которые играют важную роль в гомеостазе кишечника, помогая поддерживать здоровье желудочно-кишечной системы.
Исследования также показали, что кишечные бактерии смягчают связь между кишечником и мозгом посредством взаимодействия с кишечной нервной системой и другими механизмами, которые могут быть гормональными или иммунологическими.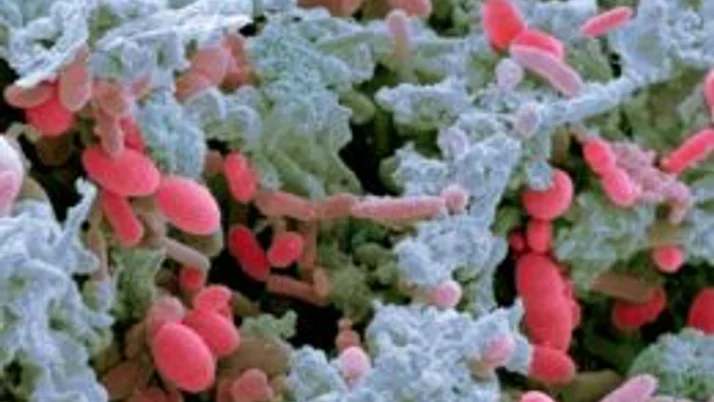
Основными типами или типами бактерий, присутствующими в кишечнике, являются Firmicutes и Bacteroidetes , которые составляют 90% микробиоты кишечника.
Другие: Actinobacteria , Proteobacteria , Fusobacterua и Verrucomicrobia .К ним относятся некоторые знакомые группы или роды бактерий из филы Firmicutes , такие как Lactobacillus , который известен своим положительным влиянием на здоровье.
С другой стороны, некоторые виды Firmicutes могут быстро вызвать заболевание, если они разрастаются, например Staphylococcus aureus и Clostridium perfringens .
Тип Proteobacteria включает некоторые хорошо известные патогенные группы, такие как Enterobacter, Helicobacter , Shigella и Salmonella , а также Escherichia coli .
Между тем, тип Actinobacteria включает вид Bifidobacterium bifidum , который обычно полезен для здоровых людей.
Однако этот список ни в коем случае не является исчерпывающим. Согласно собранным данным, в желудочно-кишечном тракте человека насчитывается около 2172 видов бактерий.
Если некоторые из этих названий казались неприятно знакомыми, это потому, что многие из этих бактерий могут вызвать инфекцию, если они чрезмерно колонизируют. А некоторые штаммы могут заразить кишечник через испорченную пищу или контакт с нечистыми поверхностями.
Некоторые штаммы E. coli могут вызывать инфекции, которые приводят к диарее и рвоте, некоторые штаммы S. aureus могут становиться устойчивыми к антибиотикам и вызывать тяжелые заболевания, а инфекции Salmonella могут вызывать диарейные заболевания.
Но кишечные бактерии обычно могут быть сильными союзниками в поддержании здоровья, и специалисты продолжают изучать множество способов, которыми эти микроорганизмы помогают нам оставаться в хорошей форме.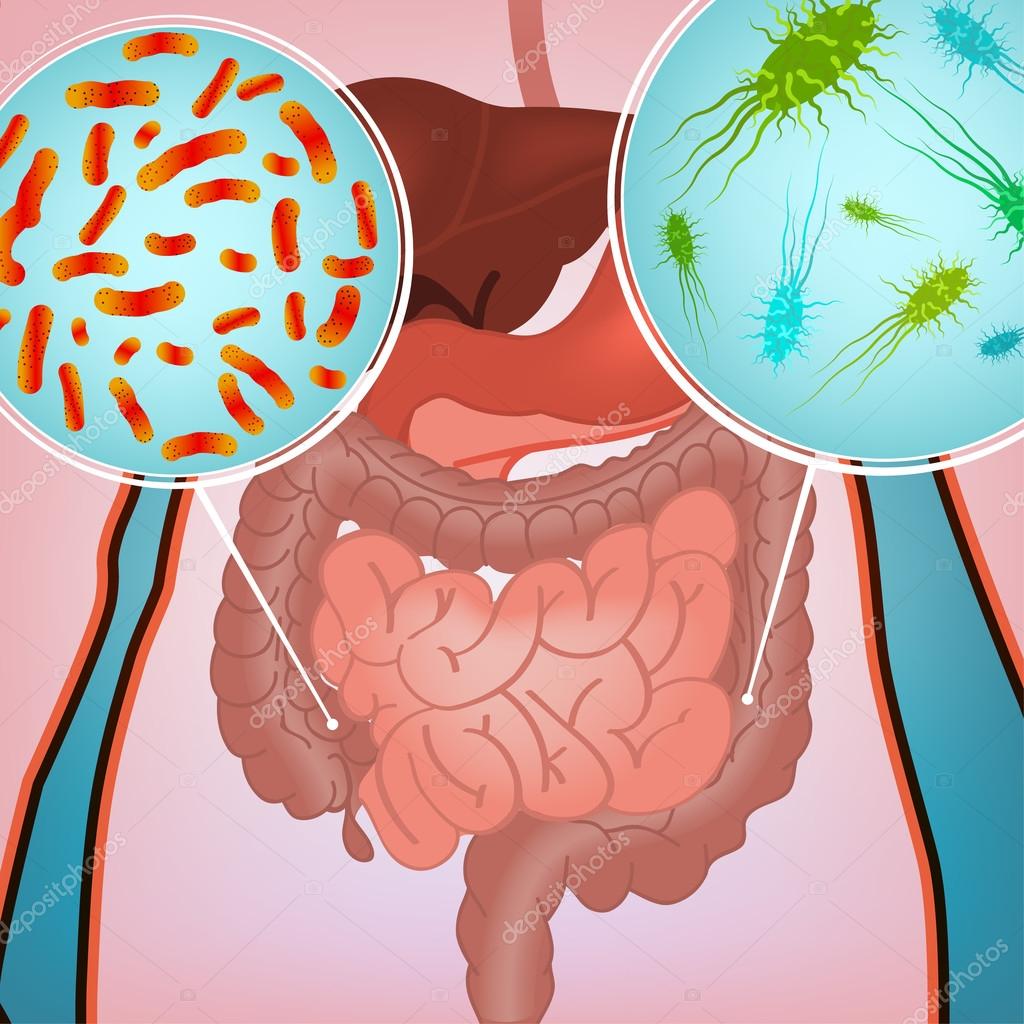
«Это новый рубеж медицины, и многие рассматривают микробиоту кишечника как дополнительную систему органов», — сказал специалист по инфекционным заболеваниям д-р.Элизабет Хохманн в интервью Гарвардской медицинской школе.
«[Микробиота кишечника] наиболее важна для здоровья нашей желудочно-кишечной системы, но может иметь еще более далеко идущие последствия для нашего благополучия», — добавила она.
Другие микроорганизмы, присутствующие в кишечнике, являются вирусами, но не теми, которые обычно вызывают болезни. Они относятся к типу, называемому «бактериофагами» — буквально «поедатели бактерий», — которые помогают поддерживать микробный баланс, беря на себя внутреннюю работу бактерий.
Бактериофаги «составляют подавляющее большинство вирусного компонента микробиома кишечника», и исследователи утверждали, что часть их роли заключается в заражении определенных бактерий для сохранения здорового баланса микроорганизмов в кишечнике. Тем не менее многое в них остается малоизученным.
Как и кишечник, во рту также содержится множество бактерий, необходимых для гомеостаза.
«В полости рта присутствует широкий спектр микроорганизмов. Он находится в постоянном контакте с окружающей средой и, как было доказано, уязвим к ней », — объясняют авторы обзора, опубликованного в журнале Journal of Oral and Maxillofacial Pathology в 2019 году.
Они продолжают, отмечая, что «различные поверхности во рту заселяются преимущественно бактериями полости рта», в зависимости от типа поверхности, к которой они прилипают, например, щеки, языка или зубов.
Микробиота полости рта содержит 12 типов бактерий — Firmicutes , Fusobacteria , Proteobacteria , Actinobacteria , Bacteroidetes , Chlamydiae , Chloroflexis SR , , Spirotetes Synergy , , Spirotetes Synergytes , , Spirotetes , Saccharibacteria и Gracilibacteria — с несколькими видами, названными или безымянными.
Но во рту также находятся другие микроорганизмы, а именно простейшие, наиболее распространенными из которых являются Entamoeba gingivalis и Trichomonas tenax , а также грибы и вирусы.
В ротовой полости насчитывается 85 родов грибов, включая Candida, Cladosporium, Aureobasidium, Saccharomycetales, Aspergillus, Fusarium и Cryptococcus .
«[Микробиота полости рта] играет решающую роль в поддержании гомеостаза полости рта, защите полости рта и предотвращении развития заболеваний», — пишут авторы обзора за 2019 год.
Как и в случае с другой микробиотой, несбалансированное количество микроорганизмов, населяющих ротовую полость, может привести к развитию болезни, например, различных бактериальных инфекций.
Гениталии человека и мочевыводящие пути также являются местом обитания большого количества микроорганизмов.
Что касается влагалища, исследования показывают, что «бактерии доминируют» в ландшафте, хотя на какие бактерии и в каком количестве трудно ответить.
Недавние исследования показывают, что компоненты бактериальных популяций во влагалище могут не только колебаться на разных стадиях менструального цикла, но также могут различаться у людей разных рас и этнических групп.
Некоторые типы бактерий, обнаруженные во влагалищном канале, включают Lactobacilli , Prevotella , Dialister , Gardnerella , Megasphaera , Eggerthella и Aerococcus .
«Кажется, что микробиота влагалища человека играет ключевую роль в предотвращении ряда урогенитальных заболеваний, таких как бактериальный вагиноз, дрожжевые инфекции, инфекции, передаваемые половым путем, инфекции мочевыводящих путей и ВИЧ-инфекция», — говорится в обзоре PNAS .
Вот почему специалисты советуют проявлять особую осторожность, когда дело касается интимной гигиены: многие продукты могут нарушить хрупкий бактериальный баланс в этой области.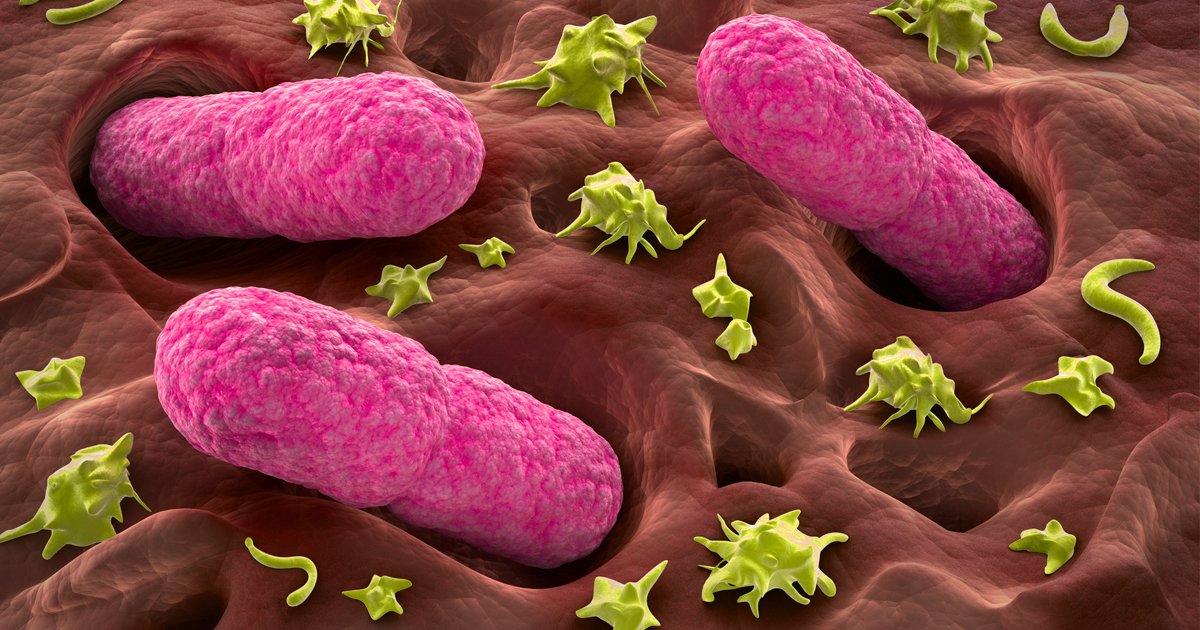
Однако в обзоре PNAS также отмечается, что «средства, с помощью которых [бактерии защищают от инфекции], плохо изучены».
Кроме того, о микробиоте матки известно немного. Ученые начали его изучать совсем недавно и пока только небольшими группами. Одно исследование показало, что Lactobacillus и Flavobacterium оказались наиболее распространенными бактериями в матке, независимо от того, беременна ли женщина.Более глубокие исследования продолжаются.
Мало что известно о микробиоте женского мочевого пузыря и уретры. В исследовании, опубликованном в журнале Current Opinion в Urology в 2017 году, отмечается, что «подавляющее большинство исследований здоровья мочевыводящих путей проводилось без знания или учета микробиоты женской мочевой системы».
После недавних исследований выяснилось, что наиболее распространенными типами бактерий в уретре женщин являются Lactobacillus , за которыми следуют Gardnerella, Corynebacterium, Streptococcus и Staphylococcus .
И хотя некоторые исследователи предполагают, что микробиота мочевого пузыря и женских мочевыводящих путей в значительной степени одинакова, другие допускают различия. Одно исследование, опубликованное в этом году в журнале Journal of Urology , обнаружило значительные различия.
Его авторы также предполагают, что бактериальные популяции женских нижних мочевыводящих путей могут варьироваться в зависимости от возраста, уровня сексуальной активности и от того, вступил ли человек в менопаузу.
Если исследователи все еще мало знают о микробиоте женских мочеполовых органов, они, похоже, еще меньше знают о микробиоте мужских мочеполовых органов.
A PLOS One исследование , проведенное в 2010 году, в ходе независимого от посева исследования выявило различия в микробных сообществах на обрезанных и необрезанных пенисах.
В частности, бактерии семейств Clostridiales и Prevotellaceae оказались более многочисленными на необрезанных пенисах.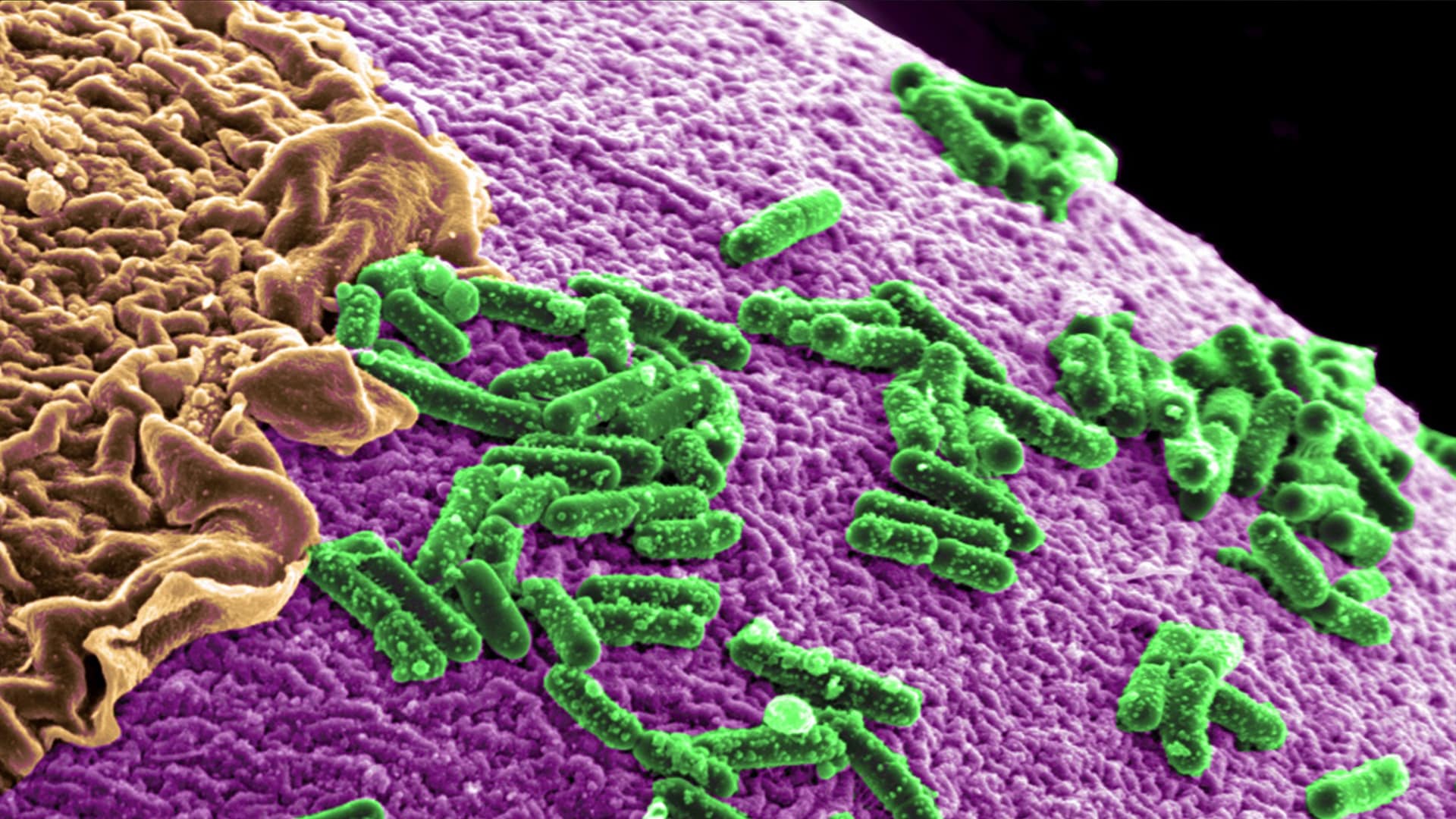
Такие различия, как отмечают авторы статьи, могут играть роль в воспалении и подверженности инфекциям.
«У необрезанных мужчин на половом члене значительно больше бактерий, и типы бактерий также сильно различаются», — отметил соавтор исследования д-р.Синди Лю в интервью.
Кроме этого, очень мало известно о микробиоте полового члена. В том же интервью профессор Дебора Андерсон, преподающая акушерство, гинекологию и микробиологию в Медицинской школе Бостонского университета, прокомментировала:
«Пенис недостаточно изучен. Там может быть очень интересная история, но мы не провели должного исследования ».
Как и кишечник, кожа человека является домом для множества бактерий и многих видов грибов.
Обзор, опубликованный в журнале Nature Reviews Microbiology в 2018 году, объясняет, что бактериальные популяции широко варьируются в зависимости от региона кожи, а также зависят от ряда факторов, таких как влажность кожи и количество натурального масла или кожного сала. .
Согласно обзору, «в сальных участках преобладали виды […] Propionibacterium , тогда как бактерии, которые процветают во влажной среде, такие как виды Staphylococcus и Corynebacterium , были преимущественно многочисленны во влажных областях, включая сгибания в локтях и стопах.”
Сообщества грибов, однако, по-видимому, довольно последовательны по составу, независимо от типа кожи, на которой они обитают.
По словам исследователей, наиболее распространены грибы рода Malassezia по всему телу и на коже рук. Напротив, комбинация Malassezia , Aspergillus , Cryptococcus , Rhodotorula и Epicoccum среди других наиболее часто встречается на коже стоп.
Наиболее распространенными микроорганизмами на коже человека являются бактерии, а наименее распространенными — грибки.
Бактерии на коже могут предотвращать вторжение патогенов и способствовать развитию болезни, в зависимости от того, какие колонии преобладают. Как пишут авторы исследования:
Как пишут авторы исследования:
«Взаимодействия между членами микробиоты как формируют резидентное микробное сообщество, так и предотвращают колонизацию патогенными бактериями в процессе, называемом« устойчивость к колонизации »».
«В определенных контекстах, — продолжают они, — бактерии, которые обычно полезны для их хозяев, могут стать патогенными.Многие распространенные кожные заболевания связаны с изменениями микробиоты, называемыми дисбактериозом ».
Бактерии преобладают на многих участках эпителиальной ткани, включая конъюнктиву, ткань, выстилающую внутреннюю часть век.
Согласно исследованию, проведенному в 2011 году, на конъюнктиве здорового человека присутствует по крайней мере пять бактериальных типов и 59 родов.
Преобладающими родами бактерий являются: Pseudomonas, Propionibacterium, Bradyrhizobium, Corynebacterium, Acinetobacter, Brevundimonas, Staphylococci, Aquabacterium, Sphingomonas, Streptococcus, Streptophyta и Streptophyta Methlobacter и .
Также присутствуют некоторые грибы, в том числе виды Candida , Aspergillus и Penicillium .
На данный момент роль микробиома конъюнктивы остается неясной.
Мы часто думаем о бактериях в легких только в контексте респираторных заболеваний. Однако бактерии присутствуют и в здоровых легких.
Некоторые из наиболее распространенных типов бактерий в здоровых легких — это Firmicutes , Bacteriodetes , Proteobacteria , Fusobacteria и Actinobacteria , согласно обзору от 2017 года.Некоторые из наиболее распространенных родов — это Prevotella , Veillonella, и Streptococcus .
Когда хрупкий баланс бактериальных популяций в легких нарушается, это может привести к развитию таких заболеваний, как астма и хроническая обструктивная болезнь легких.
При астме, например, увеличивается количество бактерий Haemophilus и Neisseria , а количество бактерий Prevotella и Veillonella уменьшается. Это подтверждает гипотезу о том, что дисбактериоз микробиома легких может быть основной причиной астмы.
Это подтверждает гипотезу о том, что дисбактериоз микробиома легких может быть основной причиной астмы.
Команда, проводившая обзор 2017 года, подчеркивает необходимость дальнейших исследований механизмов, связанных с микробиотой, которые могут влиять на здоровье легких, отмечая, что «вероятные сложные взаимодействия между бактериями, вирусами и грибами следует учитывать в будущих исследованиях».
Микробиом человека представляет собой сложную систему, и исследователи продолжают узнавать больше о ее важной роли в здоровье человека и болезнях.Забегая вперед, ученые стремятся глубже погрузиться в тайны этого микромира.
Желудочно-кишечные микроорганизмы и другие животные-хозяева
Желудочно-кишечные микроорганизмы и животные
Микроорганизмы желудочно-кишечного тракта существуют в симбиотических ассоциациях с животными. Микроорганизмы в кишечнике участвуют в переваривании кормов, защищают животное от инфекций, а некоторые микробы даже синтезируют и поставляют необходимые питательные вещества своему животному-хозяину. Следовательно, понимание сложных симбиотических взаимоотношений между желудочно-кишечными микробами и их животными-хозяевами может привести к разработке методов улучшения продуктивности животных и укрепления здоровья животных.
Пищеварительные стратегии
Животные часто классифицируются в соответствии с их физиологией пищеварения, а микроорганизмы желудочно-кишечного тракта могут быть исследованы в соответствии с расположением кишечника: передняя кишка (перед желудочным желудком), средняя кишка (тонкий кишечник) и задняя кишка (толстая кишка) (4, 5). Ферменты, выделяемые во рту и желудке, способствуют расщеплению пищи, потребляемой животными. Микроорганизмы, обитающие в других областях желудочно-кишечного тракта, также могут способствовать расщеплению кормов с помощью процесса, называемого ферментацией.Ферментация — это анаэробное разложение органических соединений.
Ферментеры преджелудочной, слепой и толстой кишки — это описательные термины, используемые для обозначения места в пищеварительном тракте, где происходит большая часть микробной активности. Преджелудочные ферментеры (перед желудочным желудком) включают жвачных животных, таких как коровы, овцы и жирафы. Когда большая часть ферментативной активности происходит в слепой кишке, животных можно охарактеризовать как ферментеров слепой кишки (морские свинки, кролики, шиншиллы, крысы и т. Д.).). Ферментеры толстой кишки (гориллы, пони, слоны и т. Д.) Имеют большую часть ферментации, происходящей в толстой кишке.
Преджелудочные ферментеры (перед желудочным желудком) включают жвачных животных, таких как коровы, овцы и жирафы. Когда большая часть ферментативной активности происходит в слепой кишке, животных можно охарактеризовать как ферментеров слепой кишки (морские свинки, кролики, шиншиллы, крысы и т. Д.).). Ферментеры толстой кишки (гориллы, пони, слоны и т. Д.) Имеют большую часть ферментации, происходящей в толстой кишке.
Лаборатория Ангерта исследовала микробные сообщества, обитающие в желудочно-кишечном тракте рыб-хирургов, морских свинок, коров и горилл. Поэтому следующее обсуждение будет сосредоточено на этих животных.
Рыба-хирург
В семействе рыб-хирургов (Acanthuridae) около 80 видов рыб. Большинство рыб-хирургов — травоядные животные (в основном едят водоросли), а у травоядных видов, как правило, длинные кишечные тракты по сравнению с хищными рыбами того же размера (4, 5).Длинный кишечник обеспечивает более длительное время удержания перевариваемой пищи и способствует интенсивной ферментации. Рыба-хирург является хозяином Epulopiscium spp., Членов линии грамположительных бактерий с низким содержанием G + C. Ученые наблюдали за поведением рыб-хирургов в дикой природе и обнаружили, что молодые рыбы-хирурги поедают фекалии взрослых рыб-хирургов (1). Такое поведение может помочь рыбам развить микробные сообщества кишечника.
Морские свинки
У морских свинок большая слепая кишка, и, как и у травоядных рыб-хирургов, морские свинки копрофаги; они едят собственные фекалии! Помимо получения кишечных микробов, прием фекалий позволяет животным восстанавливать больше питательных веществ и витаминов (2, 4).Одним из ближайших известных родственников Epulopiscium является бактерия под названием Metabacterium polyspora . M. polyspora также является грамположительной бактерией с низким содержанием G + C и желудочно-кишечным симбионтом морских свинок. Жизненный цикл M. polyspora использует копрофагальную природу морских свинок-хозяев. Эта бактерия производит спящие эндоспоры, которые можно найти в кале морской свинки. Копрофагия позволяет Metabacterium повторно проникать в желудочно-кишечный тракт хозяина или колонизировать новых хозяев.
Эта бактерия производит спящие эндоспоры, которые можно найти в кале морской свинки. Копрофагия позволяет Metabacterium повторно проникать в желудочно-кишечный тракт хозяина или колонизировать новых хозяев.
Целлюлоза, полимер, состоящий из ß 1-4-связанных глюкозных единиц, является самым распространенным в мире углеводом. Животные часто употребляют пищу, богатую целлюлозой. У млекопитающих отсутствуют ферменты, расщепляющие целлюлозу, но часто в желудочно-кишечном тракте содержатся микроорганизмы, способные выполнять эту важную функцию. Например, разлагающие волокна бактерии в рубце могут ферментировать целлюлозу.Микроскопические изображения трех распространенных целлюлолитических бактерий рубца представлены ниже: (A) Fibrobacter succinogenes , (B) Ruminococcus albus и (C) Ruminococcus flavefaciens .
Цель веб-сайта
Помимо бактерий, разлагающих целлюлозу, нашу лабораторию интересуют метаногены, группа микроорганизмов рубца, принадлежащих к домену архей. Метаногены имеют большое экономическое и экологическое значение, поскольку они производят метан (Ch5), важный парниковый газ и способствующий глобальному потеплению.Когда жвачные животные отрыгивают (отрыжка), Ch5, образующийся в рубце, выбрасывается в атмосферу. Также происходит метаногенез в задней кишке. Метан, производимый в кишечнике жвачных животных, оказывает влияние на глобальное потепление, хотя масштабы этого источника еще полностью не определены.
Гориллы
Гориллы имеют большую толстую кишку (5) и, вероятно, являются ферментерами толстой кишки. Гориллы — травоядные животные, и их рацион состоит из листьев, коры, стеблей, побегов и фруктов (3). Недавно мы выделили последовательности генов из фекалий дикой гориллы, проживающей в Национальном парке Бвинди, Уганда.Последовательности были связаны со следующими типами бактерий: Firmicutes (или грамположительные бактерии с низким G + C), Actinobacteria, Bacteriodetes, Lentisphaerae, Planctomycetes, Spirochetes и Verrucomicrobia (). Некоторые из последовательностей были очень похожи на последовательности бактерий, которые разрушают клетчатку, восстанавливают ароматические соединения (танины) и ферментируют простые и неструктурные углеводы. Эти бактерии, вероятно, сбраживают корм в желудочно-кишечном тракте горилл. Они также могут помочь вывести токсины из танинов, антипитательных соединений, которые связывают ценный белок и снижают вкусовые качества.
Некоторые из последовательностей были очень похожи на последовательности бактерий, которые разрушают клетчатку, восстанавливают ароматические соединения (танины) и ферментируют простые и неструктурные углеводы. Эти бактерии, вероятно, сбраживают корм в желудочно-кишечном тракте горилл. Они также могут помочь вывести токсины из танинов, антипитательных соединений, которые связывают ценный белок и снижают вкусовые качества.
Симбиотическое взаимодействие между желудочно-кишечными микробами и их животным-хозяином позволяет животным максимально использовать питательные вещества, которые они получают из потребляемых ими продуктов. Следует отметить, что грамположительные бактерии с низким содержанием G + C являются важными микроорганизмами в пищеварительном тракте и обычно встречаются в больших количествах у рыб-хирургов, морских свинок, жвачных животных, свиней, людей и горилл. Поскольку микробы выполняют жизненно важные функции во всем кишечнике, характеристика как типов, так и функций этих микроорганизмов позволит ученым разработать эффективные стратегии управления.Затем могут быть внедрены методы, способствующие сохранению животных, а также улучшающие здоровье и продуктивность животных.
Список литературы
- Клементс, К. Д. 1997. Ферментация и желудочно-кишечные микроорганизмы у рыб, с. 156–198. В R. I. Mackie и B.A. White (ed.), Gastrointestinal Microbiology: Gastrointestinal Ecosystems and Fermentations, vol. 1. Чепмен и Холл, Нью-Йорк.
- Holtenius, K., and C. Björnhag. 1985. Механизм разделения толстой кишки у морской свинки (Cavia porcellus) и шиншиллы (Chinchilla laniger).Комп. Биохим. Phys. А. 82: 537-542.
- Ротман, Дж. М., А. Н. Пелл, Э. С. Диренфельд, Д. О. Молина, А. В. Шоу и Х. Ф. Хинц. Пищевая химия рациона горилл в Национальном парке Бвинди, Уганда. Являюсь. J. Primatol., In Press.
- Стивенс, К. Э. и И. Д. Хьюм. 1995. Сравнительная физиология пищеварительной системы позвоночных, Кембридж, Соединенное Королевство.
 Издательство Кембриджского университета.
Издательство Кембриджского университета. - Стивенс К. Э. и И. Д. Хьюм. 1998. Вклад микробов в желудочно-кишечном тракте позвоночных в производство и сохранение питательных веществ.Physiol. Откр.78: 393-427.
- Фрей, Дж. К., Дж. М. Ротман, А. Н. Пелл, Дж. Боско Низей, М. Р. Крэнфилд и Э. Р. Ангерт. 2006. Бактериальное разнообразие фекалий у дикой гориллы. Appl Environ Microbiol 71: 3788-3792.
Полезные ссылки
Полезные книги: микробиология рубца
- Хеспелл Р. Б., Д. Э. Акин и Б. А. Дехорити. 1997. Бактерии, грибы и простейшие рубца, с. 59-141. В R. I. Mackie, B.A. White и R.E. Isaacson (ed.), Gastrointestinal Microbiology, vol.2. Чепмен и Холл, Нью-Йорк.
- Хобсон, П. Н. и С. С. Стюарт (ред.). 1997. Микробная экосистема рубца, стр. 719, 2 изд. Chapman & Hall, Саффолк, Великобритания.
- Hungate, R. E. 1966. Рубец и его микробы. Academic Press, Нью-Йорк.
Неинвазивный зонд следит за здоровьем «дружественных» кишечных бактерий
Поделиться на PinterestФотография: Бактерии в чашке Петри.Фотография любезно предоставлена Никола Фосетт / Викимедиа
- Сообщество бактерий, обитающих в кишечнике, известное как кишечная микробиота, играет ключевую роль в таких заболеваниях, как рак, диабет, ожирение, депрессия и воспалительные заболевания кишечника.
- Цель пробиотических и пребиотических добавок — восстановить здоровый баланс микробиома, но их влияние трудно изучить.
- Исследователи разработали зонд, который может измерять уровень активности фермента, продуцируемого бактериями, который играет ключевую роль в укреплении их здоровья.
- Женщина-доброволец проглотила две капсулы, содержащие зонд, который контролировал микробное здоровье по всей длине ее пищеварительной системы.
Микробиота кишечника — это сообщество бактерий, грибов, вирусов и других микроорганизмов, обитающих в пищеварительном тракте человека.
В последние годы ученые обнаружили удивительный диапазон взаимодействий между кишечной микробиотой и здоровьем человека. К ним относятся влияние на настроение, расстройства пищевого поведения и иммунитет.
Недавнее исследование, опубликованное Medical News Today, также обнаружило связь между конкретными видами бактерий и риском развития диабета, сердечных заболеваний и ожирения.
Бактерии в кишечнике вырабатывают фермент, называемый гидролазой желчных солей (BSH), который может иметь важное значение для многих их полезных эффектов.
Например, ученые связали высокую активность BSH со снижением воспаления, снижением уровня холестерина в крови и защитой от рака толстой кишки и инфекций мочевыводящих путей.
Ученые все еще на удивление мало знают о сложных взаимодействиях между диетой, кишечной микробиотой и активностью BSH.
Недавно международная группа исследователей приступила к изучению влияния пребиотиков — нерастворимых пищевых волокон, которые способствуют росту «дружественных» бактерий — на активность BSH.
Они также хотели разработать клинический тест для оценки активности фермента у людей с воспалительным заболеванием кишечника.
В настоящее время микробиологи используют косвенные методы для измерения активности фермента, например, анализируя образцы фекалий или культивируя бактерии в лаборатории. Но эти усилия не отражают разнообразие бактерий и химическую сложность их естественной среды, которая варьируется в зависимости от того, где они живут в желудочно-кишечном тракте.
Итак, группа ученых под руководством исследователей из Университета Миссури в Колумбии и Швейцарского федерального технологического института в Лозанне разработала неинвазивный химический зонд, который измеряет активность BSH по всей длине кишечника.
Они опубликовали свои выводы в журнале Science Advances .
Зонд основан на естественном соединении под названием люциферин, которое излучает свет в присутствии кислорода, и ферменте люциферазе, который образуется у светлячков.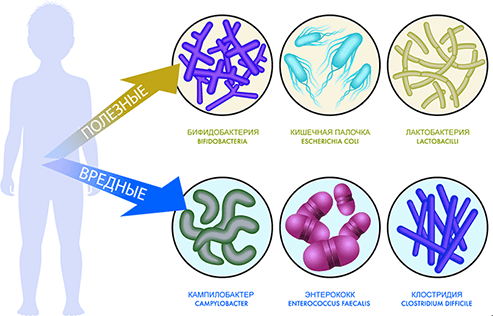
Чтобы создать зонд, исследователи химически «заключили» люциферин в клетку, соединив его с небольшой молекулой, которая защищает его от люциферазы.
Они сконструировали клетку так, что только фермент BSH может высвобождать молекулу люциферина из зонда.В результате количество света, которое производит образец кала в присутствии люциферазы, пропорционально количеству BSH по длине кишечника.
Ученые сначала проверили свой зонд на образцах в лаборатории. Затем женщина-доброволец проглотила две капсулы, содержащие зонд, и они успешно измерили активность фермента при прохождении через ее кишечник.
«До сих пор у нас не было никаких способов неинвазивного мониторинга активности в неповрежденном желудочно-кишечном тракте, учитывая уникальную химическую среду, изменчивое распределение и очень динамичный характер микробиоты кишечника», — говорит д-р.Елена Гун, доцент кафедры химии университета и старший автор статьи.
В другом эксперименте на мышах команда использовала зонд, чтобы проверить способность различных типов пребиотических добавок — инулина и фруктоолигосахаридов (ФОС) — увеличивать производство BSH.
Они обнаружили, что инулин не вызывает значительного изменения уровня BSH в кишечнике животных, но ФОС удваивают эти уровни.
Доктор Гун объясняет важность результатов своей команды:
«Пребиотики часто используются в сочетании с пробиотиками для улучшения их функций в организме.[…] Мы впервые показываем, что определенные типы пребиотиков сами по себе способны увеличивать активность [BSH] микробиоты кишечника, что, помимо других преимуществ для здоровья, снижает воспаление, снижает уровень холестерина в крови и защищают от рака толстой кишки и инфекций мочевыводящих путей ».
Старший научный сотрудник добавляет, что также может быть существенная экономическая выгода, поскольку производство и хранение пребиотиков обходятся дешевле, чем пробиотики.
Ваши кишечные бактерии и ваше здоровье
В течение многих лет мы думали о бактериях как о организмах, которых следует избегать. Оказывается, наши тела уже загружены триллионами бактерий. Они помогают переваривать пищу и играют важную роль в вашем благополучии.
Оказывается, наши тела уже загружены триллионами бактерий. Они помогают переваривать пищу и играют важную роль в вашем благополучии.
Исследования показывают, что кишечные бактерии связаны с вероятностью таких заболеваний, как диабет, ожирение, депрессия и рак толстой кишки.
Что такое кишечные бактерии?
Внутри кишечника живут от 300 до 500 различных видов бактерий, содержащих почти 2 миллиона генов. В сочетании с другими крошечными организмами, такими как вирусы и грибы, они образуют так называемую микробиоту, или микробиом.
Подобно отпечатку пальца, микробиота каждого человека уникальна: смесь бактерий в вашем теле отличается от смеси всех остальных. Это частично определяется микробиотой вашей матери — окружающей средой, в которой вы находитесь при рождении, — а частично — вашим питанием и образом жизни.
Бактерии живут по всему телу, но те, что находятся в кишечнике, могут иметь наибольшее влияние на ваше самочувствие. Они выстилают всю вашу пищеварительную систему. Большинство из них живут в кишечнике и толстой кишке. Они влияют на все, от вашего метаболизма до настроения и иммунной системы.
Кишечные бактерии и болезни
Исследования показывают, что кишечные бактерии у здоровых людей отличаются от бактерий, страдающих определенными заболеваниями. У больных людей может быть слишком мало или слишком много определенного типа. Или в них может отсутствовать большое количество бактерий. Считается, что некоторые виды могут защитить от болезней, а другие могут повысить риск.
Ученые начали устанавливать связь между следующими заболеваниями и бактериями в кишечнике:
Ожирение, диабет 2 типа и болезни сердца: Кишечные бактерии влияют на обмен веществ в организме.Они определяют такие вещи, как количество калорий, которые вы получаете из пищи, и какие питательные вещества вы из нее извлекаете. Слишком большое количество кишечных бактерий может заставить вас превратить клетчатку в жирные кислоты. Это может вызвать жировые отложения в печени, что может привести к так называемому «метаболическому синдрому» — состоянию, которое часто приводит к диабету 2 типа, сердечным заболеваниям и ожирению.
Это может вызвать жировые отложения в печени, что может привести к так называемому «метаболическому синдрому» — состоянию, которое часто приводит к диабету 2 типа, сердечным заболеваниям и ожирению.
Воспалительные заболевания кишечника, включая болезнь Крона и язвенный колит: Считается, что у людей с этими состояниями более низкий уровень некоторых противовоспалительных кишечных бактерий.Точная связь пока неясна. Но считается, что некоторые бактерии могут заставить ваше тело атаковать кишечник и подготовить почву для этих заболеваний.
Продолжение
Рак толстой кишки: Исследования показывают, что у людей с этим заболеванием другая кишечная микробиота, включая более высокий уровень болезнетворных бактерий, чем у здоровых людей.
Беспокойство, депрессия и аутизм: Кишечник заполнен нервными окончаниями, которые взаимодействуют с мозгом. Ваш врач может назвать эту связь «осью кишечник-мозг».Исследования показали связь между кишечными бактериями и расстройствами центральной нервной системы, такими как тревога, депрессия и расстройство аутистического спектра.
Артрит: Считается, что у людей с ревматоидным артритом может быть большее количество бактерий, связанных с воспалением, чем у людей без них.
Что ты умеешь?
Как получить здоровые кишечные бактерии?
Начните с питательной диеты с высоким содержанием пищевых волокон, таких как фрукты, овощи и цельнозерновые продукты.«Западная» диета с высоким содержанием жира и сахара и низким содержанием клетчатки может убить определенные типы кишечных бактерий, что сделает вашу микробиоту менее разнообразной.
Ограничьте использование антибиотиков, которые могут уничтожить здоровые бактерии вместе с проблемными бактериями, только в случае необходимости, как это определено вашим доктором.
Продолжение
Физические упражнения также могут стимулировать рост различных кишечных бактерий. Более разнообразная микробиота кишечника может способствовать лучшему здоровью и, в свою очередь, снизить риск заболевания.
Пробиотики нельзя принимать только для предотвращения диабета или лечения артрита. Эксперты говорят, что необходимо провести дополнительные исследования, чтобы точно определить типы бактерий, которые вызывают определенные заболевания.
Вскоре вы сможете принимать лекарства или добавки, приготовленные из определенного штамма кишечных бактерий, чтобы снизить риск или даже вылечить определенные заболевания.
Микробиом | Источник питания
Перейти к:
Что такое микробиом?
Как микробиота приносит пользу организму
Роль пробиотиков
Может ли диета повлиять на микробиоту человека?
Будущие направления исследований
Что такое микробиом?
Представьте себе шумный город утром в будний день, тротуары заполнены людьми, спешащими на работу или на встречи.Теперь представьте это на микроскопическом уровне, и вы получите представление о том, как выглядит микробиом внутри нашего тела, состоящий из триллионов микроорганизмов (также называемых микробиотой или микробами) тысяч различных видов. [1] К ним относятся не только бактерии, но и грибы, паразиты и вирусы. У здорового человека эти «жучки» мирно сосуществуют, причем наибольшее их количество обнаруживается в тонком и толстом кишечнике, а также во всем теле. Микробиом даже называют поддерживающим органом, потому что он играет очень много ключевых ролей в обеспечении бесперебойной повседневной работы человеческого тела.
У каждого человека есть совершенно уникальная сеть микробиоты, которая изначально определяется его ДНК. Человек впервые сталкивается с микроорганизмами в младенчестве, во время родов через родовые пути и через грудное молоко матери. [1] То, каким именно микроорганизмам подвергается младенец, зависит исключительно от вида, обнаруженного у матери. Позже воздействие окружающей среды и диета могут изменить микробиом человека, сделав его полезным для здоровья или подвергнуть его большему риску заболевания.
Микробиом состоит из полезных и потенциально вредных микробов. Большинство из них являются симбиотическими (от которых выигрывают и человеческое тело, и микробиота), а некоторые, в меньшем количестве, являются патогенными (способствуют развитию болезни). В здоровом организме без проблем сосуществуют патогенная и симбиотическая микробиота. Но если есть нарушение этого баланса, вызванное инфекционными заболеваниями, определенными диетами или длительным использованием антибиотиков или других препаратов, уничтожающих бактерии, возникает дисбактериоз, прекращающий эти нормальные взаимодействия.В результате организм может стать более восприимчивым к болезням.
Как микробиота приносит пользу организму
Микробиота стимулирует иммунную систему, расщепляет потенциально токсичные пищевые соединения и синтезирует определенные витамины и аминокислоты [2], включая витамины группы B и витамин K. Например, ключевые ферменты, необходимые для образования витамина B12, содержатся только в бактериях, не у растений и животных. [3]
Сахара, такие как столовый сахар и лактоза (молочный сахар), быстро всасываются в верхней части тонкой кишки, но более сложные углеводы, такие как крахмалы и волокна, не так легко перевариваются и могут перемещаться ниже в толстую кишку.Там микробиота помогает расщеплять эти соединения с помощью их пищеварительных ферментов. Ферментация неперевариваемых волокон вызывает производство короткоцепочечных жирных кислот (SCFA), которые могут использоваться организмом в качестве источника питательных веществ, но также играют важную роль в функции мышц и, возможно, в профилактике хронических заболеваний, включая некоторые виды рака и расстройства кишечника. . Клинические исследования показали, что SCFA могут быть полезны при лечении язвенного колита, болезни Крона и диареи, связанной с антибиотиками.[2]
Микробиота здорового человека также обеспечивает защиту от патогенных организмов, попадающих в организм, например, через питье или употребление зараженной воды или пищи.
Крупные семейства бактерий, обнаруженных в кишечнике человека, включают Prevotella , Ruminococcus , Bacteroides и Firmicutes . [4] В толстой кишке, в среде с низким содержанием кислорода, вы найдете анаэробные бактерии Peptostreptococcus, Bifidobacterium , Lactobacillus и Clostridium .[4] Считается, что эти микробы предотвращают чрезмерный рост вредных бактерий, конкурируя за питательные вещества и места прикрепления к слизистой оболочке кишечника, которая является основным местом иммунной активности и производства антимикробных белков. [5,6]
Роль пробиотиков
Если микробиота так важна для нашего здоровья, как мы можем гарантировать, что у нас есть достаточное количество или правильные типы? Возможно, вы знакомы с пробиотиками или, возможно, уже используете их. Это либо продукты, которые от природы содержат микробиоту, либо таблетки-добавки, содержащие живые активные бактерии, рекламируемые для улучшения здоровья пищеварительной системы.Продажи пробиотических добавок превысили 35 миллиардов долларов в 2015 году с прогнозируемым увеличением до 65 миллиардов долларов к 2024 году. Верите ли вы в заявления о здоровье или думаете, что это еще одна афера со змеиным маслом, они составляют многомиллиардную отрасль, которая развивается в тандеме с быстро появляющиеся исследования.
Д-р Аллан Уокер, профессор питания Гарвардской школы общественного здравоохранения и Гарвардской медицинской школы, считает, что, хотя опубликованные исследования противоречат друг другу, существуют определенные ситуации, когда пробиотические добавки могут быть полезны.«Пробиотики могут быть наиболее эффективными для обоих концов возрастного спектра, потому что в этом случае ваши микробы не так устойчивы, как обычно», — объясняет Уокер. «В эти периоды вы можете более эффективно влиять на этот огромный процесс бактериальной колонизации с помощью пробиотиков». Он также отмечает ситуации стресса для организма, когда пробиотики могут быть полезны, например, уменьшение тяжести диареи после контакта с патогенами или восстановление нормальных бактерий в кишечнике после того, как пациент принимает антибиотики. Тем не менее, Уокер подчеркивает, что «это все обстоятельства, при которых происходит нарушение баланса в кишечнике. Если вы имеете дело со здоровым взрослым или более старшим ребенком, который не принимает антибиотики, я не думаю, что введение пробиотика будет настолько эффективным для общего улучшения их здоровья ».
Тем не менее, Уокер подчеркивает, что «это все обстоятельства, при которых происходит нарушение баланса в кишечнике. Если вы имеете дело со здоровым взрослым или более старшим ребенком, который не принимает антибиотики, я не думаю, что введение пробиотика будет настолько эффективным для общего улучшения их здоровья ».
Поскольку пробиотики относятся к категории добавок, а не продуктов питания, они не регулируются Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США.Это означает, что если компания, производящая добавки, добровольно не раскроет информацию о качестве, например, наличие USP (U.S. Pharmacopeial Convention) печать, которая обеспечивает стандарты качества и чистоты, пробиотические таблетки могут не содержать количества, указанные на этикетке, или даже не гарантировать, что бактерии живы и активны во время использования.
Может ли диета повлиять на микробиоту человека?
Помимо семейных генов, окружающей среды и использования лекарств, диета играет большую роль в определении того, какие виды микробиоты обитают в толстой кишке. [2] Все эти факторы создают уникальный микробиом от человека к человеку.В частности, диета с высоким содержанием клетчатки влияет на тип и количество микробиоты в кишечнике. Пищевые волокна могут быть расщеплены и ферментированы только ферментами микробиоты, обитающей в толстой кишке. Короткоцепочечные жирные кислоты (SCFA) высвобождаются в результате ферментации. Это снижает pH толстой кишки, что, в свою очередь, определяет тип присутствующей микробиоты, которая выживет в этой кислой среде. Более низкий уровень pH ограничивает рост некоторых вредных бактерий, таких как Clostridium difficile . Растущие исследования SCFA исследуют их широкое влияние на здоровье, включая стимуляцию активности иммунных клеток и поддержание нормального уровня глюкозы и холестерина в крови.
Продукты, поддерживающие повышенный уровень SCFA, — это неперевариваемые углеводы и волокна, такие как инулин, резистентные крахмалы, камеди, пектины и фруктоолигосахариды. Эти волокна иногда называют пребиотиками, потому что они питают нашу полезную микробиоту. Хотя существуют добавки, содержащие пребиотические волокна, существует множество полезных для здоровья продуктов, содержащих пребиотики. Наибольшее количество содержится в сырых вариантах следующих ингредиентов: чеснок, лук, лук-порей, спаржа, топинамбур, зелень одуванчика, бананы и водоросли.В целом, фрукты, овощи, бобы и цельнозерновые продукты, такие как пшеница, овес и ячмень, являются хорошими источниками пребиотических волокон.
Эти волокна иногда называют пребиотиками, потому что они питают нашу полезную микробиоту. Хотя существуют добавки, содержащие пребиотические волокна, существует множество полезных для здоровья продуктов, содержащих пребиотики. Наибольшее количество содержится в сырых вариантах следующих ингредиентов: чеснок, лук, лук-порей, спаржа, топинамбур, зелень одуванчика, бананы и водоросли.В целом, фрукты, овощи, бобы и цельнозерновые продукты, такие как пшеница, овес и ячмень, являются хорошими источниками пребиотических волокон.
Имейте в виду, что высокое потребление пребиотических продуктов, особенно если их вводить внезапно, может увеличить газообразование (метеоризм) и вздутие живота. Лица с чувствительностью желудочно-кишечного тракта, такой как синдром раздраженного кишечника, должны вводить эти продукты в небольших количествах, чтобы сначала оценить переносимость. При продолжении использования переносимость может улучшиться с меньшим количеством побочных эффектов.
Если человек не чувствителен к пище, важно постепенно внедрять диету с высоким содержанием клетчатки, потому что диета с низким содержанием клетчатки может не только уменьшить количество полезной микробиоты, но и увеличить рост патогенных бактерий, которые процветают в менее кислой среде. .
Продукты с пробиотиками содержат полезную живую микробиоту, которая может еще больше изменить микробиом человека. К ним относятся ферментированные продукты, такие как кефир, йогурт с живыми активными культурами, маринованные овощи, темпе, чайный гриб, кимчи, мисо и квашеная капуста.
Будущие направления исследований
Микробиом — это живая динамическая среда, в которой относительная численность видов может колебаться ежедневно, еженедельно и ежемесячно в зависимости от диеты, лекарств, физических упражнений и множества других факторов окружающей среды.Однако ученые все еще находятся на ранних этапах понимания широкой роли микробиома для здоровья и масштабов проблем, которые могут возникнуть в результате прерывания нормальных взаимодействий между микробиомом и его хозяином. [7]
[7]
Некоторые актуальные темы исследований:
- Как микробиом и их метаболиты (вещества, вырабатываемые метаболизмом) влияют на здоровье и болезни человека.
- Какие факторы влияют на структуру и баланс микробиома человека.
- Разработка пробиотиков в качестве функционального продукта питания и решение нормативных вопросов.
Конкретные области интересов:
- Факторы, влияющие на микробиом беременных женщин, младенцев и детей.
- Манипулирование микробами, чтобы противостоять болезням и лучше реагировать на лечение.
- Различия в микробиоме здоровых людей и людей с хроническими заболеваниями, такими как диабет, желудочно-кишечные заболевания, ожирение, рак и сердечно-сосудистые заболевания.
- Разработка диагностических биомаркеров микробиома для выявления болезней до их развития.
- Изменение микробиома в результате трансплантации микробов между людьми (например, трансплантация фекалий).
Связанные Ссылки
- Ursell, L.K., et al. Определение микробиома человека. Nutr Ред. , август 2012 г .; 70 (Дополнение 1): S38 – S44.
- den Besten, Gijs., Et al. Роль короткоцепочечных жирных кислот во взаимодействии между диетой, кишечной микробиотой и энергетическим обменом хозяина .J Lipid Res. 2013 сен; 54 (9): 2325–2340.
- Morowitz, M.J., Carlisle, E., Alverdy, J.C. Вклад кишечных бактерий в питание и метаболизм у критически больных. Surg Clin North Am. 2011 Aug; 91 (4): 771–785.
- Arumugam, M., et al. Энтеротипы микробиома кишечника человека. Природа. 12 мая 2011 г .; 473 (7346): 174-80.
- Кэнни, Г.О., Маккормик, Б.А. Бактерии в кишечнике, полезные жители или враги изнутри. Инфекция и иммунитет. Август 2008 г. 76 нет. 8, 3360-3373.
- Джандхьяла, С. Роль нормальной микробиоты кишечника. World J Gastroenterol. 2015, 7 августа; 21 (29): 8787–8803.
- Proctor, L.M. The Human Microbiome Project в 2011 г. и позже. Клеточный хозяин и микроб. Том 10, выпуск 4, 20 октября 2011 г., стр. 287-91.
Условия использования
Содержание этого веб-сайта предназначено для образовательных целей и не предназначено для предоставления личных медицинских консультаций.Вам следует обратиться за советом к своему врачу или другому квалифицированному поставщику медицинских услуг с любыми вопросами, которые могут у вас возникнуть относительно состояния здоровья. Никогда не игнорируйте профессиональные медицинские советы и не откладывайте их поиск из-за того, что вы прочитали на этом веб-сайте. Nutrition Source не рекомендует и не поддерживает какие-либо продукты.
Микробиом человека | Резюме
Определение
Термин «микробиом человека» относится к полному набору генов, содержащихся во всей коллекции микроорганизмов, обитающих в организме человека.
Важность
Триллионы симбиотических микробных организмов живут внутри и на поверхности человеческого тела. Их можно найти практически в любой части тела, включая кишечник, мозг, ухо, кожу, нос, ротовую полость, желудочно-кишечный тракт, дыхательные пути, мочевыводящие пути и влагалище, а также кровоток. В настоящее время считается, что их гены вносят больший вклад в выживание человека, чем гены человека. Такие гены, микробиом человека, имеют, например, решающее значение для процесса старения, пищеварения, иммунной системы, модуляции центральной нервной системы, а также настроения и когнитивных способностей человека.Это делает микробиом человека важным органом человеческого тела. Без него человеческое тело не может функционировать.
Наше микробное сообщество, известное как микробиота человека, состоит из бактерий, дрожжей и других эукарий, архей (примитивных одноклеточных организмов), грибов, простейших и неживых вирусов (бактериофагов). Бактерии составляют подавляющую часть микроорганизмов, населяющих наш организм. На данный момент это наиболее изученные микробы. По оценкам, в организме обитает более 10 000 видов бактерий.По данным исследователей из Human Microbiome Project, соотношение бактериальных генов, кодирующих белок, к человеческим генам составляет 360: 1. (1) Подавляющее большинство бактерий обитает в кишечнике. Эти бактерии играют решающую роль в расщеплении и усвоении питательных веществ, помогают расщеплять крахмалы, сахара и белки, которые люди не могут переварить иным образом, и синтезировать незаменимые аминокислоты и витамины. Они также играют роль в накоплении жира и производстве противовоспалительных факторов.
Помимо обилия бактерий, микробиота человека содержит большое количество разнообразных вирусов, включая вирусы растительного происхождения, эукариотические вирусы и гигантские вирусы.Бактериофаги, или сокращенно фаги, являются одними из наиболее распространенных вирусов. Это типичный вирус, поражающий бактерии. Помогая передавать гены от одной бактерии к другой, бактериофаги играют важную роль в генетической модификации бактерий, процессе, который, в свою очередь, может изменять человека. В целом вирусы играют важную роль в динамике экосистемы микробного сообщества, помогая, например, повысить устойчивость микробов к нарушениям, уклонению от иммунитета, поддержанию физиологических процессов.Кроме того, они важны для стимулирования и предотвращения колонизации болезнетворными микроорганизмами.
Ни у одного человека нет такого же микробиома. Он так же уникален, как отпечаток пальца человека. Однако микробиом человека — это динамическая система, которая изменяется в течение жизни человека. Некоторые из самых драматических изменений происходят в младенчестве и раннем детстве. Факторы окружающей среды и привычки образа жизни, например, как часто человек моется, что он ест, тип одежды, которую он носит, сколько времени он проводит на улице, с кем взаимодействуют и где живут, также определяют состав микробиома человека.Потребление антибиотиков также влияет на микробиом. (2)
Микробиом человека в настоящее время является горячей областью исследований. О том, насколько большое значение придается этой области, можно судить по 170 миллионам долларов США, выделенным Национальными институтами здравоохранения проекту микробиома человека (HMP), созданным в 2008 году и завершенным в 2017 году. После HMP венчурные капиталисты теперь вкладывают значительные средства в компании, занимающиеся микробиомом. Венчурные инвестиции в такие компании выросли на 458 человек.5%, до 114,5 млн долларов США в период с 2011 по 2015 год. Это контрастирует с общим объемом венчурных инвестиций за этот период, которые выросли всего на 103,4%, до 75,29 млрд долларов США. В 2016 году инвестиции в микробиом продолжали расти. К сентябрю 2016 года компании, занимающиеся микробиомом, привлекли 616,9 млн долларов США в виде венчурного капитала. Многие фармацевтические компании, в том числе Pfizer и Roche, также активно инвестируют в эту область. (3, 4) Компании, занимающиеся микробиомом, варьируются от исследовательских фирм, которые специализируются на сборе данных для потенциального партнерства с фармацевтическими компаниями, до тех, кто разрабатывает препараты для микробиома устройства, пробиотики и пребиотики.Некоторые компании также предоставляют услуги по секвенированию микробиома напрямую потребителю. Вместе эти компании становятся важным сектором биотехнологической промышленности.
Discovery
Разнообразие человеческого микробиома впервые было обнаружено Антони ван Ливенгук, голландским торговцем. В начале 1680-х годов он отметил поразительную разницу между микробами, обнаруженными в образцах, взятых изо рта, и микробами в фекальном стуле. Это было основано на образцах, которые он взял у себя и у здоровых и больных членов семьи, которые он исследовал под микроскопом.(5,6) Отражая преобладавшее в то время отношение к болезни, связанной с неприятным запахом или уравновешенным состоянием человеческого организма, ван Ливенгук не установил никакой связи между микробами и здоровьем.
Пройдет еще два столетия, прежде чем ученые начнут понимать связь между микробами и болезнями. Этому способствовала работа французского химика Луи Пастера и немецкого врача Роберта Коха, инициировавших разработку новых инструментов для выращивания и изучения микробов в связи с инфекционными заболеваниями в конце 19 века.Науке медицинской микробиологии в значительной степени способствовало создание чашек с неглубокой крышкой (чашка Петри) и использование агара, твердой питательной среды, которые вместе изменили процесс культивирования бактерий в лаборатории. В этот период также был разработан ряд методов выращивания вирусов, в том числе их культивирование в фертильных куриных яйцах, введенное в 1898 году. Наряду с успехами, достигнутыми в культивировании микроорганизмов, их идентификация также стала проще с улучшением увеличения микроскопов.(7) Процессу идентификации также способствовало появление новых методов окрашивания. Ранее организмы характеризовались путем изучения их формы и движения. (8)
Самая первая связь, установленная между конкретным организмом и конкретной болезнью, была установлена Кохом. В 1876 году он продемонстрировал, что разновидность бактерий Bacillus anthracis ответственна за смертельную болезнь сибирской язвы. Далее он определил микробные причины двух других инфекционных заболеваний — туберкулеза и холеры.К 1930 году микробиологи выяснили, что бактерии являются причиной более десятка болезней. Сюда входили те, которые были ответственны за гонорею, дизентерию и коклюш. (8)
Исследователи не ограничивались выявлением болезнетворных микроорганизмов. Некоторые также исследовали взаимосвязь между непатогенными микроорганизмами и хозяином. (9) Еще в 1901 году Эли Метчкинов, русский зоолог и иммунолог, указал на возможность использования живых микробов (пробиотиков) для улучшения кишечной микробиоты, чтобы способствовать хорошему здоровью. здоровье.(10) Вскоре после этого американский бактериолог Артур Кендалл начал исследовать нормальную кишечную флору и условия, необходимые им для поддержания и воспроизводства. В 1909 году он показал влияние диеты на состав кишечных бактерий у обезьян и влияние, которое это оказало на их здоровье. (11)
Определение характеристик микроорганизмов оставалось трудоемким процессом и сопровождалось трудностями на протяжении большей части начала двадцатого века. . Одна из ключевых проблем заключалась в том, что большинство методов окрашивания позволяло различать только широкие группы бактерий.Единственный способ идентифицировать конкретный вид — это культивировать образец. Обнаружение производилось путем помещения образцов на чашку и оценки их роста на различных питательных средах, морфологических характеристик колоний и метаболического производства или потребления организмом. Учитывая, что в лаборатории можно было легко выращивать лишь несколько видов, этот подход был сильно ограничен. Кроме того, количество организмов в образце, подсчитанное под микроскопом, никогда не совпадало с количеством колоний, выращенных на чашке с агаром.(9, 11)
Новая глава открылась для изучения микробов в 1950-х годах с появлением животных, свободных от микробов. (8) Это животные, осторожно извлеченные из матки их матери с помощью хирургического вмешательства, чтобы избежать контакта с микроорганизмами в материнской утробе. влагалище и кожу, а затем подняли в стерильной среде со стерильной пищей и водой. После создания стерильная мать родит беспроблемное потомство естественным образом. Имея животных, свободных от микробов, у ученых теперь были средства для изучения взаимодействий между хозяином и микробом и микробом с микробом путем преднамеренного введения в организм животных отобранных микроорганизмов или микробных популяций.(8)
Одним из первых микробиологов, использовавших преимущества стерильных животных, был Рене Дубос из Института медицинских исследований Рокфеллера (позже переименованного в Университет Рокфеллера). К середине 1950-х он пришел к выводу, что не все микробы, живущие в организме, вредны и являются частью четко определенной экосистемы, и что необходимы определенные условия, чтобы превратить микробы в вирулентные патогены, вызывающие болезни. (12) был проинформирован его более ранним исследованием, чтобы понять механизмы иммунологической устойчивости к туберкулезу.Поскольку микробы могут подавлять и усиливать рост и поведение друг друга, Дюбос подчеркнул необходимость не ограничиваться изучением каждого микроба по отдельности и рассматривать экосистему в целом. Это означало смотреть на то, как разные организмы общаются друг с другом, взаимодействуют с окружающей средой и изменяют ее. Поскольку большинство микробов все еще неизвестны, это была непростая задача. кишка.Это потребовало от команды разработки новых количественных методов для подсчета анаэробной бактериальной флоры в кишечнике и новой питательной среды для выращивания определенных кишечных бактерий. (8, 13) К середине 1960-х годов группа Дубоша обнаружила много различной местной флоры в кишечнике. . Многие из представленных ими видов микробов были далеки от случайных или инертных вторжений, как ранее предполагали исследователи. Действительно, они оказались важны для физиологии и здоровья желудочно-кишечного тракта. Лаборатория Dubos также продемонстрировала наличие важной взаимосвязи между диетой, стрессом и противомикробными препаратами в здоровье и росте микробов, что, в свою очередь, оказало множественное влияние на здоровье хозяина.Например, у самок мышей без микробов, которых кормили низкокачественной белковой диетой во время пренатального периода, было обнаружено потомство с низким уровнем дофамина и норэпинефрина в мозгу. (14, 15)
Изучение микробиоты человека стало неизмеримо проще. с появлением в 1980-х годах методов амплификации и секвенирования ДНК. Это позволило охарактеризовать микробы на основе их генетического профиля без необходимости сначала культивировать рассматриваемый организм. Исследованиям в этой области также способствовало принятие генов рибосомной РНК в качестве молекулярных маркеров в середине 1980-х годов, впервые предложенное Карлом Вёзе и Норманом Пейсом.Маркеры предоставили средства для определения эволюционных отношений между микробными сообществами. Вооруженные новыми методами, ученые теперь получили возможность более точно характеризовать и количественно определять, какие типы микробов присутствуют в том или ином сообществе, и впервые определять их биологические функции. Такая работа была стимулирована появлением в конце 1990-х годов новых секвенсорных машин. Это увеличило возможности секвенирования ДНК и ускорило процесс, а также снизило стоимость процесса.Совместное развитие вычислительных инструментов также открыло возможность анализировать постоянно увеличивающийся объем генерируемых данных. К 2005 году технология ДНК продвинулась настолько далеко, что большинство ученых теперь могли экономично и эффективно секвенировать ДНК целого микробного сообщества в образце. Это помогло сместить исследования с изучения свойств отдельных типов организмов изолированно на рассмотрение всей сети целых сообществ. (8, 16)
Новый этап в понимании человеческого микробиома начался с создания человеческого микробиома. Проект 2007 года.Это была серия скоординированных проектов, которые были запущены консорциумом из почти 80 университетов и научных учреждений из разных уголков мира. Проект, финансируемый NIH, был разработан для понимания микробных компонентов генетического и метаболического ландшафта человека и их роли в нормальной физиологии человека и его восприимчивости к болезням. К 2012 году исследователи HMP установили нормальный состав бактерий у здорового западного населения. Это включало очистку и анализ всей человеческой и микробной ДНК в 5000 образцах, взятых из полости рта, носа, кожи и влагалища у 242 здоровых американских добровольцев.Это было грандиозное мероприятие, которое было бы невозможно без резкого снижения стоимости секвенирования ДНК. В целом исследователям удалось идентифицировать от 81 до 99 процентов из более чем 10 000 видов микробов, обитающих в человеческой экосистеме. Их достижение было замечательным, учитывая, что до этого были изолированы лишь несколько сотен видов бактерий. (1)
Исследователи HMP также провели ряд исследований, чтобы изучить связь между микробиомом и болезнью.Было обнаружено, что разнообразие видов бактерий во влагалище женщины во время подготовки к родам резко сократилось. Другой показал пятикратное увеличение вирусной ДНК в образцах из носа, взятых у детей с лихорадкой, по сравнению с детьми без лихорадки. Был также предпринят ряд проектов по изучению взаимосвязи микробиома при определенных заболеваниях, включая болезнь Крона, язвенный колит, рак пищевода, акме, псориаз, атопический дерматит и иммунодефицит.
В 2014 году NIH профинансировал вторую фазу исследования, названную «Проект интегративного микробиома», направленную на углубление понимания того, как микробиом влияет на болезнь.Это направлено на понимание роли микробиома при беременности и преждевременных родах, воспалительных заболеваниях кишечника и диабете 2 типа.
Приложение
Изучение микробиома человека помогает исследователям понять, как организм реагирует на различные диеты, болезни и лекарства. Такая работа рассматривается как важный ключ к персонализированной медицине. Большая часть исследований современного микробиома человека сосредоточена на микроорганизмах, особенно бактериях, которые обитают в кишечнике.
Одно из первых результатов исследования было замечено в лечении хронического гастрита, состояния, которое, если его оставить, может вызвать язву двенадцатиперстной кишки и рак желудка. В 1982 году австралийские ученые Барри Маршалл и Робин Уоррен показали, что присутствие Helicobacter pylori в желудке может вызвать хронический гастрит. Их открытие положило конец десятилетиям медицинских учений о том, что бактерии не могут жить в кислой среде желудка, и убеждению, что пептические язвы вызваны стрессом, острой пищей и слишком большим количеством кислоты.Маршалл продемонстрировал связь, выпив бульон, содержащий Helicobacter pylori. Через пять дней у него появились симптомы. Благодаря этой работе теперь можно лечить пептические язвы коротким курсом антибиотиков и ингибиторов секреции кислоты.
Другой областью, где микробиом оказался важным, было лечение пациентов, инфицированных Clostridium difficile, типом бактерий, которые могут захватить желудочно-кишечный тракт пациента, когда антибиотики уменьшают или устраняют резидентные микробы.Некоторые пациенты выздоравливают от инфекции после прекращения приема антибиотиков. Многие, однако, многие этого не делают, и около 20% выздоравливающих продолжают иметь рецидивирующие инфекции. Это серьезная проблема, поскольку инфекции, вызванные C. difficile (CDI), могут приводить к тяжелой диарее и обезвоживанию, а также являются основной причиной заболеваемости и смертности у пожилых людей и пациентов с ослабленным иммунитетом.
В настоящее время разработан ряд методов для работы с CDI. Один из них предполагает передачу фекального материала от здорового донора пациенту.Этот подход был впервые использован для лечения пациента с псевдомембранозным колитом в 1958 году (19), но не получил широкого распространения до 2000-х годов, когда количество пациентов, страдающих ИКД, достигло масштабов эпидемии и началось секвенирование микробов. Лечение направлено на увеличение разнообразия кишечной флоры и изменение активности их метаболических путей, чтобы пациент мог противостоять атаке бактерий C. difficile. Использование трансплантации фекальной микробиоты у пациентов с ИКД стало настолько популярным, что в 2014 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США выпустило рекомендации по регулированию терапии, чтобы предотвратить наводнение рынка не прошедшими проверку и потенциально опасными образцами фекалий.Теперь любой донор должен пройти скрининг на патогены, чтобы реципиенты не заболели. Большая часть донорского материала первоначально была получена у друга или члена семьи пациента, которую затем обработал врач. Теперь лечение может проводиться с использованием пожертвований из банков стула. (20)
Помимо трансплантации фекальной микробиоты, фаговая терапия также исследуется в качестве лечения ИКД. Одно из преимуществ использования фагов в качестве терапевтических агентов состоит в том, что они самовоспроизводятся и имеют высокоспецифичные взаимодействия со своими бактериальными хозяевами.Они также оказывают минимальное воздействие на нецелевые бактерии или ткани тела. Таким образом, фаги можно использовать для заражения и уничтожения определенных патогенных бактерий. Использование фагов для лечения бактериальных инфекций у людей насчитывает почти столетие. (21) Тем не менее, этот метод имеет определенные проблемы. Одна из основных проблем — найти подходящий фаг для лечения ИКД. Это сложно из-за разнообразия бактерий C. difficile и постоянного появления новых красителей в клинических условиях. (22)
За последние двадцать лет Джеффри Гордон и его коллеги из Вашингтонского университета в Санкт-Петербурге провели несколько исследований.Луи также обнаружил важную связь между микрофлорой кишечника и ожирением. Это было обнаружено в ходе серии экспериментов на мышах. В одном исследовании они продемонстрировали, что стерильные мыши с большей вероятностью набирают вес при трансплантации кишечных микробов от мышей с генетическим или диетическим ожирением, чем при получении кишечных микробов от тощих мышей. Другой эксперимент включал трансплантацию микробов кишечника мышей без микробов, взятых от четырех пар человеческих близнецов, в каждой паре был один худой и один тучный близнец.Исходя из этого, команда обнаружила, что мыши, получившие микробы от близнецов с ожирением, стали толстыми, тогда как мыши, которым вводили микробы от худых близнецов, — нет. Этот эффект, однако, наблюдался только тогда, когда мышей содержали отдельно. Как только они были размещены вместе, все мыши остались худыми, что позволяет предположить, что мыши, которым была проведена трансплантация тучных микробов, приобрели микробы от худых мышей. (8)
Ряд исследований на людях, животных и in vivo также начал показывать, что кишечные бактерии могут определять, как больной раком реагирует на некоторые виды химиотерапии и иммунотерапии.На основании этого некоторые клиницисты начали попытки восстановить равновесие кишечного микробиома пациента, нарушенного радиацией и химиотерапией, давая им фекальную микробиоту, собранную до лечения. (18)
Issues
В настоящее время существует множество состояний. считается, что это связано с нарушением микрофлоры кишечника. Это включает не только ожирение, но и диабет, аутизм, беспокойство, сердечно-сосудистые проблемы и аутоиммунные расстройства. Однако большая часть работы, проведенной в этой области, пока выявляет только ассоциации, а не причинно-следственные связи.Также неясно, являются ли такие связи побочным эффектом, а не прямой причиной заболевания. Делать выводы еще больше затрудняет тот факт, что большая часть доказательств, которые мы сейчас имеем, основаны на экспериментах на мышах, свободных от микробов, а не на людях.
Несмотря на то, что проблемы остаются, исследования микробиома человека продолжаются. Каждый год мы наблюдаем беспрецедентный рост данных, собранных в этой области, чему способствуют достижения в области секвенирования всего генома и возможность трансплантировать и наблюдать микробные сообщества человека у мышей с более высокой эффективностью.Все это дает более глубокое понимание микробиома человека, а вместе с ним и способы манипулирования им для улучшения здоровья в будущем. Целевое использование антибиотиков для уничтожения отдельных микробов, пробиотики и пребиотики для распространения полезных бактерий, использование трансплантатов фекальной микробиоты для восстановления бактериальных сообществ и использование генетически модифицированных фагов — это лишь некоторые из методов, которые сейчас исследуются в медицинских целях.
Этот профиль написала Лара Маркс, сентябрь 2018 г..
Список литературы
1) NIH, «Проект NIH Human Microbiome Project определяет нормальный бактериальный состав организма» (13 июня 2012 г.), https://www.nih.gov/news-events/news-releases/nih-human-microbiome-project -Определяет-нормальный-бактериальный-макияж-тело.
2) П Амон, И. Сандерсон, «Что такое микробиом», BMJ: Архивы болезней детства — издание для образования и практики, (февраль 2017 г.), DOI 10.1136 / archdischild-2016-311643, https: // ep. bmj.com/content/102/5/257.
3) Б. Гормли, «Компании, занимающиеся микробиомом, привлекают крупные инвестиции», The Wall Street Journal, 18 сентября 2016 г.
4) E Branch, «Новые предприятия в микробиоме», Pharma’s Almanac, 8 мая 2017 г., https://www.pharmasalmanac.com/articles/new-ventures-in-the-microbiome.
5) Ван Левенгук, «Отрывок из письма Антони ван Левенгука», 12 сентября 1683 г.
6) Ван Левенгук, «О животных в зубной корке», Философские труды Лондонского королевского общества, 14 (1684), 568–74.
7) М. Уэйнрайт, Дж. Ледерберг, «История микробиологии», Энциклопедия микробиологии, том 2 (1992), https: // profiles.nlm.nih.gov/ps/access/bbabon.pdf.
8) JJ Houtman, «Микробиом человека, ваша собственная личная экосистема», FASEB, 24 марта 2015 г., https://www.faseb.org/Portals/2/PDFs/opa/2015/Breakthroughs%20In%20Bioscience%20Human % 20Microbiome.pdf.
9) Р.К. Азиз, «Взгляд столетней давности на микробиом кишечника!», Gut Pathogens, 1, 21 (2009), http://doi.org/10.1186/1757-4749-1-21.
10) Э. Мечников, «Медаль Уайльда и лекция Манчестерского литературно-философского общества.Br Med J, 1 (1901), 1027–28.
11) А.И. Кендалл, «Некоторые наблюдения по изучению кишечных бактерий», Journal of Biological Chemistry, 6 (1909), 499-507. Р. К. Ззир, «Взгляд столетней давности на микробиом кишечника», Патология кишечника, 1 (2009), 21, https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2797815/.
12) М. Хонигсбаум, «Рене Дубос, туберкулез и экологические аспекты вирулентности», История и философия наук о жизни, 39/3 (2017), 15.
13) F Sangodeyi, «Рене Дубос и развивающаяся наука о микробной экологии человека», неопубликованная статья, Гарвардский университет, 2012 г., http: // rockarch.org / публикации / resrep / sangodeyi.pdf.
14) Рене Дубос, Рассел Шедлер и Дуэйн Сэвидж, «Коренная флора желудочно-кишечного тракта», Болезнь толстой и прямой кишки, 10 (1966), 23-33. Поставлено 21 июня 1966 г., стр. 23.
15) Р. Дубос, Р. В. Шедлер, «Некоторые биологические эффекты пищеварительной флоры», Am J Med Sci, 244 (1962), 265–71.
16) XC Morgan, C Huttenhower (2012) Глава 12: Анализ микробиома человека. PLoS Comput Biol 8 (12): e1002808. https: // doi.org / 10.1371 / journal.pcbi.1002808species.
17) Дж. Л. Александер и др. «Модуляция эффективности и токсичности химиотерапии микробиотой кишечника», Nature, 14 (июнь 2017 г.), 356-65.
18) Л.М. Проктор, «Микробиом человека: правдивая история о вас и триллионах ваших ближайших (микроскопических) друзей», Action Bioscience, сентябрь 2013 г., http://www.actionbioscience.org/genomics/the_human_microbiome.html.
19) B Eiseman, W Silen, GS Bascom, AJ Kauvar, «Фекальная клизма как дополнение к лечению псевдомембранозного энтероколита», Surgery, 44/5 (ноябрь 1958), 854-9.
20) Б. Брукшир, «Чтобы регулировать трансплантацию фекалий, FDA должно сначала ответить на серьезный вопрос: что такое фекалии?», Science News, 18 мая 2018 г., https://www.sciencenews.org/blog/scicurious/fecal- трансплантаты-регуляция.
21) ST Abedon, SJ Kuhl, BG Blasdel, EM Kutter, «Фаговое лечение человеческих инфекций», Bacteriophage, 1/2 (март / апрель 2011 г.), 66-85.
22) KR Hargreaves, MRJ Clokie, «Clostridium difficile фаги: все еще сложно?», Microbiology (28 апреля 2014 г.), https: // doi.org / 10.3389 / fmicb.2014.00184.
Микробиом человека: хронология ключевых событий
| Дата | Событие | Люди | Мест |
|---|---|---|---|
| 1683 — 1684 | Антони ван Ливенгук, голландский торговец, заметил разительные различия между микробами в образцах ротовой полости и фекалий, взятых у него самого и взятых у больных и здоровых людей | van Leeuwenhoek | |
| 1885 | Луи Пастер выдвинул концепцию стерильных животных | Пастер | |
| 1901 | Илья Ильич Мечников обрисовал различия в микробном разнообразии, преобладающем в среде обитания человека, и указал, что микробы могут быть полезны для благополучия | Мечников | |
| 1909 | Доказано, что диета влияет на состав кишечных бактерий и здоровье обезьян | Кендалл | |
| 1940 | Исследователи подчеркнули, что стоматологические проблемы могут быть связаны с изменениями в экологии микробного сообщества во рту | Appleton | |
| 1944-1956 | Рене Дубос, микробиолог, провел исследования, чтобы понять условия, при которых туберкулезная палочка становится вирулентной | Dubos | |
| 1962-1966 | Американские ученые утверждали, что уничтожение одного типа бактерий, мирно живущих в людях, открывает вакуум для опасных захватчиков | Dubos, Schaedler, Savage | |
| 1 июля 1965 г. | Эксперименты на стерильных мышах показывают наличие микробов, необходимых для физиологии и здоровья желудочно-кишечного тракта | Дубос, Шедлер, Сэвидж, Костелло | Институт Рокфеллера |
| 9 мая 1986 г. | Исследования показывают, что гены рибосомной РНК могут использоваться в качестве молекулярных маркеров микробов | Woese, Pace, Olsen | Университет Индианы, Университет Иллинойса |
| 2007-2016 гг. | Проект микробиома человека (HMP) выполнен | ||
| 2008 | Проект микробиома человека запущен | Национальные институты здравоохранения | |
| 2008-2012 | Выполнен проект «МЕТАгеномика кишечного тракта человека (MetaHIT)» | ||
| 1 января 2009 г. | Эксперименты на стерильных мышах выявили роль кишечного микробиома в ожирении | Тернбо, Хамади, Яцуненко, Кантарель, Дункан, Лей, Согин, Джонс, Роу, Affourtit , Egholm, Henriss, AC Heath, R Knight, JI Gordon | |
| 2014 | Запущен проект интегративного микробиома | Национальный Институты здравоохранения | |
| 27 ноября 2015 г. | Эксперименты на мышах показывают, что реакция опухоли на иммунотерапию рака с использованием CTLA-4 Ингибитор контрольных точек можно улучшить, изменив микробиом кишечника. | Zitvogel, Veitzou, | Institut Gustave Roussy |
| 1 января 2017 г. | Проект микробиома человека завершен | Национальные институты здравоохранения | |
| 24 фев 2017 | Исследователи сообщают, что пациенты с большим разнообразием кишечных бактерий лучше реагируют на иммунотерапию рака | Варго, Гопалакришнан | Онкологический центр Андерсона, доктор медицины |
| 2 ноября 2017 г. | Больные раком, принимающие обычные антибиотики до или вскоре после приема ингибитора контрольной точки PD-1, быстрее рецидивируют и имеют более короткое время выживания | Зитвогель, Кремер | Institut Gustave Roussy |
| 2 Ноябрь 2017 г. | Эксперименты на мышах показывают, что рост опухоли можно уменьшить путем трансплантации фекалий пациентов, положительно ответивших на иммунотерапию рака | Варго, Гопалакришнан | Онкологический центр Андерсона, Институт Густав-Русси |
Антони ван Левенгук, голландский торговец, обнаружил поразительные различия между микробами в образцах ротовой полости и фекалий, взятых у него самого и у больных и здоровых людей.
Луи Пастер выдвинул концепцию стерильных животных.
Илья Ильич Мечников обозначил различия в микробной биохимии. разнообразие, преобладающее в среде обитания человека, и указанные микробы могут иметь преимущества для благополучия
Доказано, что диета влияет на состав кишечных бактерий и здоровье обезьян
Исследователи подчеркнули, что стоматологические проблемы могут быть связаны с изменениями в экологии микробного сообщества в рот
Рене Дубос, микробиолог, провел исследования, чтобы понять условия, при которых туберкулезная палочка становится вирулентной
Американские ученые утверждали, что уничтожение одного типа бактерий, мирно живущих в организме человека, открывает вакуум для опасных захватчиков
Эксперименты на стерильных мышах показывают наличие микробов важно для физиологии ология и здоровье желудочно-кишечного тракта
Исследования показывают, что гены рибосомной РНК могут использоваться в качестве молекулярных маркеров микробов
Осуществлен проект по микробиому человека (HMP)
Начался проектМикробиом человека
Осуществлен проект METAgenomics of the Human Intestinal Tract (MetaHIT) out
Эксперименты на стерильных мышах показывают роль кишечного микробиома в ожирении
Запуск проекта интегративного микробиома
Эксперименты на мышах показывают, что опухоль реагирует на иммунотерапию рака с использованием CTLA-4 Ингибитор контрольных точек можно улучшить, изменив микробиом кишечника
Проект микробиома человека завершен
Исследователи сообщают, что пациенты с большим разнообразием кишечных бактерий лучше реагируют на иммунотерапию рака
Больные раком, принимающие обычные антибиотики до или вскоре после приема ингибитора контрольной точки PD-1 было обнаружено, что рецидивы быстрее и меньше время выживания
Эксперименты на мышах показывают, что рост опухоли можно уменьшить, сделав трансплантаты фекалий от пациентов, которые положительно ответили на иммунотерапию рака
.
 А это влияет на наши суставы, сосуды, кроветворение, нервную систему.
А это влияет на наши суставы, сосуды, кроветворение, нервную систему. Издательство Кембриджского университета.
Издательство Кембриджского университета.