Гематологические нарушения у ВИЧ-инфицированных детей на фоне антиретровирусной терапии | Даминов
1. Хасанова Г.Р., Степанова Е.Ю., Анохин В.А., Абросимова A.A. Анемия и ВИЧ-инфекция // Инфекционные болезни. 2009. Т. 7, № 3. С. 58–61. [Khasanova G.R., Stepanova E.Yu., Anokhin V.A., Abrosimova A.A. Anemia and HIV infection. Infectious diseases, 2009, Vol. 7, No. 3, рр. 58–61 (In Russ.)].
2. Канестри В.Г. Гематологические нарушения у больных с ВИЧ-инфекцией, получающих антиретровирусную терапию // ВИЧ-инфекция и иммуносупрессии. 2013. Т.5, №3. C. 63–70. [Kanestri V.G. Hematological disorders in patients with HIV infection receiving antiretroviral therapy. HIV Infection and Immunosuppressive Disorders, 2013, Vol. 5, No. 3, рр. 63–70 (In Russ.)].
3. Petrache, A., Moller M.B., Frederiksen H. Hemophagocytosis associated with cytomegalovirus infection and azathioprin treatment for inflammatory bowel disease // Ugeskr. Laeger. 2010. Bd. 172, No. 1. P. 52–53.
4. Бартлет Дж. Клинические аспекты ВИЧ-инфекции: пер. с англ. М., 2012. С. 474 [Bartlett J. Clinical aspects of HIV. Moscow, 2012, 474 р. (In Russ.)].
Клинические аспекты ВИЧ-инфекции: пер. с англ. М., 2012. С. 474 [Bartlett J. Clinical aspects of HIV. Moscow, 2012, 474 р. (In Russ.)].
5. Старец Е.А., Котова Н.В. Анемия в раннем возрасте у детей с перинатальным контактом с ВИЧ // Клиническая педиатрия. 2008. № 5. С. 14. [Elder E.A., Kotova N.V. Anemia at an early age in children with perinatal contact with HIV. Clinical Pediatrics, 2008, No. 5, рр. 14 (In Russ.)].
6. Абросимова A.A., Хасанова Г.Р., Макарова М.В. Анемии у ВИЧ-инфицированных детей // Актуальные вопросы инфекционной патологии. Казань, 2007. 39 с. [Abrosimova A.A., Khasanova G.R., Makarova M.V. Anemia in HIV-infected children. Actual problems of infectious pathology. Kazan, 2007. 39 р. (In Russ.)].
7. Calis J.C.J., van Hensbroek, M.B., de Haan R.J., Moons P., Brabin B.J., Bates I. HIV-associated anemia in children: a systematic review from a global perspective // AIDS. 2008. Vol. 22. Р. 1099–1112.
8. Snopkova S., Matyskova M., Husa P., Svoboda R. Haemopoiesis defects in HIV/AIDS-anaemia // Klin. Mikrobiol. Infekс. Lek. 2005. Vol. 11, No. 4. P. 123–127.
Mikrobiol. Infekс. Lek. 2005. Vol. 11, No. 4. P. 123–127.
9. Baillou C., Simon A., Leclercq V., Azar N., Rosenzwajg M., Herson S., Klatzmann D., Lemoine F.M. Highly active antiretroviral therapy corrects hematopoiesis in HIV-1 infected patients: interest for peripheral blood stem cell-based gene therapy // AIDS. 2003. Vol. 17, No. 4. P. 563–574.
10. Clarke S.M., Mulcahy F., Healy C.M. et al. The efficacy and tolerability of combination antiretroviral therapy in pregnancy: infant and maternal outcome // Int. J. STD. AIDS. 2000. Vol. 11, No. 4. P. 220–223.
11. Lorenzi P., Spicher V.M., Laubereau B. Antiretroviral therapies in pregnancy: maternal, fetal and neonatal effects. Swiss HIV Cohort Study, the Swiss Collaborative HIV and Pregnancy Study, and the Swiss Neonatal HIV Study // AIDS. 2008. Vol. 12, No. 18. P. F241–F247.
12. Шифман Е.М., Ройтман Е.В., Кругова Л.В., Вартанов В.Я., Хуторская Н.Н. Гематологические изменения у ВИЧ-инфицированных беременных на фоне химиопрофилактики антиретровирусными препаратами // Акушерство и гинекология. 2012. Т. 4/2. С. 39–46. [Shifman E.M., Roitman E.V., Krugova L.V., Vartanov V.Ya., Khutorskaya N.N. Hematological changes in HIV-infected pregnant women against the background of chemoprophylaxis with antiretroviral drugs. Obstetrics and gynecology, 2012, Vol. 4/2, рp. 39–46 (In Russ.)].
2012. Т. 4/2. С. 39–46. [Shifman E.M., Roitman E.V., Krugova L.V., Vartanov V.Ya., Khutorskaya N.N. Hematological changes in HIV-infected pregnant women against the background of chemoprophylaxis with antiretroviral drugs. Obstetrics and gynecology, 2012, Vol. 4/2, рp. 39–46 (In Russ.)].
Диагностика и лечение ВИЧ
Диагностика ВИЧ-инфекции Лечение ВИЧ-инфекции (перейти)
Диагноз ВИЧ-инфекции устанавливает врач-инфекционист Центра СПИД путём комплексной оценки эпидемиологических данных, результатов клинического обследования и лабораторных исследований
Первым шагом и стандартным методом лабораторной диагностики ВИЧ-инфекции служит одновременное определение антител к ВИЧ 1, 2 и антигена р25/24 ВИЧ. Антиген р24 может обнаруживаться на 15-й, первые антитела – на 30-й, поздние – к 3-6 месяцам.
В лаборатории СПИД-центра можно пройти тест на ВИЧ на выявление антител и антигена. Услуга совершенно бесплатна для граждан РФ, конфиденциальна и, по желанию обратившегося, анонимна.
Процедура достаточно простая и состоит из трех этапов:
1. дотестовое консультирование (проводится по желанию пациента) — это конфиденциальный диалог со специалистом.
2. забор материала на исследование,
3. выдача результат и послетестовое консультирование.
Кроме стандартного теста на ВИЧ, при котором проводится забор крови из вены, существуют экспресс-тесты на ВИЧ.
Они могут проводиться по капле крови из пальца или по слюне. Такие тесты чаще ориентированы на выявление антител. Экспресс-тесты используют в тест-мобилях, на выездных акциях по информированию, консультированию и добровольному обследованию на ВИЧ.
Это закон: каждое исследование на ВИЧ с применением простых/быстрых тестов должно сопровождаться исследованием крови стандартными методами исследования на антитела к ВИЧ 1,2 и антиген p24 или направлением пациента на обследование стандартными методами.
Выдача заключения о наличии или отсутствии ВИЧ-инфекции только по результатам простого (быстрого) теста не допускается.
Лабораторную диагностику ВИЧ-инфекции можно пройти как в СПИД-центре, так и в поликлинике по месту жительства, женской консультации или диспансере, если Вы там состоите на учете и проходите регулярное лечение.
Тест на ВИЧ — единственный способ узнать, есть заболевание или нет. У ВИЧ-инфекции нет внешних специфических признаков или симптомов, если в острый период (это примерно год от момента заражения) и появляются какие-то недомогания, то все они протекают как известные нам болезни, например простудное заболевание или ангина.
Важно помнить, у ВИЧ-инфекции существует инкубационный период. Т.е. первые антитела можно обнаружить примерно через месяц, от момента заражения, а поздние — через три. Все это время человек может передать вирус другому, например, при незащищенном половом контакте, при этом тест на ВИЧ может быть отрицательным (антитела не будут выявлены).
Поэтому так важно сдавать тест на ВИЧ регулярно.
Дотестовое консультирование — беседа пациента со специалистом — проводиться перед сдачей анализа (теста на ВИЧ) и служит для того, чтобы:
— уточнить и оценить риски заражения ВИЧ-инфекцией;
— актуализировать информацию о ВИЧ, информировать или исправить неверные представления о заболевании;
— рассказать о процедуре забора анализа
— обсудить возможные результаты теста и подготовить пациента к результату исследования.
Итогом консультирования становится информированное добровольное согласие на прохождение процедуры — освидетельствования на ВИЧ. Оно заполняется в письменном виде и подтверждает решение пациента пройти анализ.
В каких случаях и как часто надо проходить тест на ВИЧ?
Если в вашей жизни нет риска заражения, то тест на ВИЧ можно проходить 1 раз в 1-3 года, например, при диспансеризации.
Если у Вас был риск — тест на ВИЧ необходимо сдать в ближайшее время от ситуации риска, повторно — через 3 месяца, т.е. после окончания периода инкубационного окна.
Тест на ВИЧ может быть как положительный — антитела к ВИЧ, и/или антиген ВИЧ обнаружены, так и отрицательным — антитела/антиген не обнаружены.
Отрицательный результат обследования на антитела к ВИЧ не является абсолютным подтверждением отсутствия заболевания. В течение нескольких месяцев после заражения ВИЧ (до 3 месяцев), результат обследования может быть отрицательным. Этот период назван «серонегативным окном» или «инкубационный период», о нём мы писали выше — период между заражением и появлением антител к ВИЧ.
Важно помнить: результаты исследования по телефону, электронной почте, путем СМС-информирования не сообщаются. Результат выдается при личном обращении обследуемого или его законного представителя.
После получения положительного результата методом ИФА или ИХЛА наступает следующий этап диагностики
 Для подтверждения результатов в отношении ВИЧ применяются подтверждающие тесты (иммунный, линейный блот и определение РНК/ДНК ВИЧ молекулярно-биологическими методами).
Для подтверждения результатов в отношении ВИЧ применяются подтверждающие тесты (иммунный, линейный блот и определение РНК/ДНК ВИЧ молекулярно-биологическими методами).Иммунный или линейный блот ориентированы на выявление антител к ВИЧ, но уже к конкретным гликопротеидам вируса. Моелкулярно-биологическией метод исследования (ПЦР) позволяет выявить генный материал ВИЧ — РНК или ДНК вируса. На этапе диагностики применяется качественный, анализ. В отличие от количественного он показывает только наличие или отсутствие генного материала ВИЧ в биологическом образце (крови), а не количество вирусных частиц.
К выявлению генного материала ВИЧ прибегают в случаях, когда пациенту требуется срочно начать прием препаратов, например, если новорожденный ребенок заразился от матери во время беременности и/или родов, если женщина беременна и необходимо принять решение о начале профилактики передачи ВИЧ от матери ребенку. Например, при наличии высокого риска заражения ВИЧ исследование проводится в первые 48 часов жизни ребенка и повторно и в возрасте 14 — 21 дня. Преимущественно применяется метод выявления ДНК ВИЧ. Получение положительных результатов обследования на ДНК ВИЧ или РНК ВИЧ в двух отдельно взятых образцах крови у ребенка в любом возрасте является лабораторным подтверждением диагноза ВИЧ-инфекции.
Преимущественно применяется метод выявления ДНК ВИЧ. Получение положительных результатов обследования на ДНК ВИЧ или РНК ВИЧ в двух отдельно взятых образцах крови у ребенка в любом возрасте является лабораторным подтверждением диагноза ВИЧ-инфекции.
Исследование антител к ВИЧ у детей, рожденных от ВИЧ-положительных мам будет давать положительный результат примерно до 18 месяцев. Это связано с наличием в крови ребенка материнских антител.
На каких сроках и какими тестами можно выявить генный материал ВИЧ, антиген р24 и антитела к ВИЧ
Самое раннее обнаружение генного материала ВИЧ может происходить на 7-10-й день от ситуации риска. Это исследование проводится методом ПЦР (полимеразно-цепная реакция) и выявляет РНК или ДНК ВИЧ. Обычно такие тесты ориентированы на качественную диагностику — то есть дают ответ, есть ВИЧ (положительный результат) или нет (отрицательный результат).
Тесты 4го поколения, которые используют сегодня во всех лабораториях России, выявляют антиген р24 ВИЧ-1, который появляется раньше, чем первые антитела. Но позже исчезает. И для диагностики остаются доступны антитела к ВИЧ-1 и антитела к ВИЧ-2. инкубационный период для таких тестов в среднем составляет 3 месяца.
Но позже исчезает. И для диагностики остаются доступны антитела к ВИЧ-1 и антитела к ВИЧ-2. инкубационный период для таких тестов в среднем составляет 3 месяца.
Это значит, что такой тест может выявить антитела уже к концу первого месяца (если они выработались у человека в достаточно для определения количестве), но при отрицательном результате тест на сроке до 3-х месяцев, тест на ВИЧ необходимо повторить по истечении периода серонегативного (инкубационного) окна.
В единичных случаях, связанных как правило с серьезными нарушениями работы иммунной системы, антитела могут вырабатываться позднее 3-х месяцев (например, при приеме цитостатиков при онкологических заболеваниях). В этом случае, тест на ВИЧ проводят повторно в более поздние сроки. Например в 6 месяцев, а при применении постконтактной химиопрофилактики препаратами АРВТ еще и в 12 месяцев. Но такие схемы обследования рекомендуется обсудить с врачом и проводить исследование под медицинским наблюдением с учетом всех факторов и особенностей здоровья человека.
Тесты третьего поколения можно чаще встретить сегодня в виде экспресс-тестов для самостоятельной диагностики или для диагностики в ситуациях, когда решение надо принять очень быстро (например, поступление на роды женщины, не обследованной на ВИЧ, травма острым инструментом медицинского работника, оказывающего помощь человеку, с неизвестным ВИЧ-статусом). Так же такие тесты используются на экспресс-акциях. Для тестов третьего поколения инкубационный период также составляет в среднем 3 месяца.
СанПиН 3.3686-21
Клинические рекомендации МЗ РФ «ВИЧ-инфекция у взрослых» (2020): «Стадия инкубации – период от момента заражения до появления реакции организма в виде клинических проявлений «острой инфекции» и/или выработки антител. Продолжительность обычно составляет от 4 недель до 3 месяцев, но в единичных случаях может увеличиться до 1 года. В этот период происходит активное размножение ВИЧ в отсутствие клинических проявлений заболевания, антитела к ВИЧ могут не выявляться. Диагноз ВИЧ-инфекции на данной стадии ставят на основании эпидемиологических данных; он может быть лабораторно подтверждён обнаружением в крови пациента ВИЧ, его антигенов (р24), нуклеиновых кислот (РНК или ДНК)».
Продолжительность обычно составляет от 4 недель до 3 месяцев, но в единичных случаях может увеличиться до 1 года. В этот период происходит активное размножение ВИЧ в отсутствие клинических проявлений заболевания, антитела к ВИЧ могут не выявляться. Диагноз ВИЧ-инфекции на данной стадии ставят на основании эпидемиологических данных; он может быть лабораторно подтверждён обнаружением в крови пациента ВИЧ, его антигенов (р24), нуклеиновых кислот (РНК или ДНК)».
Если у Вас обнаружили ВИЧ-инфекцию, то специалист обязан Вас сообщить об этом при личном визите. Вот почему так важно приходить за результатами анализа. Чаще всего диагноз устанавливает врач-специалист СПИД-центра. Именно поэтому в медицинской организации, где Вы сдавали анализ, врач может сообщить Вам лишь результат исследования и рекомендовать обратиться в СПИД-центр для установления диагноза и постановки на учет для диспансерного наблюдения и лечения.
Во время консультации специалист Вам должен сообщить:
— результат исследования
— разъяснить меры предосторожности, чтобы не допустить распространения ВИЧ-инфекции
— объяснить гарантии получения медицинской помощи и соблюдения прав и свобод
— предупредить об уголовной ответственности за создание угрозы заражения, либо за заражение другого лица ВИЧ-инфекцией.
Врач-эпидемиолог СПИД-центра обязан провести расследование и уточнить источник заражения. А также возможное дальнейшее распространение вируса. Поэтому человека с ВИЧ ждут вопросы, касающиеся любых ситуаций, связанных с возможностью передачи вируса:
— контактны с кровью в медицинских и немедицинских организациях
— употребление ПАВ
— сексуальные контакты и др.
Врач-инфекционист на приеме проведет осмотр и опросит Вас на предмет проявления острого заболевания ВИЧ-инфекцией. В 30-50% случаев у людей в первый год заражения появляются симптомы, напоминающие другие заболевания.
После установления диагноза проводится уточнение стадии заболевания и назначается лечение ВИЧ-инфекции.
Всем пациентам при постановке на диспансерный учет проводится комплекс лабораторных диагностических исследований для выявления следующих заболеваний:
сифилис (далее каждые 12 мес.)
вирусный гепатит С (далее каждые 12 мес.)
вирусный гепатит В (далее каждые 12 мес. )
)
токсоплазмоз (Toxoplasma gondii)
цитомегаловирус (Cytomegalovirus)
туберкулёз (далее каждые 6 мес.).
Вопросы
Есть ли доказательства существования ВИЧ?
Да, есть. ВИЧ является одним из самых изученных вирусов. Люди, отрицающие научно-доказанные факты, идущие против общественного мнения называются диссидентами. Узнать больше фактов о существовании ВИЧ Вам поможет эта брошюра (скачать).
Лечение ВИЧ
Ролик «Стадии развития ВИЧ. Лечение ВИЧ»
Препаратов, которые могли бы полностью вылечить ВИЧ, пока не существует. Вирус остается в организме человека на протяжении всей жизни. Однако в настоящее время разработаны специальные антиретровирусные препараты (АРВП), которые препятствуют размножению и снижают количество вируса в организме, позволяют сохранить или восстановить иммунные функции и предотвратить либо вылечить оппортунистические инфекции, возникающие на фоне иммунодефицита. Своевременно и правильно назначенное лечение позволяет сохранить здоровье и на много лет продлить жизнь пациентов с ВИЧ-инфекцией.
Своевременно и правильно назначенное лечение позволяет сохранить здоровье и на много лет продлить жизнь пациентов с ВИЧ-инфекцией.
Лечение таким препаратами называется комбинированной терапией, или антиретровирусной терапией (АРВТ). Это подразумевает прием трех или четырех препаратов одновременно. Сегодня лечение ВИЧ-инфекции рекомендуется начинать сразу после выявления заболевания. Это позволяет сохранить иммунную систему и быстро подавить активность вируса, поддержать качество жизни и предупредить развитие сопутствующих заболеваний.
Основной задачей АРТ является максимальное подавление размножения ВИЧ, что сопровождается снижением содержания РНК ВИЧ в крови (ВН) до неопределяемого (методом ПЦР) уровня.
Однако, не все люди сразу готовы начать принимать препараты, некоторым людям понадобится год или два, а то и больше для того чтобы решиться начинать прием АРВ-препаратов.
Принципами АРТ являются:
добровольность – осознанное принятие решения о начале лечения и его проведении,
документированное «информированное согласие»;
своевременность – как можно более раннее начало АРТ;
непрерывность – длительное (пожизненное) соблюдение режима приёма АРВП.
Начав такую терапию, ВИЧ-позитивный человек должен принимать ее всю жизнь регулярно и без перерыва. В противном случае у человека, пропускающего прием препаратов или вообще прекратившего лечение, вырабатывается резистентность.
Резистентность – это приспособляемость вируса к данному лекарству. Это означает, вирус изменился таким образом, что этот препарат престает на него действовать. Набор медикаментов, используемых при АРВТ, ограничен, поэтому в следующий раз выбор комбинации лекарств сокращается. Самое страшное, что изменения в вирусе будут передаваться при заражении дальше. Поэтому при принятии решения о начале лечения очень важна так называемая приверженность или готовность к АРВТ.
Законодательно в нашей стране лечение ВИЧ – инфекции обеспечивается бесплатно всем нуждающимся в нем гражданам.
Знакомство с комбинированной антиретровирусной терапией (скачать)
Мифы и страхи антиретровирусной терапии (скачать)
Усталость от антиретровирусной терапии (скачать)
Согласие пациента на начало лечения подтверждается заполнением и подписанием Информированного согласия на проведение АРТ
Схема терапии подбирается каждому пациенту с учетом выявленных особенностей — хронических заболеваний, мутации и резистентности, переносимости препаратов и эффективности их действия.
Контроль эффективности лечения
Для того, чтобы оценить, как проходит лечение, действует ли АРВТ и насколько сохранна иммунная система, врачи назначают комплекс анализов. Среди них есть два, на которые стоит обратить особе внимание.
Иммунный статус и вирусная нагрузка.
Существуют два очень важных анализа, которые необходимы всем людям с ВИЧ – иммунный статус и вирусная нагрузка. Именно благодаря им можно определить степень поражения иммунной системы и эффективность препаратов.
Что такое иммунный статус?
Иммунный статус определяет количество различных клеток иммунной системы. Для людей с ВИЧ имеет значение количество клеток CD4 или Т-лимфоцитов – белых клеток крови, которые отвечают за «опознание» различных болезнетворных бактерий, вирусов и грибков, которые должны уничтожаться иммунной системой.
Количество клеток CD4 у взрослого человека обычно составляет от 600 до 1200 клеток/мл.
В соответствии с классификацией иммунных нарушений ВОЗ выделяют следующие степени иммунных нарушений:
— отсутствие иммунодефицита или незначительный: CD4 >500 мкл ;
— умеренный иммунодефицит: CD4 350 — 499 мкл ;
— выраженный иммунодефицит: CD4 200 — 349 мкл ;
— тяжёлый иммунодефицит: CD4 <200 мкл или <15%.
Если количество клеток CD4 ниже 350 клеток/мл, рекомендуется начало антиретровирусной терапии (АРВТ) «по жизненным показаниям», так как при таком иммунной статусе возникает риск возникновения СПИД-ассоциированных заболеваний.
Число CD4 ниже 350 клеток/мл говорит о серьезном иммунодефиците. В этом случае надо принимать препараты не только для лечения ВИЧ-инфекции, но и для профилактики оппортунистических заболеваний: туберкулеза, грибковых, бактериальных и вирусных инфекций.
Главное, о чем говорит количество CD4 – о здоровье иммунной системы: ухудшается оно или улучшается.
Изменения в количестве CD4
Количество ваших клеток СD4 может то подниматься, то снова падать в результате инфекций, стресса, курения, физических упражнений, менструального цикла, приема контрацептивных таблеток, времени суток и даже времени года, более того, различные тест-системы могут давать разные результаты по количество CD4.
Именно поэтому очень важно регулярно сдавать анализ на иммунный статус и смотреть на изменения в результатах. Нельзя оценит состояние здоровья ВИЧ-положительного человека по одному единственному анализу. Если у вас есть инфекция, например, простуда или герпес, лучше отложить сдачу анализа до того момента, пока симптомы не пройдут.
Если у вас относительно высокое количество клеток CD4 (более 500), достаточно сдавать анализ на иммунный статус раз в 6 месяцев. При количестве клеток менее 500 клеток/мл, обследование необходимо проводить 1 раз в 3 месяца.
Без регулярного обследования иммунного статуса сложно определить, как развивается болезнь и необходима ли коррекция назначенной АРВ-терапии.
Что такое вирусная нагрузка?
Вирусная нагрузка показывает количество вирусных частиц в 1 мл крови. Вирусная нагрузка до 10 000 копий/мл считается не высокой.
От 10 000 до 50 000 копий/мл – средней
От 50 000 до 100 000 копий/мл и выше – высокой.
Если сравнить развитие ВИЧ-инфекции с поездом, который идет к станции СПИДа, то иммунный статус – это расстояние, которое осталось, а вирусная нагрузка – это скорость, с которой движется поезд.
По изменению вирусной нагрузки судят об эффективности терапии и правильности подбора препаратов при приеме АРВТ.
У человека, регулярно принимающего препараты АРВТ через 3 месяца от начала лечения вирусная нагрузка должны достигнуть неопределяемого уровня и сохраняться на этом уровне на протяжении всего периода лечения.
Неопределяемая вирусная нагрузка говорит о том, что вируса в организме человека очень мало, а значит и шансов передать ВИЧ другим людям, даже при незащищенном сексуальном контакте тое, очень мало. Именно на этом основано движение «Н=Н» — неопределяемая нагрузка=невозможность передачи ВИЧ. Любой риск передачи ВИЧ половым путем связан с вирусной нагрузкой, а неопределимость сводит этот риск к нулю.
АРТ не только полезна для вашего здоровья, но и защищает ваших партнеров.
Лечение сопутствующих заболеваний — гепатитов В и С, туберкулеза, герпес-вирусной инфекции, токсоплазмоза и др. — проводятся в соответствии с рекомендуемыми схемами и зависит от тяжести заболевания и степени пораженности иммунной системы.
Первичная профилактика (превентивное лечение) вторичных (оппортунистических) инфекций
При глубоком поражении иммунной системы важно не допустить развития заболеваний, возбудителям которых появилась возможность паразитировать в организме, оказавшемся без защиты. Такие заболевания называют оппортунистическими, а возбудителей оппортунистами от латинского opportunus — возможность.
Именно для этого были созданы схемы профилактики оппортунистических заболеваний для тех пациентов, у которых иммунодефицит не позволяет эффективно защищаться. Эти схемы включают прием препаратов, которые используются для лечения, но в дозах, меньших чем требуется для борьбы с уже имеющейся инфекцией.
Очень важно принимать препараты по назначению врача в соответствии с назначенной схемой. Это может спасти жизнь, ведь на фоне ослабленного иммунитета такие заболевания могут стать смертельными.
Это может спасти жизнь, ведь на фоне ослабленного иммунитета такие заболевания могут стать смертельными.
Для проведения профилактики вторичных инфекцией необходимо исключить их наличие.
Профилактика пневмоцистной пневмонии и токсоплазмоза при числе CD4 < 200 мкл-1 (менее 15%) — рекомендуется прием Ко-тримоксазола по схеме до повышения количества CD4+лимфоцитов на фоне АРТ > 200 клеток/мкл в течение 3 мес.
Профилактика грибковых заболеваний, в т.ч. кандидоза — противогрибковые препараты по назначению врача.
Профилактика нетуберкулёзных микобактериозов — азитромицин либо кларитромицин по схеме.
Профилактика туберкулеза — изониазид по схеме (либо другой препарат, сочетающийся в АРВТ).
Дозы препаратов и курс лечения зависят от степени иммунодефицита, тяжести состояния пациента.
ВИЧ и другие заболевания
Смотреть видеоролик о вирусных гепатитах В и С https://www.aids43.ru/profilactica/about-hiv/prevention-hiv-and-hepatitis/
Информация о вирусном гепатите С
Памятка для ВИЧ-положительных: что важно помнить о своем здоровье
Изучить всю информацию о лечении ВИЧ-инфекции — задача не из легких.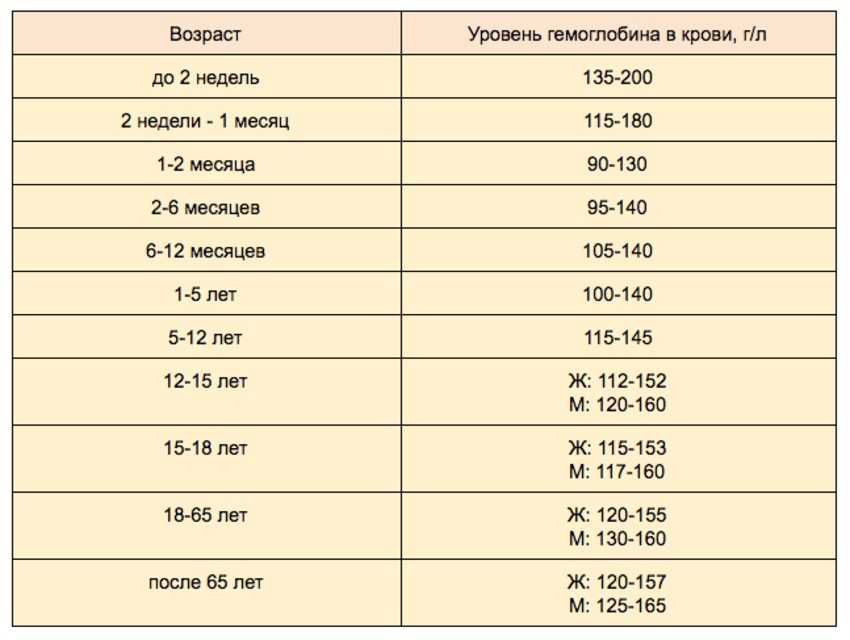 Для того, чтобы помочь людям с ВИЧ лучше ориентироваться в вопросах здоровья, нужно знать краткую информацию, которая может помочь сохранить свое здоровье.
Для того, чтобы помочь людям с ВИЧ лучше ориентироваться в вопросах здоровья, нужно знать краткую информацию, которая может помочь сохранить свое здоровье.
1. Избегайте есть сырое или не прожаренное мясо, сырую рыбу или сырые яйца. В них могут находиться опасные для вас микробы.
2. Если у вас никогда не было гепатита А или В, поговорите с врачом о вакцинации против них.
3. Проходите диспансеризацию, назначенную лечащим врачом СПИД-центра:
Флюорография или рентгенография ОГК – диагностика туберкулёза (1 раз в 6 мес.)
электрокардиограмма
ультразвуковое исследование органов брюшной полости (комплексное)
ультразвуковое исследование почек и надпочечников
Осмотры врачей в зависимости от клинических проявлений вторичных заболеваний (врач-дерматовенеролог, врач-терапевт, врач-невролог, врач-оториноларинголог, врач-офтальмолог, врач-акушер-гинеколог, врач-онколог и другие).
4. Регулярно ходить к «зубному» очень важно. Стоматологический осмотр желательно проходить дважды в год. Первые связанные с ВИЧ заболевания обычно проявляются в полости рта.
Стоматологический осмотр желательно проходить дважды в год. Первые связанные с ВИЧ заболевания обычно проявляются в полости рта.
5. Не отказывайтесь от визитов к врачу СПИД-центра. Необходимо регулярно сдавать анализы на вирусную нагрузку и иммунный статус.
6. Лучше избегать ненужной «активации» иммунной системы, из-за ВИЧ у нее и так хватает работы. Все заболевания, особенно инфекции, даже не связанные с ВИЧ нужно как можно скорее лечить. При «активации» иммунной системы вирус может размножаться быстрее.
7. ВИЧ-положительным женщинам нужно следить за состоянием шейки матки. Каждые 6 месяцев нужно проходить полный гинекологический осмотр, при этом желательно сделать цитологический анализ слизистой шейки матки. Это поможет предотвратить рак шейки матки.
8. Если вы чувствуете постоянную усталость, поговорите с вашим врачом о возможной анемии (низком уровне гемоглобина в крови) или низком уровне гормонов. Своевременная диагностика и лечение этих проблем может помочь.
9. Если вы внезапно и быстро теряете вес, понадобится лечение синдрома потери веса.
10. Если ваш иммунный статус выше 200 клеток/мл, проходите вакцинацию, предусмотренную национальным календарём прививок, это позволит избежать тяжелого течения инфекционных заболеваний — гриппа, коронавирусной инфекции.
11. Если у вас ВИЧ, это не значит, что он будет у вашего ребенка. На данный момент риск передачи ВИЧ от матери к ребенку составляет менее 2%.
12. Препараты АРВТ могут вызывать в первый месяц приема нежелательный (побочные) эффекты. Если через месяц они продолжают Вас беспокоить, проконсультируйтесь с лечащим врачом, возможно предложенная схема лечения Вам не подходит.
13. Иммунный статус определяет состояние иммунной системы, и является даже более важным анализом, чем вирусная нагрузка. ВИЧ-инфекция влияет на количество клеток CD4, которые разрушаются вирусом. Количество CD4 бывает процентным (от общего числа лимфоцитов), и абсолютным (количество CD4 в миллилитре крови). Процентное количество — более стабильно, поэтому оно может точнее говорить о развитии ВИЧ-инфекции.
Процентное количество — более стабильно, поэтому оно может точнее говорить о развитии ВИЧ-инфекции.
14. Обычно, хотя и не всегда, вирусная нагрузка позволяет «предсказать» как быстро будет развиваться ВИЧ-инфекция. Чем выше вирусная нагрузка, тем больше вероятность, что в ближайшее время количество CD4 начнет быстро уменьшаться. Если вирусная нагрузка меньше 50 копий/мл, вероятность прогрессирования заболевания крайне мала.
15. Узнайте, какие признаки могут быть у ВИЧ-ассоциированных раков: саркомы Капоши и не Ходжкинской лимфомы. Чем быстрее эти заболевания будут диагностированы, тем легче их будет вылечить.
Основное лечение ВИЧ-инфекции — комбинация из трех или более антиретровирусных препаратов. Они позволяют сделать вирусную нагрузку ниже определяемого уровня, повысить иммунный статус и предотвратить ВИЧ-ассоциированные заболевания. Врач должен подобрать комбинацию в зависимости от истории заболевания и вашего отношения к режиму приема, ограничениям в еде (например, принимать препарат натощак, или с едой) и возможным побочным эффектам. Необходимо сотрудничать с врачом, чтобы выбрать комбинацию, которая действительно вам подходит.
Необходимо сотрудничать с врачом, чтобы выбрать комбинацию, которая действительно вам подходит.
Препараты нужно принимать каждый день, вовремя. Если вы не в состоянии это делать, лучше поговорить с врачом о прекращении терапии и возможно, смене комбинации. Регулярные пропуски приема лекарств могут привести к тому, что вирус станет устойчивым к их действию.
Правило половины времени: если Вы забыли принять препарат в назначенное время и до следующего приема осталось меньше половины времени, которое должно пройти между приемами, то таблетку пить не следует. Если меньше — то препарат можно принять. Например, если Вы принимаете препарат через каждые 12 часов (утром, в 7.00 и вечером в 19.00), то в первые 6 часов после пропуска (т.е. до 13.00) Вы можете принять пропущенную таблетку. Если Вы вспомнили о пропуске когда до следующего приема осталось менее 6 часов, таблетку необходимо принять только в положенное время, т.е. в 19.00
Не принимайте никаких лекарств, витаминов или пищевых добавок, включая продаваемые «без рецепта», пока не убедитесь, что они сочетаются с теми препаратами, которые вы принимаете.
Важно заботиться о своих глазах. Если у вас ухудшилось зрение или у вас бывает «размытая картинка» обязательно обратитесь к врачу.
Учитесь общаться и сотрудничать с врачом. У многих возникают проблемы в отношениях с врачом, другие просто избегают посещений врача. Однако в результате вы только пострадаете сами. Активно занимайтесь своим здоровьем, и это избавит вас от многих проблем в будущем.
Ответы на частые вопросы о ВИЧ-инфекции и леченииИсчезают ли антитела к ВИЧ, если я принимаю терапию?
Нет, антитела сохраняются на протяжении всего периода заболевания, т.е. всю жизнь, даже если у человека неопределяемая вирусная нагрузка.
Распространенность, тяжесть и сопутствующие факторы анемии у пациентов с ВИЧ/СПИДом
J Res Med Sci. 2012 февраль; 17(2): 138–142.
, 1 , 2 , 3 , 4 и 5
Авторская информация Примечания и лицензионная информация об отказе от ответственности. хорошо охарактеризован в Иране. Это исследование было направлено на описание распространенности анемии и связанных с ней факторов у ВИЧ-позитивных пациентов.
хорошо охарактеризован в Иране. Это исследование было направлено на описание распространенности анемии и связанных с ней факторов у ВИЧ-позитивных пациентов.
Материалы и методы:
В поперечном исследовании распространенность анемии и факторы риска были оценены у 212 ВИЧ-позитивных пациентов в консультационном центре по поведенческим заболеваниям в Исфахане. Были проанализированы взаимосвязи между анемией, демографическими переменными и историей болезни. Анемия легкой и средней степени тяжести определялась при уровне гемоглобина 8–13 г/дл у мужчин и 8–12 г/дл у женщин. Тяжелая анемия определялась как уровень гемоглобина 8 г/дл.
Результаты:
Всего 212 ВИЧ-позитивных пациентов со средним возрастом ± стандартное отклонение 36,1 ± 9 лет..1 года были оценены. Мы обнаружили, что уровень гемоглобина был между 4,7 и 16,5 г/дл. В этом исследовании общая распространенность анемии составила 71%, при этом у большинства пациентов была легкая или умеренная анемия. Анемия легкой и средней степени тяжести и тяжелая анемия наблюдались у 67% и 4% пациентов соответственно. Среднее абсолютное количество CD4 составило 348 ± 267,8 клеток/м3. У 61 из 212 пациентов была поздняя стадия ВИЧ-инфекции (мужчины = 51 и женщины = 10). Из 212 ВИЧ-позитивных пациентов, включенных в исследование, 17 (8%) имели положительный анамнез на туберкулез. Мы обнаружили сильную связь между анемией и смертью.
Анемия легкой и средней степени тяжести и тяжелая анемия наблюдались у 67% и 4% пациентов соответственно. Среднее абсолютное количество CD4 составило 348 ± 267,8 клеток/м3. У 61 из 212 пациентов была поздняя стадия ВИЧ-инфекции (мужчины = 51 и женщины = 10). Из 212 ВИЧ-позитивных пациентов, включенных в исследование, 17 (8%) имели положительный анамнез на туберкулез. Мы обнаружили сильную связь между анемией и смертью.
Заключение:
Нормоцитарная анемия со сниженным количеством ретикулоцитов была наиболее распространенным типом анемии в целом. Распространенность анемии в этом исследовании относительно выше, чем в других подобных исследованиях. Такая высокая распространенность анемии требует тщательного наблюдения за пациентами, получающими лечение на основе зидовудина. Улучшение скрининга на анемию и инфекционные заболевания, а также модифицированная стратегия снижения вреда (HRS) для потребителей инъекционных наркотиков являются основными потребностями ВИЧ-серопозитивных пациентов.
Ключевые слова: СПИД, анемия, ВИЧ-положительные
Сразу после первых сообщений о случаях синдрома приобретенного иммунодефицита (СПИД) у больных с ВИЧ-инфекцией все чаще выявляли цитопении всех основных линий крови. Анемия является наиболее распространенной гематологической аномалией, связанной с ВИЧ-инфекцией, от 60% до 80% пациентов на поздних стадиях заболевания. В то время как у некоторых людей анемия может проявляться просто как лабораторная аномалия, у других могут наблюдаться типичные симптомы (например, утомляемость, одышка, снижение толерантности к физической нагрузке и снижение функциональных возможностей), напрямую связанные со снижением концентрации гемоглобина.[1] Патофизиология ВИЧ-ассоциированной анемии может включать три основных механизма: снижение продукции эритроцитов, усиление разрушения эритроцитов и неэффективное производство эритроцитов. Как правило, к ним относятся инфильтрация костного мозга новообразованиями или инфекциями, снижение продукции эндогенного эритропоэтина, гемолитическая анемия, применение миелодепрессивных препаратов, таких как зидовудин (зидовудин), или развитие в результате применения многочисленных лекарств. Анемия также может быть результатом дефицита питательных веществ — чаще всего дефицита железа, фолиевой кислоты или витамина B12. Дефицит витамина B12 может быть результатом мальабсорбции в подвздошной кишке или желудочной патологии, вызванной множеством инфекций или других состояний, поражающих слизистую оболочку желудка у ВИЧ-инфицированных пациентов. патология тощей кишки.[2]
Анемия также может быть результатом дефицита питательных веществ — чаще всего дефицита железа, фолиевой кислоты или витамина B12. Дефицит витамина B12 может быть результатом мальабсорбции в подвздошной кишке или желудочной патологии, вызванной множеством инфекций или других состояний, поражающих слизистую оболочку желудка у ВИЧ-инфицированных пациентов. патология тощей кишки.[2]
Овиреду и др. . сообщили, что высокоактивная антиретровирусная терапия-ВААРТ может повысить уровень B12 в сыворотке, а у пациентов с низким уровнем B12 в сыворотке в их исследовании не было характерных признаков дефицита витамина B12, а именно макроцитарной анемии и невропатии. [3] Анемия независимо снижает выживаемость (отношение рисков 2,6, 95% ДИ 1,9–3,4), ускоряет прогрессирование заболевания и увеличивает смертность среди ВИЧ-инфицированных. Эта проблема была описана в нескольких исследованиях в развивающихся странах.[4,5] В обзоре более 32 000 пациентов, инфицированных ВИЧ, ежегодная заболеваемость анемией увеличивалась по мере прогрессирования заболевания, поражая 3% всех пациентов с бессимптомной ВИЧ-инфекцией. 12% бессимптомных пациентов с числом клеток CD4 <200/мкл и 37% пациентов с заболеваниями, связанными со СПИДом.[6] Было обнаружено, что связь между анемией и снижением выживаемости не зависит от CD4+, количества Т-лимфоцитов и концентрации РНК ВИЧ в плазме. Анемичные ВИЧ-инфицированные люди, которые выздоравливают от анемии, имеют более высокие показатели выживаемости, чем те, кто не выздоравливает. , использование ZDV, низкое количество клеток CD4+ (<200 клеток/мл) и более высокие уровни РНК ВИЧ-1 в плазме. 15], что чаще всего происходит в течение 4–12 недель после начала приема зидовудина [16,17] 9.0003
12% бессимптомных пациентов с числом клеток CD4 <200/мкл и 37% пациентов с заболеваниями, связанными со СПИДом.[6] Было обнаружено, что связь между анемией и снижением выживаемости не зависит от CD4+, количества Т-лимфоцитов и концентрации РНК ВИЧ в плазме. Анемичные ВИЧ-инфицированные люди, которые выздоравливают от анемии, имеют более высокие показатели выживаемости, чем те, кто не выздоравливает. , использование ZDV, низкое количество клеток CD4+ (<200 клеток/мл) и более высокие уровни РНК ВИЧ-1 в плазме. 15], что чаще всего происходит в течение 4–12 недель после начала приема зидовудина [16,17] 9.0003
Это исследование было проведено для изучения распространенности анемии и связанных с ней факторов у пациентов с ВИЧ-инфекцией в Исфахане, Иран.
Это одноцентровое популяционное исследование было проведено в 2010 году. В консультационном центре по поведенческим заболеваниям в Исфахане, Иран, оценивалась распространенность анемии и коррелирующих факторов у общего числа зарегистрированных пациентов из 212 ВИЧ-позитивных. Зарегистрированные пациенты с ВИЧ-инфекцией были субъектами, прошедшими тестирование с помощью твердофазного иммуноферментного анализа (ИФА), которое было подтверждено с помощью теста Вестерн-блоттинг. Исследование было одобрено комитетом по этике медицинского университета Исфаханского университета медицинских наук.
Зарегистрированные пациенты с ВИЧ-инфекцией были субъектами, прошедшими тестирование с помощью твердофазного иммуноферментного анализа (ИФА), которое было подтверждено с помощью теста Вестерн-блоттинг. Исследование было одобрено комитетом по этике медицинского университета Исфаханского университета медицинских наук.
Лабораторные и демографические данные, собранные в консультационном центре по поведенческим заболеваниям, такие как гемоглобин, средний объем эритроцитов-MCV, количество CD4, возраст, пол, семейное положение, уровень образования, история употребления наркотиков (антиретровирусных или неантиретровирусных и профилактических), история болезни (лечение или документально подтвержденная инфекция вирусом гепатита B-HBV, вирусом гепатита C-HCV и микобактериями туберкулеза), стадия инфекции ВИЧ и СПИД на основании заявления ВОЗ о IV стадии ВИЧ-инфекции[18] и поведении с высоким риском инфицирования ВИЧ приобретение. Дополнительные биохимические исследования сывороточного ферритина, количества ретикулоцитов, сывороточного уровня В12 и фолиевой кислоты были проведены у 50 доступных пациентов с анемией (41 мужчина и 9 мужчин). женщины).
женщины).
Анемия легкой и средней степени тяжести определялась как уровень гемоглобина 8–13 и 8–12 г/дл у мужчин и женщин соответственно. Тяжелая анемия определялась как уровень гемоглобина ≤ 8 г/дл. Одномерные сравнения между пациентами с анемией и пациентами без анемии были выполнены с использованием точного Фишера, критерия Манна-Уитни и логистического регрессионного анализа. Все тесты значимости были двусторонними, и значение P менее 0,05 считалось значимым с использованием статистического программного обеспечения SPSS версии 18 для Windows.
Мы зарегистрировали в общей сложности 212 ВИЧ-позитивных случаев (мужчины = 179 (84,8%)) со средним возрастом ± стандартное отклонение 36,2 ± 9,1 года (мужчины = 36,8 ± 8,5 года; женщины = 32,9 ± 11,2 года). Из них 126 (77,8%) были неграмотными или имели начальное образование, 36 (22,2%) имели среднее или высшее образование. Демографические и лабораторные данные обобщены в []. Показатели (%) потребителей инъекционных наркотиков (ПИН) и имеющих гомосексуальные и/или гетеросексуальные контакты составили 123/151 (81,5%) и 88/106 (83%) соответственно. Однако у 61 и 106 пациентов отсутствовала информация об указанных факторах риска соответственно. От 9Из 8 пациентов, ответивших на вопросы относительно двух факторов риска, 61 (62,2%) ответили положительно на оба из них.
Однако у 61 и 106 пациентов отсутствовала информация об указанных факторах риска соответственно. От 9Из 8 пациентов, ответивших на вопросы относительно двух факторов риска, 61 (62,2%) ответили положительно на оба из них.
Таблица 1
Сравнение демографических и лабораторных данных между пациентами с анемией и без анемии ВИЧ/СПИД ± стандартное отклонение продолжительности диагностики ВИЧ у пациентов с анемией составило 3,91 ± 2,8 года, а у пациентов без анемии — 3,9 года.2±2,1 года, но эта разница была недостоверна ( P — значение=0,74).
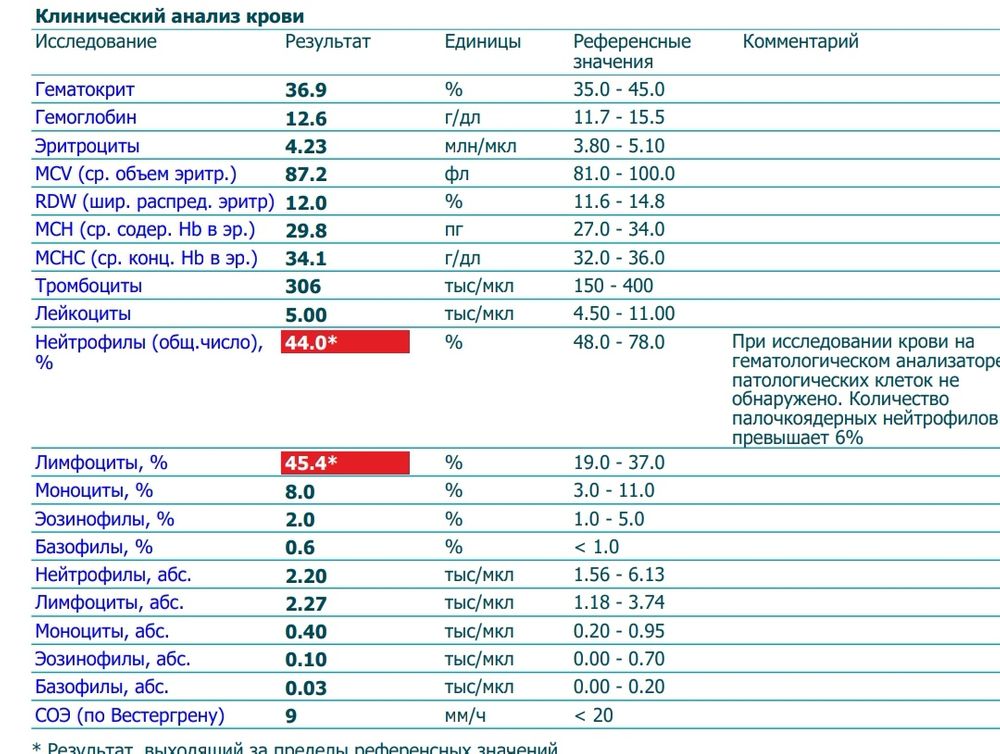
Общая распространенность анемии составила 71%, при этом у большинства пациентов была анемия легкой и средней степени тяжести. Анемия легкой и средней степени тяжести и тяжелая анемия наблюдались у 67% и 4% пациентов соответственно.
Уровень гемоглобина у пациентов составлял от 4,7 до 16,5 г/дл. Среднее значение ± стандартное отклонение гемоглобина у пациентов с анемией и без анемии составило 11,2 ± 1,3 и 14,22 ± 1,1 г/дл соответственно.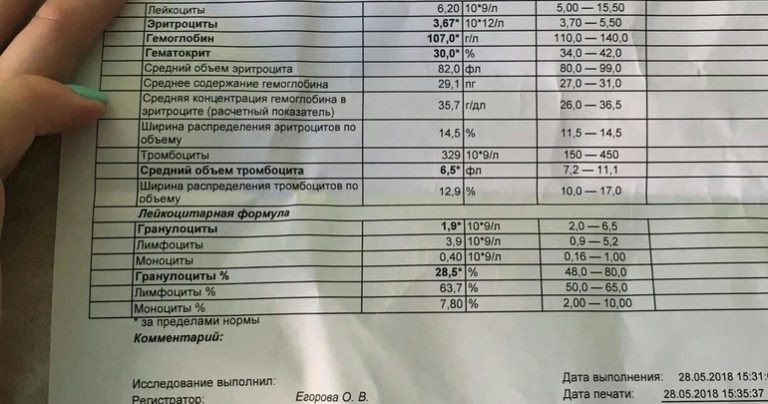 Однако разница не была статистически значимой ( P -значение = 0,41). Микроцитоз чаще встречался у женщин, чем у мужчин (19% против ± 15%; P -значение = 0,418). В этом исследовании 88 (72,7%) пациентов с анемией имели нормоциты со сниженным уровнем ретикулоцитов (мужчины = 74,3%, женщины = 62%). Двадцать (16,5%) и 13 (10,7%) имеют микроцитарную анемию и макроцитарную анемию соответственно.
Однако разница не была статистически значимой ( P -значение = 0,41). Микроцитоз чаще встречался у женщин, чем у мужчин (19% против ± 15%; P -значение = 0,418). В этом исследовании 88 (72,7%) пациентов с анемией имели нормоциты со сниженным уровнем ретикулоцитов (мужчины = 74,3%, женщины = 62%). Двадцать (16,5%) и 13 (10,7%) имеют микроцитарную анемию и макроцитарную анемию соответственно.
Среднее ± стандартное отклонение абсолютного количества CD4 составило 348 ± 267,8 клеток/м3 (диапазон 8–1594). В целом зидовудин принимали 54 пациента (600 мг в сутки). Среди пользователей ZDV 43 (79,6%) страдали анемией ( P -значение=0,38).
Из 212 пациентов 75 пропустили общий анализ крови. Из всех пациентов с анемией у 40% наблюдался дефицит железа (ферритин <30 мкг/л) и у 23% — дефицит витамина B 12 (<200 пг/мл). Пациентов с дефицитом фолиевой кислоты (<6 нг/мл) не было. Среднее значение ± стандартное отклонение фолиевой кислоты, витамина B12 и ферритина у пациента с анемией составило 16,9 ± 7,1 нг/мл, 347,2 ± 227,5 пг/мл и 74,6 ± 66,6 мкг/л соответственно.
Пролеченные пациенты получали тройную терапию, включающую ZDV, плюс ламивудин и эфавиренз, за исключением 4% пролеченных пациентов, которым ZDV был заменен на ставудин. Все пациенты с CD4<200 клеток/мкл получали ко-тримоксазол с целью профилактики токсоплазмоза. Ни один из пациентов не получал анти-HCV терапию.
Кроме того, 57/212 (26,9 %) когорты получали ZDV (600 мг в день), 37/212 (17,5 %) ко-тримоксазол (таблетки в дозе 1 раз в 12 ч) и 7/212 (3,3 %) капсулы. флуконазол (100-200 мг в сутки). 41/57 (71,9%) и 27/36 (75,0%) пациентов, принимавших ZDV и ко-тримоксазол, соответственно, страдали анемией.
Из 212 включенных ВИЧ-позитивных пациентов 61 (28,8%) находились на поздней стадии ВИЧ (СПИД) (мужчины = 51 и женщины = 10). Из 61 случая, у которых был диагностирован СПИД, у 16 (26,2%) CD4>200 клеток/мкл. Однако из-за орального кандидоза или рецидивирующей пневмонии выделяют СПИД в IV стадию ВИЧ-инфекции. Анемия чаще встречалась у больных СПИДом (41/52 (78,8%)), чем у других, эта разница была незначительно значимой (9). 0042 P -значение=0,055).
0042 P -значение=0,055).
Мы обнаружили сильную связь между анемией и смертью ( P — значение = 0,007). Кроме того, была проведена логистическая регрессия для проверки факторов, связанных с анемией. Для включения в модель были выбраны переменные, у которых в исходном анализе P-значение было больше 0,3. Качество подгонки логистической регрессии проверяли с помощью теста Хосмера и Лемешова. Критерий хи-квадрат (8 степеней свободы) был равен X 2 (8) = 6,37 ( P -значение = 0,606). Риск анемии при повышенном и пониженном MCV был примерно в два и шесть раз выше, чем при нормальном MCV, соответственно, но не был статистически значимым (OR=2,04 и 6,08 соответственно). Более подробная информация представлена в [Таблицах и ].
Таблица 2
Обобщенные результаты подбора логистической регрессии для 99 пациентов с ВИЧ/СПИДом
Открыть в отдельном окне клинически важным. Многофакторное происхождение анемии затрудняет определение ее первоначальной причины и/или ее надлежащее лечение. [19] Распространенность анемии в этом исследовании составила 71%, что значительно выше, чем распространенность анемии, зарегистрированная в аналогичных исследованиях не только в Иране, но и в других странах. [20,21] В Иране Ramezani и др. . (2008) сообщили, что легкая анемия имела место у 46% субъектов, в то время как тяжелой анемии не наблюдалось.[22] В исследовании 642 иранских ВИЧ-позитивных пациентов Джаббари и др. . сообщили, что распространенность анемии (определяемой как уровень гемоглобина <10 мг/дл) составляла 10,3% [23]. Чакраварти и др. . изучено на 1256 больных ЗДВ; У 203 (16,2%) (143 женщины) развилась анемия (<8 г/дл). Тяжелая анемия (<6,5 г/дл) была зарегистрирована у 100 (7,9%) пациентов [24].
[19] Распространенность анемии в этом исследовании составила 71%, что значительно выше, чем распространенность анемии, зарегистрированная в аналогичных исследованиях не только в Иране, но и в других странах. [20,21] В Иране Ramezani и др. . (2008) сообщили, что легкая анемия имела место у 46% субъектов, в то время как тяжелой анемии не наблюдалось.[22] В исследовании 642 иранских ВИЧ-позитивных пациентов Джаббари и др. . сообщили, что распространенность анемии (определяемой как уровень гемоглобина <10 мг/дл) составляла 10,3% [23]. Чакраварти и др. . изучено на 1256 больных ЗДВ; У 203 (16,2%) (143 женщины) развилась анемия (<8 г/дл). Тяжелая анемия (<6,5 г/дл) была зарегистрирована у 100 (7,9%) пациентов [24].
Следует исследовать мазок периферической крови, так как он дает много информации о морфологии клеток и может указать на причину изменения кроветворения. Согласно нашему исследованию, нормоцитарная анемия со сниженным количеством ретикулоцитов является наиболее распространенной формой анемии у ВИЧ-позитивных пациентов в Исфахане. Эта форма анемии может быть вызвана лекарственной токсичностью, подавлением вируса, инфильтрацией костного мозга злокачественными новообразованиями, смешанным дефицитом питательных веществ и хроническими инфекциями. Мата-Марин и др. . сообщили о нормоцитарной нормохромной анемии как о наиболее распространенной форме анемии (85%) у ВИЧ-позитивных пациентов, и в их исследовании не было случаев макроцитарной анемии.[25] В Иране Джаббари и др. . сообщили о макроцитозе у 11%, нормоцитозе плюс нормохромия у 41,1% и микроцитозе плюс гипохромия у 47,9% пациентов [21]. Чакраварти и др. . сообщили о нормоцитарной, нормохромной картине у 42% пациентов, а у других были обнаружены макроцитарные изменения.
Эта форма анемии может быть вызвана лекарственной токсичностью, подавлением вируса, инфильтрацией костного мозга злокачественными новообразованиями, смешанным дефицитом питательных веществ и хроническими инфекциями. Мата-Марин и др. . сообщили о нормоцитарной нормохромной анемии как о наиболее распространенной форме анемии (85%) у ВИЧ-позитивных пациентов, и в их исследовании не было случаев макроцитарной анемии.[25] В Иране Джаббари и др. . сообщили о макроцитозе у 11%, нормоцитозе плюс нормохромия у 41,1% и микроцитозе плюс гипохромия у 47,9% пациентов [21]. Чакраварти и др. . сообщили о нормоцитарной, нормохромной картине у 42% пациентов, а у других были обнаружены макроцитарные изменения.
Мы обнаружили, что анемия несколько чаще встречается у женщин, чем у мужчин. Уиллс и др. . и Диалло и др. . показали, что анемия чаще встречается у женщин, чем у мужчин. [26,27] Джаббари и др. . сообщили о пограничной связи между женским полом и анемией и уровнем CD4 (количество CD4 <200) [23].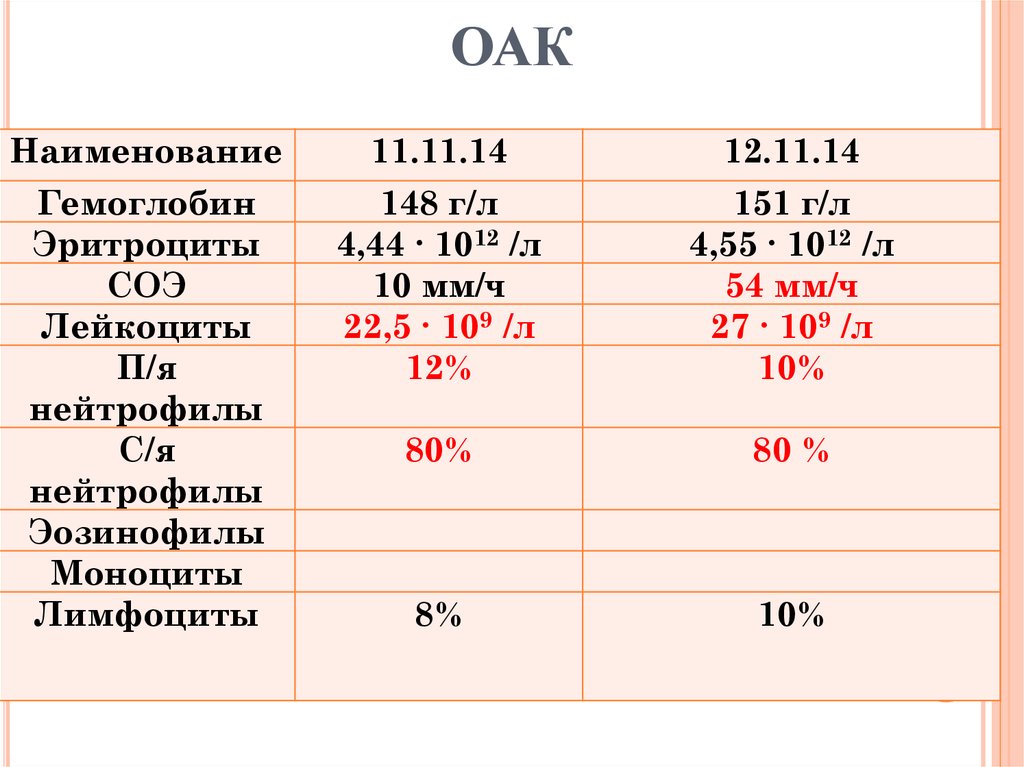 Милдван и др. . изучили распространенность анемии у 9690 ВИЧ-инфицированных пациентов и показали, что 39,5% (1721) пациентов, не получавших антиретровирусную терапию, и 35,5% (7252) пациентов, получавших ВААРТ, страдали анемией. Они обнаружили, что анемия более распространена среди мужчин и пациентов с CD4<200 клеток/мкл.0005 3 .[28] Мата-Марин и др. . в поперечном исследовании населения Мексики (54 мужчины и 9 женщин) без антиретровирусной терапии была обнаружена анемия и тяжелая анемия у 20,3% и 1,58% пациентов соответственно.[25]
Милдван и др. . изучили распространенность анемии у 9690 ВИЧ-инфицированных пациентов и показали, что 39,5% (1721) пациентов, не получавших антиретровирусную терапию, и 35,5% (7252) пациентов, получавших ВААРТ, страдали анемией. Они обнаружили, что анемия более распространена среди мужчин и пациентов с CD4<200 клеток/мкл.0005 3 .[28] Мата-Марин и др. . в поперечном исследовании населения Мексики (54 мужчины и 9 женщин) без антиретровирусной терапии была обнаружена анемия и тяжелая анемия у 20,3% и 1,58% пациентов соответственно.[25]
Доля анемии, вызванной дефицитом железа, может быть недооценена в нашем исследовании, поскольку диагноз дефицита железа основывался только на концентрации ферритина. Ферритин является белком острой фазы, уровень которого повышается при инфекциях.
Мур и др. . проанализировали данные 905 пациентов и обнаружили, что ВААРТ является эффективным методом лечения анемии при ВИЧ-инфекции.[29]
Кирагаа и коллеги в исследовании 5494 пациентов предполагают, что исходная тяжелая анемия (Hb ≤8 г/дл) не должна использоваться в качестве критерия для отказа от использования зидовудина при начале ВААРТ в условиях ограниченных ресурсов. [20] Они обнаружили, что ранняя тяжелая анемия возникала у 4% пациентов в течение первых 6 месяцев АРВТ, а исходная тяжелая анемия OR = 5,27 (9).5% ДИ 3,00–9,26), связанный с ранней тяжелой анемией. Употребление инъекционных наркотиков было независимым фактором риска железодефицитной анемии среди ВИЧ-инфицированных.[30] Мы обнаружили, что анемия чаще встречается у пациентов с поздними стадиями заболевания (СПИД), чем при самой ВИЧ-инфекции. Анемия является предиктором смерти у ВИЧ-позитивных пациентов. [31,32] В нашем исследовании была выявлена сильная связь между анемией и смертью.
[20] Они обнаружили, что ранняя тяжелая анемия возникала у 4% пациентов в течение первых 6 месяцев АРВТ, а исходная тяжелая анемия OR = 5,27 (9).5% ДИ 3,00–9,26), связанный с ранней тяжелой анемией. Употребление инъекционных наркотиков было независимым фактором риска железодефицитной анемии среди ВИЧ-инфицированных.[30] Мы обнаружили, что анемия чаще встречается у пациентов с поздними стадиями заболевания (СПИД), чем при самой ВИЧ-инфекции. Анемия является предиктором смерти у ВИЧ-позитивных пациентов. [31,32] В нашем исследовании была выявлена сильная связь между анемией и смертью.
Основные ограничения нашего исследования включают отсутствие измерений уровней эритропоэтина, вирусной нагрузки и титров парвовирусных IgM, а также относительно умеренное или большое количество отсутствующих данных когорты.
Распространенность анемии в этом исследовании относительно выше, чем в других подобных исследованиях. Такая высокая распространенность анемии требует тщательного наблюдения за пациентами, получающими лечение на основе зидовудина, особенно у женщин, ПИН и пациентов, получающих препараты с угнетающим действием на костный мозг, такие как котримоксазол. Нормоцитоз со сниженным уровнем ретикулоцитов является наиболее распространенной формой анемии в Исфахане и может быть вызван медицинской токсичностью, хроническими инфекциями или смешанным дефицитом питательных веществ. Улучшение скрининга на анемию и инфекционные заболевания, а также модифицированная стратегия снижения вреда (HRS) для ПИН (особенно среди женщин) являются основными потребностями ВИЧ-серопозитивных пациентов в Исфахане.
Нормоцитоз со сниженным уровнем ретикулоцитов является наиболее распространенной формой анемии в Исфахане и может быть вызван медицинской токсичностью, хроническими инфекциями или смешанным дефицитом питательных веществ. Улучшение скрининга на анемию и инфекционные заболевания, а также модифицированная стратегия снижения вреда (HRS) для ПИН (особенно среди женщин) являются основными потребностями ВИЧ-серопозитивных пациентов в Исфахане.
Мы благодарим вице-канцлера по здравоохранению Исфаханского университета медицинских наук и членов Консультационного центра по поведенческим заболеваниям в Исфахане за их сотрудничество.
Источник поддержки: Нет
Конфликт интересов: Не объявлено.
1. Зон Л.И., Аркин С., Групман Дж.Е. Гематологические проявления вируса иммунодефицита человека (ВИЧ) Br J Гематол. 1987; 66:251. [PubMed] [Google Scholar]
2. Volberding PA, Levine AM, Dieterich D, Mildvan D, Mitsuyasu R, Saag M для рабочей группы по анемии при ВИЧ. Анемия при ВИЧ-инфекции: клиническое воздействие и стратегии лечения, основанные на фактических данных. Клин Инфекция Дис. 2004; 38: 1454–63. [PubMed] [Академия Google]
Анемия при ВИЧ-инфекции: клиническое воздействие и стратегии лечения, основанные на фактических данных. Клин Инфекция Дис. 2004; 38: 1454–63. [PubMed] [Академия Google]
3. Owiredu WKBA, Quaye L, Amidu A, Addai-Mensah O. Распространенность анемии и иммунологических маркеров среди ВИЧ-пациентов из Ганы, ранее не получавших ВААРТ, и пациентов, получающих ВААРТ. Afr Health Sci. 2011; 11:2–15. [Бесплатная статья PMC] [PubMed] [Google Scholar]
4. Subbaraman R, Devaleenal B, Selvamuthu P, Yepthomi T, Solomon SS, Mayer KH, et al. Факторы, связанные с анемией у ВИЧ-инфицированных на юге Индии. Int J STD AIDS. 2009; 20: 489–92. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Berhane K, Karim R, Cohen MH, et al. Влияние высокоактивной антиретровирусной терапии на анемию и взаимосвязь между анемией и выживаемостью в большой когорте ВИЧ-инфицированных женщин: межведомственное исследование ВИЧ среди женщин. J Приобретение иммунодефицитного синдрома. 2004; 37:1245. [PubMed] [Google Scholar]
6. Салливан П.С., Хэнсон Д.Л., Чу С.Ю., Джонс Дж.Л., Уорд Дж.В. Эпидемиология анемии у лиц, инфицированных вирусом иммунодефицита человека (ВИЧ): результаты многогосударственного проекта по эпиднадзору за ВИЧ-инфекцией среди взрослых и подростков. Кровь. 1998;91:301–8. [PubMed] [Google Scholar]
Салливан П.С., Хэнсон Д.Л., Чу С.Ю., Джонс Дж.Л., Уорд Дж.В. Эпидемиология анемии у лиц, инфицированных вирусом иммунодефицита человека (ВИЧ): результаты многогосударственного проекта по эпиднадзору за ВИЧ-инфекцией среди взрослых и подростков. Кровь. 1998;91:301–8. [PubMed] [Google Scholar]
7. Бускин С., Салливан П. Анемия, ее лечение и исходы у лиц, инфицированных вирусом иммунодефицита человека. Переливание. 2004;44:826–32. [PubMed] [Google Scholar]
8. Мозес А., Нельсон Дж., Бэгби Г. Влияние вируса иммунодефицита человека-1 на гемопоэз. Кровь. 1998; 91: 1479–95. [PubMed] [Google Scholar]
9. Кодури П.Р., Сигна П., Николинакос П. Аутоиммунная гемолитическая анемия у больных, инфицированных вирусом иммунодефицита человека-1. Am J Гематол. 2002; 70: 174–176. [PubMed] [Академия Google]
10. Белперио PS, округ Колумбия. Распространенность и исходы анемии у лиц с вирусом иммунодефицита человека: систематический обзор литературы. Am J Med. 2004; 116 (Приложение 7A): 27S–43S. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
11. Bain BJ. Патогенез и патофизиология анемии при ВИЧ-инфекции. Карр Опин Гематол. 1999; 6: 89–93. [PubMed] [Google Scholar]
12. Levine AM, Berhane K, Masri-Lavine L, Sanchez M, Young M, Augenbraun M, et al. Распространенность и корреляты анемии в большой когорте ВИЧ-инфицированных женщин: Женское межведомственное исследование ВИЧ. J Приобретение иммунодефицитного синдрома. 2001; 26: 28–35. [PubMed] [Академия Google]
13. Семба Р.Д., Шах Н., Кляйн Р.С., Майер К.Х., Шуман П., Влахов Д. и соавт. Распространенность и кумулятивная заболеваемость и факторы риска анемии в многоцентровом когортном исследовании инфицированных и неинфицированных женщин, инфицированных вирусом иммунодефицита человека. Клин Инфекция Дис. 2002; 34: 260–6. [PubMed] [Google Scholar]
14. Richman DD, Fischl MA, Grieco MH, Gottlieb MS, Volberding PA, Laskin OL, et al. Токсичность азидотимидина (АЗТ) в лечении больных СПИДом и СПИД-ассоциированным комплексом. Двойное слепое плацебо-контролируемое исследование. N Engl J Med. 1987;317:192–7. [PubMed] [Google Scholar]
Двойное слепое плацебо-контролируемое исследование. N Engl J Med. 1987;317:192–7. [PubMed] [Google Scholar]
15. Volberding PA, Lagakos SW, Koch MA, Pettinelli C, Myers MW, Booth DK, et al. Зидовудин при бессимптомной инфекции вирусом иммунодефицита человека. Контролируемое исследование с участием людей с менее чем 500 CD4-положительными клетками на кубический миллиметр. Группа клинических испытаний СПИДа Национального института аллергии и инфекционных заболеваний. N Engl J Med. 1990;322:941–9. [PubMed] [Google Scholar]
16. Ssali F, Stohr W, Munderi P, Reid A, Walker AS, Gibb DM, et al. Распространенность, заболеваемость и предикторы тяжелой анемии при применении схем, содержащих зидовудин, у взрослых африканцев с ВИЧ-инфекцией в рамках исследования DART. Антивир Тер. 2006; 11: 741–9.. [PubMed] [Google Scholar]
17. Hoffmann CJ, Fielding KL, Charalambous S, Sulkowski MS, Innes C, Thio CL, et al. Антиретровирусная терапия с использованием зидовудина, ламивудина и эфавиренца в Южной Африке: переносимость и клинические проявления. СПИД. 2008; 22: 67–74. [Бесплатная статья PMC] [PubMed] [Google Scholar]
СПИД. 2008; 22: 67–74. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Hare CB. Система стадирования ВОЗ для ВИЧ-инфекции и заболеваний у подростков и взрослых, таблица 3; Клинический обзор ВИЧ-инфекции. В: Пайперл Л., Коффи С., Фольбердинг П.А., редакторы. База знаний HIV InSite [учебник онлайн] Сан-Франциско: Центр информации о ВИЧ UCSF; 2006. [Последний доступ 23 марта 2006 г.]. Доступна с: http://www.hivinsite.ucsf.edu/InSite?page=kb-03-01-01. [Академия Google]
19. Кройцер К.А., Рокстро Дж.К. Патогенез и патофизиология анемии при ВИЧ-инфекции. Энн Хематол. 1997; 75: 179–87. [PubMed] [Google Scholar]
20. Кирагга А.Н., Кастельнуово Б., Наканьяко Д., Манабе Ю.К. Исходная тяжелая анемия не должна препятствовать использованию зидовудина у пациентов, которым показана антиретровирусная терапия, в условиях ограниченных ресурсов. J Int AIDS Soc. 2010;13:42. [Бесплатная статья PMC] [PubMed] [Google Scholar]
21. Moore RD, Creagh-Kirk T, Keruly J, Link G, Wang MC, Richman D, et al. Долгосрочная безопасность и эффективность зидовудина у пациентов с прогрессирующим заболеванием, вызванным вирусом иммунодефицита человека. Группа изучения эпидемиологии зидовудина. Arch Intern Med. 1991;151:981-6. [PubMed] [Google Scholar]
Долгосрочная безопасность и эффективность зидовудина у пациентов с прогрессирующим заболеванием, вызванным вирусом иммунодефицита человека. Группа изучения эпидемиологии зидовудина. Arch Intern Med. 1991;151:981-6. [PubMed] [Google Scholar]
22. Рамезани А., Агахани А., Шариф М.Р., Банифазл М., Эсламифар А., Велаяти А.К. Распространенность анемии и сопутствующие факторы у ВИЧ-инфицированных пациентов: когортное исследование. Иран Дж. Патол. 2008;3:125–8. [Google Scholar]
23. Джем С., Рамезани А., Сабзвари Д., Морадманд-Бади Б., Сейедалинаги С.А., Джаббари Х. и др. Поперечное исследование анемии у пациентов, инфицированных вирусом иммунодефицита человека, в Иране. Арх Иран Мед. 2009; 12:145–50. [PubMed] [Академия Google]
24. Агарвал Д., Чакраварти Дж., Чаубе Л., Рай М., Агравал Н.Р., Сундар С.Х. Высокая частота зидовудин-индуцированной анемии у ВИЧ-инфицированных пациентов в восточной Индии. Индийская J Med Res. 2010; 132:386–9. [PubMed] [Google Scholar]
25. Mata-Marín JA, Gaytán-Martínez JE, Martinez-Martínez RE, Arroyo-Anduiza CI, Fuentes-Allen JL, Casarrubias-Ramirez M. Факторы риска и корреляты анемии при лечении ВИЧ — наивные инфицированные пациенты: перекрестное аналитическое исследование. Примечания BMC Res. 2010;3:230. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Mata-Marín JA, Gaytán-Martínez JE, Martinez-Martínez RE, Arroyo-Anduiza CI, Fuentes-Allen JL, Casarrubias-Ramirez M. Факторы риска и корреляты анемии при лечении ВИЧ — наивные инфицированные пациенты: перекрестное аналитическое исследование. Примечания BMC Res. 2010;3:230. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Диалло Д.А., Бэби М., Дембеле М., Кейта А., Сидибе А.Т., Сиссе И.А. и др. Частота, факторы риска и прогностическое значение анемии, связанной с ВИЧ/СПИДом, у взрослых в Мали. Бык Сок Патол Экзот. 2003; 96: 123–7. [PubMed] [Google Scholar]
27. Wills TS, Nadler JP, Somboonwit C, Vincent A, Leitz G, Marino K, et al. Распространенность анемии и связанные с ней факторы риска в одноцентровой амбулаторной клинической когорте ВИЧ. СПИД Читать. 2004; 14:305–10. 313-5. [PubMed] [Академия Google]
28. Mildvan D, Creagh T, Leitz G. Распространенность анемии и корреляция с биомаркерами и конкретными схемами антиретровирусной терапии у 9690 пациентов, инфицированных вирусом иммунодефицита человека: результаты исследования распространенности анемии. Curr Med Res Opin. 2007; 23: 343–55. [PubMed] [Google Scholar]
Curr Med Res Opin. 2007; 23: 343–55. [PubMed] [Google Scholar]
29. Moore RD, Forney D. Анемия у ВИЧ-инфицированных пациентов, получающих высокоактивную антиретровирусную терапию. J Приобретение иммунодефицитного синдрома. 2002; 29:54–7. [PubMed] [Google Scholar]
30. Данчек Б., Танг А.М., Томас А.М., Смит Э., Влахов Д., Семба Р.Д. Употребление инъекционных наркотиков является независимым фактором риска дефицита железа и железодефицитной анемии среди ВИЧ-серопозитивных и ВИЧ-серонегативных женщин. J Приобретение иммунодефицитного синдрома. 2005;40:198–201. [PubMed] [Google Scholar]
31. Johannessen A, Naman E, Ngowi BJ, Sandvik L, Matee MI, Aglen HE, et al. Предикторы смертности у ВИЧ-инфицированных пациентов, начинающих антиретровирусную терапию в сельской больнице в Танзании. BMC Infect Dis. 2008; 8:52. [Бесплатная статья PMC] [PubMed] [Google Scholar]
32. Saah AJ, Hoover DR, He Y, Kingsley LA, Phair JP. Факторы, влияющие на выживаемость после СПИДа: отчет о многоцентровом когортном исследовании СПИДа (MACS) J Acquir Immune Defic Syndr. 1994; 7: 287–9.5. [PubMed] [Google Scholar]
1994; 7: 287–9.5. [PubMed] [Google Scholar]
Проблемы с кровью и ВИЧ | aidsmap
Тестирование и мониторинг состояния здоровья
Greta Hughson
Изображение: phloxii/Shutterstock.com
Ключевые моменты
- клетки крови.
- Некоторые из этих проблем могут быть вызваны повреждением костного мозга.
- Эти проблемы включают анемию, нейтропению и тромбоцитопению.
У людей, живущих с ВИЧ, у которых количество CD4 превышает 350 клеток/мкл 3 , проблемы с кровью, описанные ниже, встречаются редко. У людей, получающих лечение от ВИЧ, эти проблемы возникают редко, за исключением анемии, которая может быть побочным эффектом антиретровирусного препарата зидовудина (AZT, Retrovir ).
Однако у людей, живущих с ВИЧ, у которых снижено количество клеток CD4 (когда произошло некоторое повреждение иммунной системы), иногда также наблюдается снижение числа некоторых других клеток в крови. Некоторые из этих проблем могут быть вызваны повреждением костного мозга, в котором вырабатываются клетки крови.
Некоторые из этих проблем могут быть вызваны повреждением костного мозга, в котором вырабатываются клетки крови.
ВИЧ может повредить костный мозг, напрямую заражая его клетки или нарушая уровень природных химических веществ (называемых факторами роста), которые способствуют развитию клеток костного мозга. На костный мозг также могут влиять некоторые лекарства или заболевания, которые могут развиться при слабой иммунной системе (оппортунистические инфекции). Уменьшение количества клеток крови также может быть вызвано разрушением клеток в кровотоке или нарушениями свертываемости крови, такими как гемофилия.
Последние новости и исследования в области тестирования и мониторинга здоровья
Помимо снижения числа клеток CD4, у людей, живущих с ВИЧ, есть три наиболее частых заболевания крови: анемия, нейтропения и тромбоцитопения. Все они выявляются с помощью стандартных анализов крови, которые вы должны делать в рамках обычного лечения ВИЧ.
Анемия
Анемия означает нехватку эритроцитов.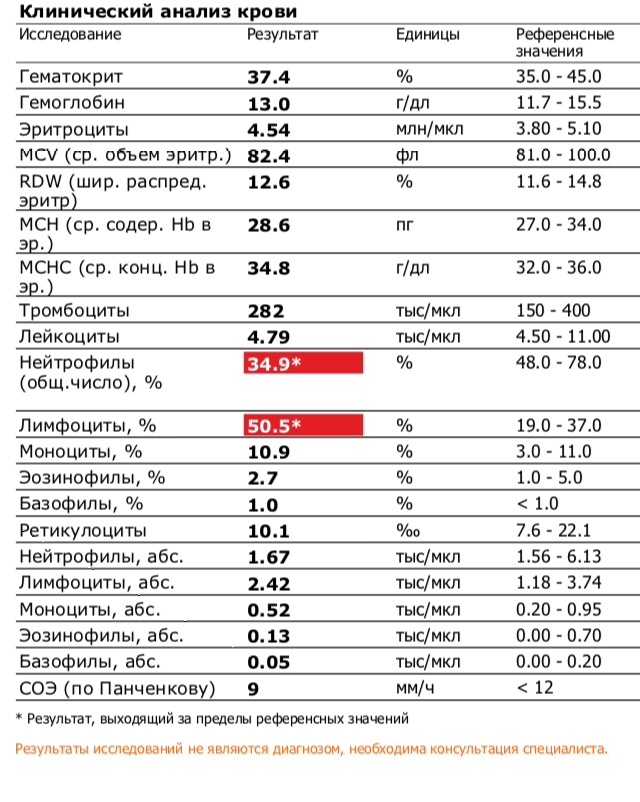 Красные кровяные тельца переносят кислород по телу, поэтому анемия может вызывать симптомы усталости и одышки. Это может быть побочным эффектом зидовудина, хотя это редко встречается у людей с числом CD4 выше 200. В настоящее время зидовудин редко используется, если вы начинаете лечение от ВИЧ. Если вы принимаете зидовудин и у вас развилась анемия, вы можете перейти на другой препарат. Но зидовудин является важным лекарственным средством для некоторых людей, особенно во время беременности.
Красные кровяные тельца переносят кислород по телу, поэтому анемия может вызывать симптомы усталости и одышки. Это может быть побочным эффектом зидовудина, хотя это редко встречается у людей с числом CD4 выше 200. В настоящее время зидовудин редко используется, если вы начинаете лечение от ВИЧ. Если вы принимаете зидовудин и у вас развилась анемия, вы можете перейти на другой препарат. Но зидовудин является важным лекарственным средством для некоторых людей, особенно во время беременности.
«Все эти проблемы выявляются с помощью стандартных анализов крови, которые вы должны делать в рамках обычного лечения ВИЧ».
Для лечения анемии врачи могут прописать инъекционный препарат под названием эритропоэтин. Это стимулирует организм вырабатывать больше эритроцитов. Людям с тяжелой анемией может потребоваться переливание крови для пополнения эритроцитов. Если анемия была вызвана приемом лекарственного средства, после лечения анемии можно возобновить прием лекарственного средства, на этот раз в более низкой дозе.
Анемия также может быть вызвана некоторыми оппортунистическими инфекциями. Если их лечить, анемия обычно улучшается.
Анемия может иметь и другие причины, не связанные с ВИЧ и медикаментозным лечением. Дефицит железа является распространенной причиной анемии в Великобритании. Это часто вызвано кровотечением, например, из-за язвы желудка или обильных менструаций. Это также довольно распространено во время беременности. Если у вас диагностирована железодефицитная анемия, врач может порекомендовать добавки или изменения в вашем рационе.
Нейтропения
Нейтропения означает недостаток нейтрофилов. Это тип лейкоцитов, которые в основном атакуют бактерии и грибки, поэтому люди с нейтропенией подвергаются повышенному риску этих инфекций. Наиболее распространенной причиной является антиретровирусный препарат зидовудин, антицитомегаловирусный (ЦМВ) препарат ганцикловир или препараты, используемые для лечения рака и опухолей. Люди, живущие с ВИЧ, часто имеют несколько более низкий уровень нейтрофилов, чем люди, у которых нет ВИЧ, но серьезная нейтропения редко встречается у людей с числом CD4 выше 200.
Глоссарий
анемия
Дефицит или изменение размера или функции эритроцитов. Эти клетки переносят кислород к органам тела. Симптомы могут включать одышку, усталость и отсутствие концентрации.
нейтропения
Недостаток нейтрофилов, типа лейкоцитов, которые борются с бактериальными инфекциями.
тромбоцитопения
Снижение количества тромбоцитов (клетки крови, отвечающие за свертываемость крови). Это приводит к спонтанным кровоподтекам и длительному кровотечению.
костный мозг
Клетки в середине костей, отвечающие за выработку клеток крови.
нейтрофилы
Иммунные клетки в крови, которые могут атаковать бактериальные и грибковые инфекции.
Нейтропению можно лечить, прекратив прием препарата, который ее вызывает, или уменьшив дозу. В качестве альтернативы, если количество нейтрофилов падает очень низко (ниже 500), врачи могут назначить Г-КСФ (гранулоцитарно-колониестимулирующий фактор), препарат, который стимулирует организм вырабатывать лейкоциты и, как было показано, улучшает нейтропению и снижает риск нейтропении.